Похожие презентации:
Углеводы. Энергетический обмен
1. Углеводы. Энергетический обмен
2. Углеводы
На долю углеводов приходится примерно 75% массы пищевого суточного
рациона и более 50% от суточного количества необходимых калорий.
Однако неправильно сводить функцию углеводов только к энергетическому
обеспечению процессов жизнедеятельности организма. Следует отметить
и структурную роль углеводов. Так, в виде гликозаминогликанов углеводы
входят в состав межклеточного матрикса. Большое число белков
(ферменты, белки-транспортёры, белки-рецепторы, гормоны) гликопротеины, углеводная составляющая которых повышает их
специфичность. Например, различия в строении олигосахаридных
фрагментов клеточной оболочки эритроцитов обеспечивают групповую
принадлежность крови. Из углеводов в процессе метаболизма образуется
большое число органических соединений, которые служат исходными
субстратами для синтеза липидов, аминокислот, нуклеотидов. Производные
углеводов - глюкурониды - участвуют в детоксикации ксенобиотиков и
инактивации веществ эндогенного происхождения. Углеводы могут быть
синтезированы в организме с использованием других метаболитов:
некоторых аминокислот, глицерина, молочной кислоты. Углеводы нельзя
считать незаменимыми компонентами пищи. Однако если исключить
углеводы из диеты, то следствием может быть гипогликемия, для
компенсации которой будут расходоваться белки и липиды. Таким образом,
углеводы - обязательные пищевые компоненты, потому что помимо их
основной энергетической функции (клеточные "дрова") углеводы участвуют
во многих метаболических клеточных процессах.
3. 1. Строение углеводов
• Термин "углеводы", предложенный в XIXстолетии, был основан на предположении,
что все углеводы содержат 2 компонента углерод и воду, и их элементарный состав
можно выразить общей формулой Cm(H2O)n.
4. Классификация
• Углеводы можно разделить на 3 основныегруппы в зависимости от количества
составляющих их мономеров:
• Моносахариды
• Олигосахариды
• Полисахариды.
5. Моносахариды
• Моносахариды - производные многоатомных спиртов,содержащие карбонильную группу. В зависимости от
положения в молекуле карбонильной группы моносахариды
подразделяют на альдозы и кетозы.
• Альдозы содержат функциональную альдегидную группу НС=О, тогда как кетозы содержат кетонную группу >С=О.
Название моносахарида зависит от числа составляющих его
углеродных атомов, например альдотриозы, кетотриозы,
альдогексозы, кетогексозы и т.д.
• Моносахариды по строению можно отнести к простым
углеводам, так как они не гидролизуются при переваривании,
в отличие от сложных, которые при гидролизе распадаются с
образованием простых углеводов
• В пище человека (фрукты, мёд, соки) содержится
небольшое количество моносахаридов, в основном глюкоза
и фруктоза (знать циклические и линейные формулы
фруктозы, глюкозы, галактозы!).
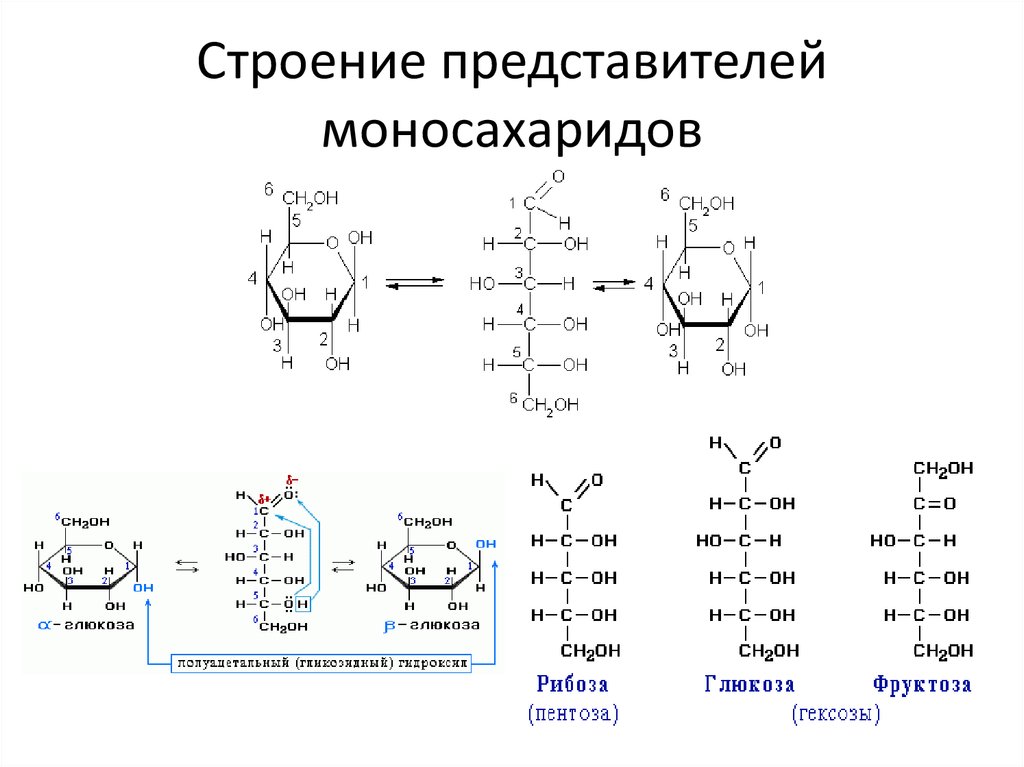
6. Строение представителей моносахаридов
7.
• Пиранозы — моносахариды, находящиеся вциклической форме и содержащие шестичленное
(пирановое) кольцо. Пиранозы образуются в
результате внутримолекулярной ацетализации
гидроксигруппы при C-5 и альдегидной группы C-1
(для гексоз). Пиранозы могут существовать в виде
α- и β-аномеров.
• Фуранозы — моносахариды, находящиеся в
циклической форме и содержащие пятичленное
(фурановое) кольцо. Фуранозы образуются в
результате внутримолекулярной ацетализации
гидроксигруппы и карбонильной группы. Наиболее
часто кольцо фуранозы является циклическим
полуацеталем (альдопентозы) или циклическим
полукеталем (кетогексозы). Фуранозы могут
существовать в виде α- и β- аномеров.
8. Строение представителей моносахаридов
9. Реакции моносахаридов (мутаротация, образование гликозидной связи, этерификация, окисление – восстановление)
• Мутаротация,или
аномеризация
взаимопревращение аномерных форм
моносахаридов, α- и β-формы аномеров
находятся в растворе в состоянии
равновесия.
При
достижении
этого
равновесия происходит мутаротация размыкание и замыкание пиранового
кольца и, соответственно, изменение
расположения Н- и ОН-групп при первом
углероде моносахарида.
10.
11. Реакции моносахаридов
• Образование гликозидов. Гликозидная связьимеет важное биологическое значение,
потому что именно с помощью этой связи
осуществляется
ковалентное
связывание
моносахаридов
в
составе
олигои
полисахаридов. При образовании гликозидной
связи
аномерная
ОН-группа
одного
моносахарида взаимодействует с ОН-группой
другого моносахарида или спирта. При этом
происходят отщепление молекулы воды и
образование О-гликозидной связи.
12. Образование гликозидов.
• Все линейные олигомеры (кроме дисахаридов) или полимерысодержат мономерные остатки, участвующие в образовании
двух гликозидных связей, кроме концевых остатков,
образующих только одну гликозидную связь. Некоторые
гликозидные остатки могут образовывать три гликозидные
связи, что характерно для разветвлённых олиго- и
полисахаридов. Олиго- и полисахариды могут иметь концевой
остаток моносахарида со свободной аномерной ОН-группой, не
использованной при образовании гликозидной связи. В этом
случае при размыкании цикла возможно образование
свободной карбонильной группы, способной окисляться. Такие
олиго- и полисахариды обладают восстанавливающими
свойствами и поэтому называются восстанавливающими, или
редуцирующими.
• Аномерная
ОН-группа
моносахарида
может
взаимодействовать с NН2-группой других соединений, что
приводит к образованию N-гликозидной связи. Подобная
связь присутствует в нуклеотидах и гликопротеинах
13. Образование гликозидной связи
A. Образование α-1,4- и α-1,6-гликозидных связей. Б. Строение линейногополисахарида: 1 - α-1,4-гликозидные связи между мономерами; 2 невосстанавливающий конец (невозможно образование свободной
карбонильной группы у аномерного углерода); 3 - восстанавливающий
конец (возможно размыкание цикла с образованием свободной
карбонильной группы у аномерного углерода).
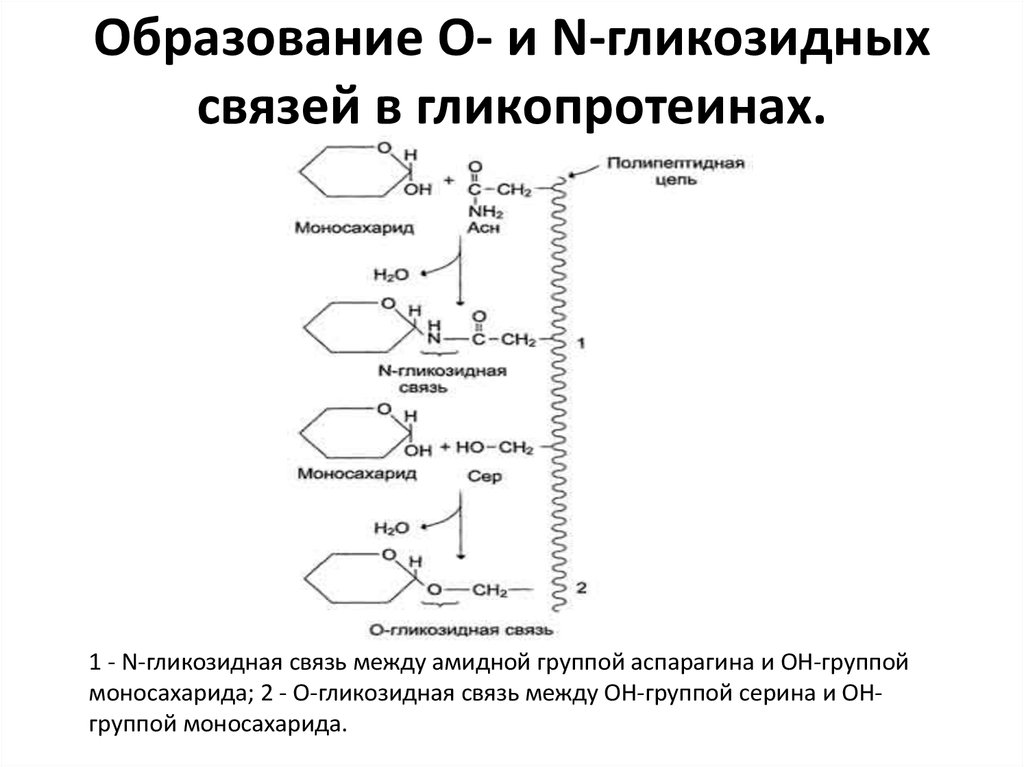
14. Образование О- и N-гликозидных связей в гликопротеинах.
1 - N-гликозидная связь между амидной группой аспарагина и ОН-группоймоносахарида; 2 - О-гликозидная связь между ОН-группой серина и ОНгруппой моносахарида.
15. Реакции моносахаридов
• Этерификация. Это реакция образования эфирной связи междуОН-группами моносахаридов и различными кислотами. В
метаболизме углеводов важную роль играют фосфоэфиры эфиры моносахаридов и фосфорной кислоты. В метаболизме
глюкозы особое место занимает глюкозо-6-фосфат.
Образование глюкозо-6-фосфата происходит в ходе АТФзависимой реакции при участии ферментов, относящихся к
группе киназ. АТФ в данной реакции выступает как донор
фосфатной группы. Фосфоэфиры моносахаридов могут
образовываться и без использования АТФ. Например, глюкозо1-фосфат образуется из гликогена при участии Н3РО4.
Физиологическое значение фос-фоэфиров моносахаридов
заключается в том, что они представляют собой
метаболически
активные
структуры.
Реакция
фосфорилирования моносахаридов важна для метаболизма
ещё и потому, что клеточная мембрана мало проницаема
для
этих
соединений,
т.е.
клетка
удерживает
моносахариды благодаря тому, что они находятся в
фосфорилированной форме.
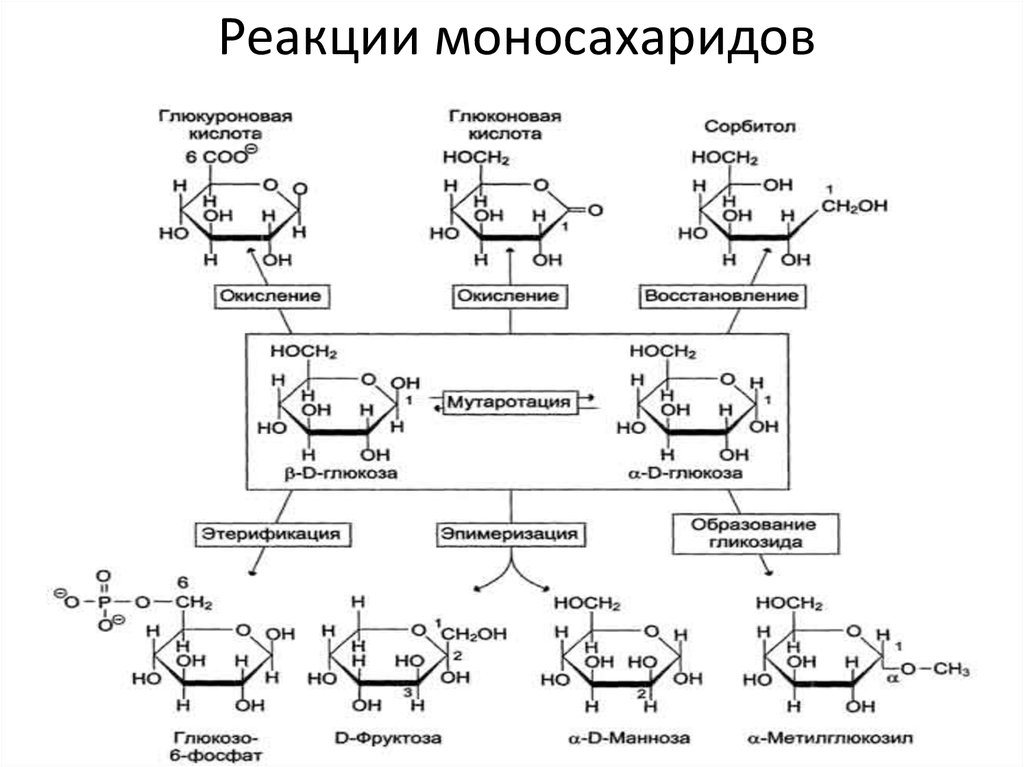
16. Реакции моносахаридов
• Окисление и восстановление. При окисленииконцевых групп глюкозы -СНО и -СН2ОН
образуются 3 различных производных. При
окислении
группы
-СНО
образуется
глюконовая
кислота.
Если
окислению
подвергается концевая группа -СН2ОН,
образуется глюкуроновая кислота. А если
окисляются обе концевые группы, то
образуется сахарная кислота, содержащая 2
карбоксильные
группы.
Восстановление
первого углерода приводит к образованию
сахароспирта - сорбитола.
17. Реакции моносахаридов
18. Олигосахариды
• Олигосахариды содержат несколько (от двух додесяти) остатков моносахаридов, соединённых
гликозидной связью. Дисахариды - наиболее
распространённые
олигомерные
углеводы,
встречающиеся в свободной форме, т.е. не
связанной с другими соединениями. По химической
природе
дисахариды
представляют
собой
гликозиды, которые содержат 2 моносахарида,
соединённые гликозидной связью в α- или βконфигурации. В пище содержатся в основном
такие дисахариды, как сахароза, лактоза и мальтоза
(знать формулы!).
19. Дисахариды пищи
Сахароза - дисахарид, состоящий из α-D-глюкозы и β-D-фруктозы, соединённых α,β-1,2гликозидной связью. В сахарозе обе аномерные ОН-группы остатков глюкозы и фруктозыучаствуют в образовании гликозидной связи. Следовательно, сахароза не относится к
восстанавливающим сахарам. Сахароза - растворимый дисахарид со сладким вкусом.
Источником сахарозы служат растения, особенно сахарная свёкла, сахарный тростник.
Лактоза - молочный сахар; важнейший дисахарид молока млекопитающих. В коровьем
молоке содержится до 5% лактозы, в женском молоке - до 8%. В лактозе аномерная ОНгруппа первого углеродного атома остатка D-галактозы связана β-гликозидной связью с
четвёртым углеродным атомом D-глюкозы (β-1,4-связь). Поскольку аномерный атом
углерода остатка глюкозы не участвует в образовании гликозидной связи,
следовательно, лактоза относится к восстанавливающим сахарам.
Мальтоза поступает с продуктами, содержащими частично гидролизованный крахмал,
например, солод, пиво. Мальтоза также образуется при расщеплении крахмала в
кишечнике. Мальтоза состоит из двух остатков D-глюкозы, соединённых α-1,4гликозидной связью.
20. Полисахариды (классификация)
Структурные различия между полисахаридамиопределяются:
• строением моносахаридов, составляющих цепь.
В зависимости от строения остатков моносахаридов
полисахариды
можно
разделить
на гомополисахариды (все мономеры идентичны)
и гетерополисахариды (мономеры различны). Оба
типа полисахаридов могут иметь как линейное
расположение мономеров, так и разветвлённое;
• типом гликозидных связей, соединяющих
мономеры в цепи;
• последовательностью остатков моносахаридов в
цепи.
21.
В зависимости от выполняемых ими функцийполисахариды можно разделить на 3 основные
группы:
• резервные полисахариды, выполняющие
энергетическую функцию. Эти полисахариды служат
источником глюкозы, используемым организмом по
мере необходимости. Резервная функция этих
углеводов обеспечивается их полимерной природой.
Полисахариды менее растворимы, чем моносахариды,
следовательно они не влияют на осмотическое
давление и поэтому могут накапливаться в клетке,
например, крахмал - в клетках растений, гликоген - в
клетках животных;
• структурные полисахариды, обеспечивающие
клеткам и органам механическую прочность;
• полисахариды, входящие в состав межклеточного
матрикса, принимают участие в образовании тканей, а
также в пролиферации и дифференцировке клеток.
22. Полисахариды пищи (крахмал, целлюлоза, гликоген)
• В пище человека в основном содержатсяполисахариды растительного происхождения крахмал, целлюлоза (знать формулы!). В меньшем
количестве поступает полисахарид животных гликоген.
• Крахмал - это резервный полисахарид растений,
содержащийся в наибольшем количестве в зёрнах
злаков (пшеница, кукуруза, рис и др.), а также
луковицах, стеблях и клубнях растений (в картофеле
примерно 65%). Крахмал - разветвлённый
полисахарид, состоящий из остатков глюкозы
(гомогликан). Он находится в клетках растений в
виде гранул, практически нерастворим в воде.
23. Крахмал
• Крахмал состоит из амилозы и амилопектина. Амилоза неразветвлённый полисахарид, включающий 200-300остатков глюкозы, связанных α-1,4-гликозидной связью.
Благодаря
α-конфигурации
глюкозного
остатка,
полисахаридная цепь имеет конформацию спирали.
Синяя окраска при добавлении йода к раствору
крахмала обусловлена наличием такой спирали.
Амилопектин имеет разветвлённую структуру. В местах
ветвления остатки глюкозы соединены α-1,6гликозидными связями. Линейные участки содержат
примерно 20-25 остатков глюкозы. При этом
формируется древовидная структура, в которой имеется
лишь одна аномерная ОН-группа. Крахмал высокомолекулярное соединение, включающее сотни
тысяч остатков глюкозы. Его молекулярная масса
составляет порядка 105-108 Д.
24.
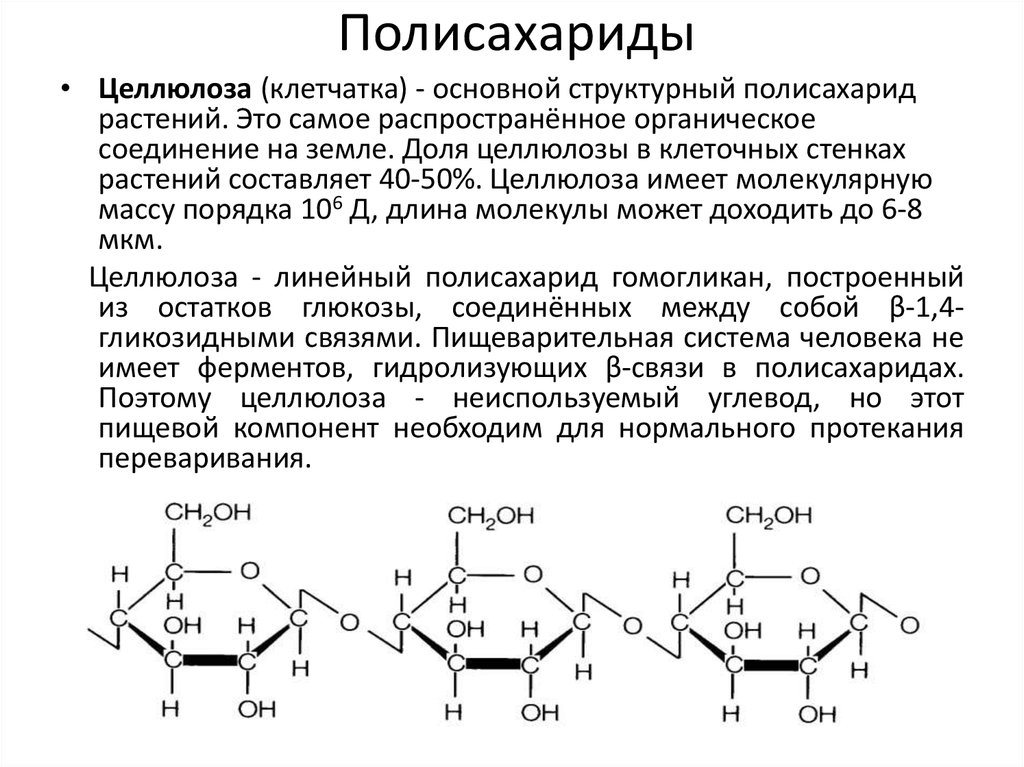
25. Полисахариды
• Целлюлоза (клетчатка) - основной структурный полисахаридрастений. Это самое распространённое органическое
соединение на земле. Доля целлюлозы в клеточных стенках
растений составляет 40-50%. Целлюлоза имеет молекулярную
массу порядка 106 Д, длина молекулы может доходить до 6-8
мкм.
Целлюлоза - линейный полисахарид гомогликан, построенный
из остатков глюкозы, соединённых между собой β-1,4гликозидными связями. Пищеварительная система человека не
имеет ферментов, гидролизующих β-связи в полисахаридах.
Поэтому целлюлоза - неиспользуемый углевод, но этот
пищевой компонент необходим для нормального протекания
переваривания.
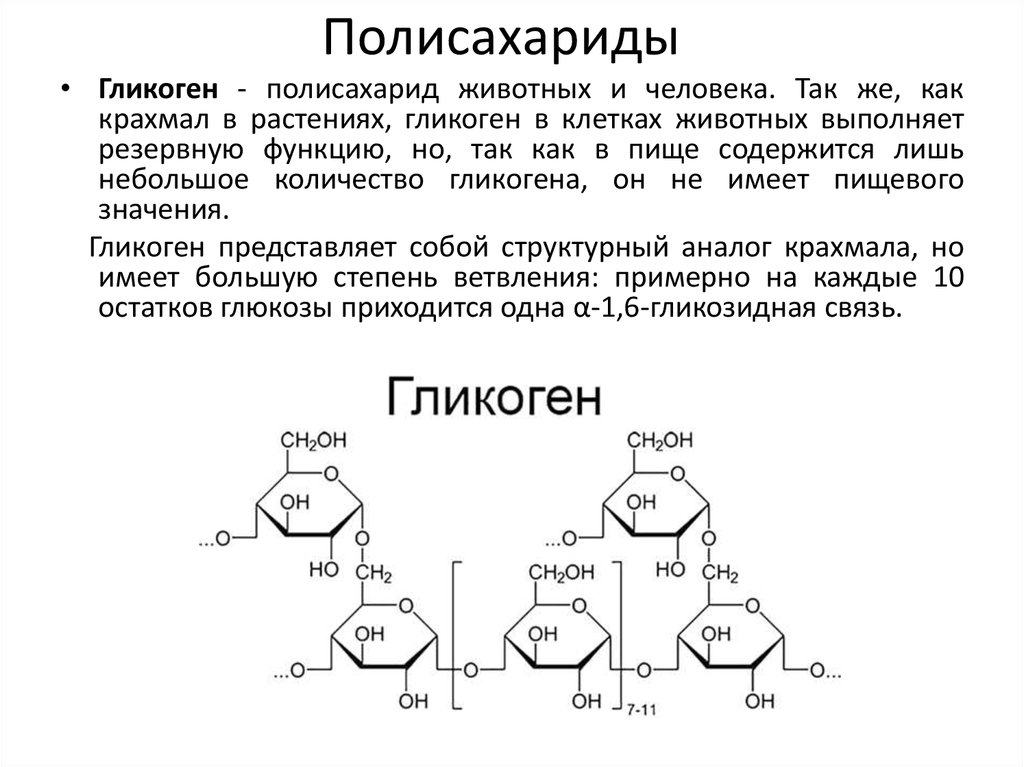
26. Полисахариды
• Гликоген - полисахарид животных и человека. Так же, каккрахмал в растениях, гликоген в клетках животных выполняет
резервную функцию, но, так как в пище содержится лишь
небольшое количество гликогена, он не имеет пищевого
значения.
Гликоген представляет собой структурный аналог крахмала, но
имеет большую степень ветвления: примерно на каждые 10
остатков глюкозы приходится одна α-1,6-гликозидная связь.
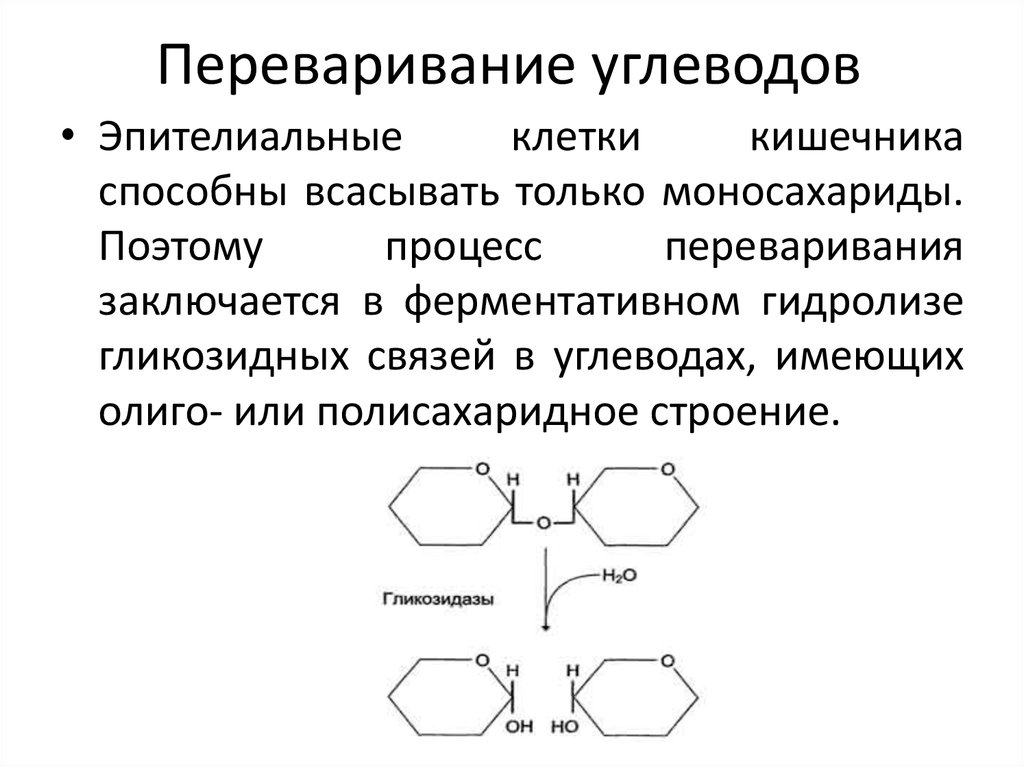
27. Переваривание углеводов
• Эпителиальныеклетки
кишечника
способны всасывать только моносахариды.
Поэтому
процесс
переваривания
заключается в ферментативном гидролизе
гликозидных связей в углеводах, имеющих
олиго- или полисахаридное строение.
28. Переваривание углеводов
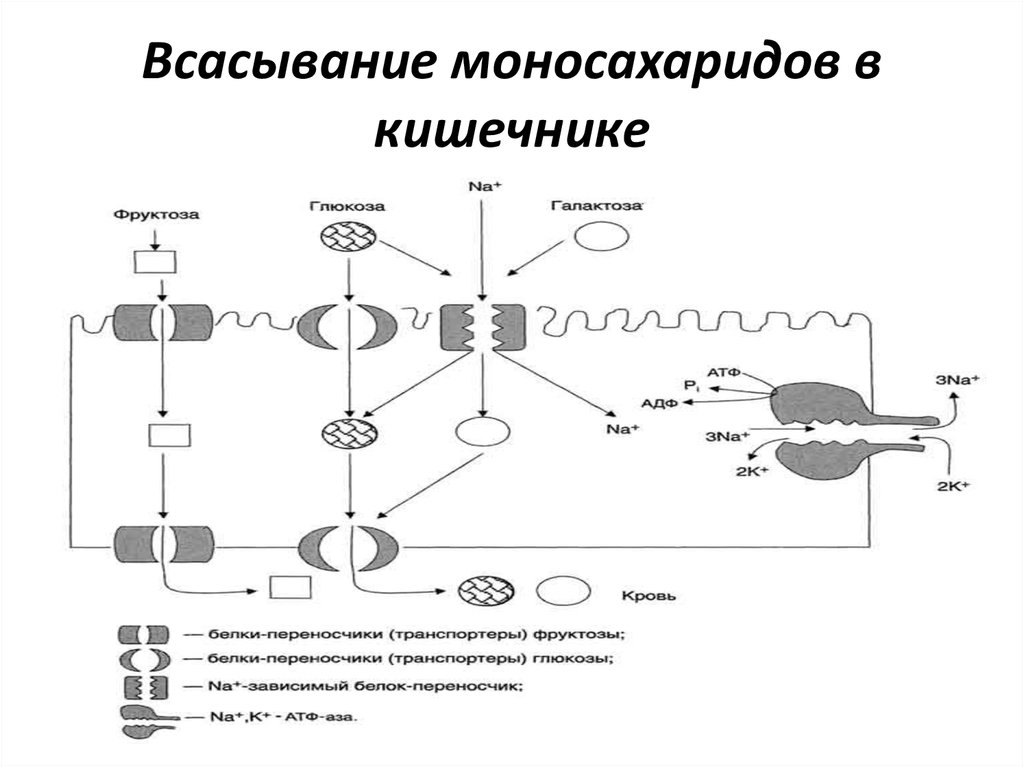
29. Всасывание моносахаридов в кишечнике
• Моносахариды, образовавшиеся в результате переваривания,всасываются эпителиальными клетками тощей и подвздошной кишок
с помощью специальных механизмов транспорта через мембраны
этих клеток.
Всасывание моносахаридов из кишечника происходит путём
облегчённой диффузии с помощью специальных белковпереносчиков (транспортёров). Кроме того, глюкоза и галактоза
транспортируются в энтероцит путём вторично-активного транспорта,
зависимого от градиента концентрации ионов натрия. Белкитранспортёры, зависимые от градиента Na+, обеспечивают
всасывание глюкозы из просвета кишечника в энтероцит против
градиента концентрации. Концентрация Na+, необходимая для этого
транспорта, обеспечивается Nа+,К+-АТФ-азой, которая работает как
насос, откачивая из клетки Na+ в обмен на К+. В отличие от глюкозы,
фруктоза транспортируется системой, не зависйщей от градиента
натрия.
30. Всасывание моносахаридов в кишечнике
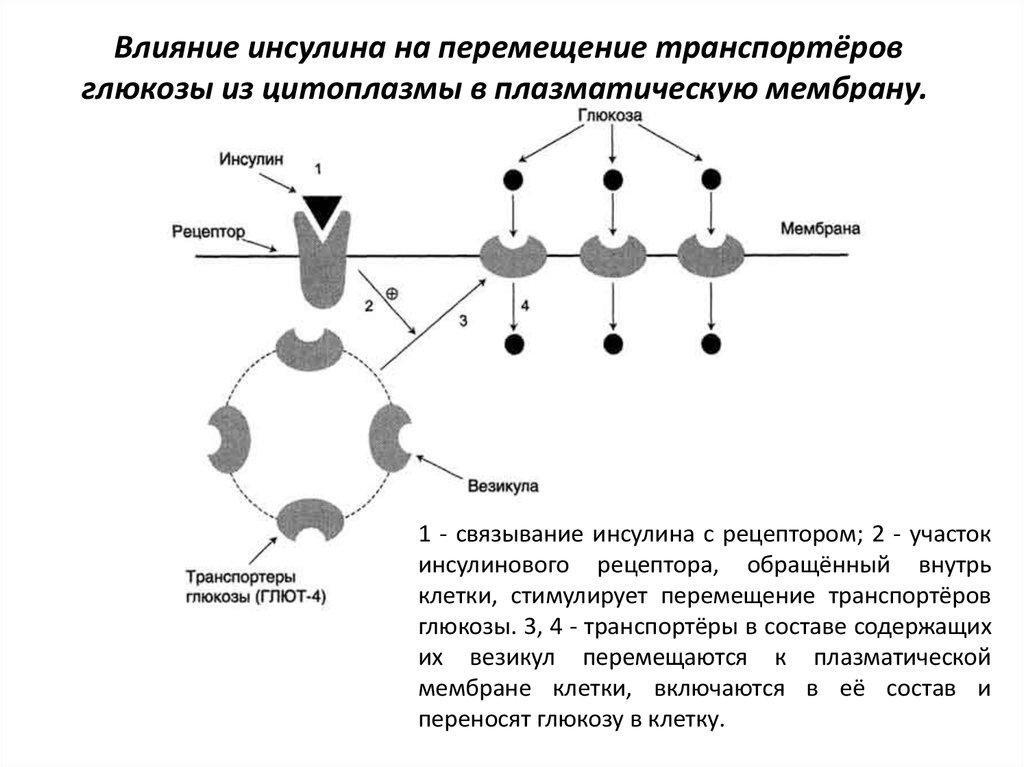
31. Влияние инсулина на перемещение транспортёров глюкозы из цитоплазмы в плазматическую мембрану.
Влияние инсулина на перемещение транспортёровглюкозы из цитоплазмы в плазматическую мембрану.
1 - связывание инсулина с рецептором; 2 - участок
инсулинового рецептора, обращённый внутрь
клетки, стимулирует перемещение транспортёров
глюкозы. 3, 4 - транспортёры в составе содержащих
их везикул перемещаются к плазматической
мембране клетки, включаются в её состав и
переносят глюкозу в клетку.
32. Метаболизм углеводов
• После всасывания в кишечнике моносахариды поступают вворотную вену и далее преимущественно в печень. Поскольку
в составе основных углеводов пищи преобладает глюкоза,
её можно считать основным продуктом переваривания
углеводов. Другие моносахариды, поступающие из кишечника
в процессе метаболизма, могут превращаться в глюкозу или
продукты её метаболизма. Часть глюкозы в печени
депонируется в виде гликогена, а другая часть через общий
кровоток доставляется и используется разными тканями и
органами. При нормальном рационе питания концентрация
глюкозы в крови поддерживается на уровне -3,3-5,5 ммоль/л
(60-100 мг/дл). А в период пищеварения её концентрация
может повышаться примерно до 150 мг/дл (8 ммоль/л).
33.
34. Фосфорилирование глюкозы
• В дальнейших превращениях в клетках глюкоза и другиемоносахариды участвуют только в виде фосфорных эфиров.
Фосфорилирование
свободных
моносахаридов
обязательная реакция на пути их использования, она
приводит к образованию более реакционно-способных
соединений и поэтому может рассматриваться как
реакция активации.
• Глюкоза, поступающая в клетки органов и тканей, сразу же
подвергается фосфорилированию с использованием АТФ. Эту
реакцию во многих тканях катализирует фермент
гексокиназа, а в печени и поджелудочной железе - фермент
глюкокиназа. Фосфорилирование глюкозы - практически
необратимая реакция, так как она протекает с использованием
значительного количества энергии. Образование глюкозо-6фосфата в клетке - своеобразная "ловушка" для глюкозы, так
как мембрана клетки непроницаема для фосфорилированной
глюкозы (нет соответствующих транспортных белков). Кроме
того, Фосфорилирование уменьшает концентрацию свободной
глюкозы в цитоплазме. В результате создаются благоприятные
условия для облегчённой диффузии глюкозы в клетки из крови.
35. Фосфорилирование глюкозы
• Глюкокиназа. Фосфорилирование глюкозы в гепатоцитах в периодпищеварения обеспечивается свойствами глюкокиназы, которая
имеет высокое значение Кm - 10 ммоль/л. В этот период концентрация
глюкозы в воротной вене больше, чем в других отделах кровяного
русла и может превышать 10 ммоль/л, а следовательно, активность
глюкокиназы в гепатоцитах повышается.
• Гексокиназа отличается от глюкокиназы высоким сродством к глюкозе
(Кm <0,1 ммоль/л). Следовательно, этот фермент, в отличие от
глюкокиназы, активен при низкой концентрации глюкозы в крови, что
характерно для постабсорбтивного состояния. Печень в этот период
поглощает гораздо меньше глюкозы, так как скорость её
внутриклеточного фосфорилирования глюкокиназой резко снижается.
Тогда как потребление глюкозы мозгом, эритроцитами и другими
тканями обеспечивается активной в этих условиях гексокиназой.
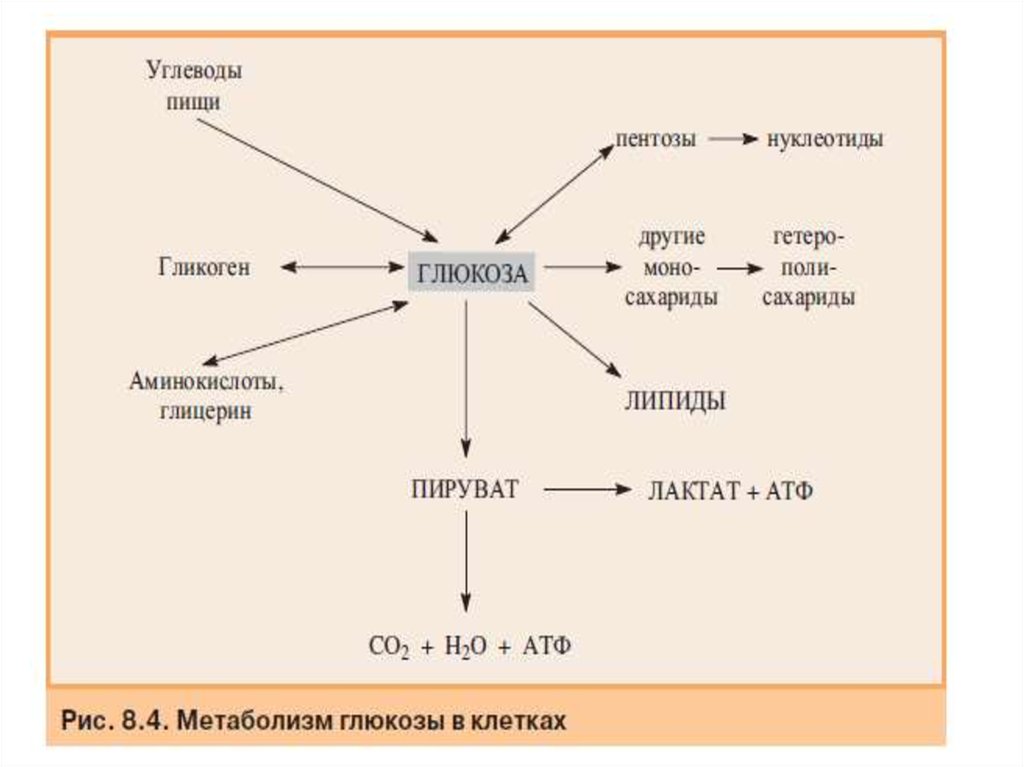
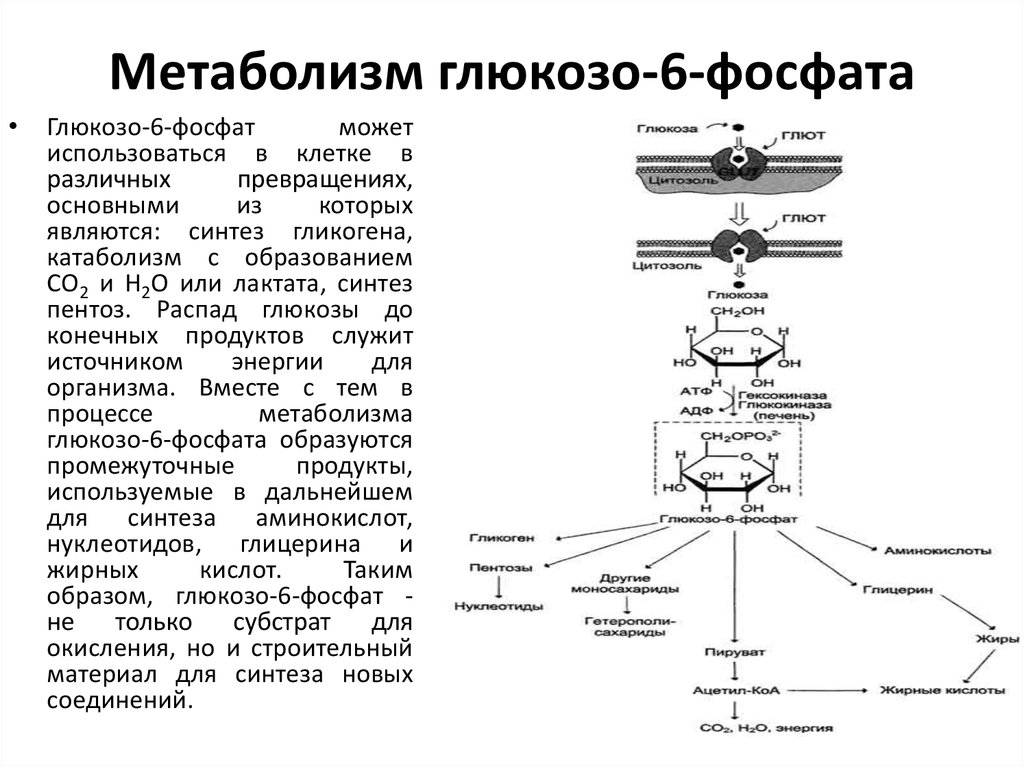
36. Метаболизм глюкозо-6-фосфата
Глюкозо-6-фосфат
может
использоваться в клетке в
различных
превращениях,
основными
из
которых
являются: синтез гликогена,
катаболизм с образованием
СО2 и Н2О или лактата, синтез
пентоз. Распад глюкозы до
конечных продуктов служит
источником
энергии
для
организма. Вместе с тем в
процессе
метаболизма
глюкозо-6-фосфата образуются
промежуточные
продукты,
используемые в дальнейшем
для синтеза аминокислот,
нуклеотидов, глицерина и
жирных
кислот.
Таким
образом, глюкозо-6-фосфат не
только
субстрат для
окисления, но и строительный
материал для синтеза новых
соединений.
37. Дефосфорилирование глюкозо-6-фосфата
Дефосфорилирование глюкозо-6фосфата• Превращение глюкозо-6-фосфата в глюкозу возможно в
печени, почках и клетках эпителия кишечника. В клетках
этих органов имеется фермент глюкозо-6-фосфатаза,
катализирующая отщепление фосфатной группы
гидролитическим путём:
Глюкозо-6-фосфат +Н2О → Глюкоза + Н3РО4
• Образовавшаяся
свободная
глюкоза
способна
диффундировать из этих органов в кровь. В других
органах и тканях глюкозо-6-фосфатазы нет, и поэтому
дефосфорилирование глюкозо-6-фосфата невозможно.
Пример подобного необратимого проникновения
глюкозы в клетку - мышцы, где глюкозо-6-фосфат может
использоваться только в метаболизме этой клетки.
38. Катаболизм глюкозы
Катаболизм глюкозы - основной поставщик энергии для
процессов жизнедеятельности организма.
Основные пути катаболизма глюкозы
Окисление глюкозы до СО2 и Н2О (аэробный
распад). Аэробный распад глюкозы можно выразить
суммарным уравнением:
С6Н12О6 + 6 О2 → 6 СО2 + Н2О + 2820 кДж/моль.
Этот процесс включает несколько стадий .
1. Аэробный гликолиз - процесс окисления глюкозы с
образованием двух молекул пирувата;
2. Общий путь катаболизма, включающий превращение
пирувата в ацетил-КоА и его дальнейшее окисление в
цитратом цикле;
3. ЦПЭ на кислород, сопряжённая с реакциями
дегидрирования, происходящими в процессе распада
глюкозы.
В определённых ситуациях обеспечение кислородом
тканей может не соответствовать их потребностям.
Например, на начальных стадиях интенсивной мышечной
работы при стрессе сердечные сокращения могут не
достигать нужной частоты, а потребности мышц в
кислороде для аэробного распада глюкозы велики. В
подобных случаях включается процесс, который протекает
без кислорода и заканчивается образованием лактата из
пировиноградной кислоты. Этот процесс называют
анаэробным распадом, или анаэробным гликолизом.
Анаэробный
распад
глюкозы
энергетически
малоэффективен, но именно этот процесс может стать
единственным источником энергии для мышечной клетки в
описанной ситуации. В даньнейшем, когда снабжение
мышц кислородом будет достаточным в результате
перехода сердца на ускоренный ритм, анаэробный распад
переключается на аэробный. Пути катаболизма глюкозы и
их энергетический эффект показаны на рис.
39. Аэробный гликолиз
Аэробным гликолизом называют процесс окисления глюкозыдо пировиноградной кислоты, протекающий в присутствии
кислорода. Все ферменты, катализирующие реакции этого
процесса, локализованы в цитозоле клетки.
В аэробном гликолизе можно выделить 2 этапа.
• Подготовительный
этап,
в
ходе
которого
глюкоза
фосфорилируется и расщепляется на две молекулы
фосфотриоз. Эта серия реакций протекает с использованием 2
молекул АТФ.
• Этап, сопряжённый с синтезом АТФ. В результате этой серии
реакций фосфотриозы превращаются в пируват. Энергия,
высвобождающаяся на этом этапе, используется для синтеза 10
моль АТФ.
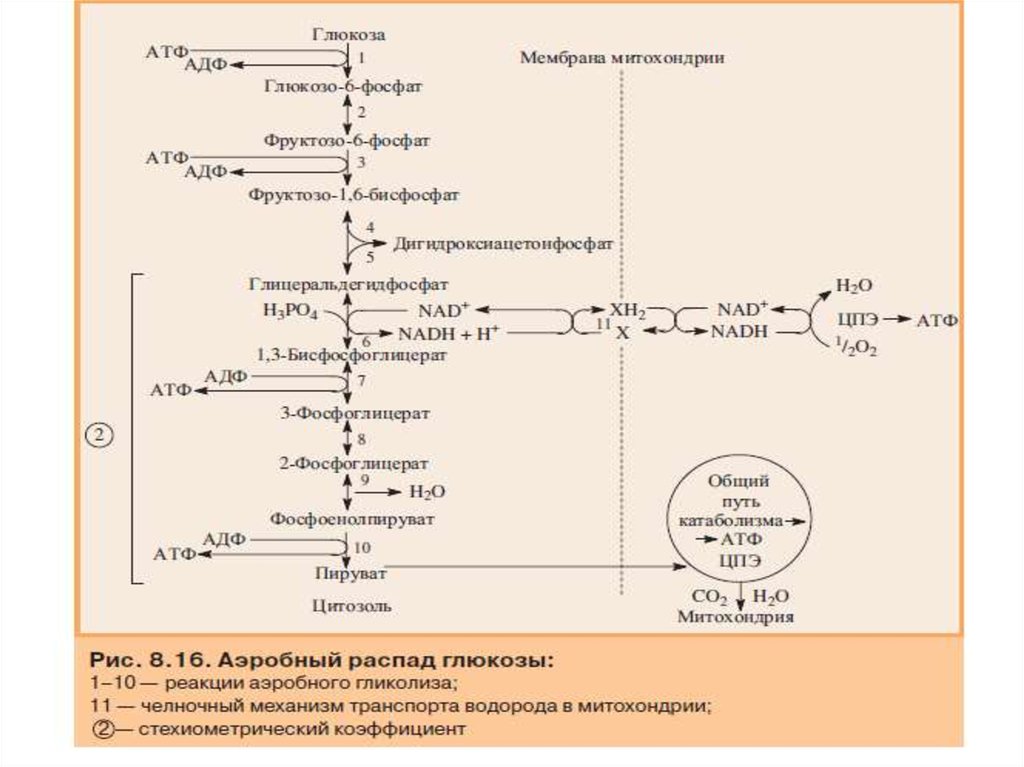
40. Реакции аэробного распада глюкозы
Гликолитическое расщепление глюкозы начинается с фосфорилипования глюкозы с
использованием одной молекулы АТФ. Далее следует:
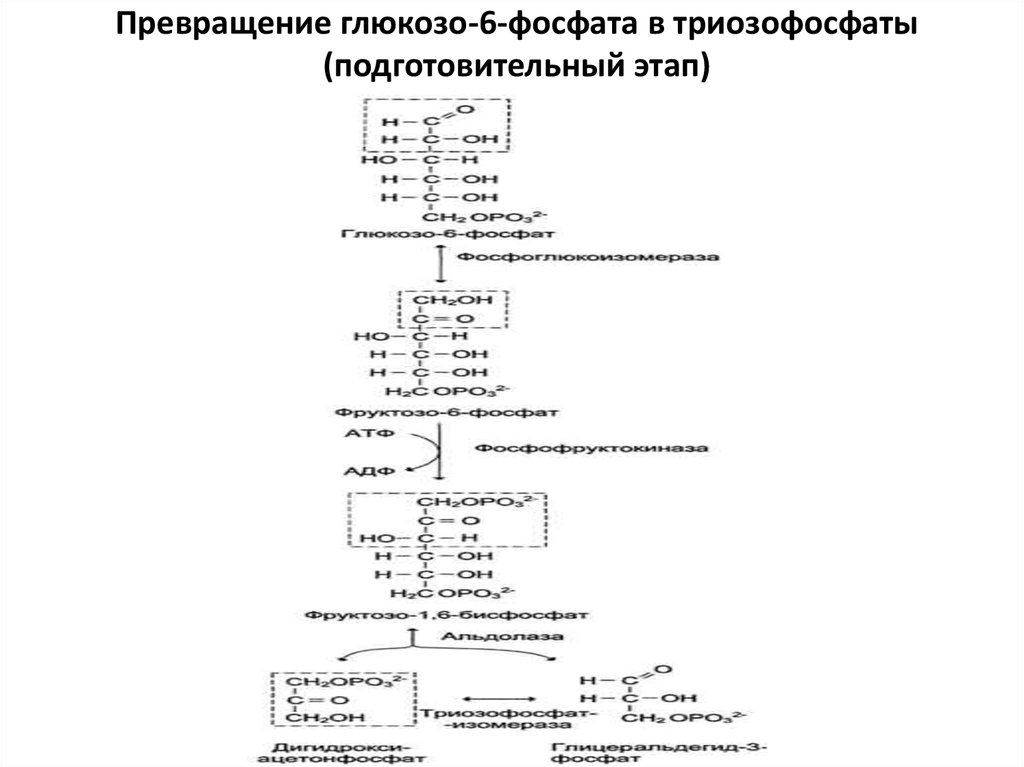
1. Превращение глюкозо-6-фосфата в 2 молекулы глицеральдегид-3-фосфата
(подготовительный этап)
Глюкозо-6-фосфат, образованный в результате фосфорилирования глюкозы с
участием АТФ, в ходе следующей реакции превращается в фруктозо-6-фосфат. Эта
обратимая реакция изомеризации протекает под действием фермента
глюкозофосфатизомеразы.
Затем следует ещё одна реакция фосфорилирования с использованием фосфатного
остатка
и
энергии
АТФ.
В
ходе
этой
реакции,
катализируемой
фосфофруктокиназой, фруктозо-6-фосфат превращается в фруктозо-1,6-бисфосфат.
Данная реакция, так же, как гексокиназная, практически необратима, и, кроме того,
она наиболее медленная из всех реакций гликолиза. Реакция, катализируемая
фосфофруктокиназой, определяет скорость всего гликолиза, поэтому, регулируя
активность фосфофруктокиназы, можно изменять скорость катаболизма глюкозы.
Фруктозо-1,6-бисфосфат далее расщепляется на 2 триозофосфата: глицеральдегид3-фосфат
и
дигидроксиацетонфосфат.
Реакцию
катализирует
фермент фруктозобисфосфатальдолаза, или просто альдолаза. Этот фермент
катализирует как реакцию альдольного расщепления, так и альдольной
конденсации, т.е. обратимую реакцию. Продукты реакции альдольного
расщепления - изомеры. В последующих реакциях гликолиза используется только
глицеральдегид-3-фосфат, поэтому дигидроксиацетонфосфат превращается с
участием фермента триозофосфатизомеразы в глицероальдегид-3-фосфат .
В описанной серии реакций дважды происходит фосфорилирование с
использованием АТФ. Однако расходование двух молекул АТФ (на одну молекулу
глюкозы) далее будет компенсировано синтезом большего количества АТФ.
41. Превращение глюкозо-6-фосфата в триозофосфаты (подготовительный этап)
42.
• 2. Эта часть аэробного гликолиза включает реакции,связанные с синтезом АТФ. Наиболее сложной в данной серии
реакций является реакция превращения глицеральдегид-3фосфата в 1,3-бисфосфоглицерат. Это превращение - первая
реакция
окисления
в
ходе
гликолиза.
Реакцию
катализирует глицеральдегид-3-фосфатдегидрогеназа, которая
является NAD-зависимым ферментом. Значение данной реакции
заключается не только в том, что образуется восстановленный
кофермент, окисление которого в дыхательной цепи сопряжено с
синтезом АТФ, но также и в том, что свободная энергия
окисления концентрируется в макроэргической связи продукта
реакции. Окисление глицеральдегид-3-фосфата приводит к
восстановлению NAD и образованию с участием Н3РО4
высокоэнергетической
ангидридной
связи
в
1,3бисфосфоглицерате в положении 1. В следующей реакции
высокоэнергетический фосфат передаётся на АДФ с
образованием АТФ. Фермент, катализирующий это превращение,
назван по обратной реакции фосфоглицераткиназой (киназы
называются по субстрату, находящемуся в уравнении реакции по
одну сторону с АТФ).
• Образование АТФ описанным способом не связано с
дыхательной цепью, и его называют субстратным
фосфорилированием АДФ. Образованный 3-фосфоглицерат уже
не содержит макроэргической связи.
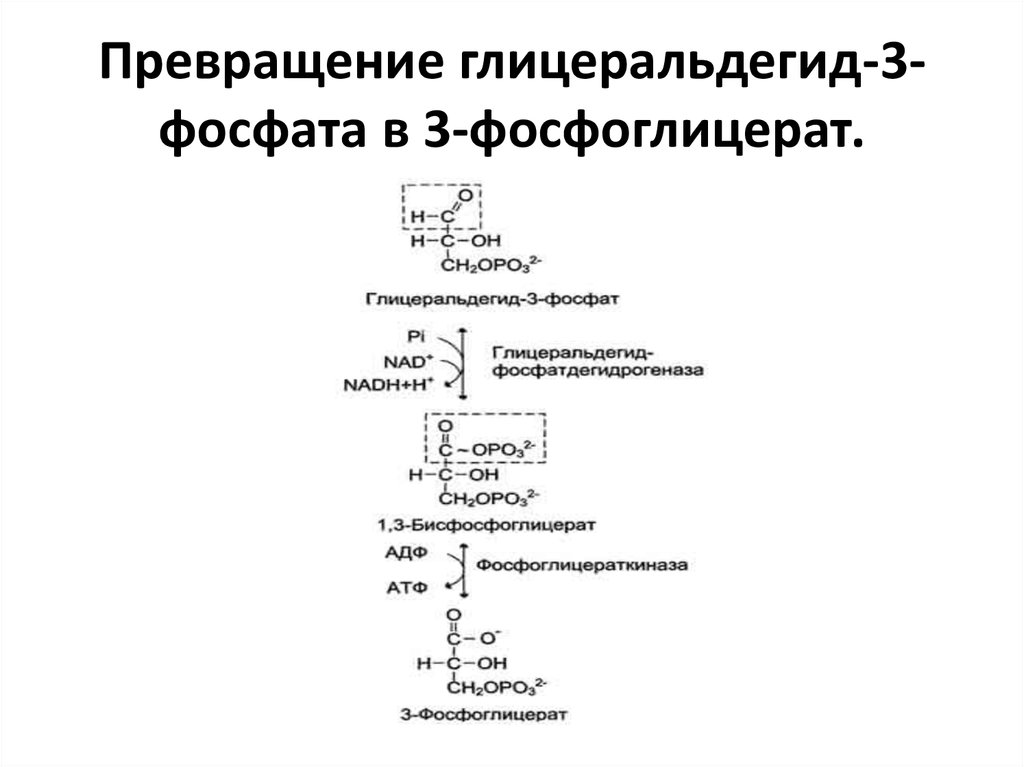
43. Превращение глицеральдегид-3-фосфата в 3-фосфоглицерат.
Превращение глицеральдегид-3фосфата в 3-фосфоглицерат.44.
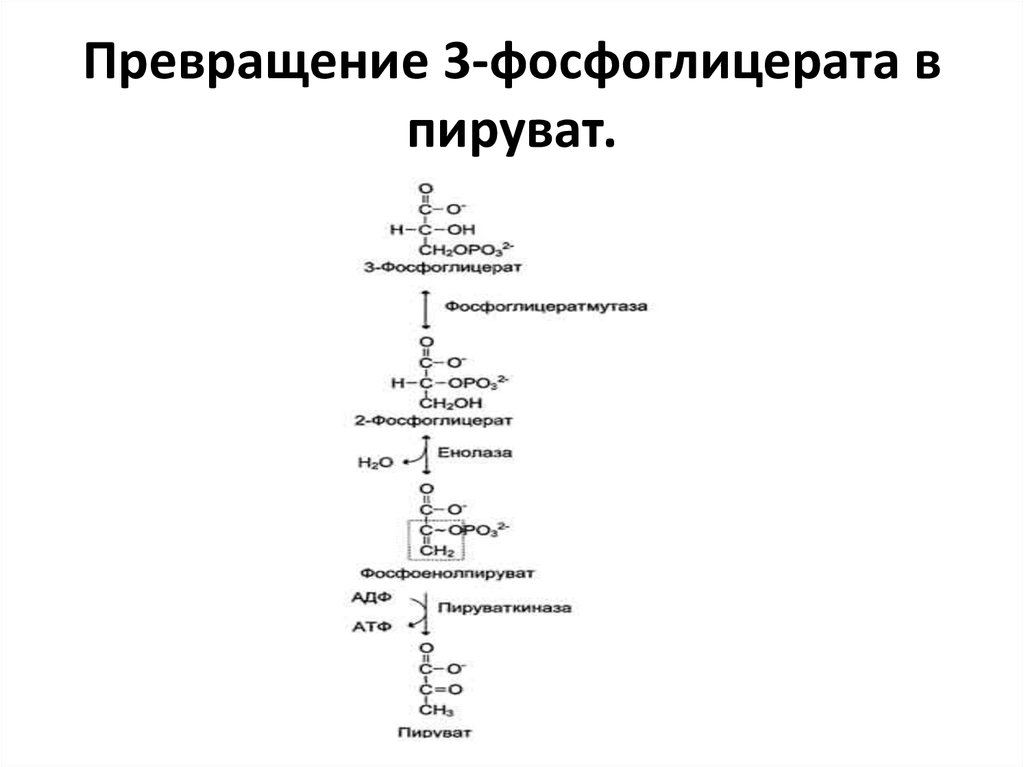
• В следующих реакциях происходят внутримолекулярныеперестройки, смысл которых сводится к тому, что
низкоэнергетический фосфоэфир переходит в соединение,
содержащее
высокоэнергетический
фосфат.
Внутримолекулярные преобразования заключаются в переносе
фосфатного остатка из положения 3 в фосфоглицерате в
положение
2
(фосфоглицератмутаза).
Затем
от
образовавшегося 2-фосфоглицерата отщепляется молекула
воды
при
участии
фермента
енолазы.
Название
дегидратирующего фермента дано по обратной реакции. В
результате реакции образуется замещённый енол фосфоенолпируват. Образованный фосфоенолпируват макроэргическое соединение, фосфатная группа которого
переносится в следующей реакции на АДФ при участии
пируваткиназы (фермент также назван по обратной реакции,
в которой происходит фосфорилирование пирувата, хотя
подобная реакция в таком виде не имеет места).
• Превращение фосфоенолпирувата в пируват - необратимая
реакция. Это вторая в ходе гликолиза реакция
субстратного фосфорилирования. Образующаяся енольная
форма пирувата затем неферментативно переходит в более
термодинамически стабильную кетоформу.
45. Превращение 3-фосфоглицерата в пируват.
46. Баланс АТФ при аэробном гликолизе и распаде глюкозы до СО2 и Н2О
Баланс АТФ при аэробном гликолизеи распаде глюкозы до СО2 и Н2О
NADH, образующийся при окислении глицеральдегид-3-фосфата в
аэробном гликолизе, подвергается окислению путём переноса атомов
водорода в митохондриальную дыхательную цепь.
Выход АТФ при аэробном гликолизе:
• На образование фруктозо-1,6-бисфосфата из одной молекулы глюкозы
требуется 2 молекулы АТФ. Реакции, связанные с синтезом АТФ,
происходят после распада глюкозы на 2 молекулы фосфотриозы, т.е.
на втором этапе гликолиза. На этом этапе происходят 2 реакции
субстратного фосфорилирования и синтезируются 2 молекулы АТФ
(реакции 7 и 10). Кроме того, одна молекула глицеральдегид-3фосфата дегидрируется (реакция 6), a NADH передаёт водород в
митохондриальную ЦПЭ, где синтезируется 3 молекулы АТФ путём
окислительного фосфорилирования. В данном случае количество АТФ
(3 или 2) зависит от типа челночной системы. Следовательно,
окисление до пирувата одной молекулы глицеральдегид-3-фосфата
сопряжено с синтезом 5 молекул АТФ. Учитывая, что из глюкозы
образуются 2 молекулы фосфотриозы, полученную величину нужно
умножить на 2 и затем вычесть 2 молекулы АТФ, затраченные на
первом этапе. Таким образом, выход АТФ при аэробном гликолизе
составляет (5×2) - 2 = 8 АТФ.
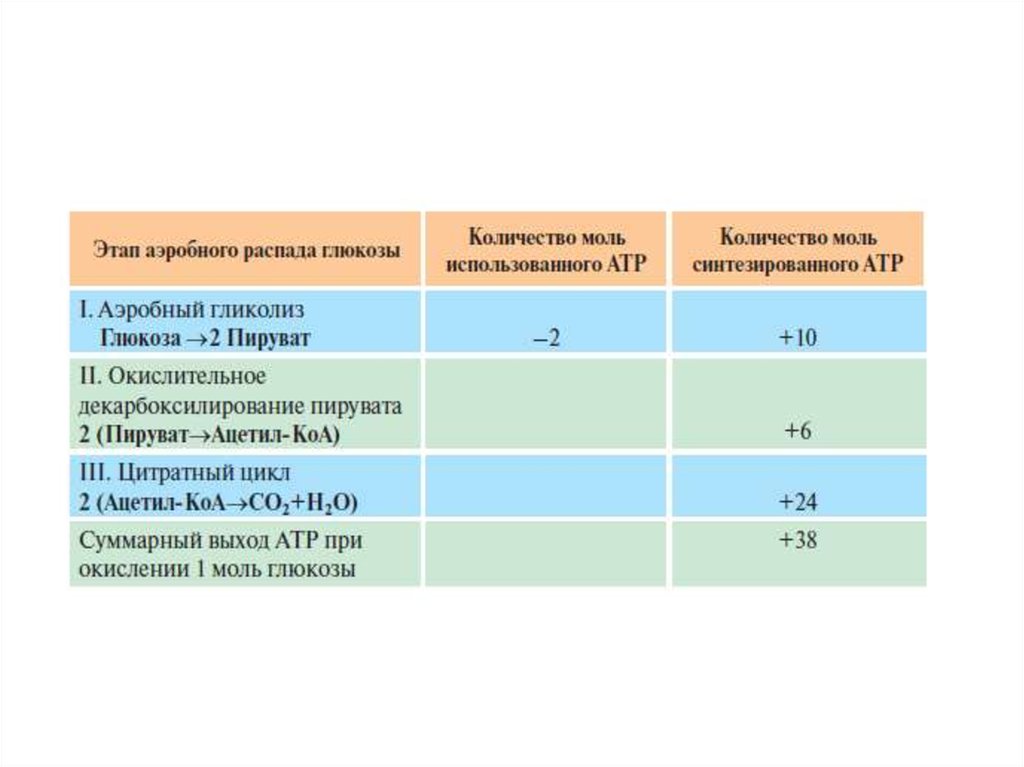
47. Выход АТФ при аэробном распаде глюкозы до конечных продуктов
• В результате гликолиза образуется пируват, который далее окисляетсядо СО2 и Н2О в ОПК, описанном в разделе 6. Теперь можно оценить
энергетическую эффективность гликолиза и ОПК, которые вместе
составляют процесс аэробного распада глюкозы до конечных
продуктов (табл. 7-4).
• Таким образом, выход АТФ при окислении 1 моль глюкозы до СО2 и
Н2О составляет 38 моль АТФ.
• В процессе аэробного распада глюкозы происходят 6 реакций
дегидрирования. Одна из них протекает в гликолизе и 5 в ОПК (см.
раздел 6). Субстраты для специфических NAD-зависимых
дегидрогеназ: глицеральдегид-3-фосфат, пируват, изоцитрат, αкетоглутарат, малат. Одна реакция дегидрирования в цитратном
цикле под действием сукцинатдегидрогеназы происходит с участием
кофермента FAD. Общее количество АТФ, синтезированное путём
окислительного фофорилирования, составляет 17 моль АТФ на 1 моль
глицеральдегидфосфата. К этому необходимо прибавить 3 моль АТФ,
синтезированных путём субстратного фосфорилирования (две
реакции в гликолизе и одна в цитратном цикле).
• Учитывая, что глюкоза распадается на 2 фос-фотриозы и что
стехиометрический коэффициент дальнейших превращений равен 2,
полученную величину надо умножить на 2, а из результата вычесть 2
моль АТФ, использованные на первом этапе гликолиза.
48.
49.
50. Анаэробный распад глюкозы (анаэробный гликолиз)
• Анаэробнымгликолизом
называют
процесс
расщепления глюкозы с обра-зованием в качестве
конечного продукта лактата. Этот процесс протекает без
использования кислорода и поэтому не зависит от
работы митохондриальной дыхательной цепи. АТФ
образуется за счет реакций субстратного фосфорилирования.
Суммарное уравнение процесса:
С6Н12О6 + 2Н3РО4 + 2АDР = 2С3Н6О3 + 2АТФ + 2Н2О.
51. Характеристика реакции анаэробного гликолиза
• При анаэробном гликолизе в цитозоле протекают все 10 реакций,идентичных аэробному гликолизу. Лишь 11 реакция, где происходит
восстановление
пирувата
цитозольным
NADН,
является
специфической для анаэробного гликолиза. Восстановление
пирувата в лактат катализирует лактатдегидрогеназа (реакция
обратимая и фермент назван по обрат- ной реакции). С помощью этой
реакции обеспечивается регенерация NAD+ из NADН без участия
митохондриальной дыхательной цепи в ситуациях, связанных с
недостаточным снабжением клеток кислородом. Роль акцептора
водо- рода от NADН (подобно кислороду в дыхательной цепи)
выполняет
пируват.
Таким
образом,
значение
реакции
восстановления пирувата заключается не в образовании лактата, а в
том, что данная цитозольная реакция обеспечивает регенерацию
NAD+. К тому же лактат не является конечным продуктом метаболизма, удаляемым из организма. Это вещество выводится в кровь
и утилизируется, превращаясь в печени в глюкозу, или при
доступности кислорода превращается в пируват, который вступает в
общий путь катаболизма, окисляясь до СО2 и Н2О.
52.
53. Баланс АТФ при анаэробном гликолизе
• Анаэробный гликолиз по сравнению с аэробным менееэффективен. В этом процессе катаболизм 1 моль глюкозы без
участия митохондриальной дыхательной цепи сопровождается
синтезом 2 моль АТФ и 2 моль лактата. АТФ образуется за счет
двух реакций субстратного фосфорилирования. Поскольку
глюкоза распадается на две фосфотриозы, то с учетом
стехиометрического коэффициента, равного 2, количество моль
синтезированного АТР равно 4. Учитывая 2 моль АТФ,
использованные на первом этапе гликолиза, получаем
конечный энергетический эффект процесса, равный 2 моль АТФ.
• Итак, 10 цитозольных ферментов, катализирующих превращение глюкозы в пируват вместе с лактатдегидрогеназой
обеспечивают в анаэробном гликолизе синтез 2 моль АТФ (на 1
моль глюкозы) без участия кислорода.
54. Значение катаболизма глюкозы
• Основноефизиологическое
назначение
катаболизма
глюкозы
заключается
в
использовании
энергии,
освобождающейся в этом процессе для синтеза АТФ.
• Кроме энергетической функции процесс катаболизма
глюкозы может выполнять и анаболические функции.
Метаболиты гликолиза используются для синтеза новых
соединений. Так, фруктозо-6-фосфат и глицеральдегид-3фосфат участвуют в образовании рибозо-5-фосфата —
структурного компонента нуклеотидов; 3-фосфоглицерат может
включаться в синтез аминокислот, таких, как серин, глицин,
цистеин. В печени и жировой ткани ацетил-КоА, образующийся
из пирувата, используется как субстрат при биосинтезе жирных
кислот, холестерина, а дигидроксиацетонфосфат как субстрат
для синтеза глицерол-3-фосфата .
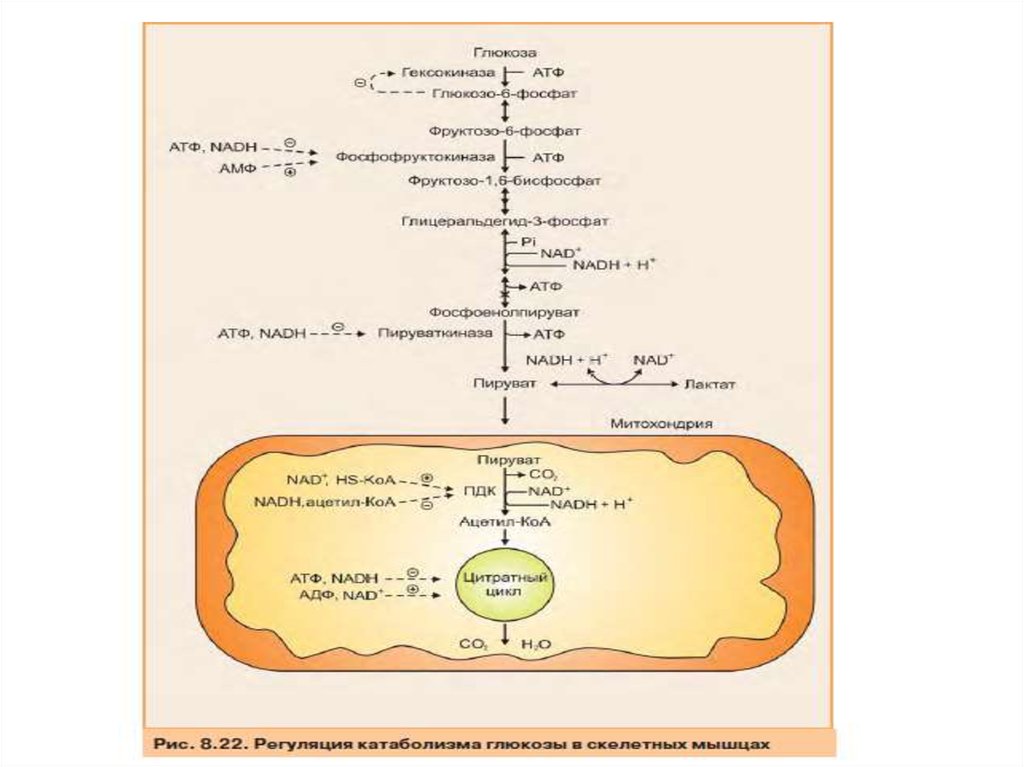
55. Регуляция катаболизма глюкозы
• Поскольку основное значение гликолиза состоит в синтезе АТФ, егоскорость должна коррелироваться с затратами энергии в организме.
Большинство реакций гликолиза обратимы, за исключением трех,
катализируемых
гексокиназой
(или
глюкокиназой),
фосфофруктокиназой и пируваткиназой. Регуляторные факторы,
изменяющие скорость гликолиза, а значит, и образование АТФ,
направлены на необратимые реакции. Показателем потребления АТФ
является накопление АДФ и АМФ. Последний образуется в реакции,
ката- лизируемой аденилаткиназой: 2АДФ ↔ АМФ + АТФ. Даже
небольшой расход АТФ ведет к заметному увеличению АМФ.
• Отношение уровня АТФ к АДФ и АМФ характеризует энергетический
статус клетки, а его составляющие служат аллостерическими
регуляторами скорости как общего пути катаболизма, так и гликолиза.
Существенное значение для регуляции гликолиза имеет изменение
актив- ности фосфофруктокиназы, потому что этот фермент, как
упоминалось ранее, катализирует наиболее медленную реакцию
процесса.
56.
• Фосфофруктокиназа активируется АМФ, но ингибируется АТФ. АМФ,связываясь с аллостерическим центром фосфофруктокиназы, увеличивает
сродство фермента к фруктозо-6-фосфату и повышает скорость его
фосфорилирования. Эффект АТФ на этот фермент — пример гомотропного
аллостеризма, поскольку АТФ может взаимодействовать как с
аллостерическим, так и с активным центром, в последнем случае как субстрат.
При физиологических значениях АТФ активный центр фосфофруктокиназы
всегда насыщен субстратами (в том числе АТФ). Повышение уровня АТФ
относительно АДФ снижает скорость реакции, поскольку АТФ в этих условиях
действует как ингибитор: связывается с аллостерическим центром фермента,
вызывает конформационные изменения и уменьшает сродство к его
субстратам. Изменение активности фосфофруктокиназы способствует
регуляции скорости фосфорилирования глюкозы гексокиназой. Снижение
активности фосфофруктокиназы при высоком уровне АТФ ведет к накоплению
как фруктозо-6-фосфата, так и глюкозо-6-фосфата, а последний ингибирует
гексокиназу. Гексокиназа во многих тканях (за исключением печени и β-клеток
поджелудочной железы) ингибируется глюкозо-6-фосфатом. При высоком
уровне АТФ снижается скорость цикла лимонной кислоты и дыхательной цепи.
В этих условиях процесс гликолиза также замедляется. Следует напомнить, что
аллостерическая регуляция ферментов ОПК и дыхательной цепи также связана
с изменением концентрации таких ключевых продуктов, как NADH, АТФ и
некоторых метаболитов. Так, NADH, накапливаясь в том случае, если не
успевает окислиться в дыхательной цепи, ингибирует некоторые
аллостерические ферменты цитратного цикла. Физиологическая роль
гликолиза в печени и жировой ткани несколько иная, чем в других тканях. В
печени и жировой ткани гликолиз в период пи- щеварения функционирует в
основном как источник субстратов для синтеза жиров.
57.
58. Значение гликолиза в печени для синтеза жиров
• Основным значением ускорения гликолиза в печени впериод
пищеварения
является
образование
дигидроксиацетонфосфата и ацетил-КоА — исходных
веществ для синтеза жира. В абсортивном периоде ПДК
находится в дефосфорилированной (активной) форме,
следовательно,
декарбоксилирование
пирувата
ускоряется. Образуемый ацетил-КоА используется в
основном двумя путями: для синтеза жирных кислот и в
цитратном цикле. В период пищеварения ускоряется образование ацетил-КоА и его использование для синтеза
жирных кислот. Необходимый для синтеза жира αглицерофосфат образуется в реакции восста- новления
из дигидроксиацетонфосфата .
59. Синтез глюкозы (глюконеогенез)
Некоторые ткани, например мозг, нуждаются в постоянном поступлении глюкозы. Когда поступление углеводов в составе пищи недостаточно, содержание
глюкозы в крови некоторое время поддерживается в пределах нормы за счет
расщепления гликогена в печени. Однако запасы гликогена в печени
невелики. Они значительно уменьшаются к 6–10 часам голодания и
практически полностью исчерпываются после суточного голодания. В этом
случае в печени начинается синтез глюкозы de novo — глюконеогенез.
Глюконеогенез — это процесс синтеза глюкозы из веществ неуглеводной
природы. Его основной функцией является поддержание уровня глюкозы в
крови в период длительного голодания и интенсивных физических нагрузок.
Процесс протекает в основном в печени и менее интенсивно в корковом
веществе почек, а также в слизистой оболочке кишечника. Эти ткани
могут обеспечивать синтез 80–100 г глюкозы в сутки. На долю мозга при
голодании приходится большая часть потребности организма в глюкозе. Это
объясняется тем, что клетки мозга не способны в отличие от других тканей
обеспечивать потребности в энергии за счет окисления жирных кислот.
60.
Первичными субстратами глюконеогенеза являются лактат,аминокислоты и глицерол. Включение этих субстратов в
глюконеогенез зависит от физиологического состояния
организма.
• Лактат является продуктом анаэробного гликолиза. Он
образуется при любых состояниях организма (эритроциты,
работающие мышцы). Таким образом, лактат используется в
глюконеогенезе постоянно.
• Глицерол высвобождается при гидролизе жиров в жировой
ткани в период голодания или при длительной физической
нагрузке.
• Аминокислоты образуются в результате распада мышечных
белков и включаются в глюконеогенез при длительном
голодании или продолжительной мышечной работе.
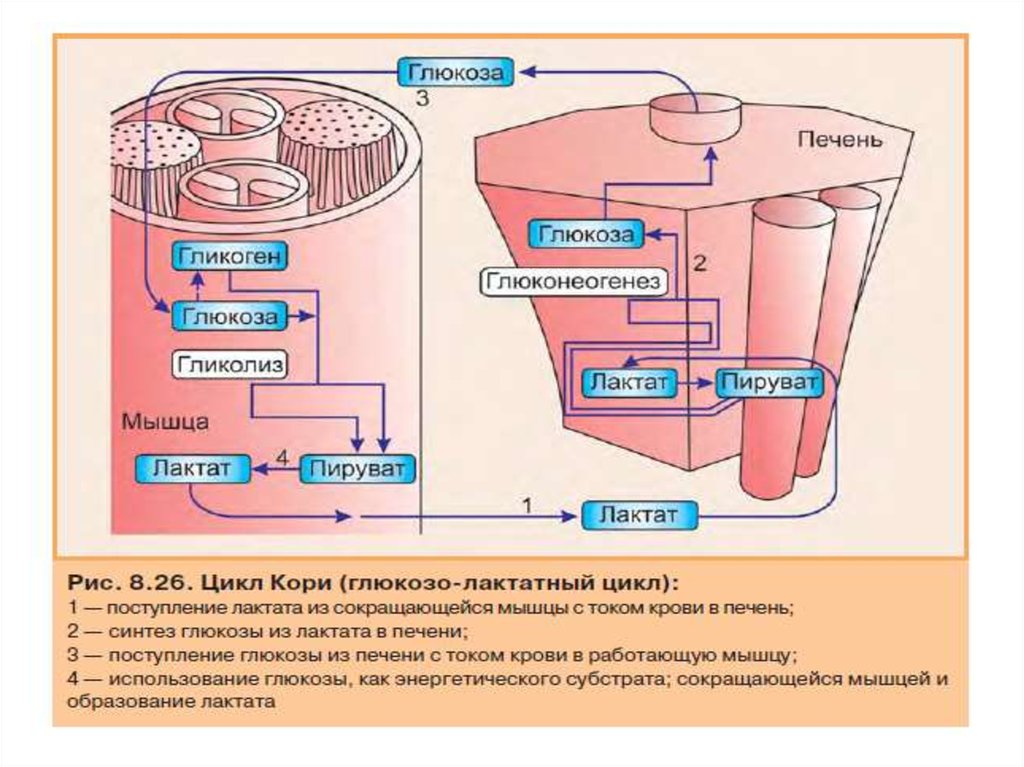
61. Синтез глюкозы из лактата (цикл Кори)
• Лактат, образовавшийся в интенсивно работающих мышцах илив клетках с преобладающим анаэробным способом
катаболизма глюкозы, поступает в кровь, а затем в печень. В
печени отношение NАDН/NАD+ ниже, чем в сокращающейся
мышце, поэтому лактатдегидрогеназная реакция протекает в
обратном направлении, т.е. в сторону образования пирувата из
лактата. Далее пируват включается в глюконеогенез, а
образовавшаяся глюкоза поступает в кровь и поглощается
скелетными мышцами. Эта последовательность событий
называется глюкозо-лактатным циклом, или циклом Кори.
Цикл Кори выполняет две важнейшие функции:
• 1 — обеспечивает утилизацию лактата, часть лактата
используется для синтеза глюкозы;
• 2 — предотвращает накопление лактата и как следствие этого
опасное снижение рН (лактоацидоз). Другая часть лактата
окисляется печенью до СО2 и Н2О. Энергия окисления может
использоваться для синтеза АТФ, необходимого для реакций
глюконеогенеза.
62.
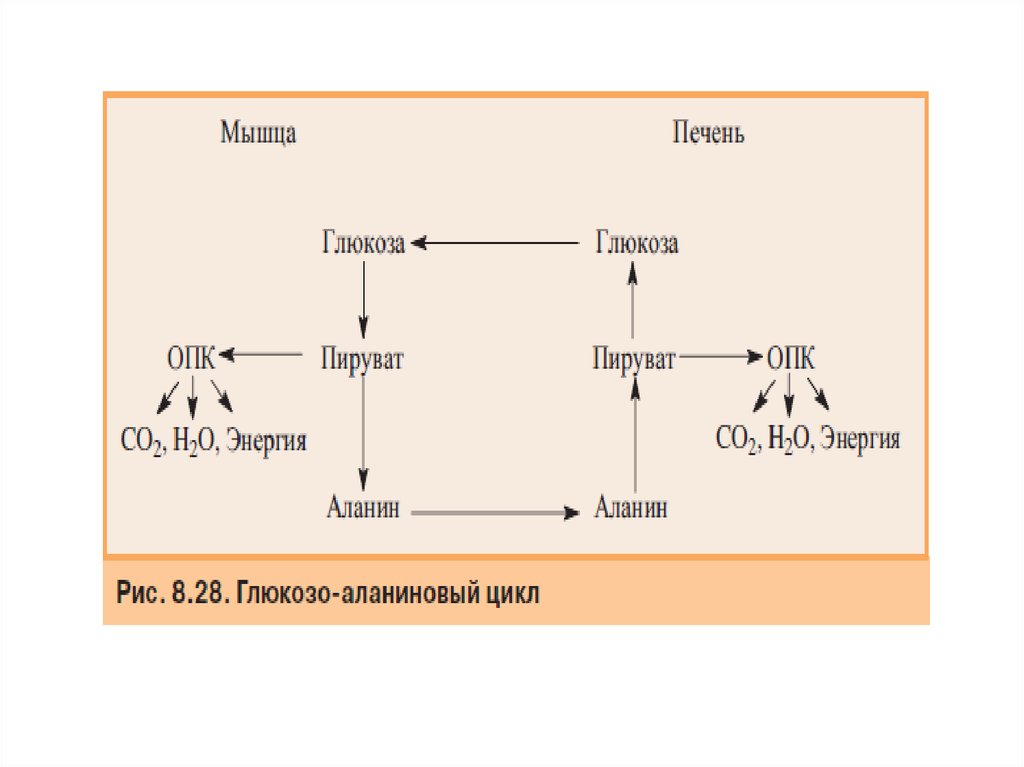
63. Синтез глюкозы из аминокислот
• Аминокислоты, которые при катаболизме превращаются в пируватили метаболиты цитратного цикла, могут рассматриваться как
потенциальные предшественники глюкозы и гликогена и носят
название гликогенных. Например, оксалоацетат, образующийся из
аспарагиновой кислоты, является промежуточным продуктом как
цитратного цикла, так и глюконеогенеза. Из всех аминокислот,
поступающих в печень, примерно 30% приходится на долю аланина.
Это объясняется тем, что при расщеплении мышечных белков
образуются аминокислоты, многие из которых превращаются в
пируват или сначала в оксалоацетат, а затем в пируват. Последний
превращается в аланин, приобретая аминогруппу от других
аминокислот. Аланин из мышц переносится кровью в печень, где
снова преобразуется в пируват, который частично окисляется и
частично включается в глюконеогенез. Следовательно, существует
следующая последовательность событий, называемая глюкозоаланиновым циклом . Весь цикл не приводит к увеличению
количества глюкозы в мышцах, но он решает проблемы транспорта
аминного азота из мышц в печень и предотвращает лактоацидоз.
64.
65. Синтез глюкозы из глицерола
• Глицерол могут использовать только те ткани,в которых имеется фермент глицеролкиназа,
например печень, почки. Этот АТФ-зависимый
фермент
катализирует
превращение
глицерола в α-глицерофосфат (глицерол-3фосфат). При включении глицерол-3-фосфата в
глюконеогенез происходит его дегидрирование NAD-зависимой дегидрогеназой с
образованием
дигидроксиацетонфосфата,
который далее превращается в глюкозу.
66.
67. Пентозофосфатный путь превращения глюкозы
• Пентозофосфатный путь (фосфоглюконатный) —альтернативный
путь
окисления
глюкозо-6фосфата. Пентозофосфатный путь состоит из двух
этапов (ча- стей): окислительного и неокислительного.
Пентозофосфатный путь обеспечивает клетки рибозой
для синтеза пурино- вых и пиримидиновых нуклеотидов
и гидрированным коферментом NADPH, который
используется
в
восстановительных
процессах.
Ферменты пентозофосфатного пути локализованы в
цитозоле. Наиболее активно пентозофосфатный путь
протекает в органах, где происходит синтез липидов, —
жировой ткани, печени, коре надпочечников, эритроцитах, молочной железе в период лактации,
семенниках.
68. Общий путь катаболизма. Энергетический обмен
Живые организмы находятся в постоянной и неразрывной связи с
окружающей средой. Эта связь осуществляется в процессе обмена веществ.
Обмен веществ включает 3 этапа: поступление веществ в организм,
метаболизм и выделение конечных продуктов из организма.
Поступление веществ в организм происходит в результате дыхания
(кислород) и питания. В ЖКТ продукты питания перевариваются
(расщепляются до простых веществ). При переваривании происходит
гидролиз полимеров (белков, полисахаридов и других сложных органических
веществ) до мономеров, всасывающихся в кровь и включающихся в
промежуточный обмен.
Промежуточный обмен (внутриклеточный метаболизм) включает 2 типа
реакций: катаболизм и анаболизм (рис. 6-1).
Катаболизм - процесс расщепления органических молекул до конечных
продуктов. Конечные продукты превращений органических веществ у
животных и человека - СО2, Н2О и мочевина. В процессы катаболизма
включаются метаболиты, образующиеся как при пищеварении, так и при
распаде структурно-функциональных компонентов клеток.
Реакции
катаболизма
сопровождаются
выделением
энергии
(экзергонические реакции).
Анаболизм объединяет биосинтетические процессы, в которых простые
строительные блоки соединяются в сложные макромолекулы, необходимые
для организма. В анаболических реакциях используется энергия,
освобождающаяся при катаболизме (эндергонические реакции).
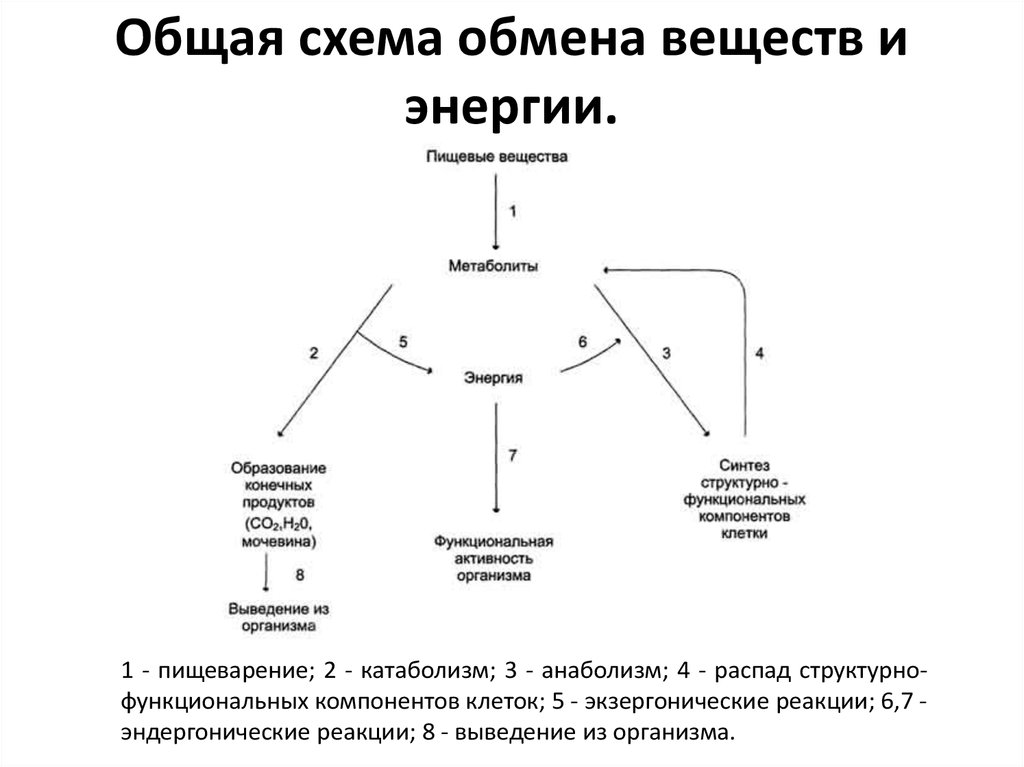
69. Общая схема обмена веществ и энергии.
1 - пищеварение; 2 - катаболизм; 3 - анаболизм; 4 - распад структурнофункциональных компонентов клеток; 5 - экзергонические реакции; 6,7 эндергонические реакции; 8 - выведение из организма.70. БИОЛОГИЧЕСКОЕ ОКИСЛЕНИЕ
• Процессыкатаболизма
в
клетках
животных
сопровождаются потреблением кислорода, который
необходим для реакций окисления. В результате этих
реакций происходит освобождение энергии, которая
необходима
организмам
в
процессах
жизнедеятельности для осуществления различных
видов работы. Небиологические системы могут
совершать работу за счёт тепловой энергии,
биологические
системы
функционируют
в
изотермическом режиме и для осуществления
процессов жизнедеятельности используют химическую
энергию.
Изучением
превращений
энергии,
сопровождающих химические реакции, занимается
биоэнергетика, или биохимическая термодинамика.
71.
• В живых организмах существует целая группа органическихфосфатов, гидролиз которых приводит к освобождению
большого количества свободной энергии. Такие соединения
называют высокоэнергетическими фосфатами.
• АТФ - молекула, богатая энергией, поскольку она содержит две
фосфоаншдридные связи (β, γ). При гидролизе концевой
фосфоангидридной связи АТФ превращается в АДФ и
ортофосфат Рi При этом изменение свободной энергии
составляет -7,3 ккал/моль.
72. Типы фосфорилирования
73.
74.
• Углеводы, белки и жиры — основные компоненты пищичеловека, являются многокомпонентными веществами и,
прежде чем включиться в метаболизм, подвергаются гидролизу
в желудочно-кишечном тракте. Продукты гидролиза, способные
всасываться из кишечника в кровь, затем в ходе катаболизма в
клетке полностью окисляются, освобождая энергию,
используемую для синтеза АТФ. Одной из основных
характеристик процесса катаболизма является соединение
метаболических путей в единый процесс, т.е. образование в
ходе катаболизма общих метаболитов, окисление которых до
конечных продуктов осуществляется с использованием одних и
тех же реакций, составляющих общий этап катаболизма. Таким
образом, конечным этапом окисления практически всех
веществ в организме, имеющих исходно разное строение,
являются реакции общего пути катаболизма, изучение которого
позволяет понять основные принципы организации процесса
метаболизма в организме человека, в ходе которого субстраты
полностью окисляются до СО2 и Н2О.
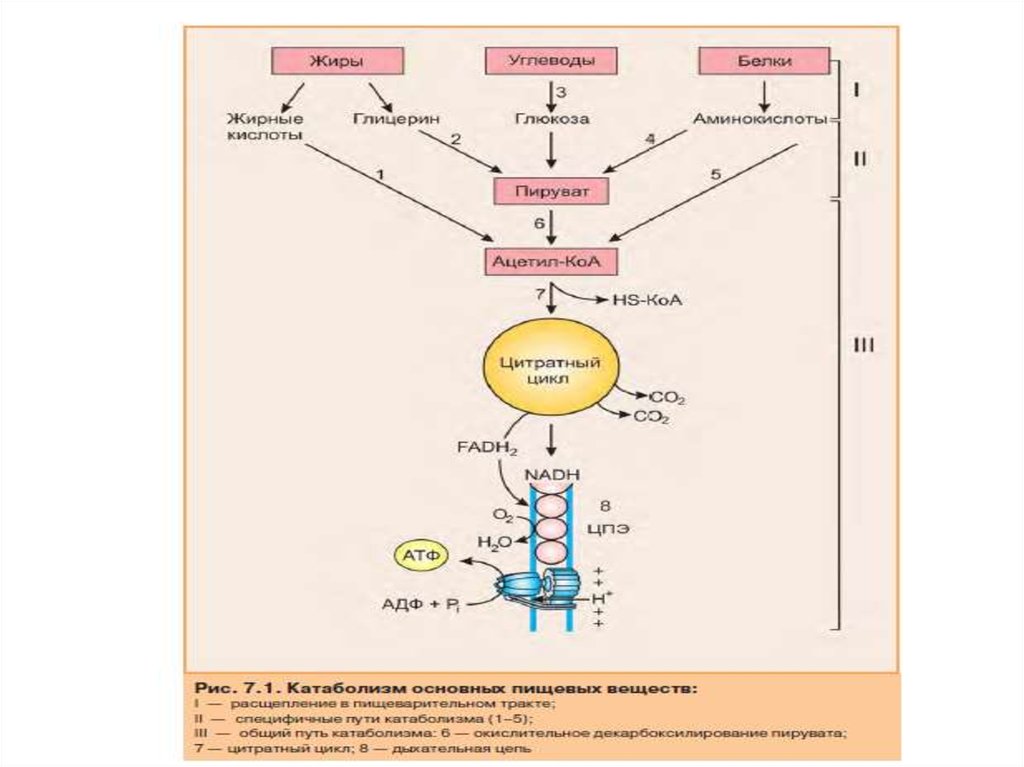
75. Основные этапы общего пути катаболизма
В процессе катаболизма можно выделить три основные его части :
1. Расщепление в пищеварительном тракте. Это гидролитические реакции,
превращающие сложные пищевые вещества в относительно небольшое
число простых метаболитов: глюкозу, аминокислоты, глицерол, жирные
кислоты.
2. Специфические пути катаболизма. На этом этапе простые метаболиты
подвергаются специфическим реакциям расщепления, в результате которых
образуется либо пировиноградная кислота, либо ацетил-КоА. Ацетил-КоА
может образоваться из пирувата, а также из жирных кислот и аминокислот. В
специфических путях катаболизма могут образоваться со единения, которые
непосредственно включаются в цитратный цикл.
3. Окислительное декарбоксилирование пирувата, цитратный цикл и
дыхательная цепь завершают расщепление пищевых веществ до конечных
продуктов — СО и Н2О.
Следовательно, начиная со стадии образования пирувата, происходит
унификация путей катаболизма. Из большого числа исходных соединений
образуется всего два — пируват и ацетил-КоА. Процесс, начинающийся с
окисления пирувата, называется общим путем катаболизма. Именно в общем
пути катаболизма образуется основное количество субстратов для реакций
дегидрирования. Совместно с дыхательной цепью и окислительным
фосфорилированием общий путь катаболизма является основным
источником энергии в форме АТФ.
76.
77. Окислительное декарбоксилирование пировиноградной кислоты
78.
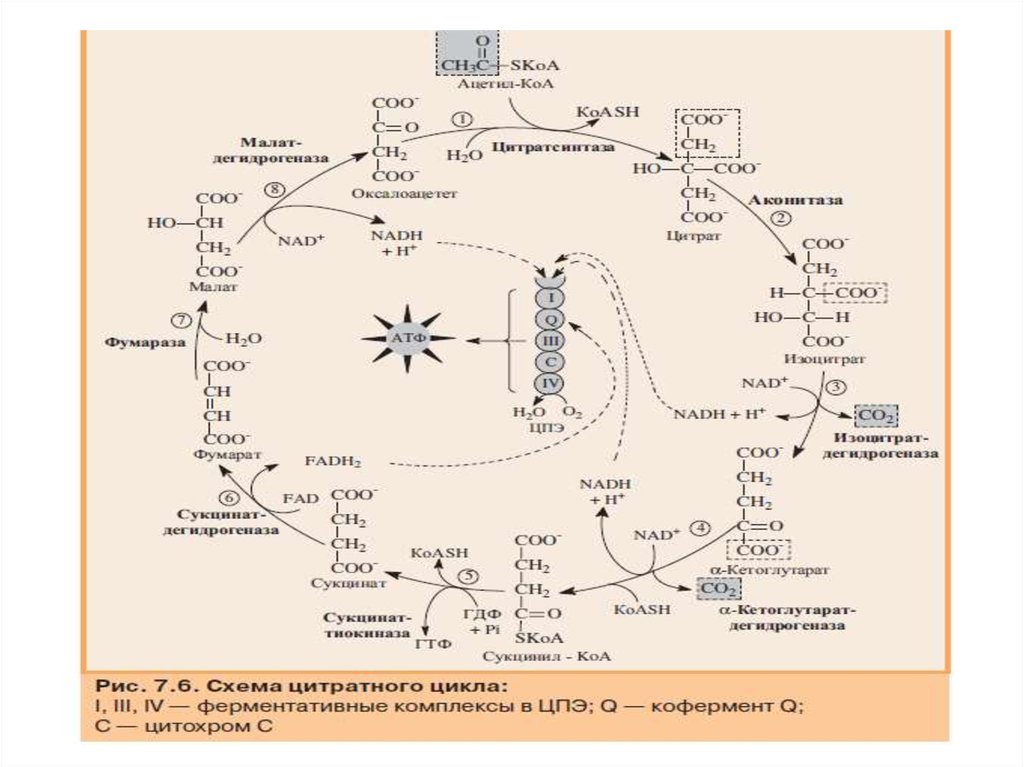
79. Цитратный цикл
• Цитратный цикл (цикл Кребса, цикл трикарбоновых кислот) —это система реакций, приводящая к полному окислению
двухуглеродного ацетильного остатка, который мог
образоваться в различных метаболических путях. Цитратный
цикл является общим конечным путем окисления белков,
жиров и углеводов. Все реакции цитратного цикла, как и
окислительного декарбоксилирования пирувата, локализованы
в митохондриях. В ходе одного полного цикла происходит:
• полное окисление ацетильного ос татка до двух молекул СО2;
• образование трех молекул восстановленного NADH + H+ и
одной молекулы FADH2;
• синтез одной молекулы ГТФ в результате субстратного фосфори
лирования.
80.
81.
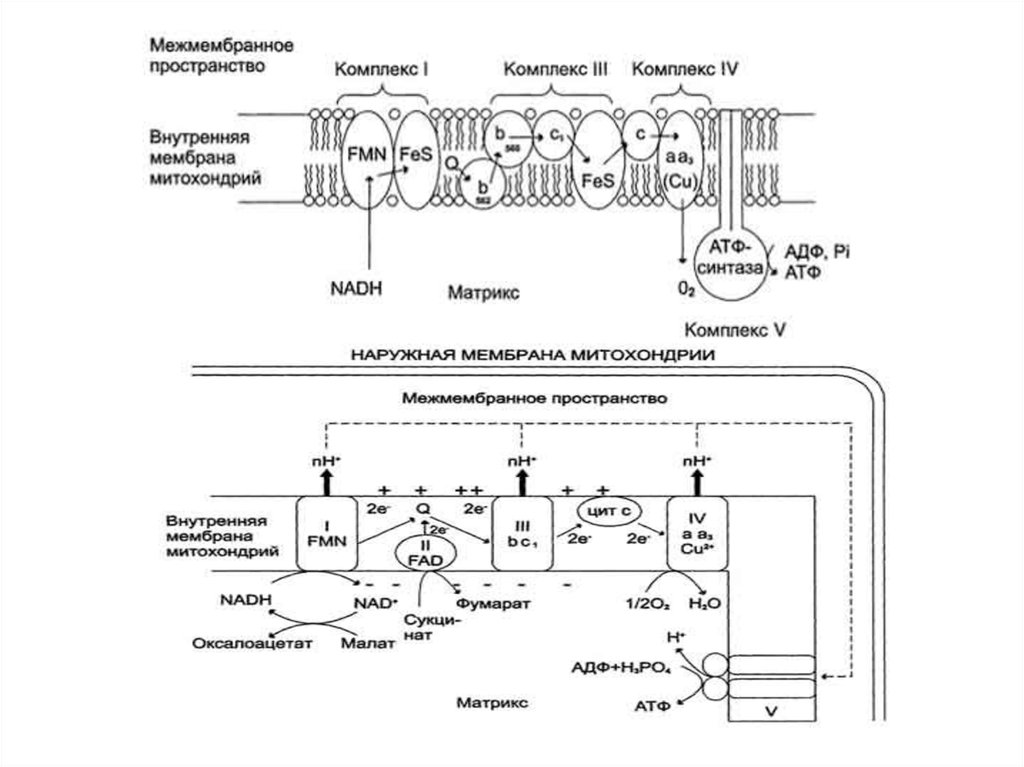
82. Дыхательная цепь (ЦПЭ)
Энергия освобождается в процессе ферментативного окисления метаболитов
специфическими дегидрогеназами. В реакциях дегидрирования электроны и
протоны переходят от органических субстратов на коферменты NAD- и FADзависимых дегидрогеназ. Электроны, обладающие высоким энергетическим
потенциалом, передаются от восстановленных коферментов NADH и FADH2 к
кислороду через цепь переносчиков, локализованных во внутренней
мембране митохондрий. Восстановление молекулы О2 происходит в
результате переноса 4 электронов. При каждом присоединении к кислороду 2
электронов, поступающих к нему по цепи переносчиков, из матрикса
поглощаются 2 протона, в результате чего образуется молекула Н2О.
Окисление органических веществ в клетках, сопровождающееся
потреблением кислорода и синтезом воды, называют тканевым дыханием, а
цепь переноса электронов (ЦПЭ) - дыхательной цепью.
Электроны, поступающие в ЦПЭ, по мере их продвижения от одного
переносчика к другому теряют свободную энергию. Значительная часть этой
энергии запасается в форме АТФ, а часть энергии рассеивается в вице тепла.
Кроме того, электроны с высоким энергетическим потенциалом,
возникающие при окислении различных субстратов, могут быть использованы
в реакциях биосинтеза, для которых помимо АТФ требуются
восстановительные эквиваленты, например NADPH.
Перенос электронов от NADH к О2 включает ряд переносчиков, которые
локализованы во внутренней мембране митохондрий. За исключением
убихинона и цитохрома С, это сложные белковые комплексы.































































 Биология
Биология








