Похожие презентации:
Адиабатический процесс в реакционном объеме. (Тема 6.3)
1. Тема 6
Химический процесс науровне реакционного
объема
2. Тема 6.3
Адиабатический процесс вреакционном объеме
• Режимы идеального вытеснения и
периодический идеального
смешения
• Режим проточный идеального
смешения (РИС-н)
• Критические тепловые явления в
адиабатическом гетерогенном
процессе
3. Адиабатический процесс в реакционном объеме
• Теплообмен с окружающейсредой отсутствует
• Показатели процесса
определяются свойствами
среды
4. РИВ и РИС-п
Математическая модель РИВ иРИС-п
при = 0, С = С0, Т = Т0
Уравнение материального
баланса (для
простой реакции W(C, T) = –r(C, T) и замены
С на х)
5. РИВ и РИС-п
Уравнение теплового баланса (дляпростой реакции W(C, T) = –r(C, T) и замены
С на х)
или при = 0, х = 0, Т = Т0
6. РИВ и РИС-п Адиабатический процесс
Уравнение теплового баланса (В=0,т.к теплообмен с окружающей средой
отсутствует)
при = 0, х = 0, Т = Т0
7. РИВ и РИС-п Адиабатический процесс
Уравнение материальногобаланса для сложной реакции
Уравнение теплового баланса для
сложной реакции
8. РИВ и РИС-п
Зависимость разогрева системыот степени превращения
Зависимость Т (х) линейная и не
зависит от вида кинетического
уравнения скорости
9. РИВ и РИС-п
Зависимость Т (х) характеристическое уравнениеадиабаты
ΔТад – температурный
коэффициент адиабаты
С увеличением конверсии при
экзотермической реакции (qp > 0)
система будет разогреваться,
при эндотермической (qp < 0) —
охлаждаться.
10. РИВ и РИС-п
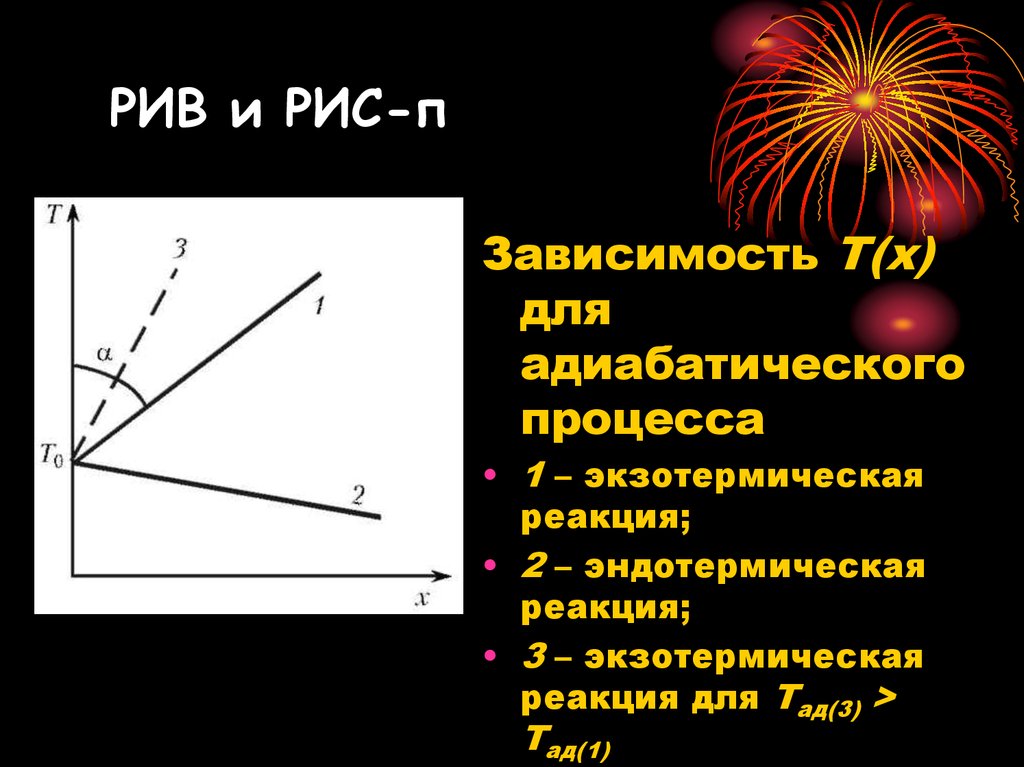
Зависимость Т(х)для
адиабатического
процесса
• 1 – экзотермическая
реакция;
• 2 – эндотермическая
реакция;
• 3 – экзотермическая
реакция для Тад(3) >
Тад(1)
11. РИВ и РИС-п
• Величина наклона определяетсясвойствами системы
Чем больше тепловой эффект
реакции qp и выше концентрация реагирующего вещества С0,
тем круче наклон и реакционная
смесь будет разогреваться или
охлаждаться
сильнее.
Большая теплоемкость реакционной
смеси ср делает наклон зависимости
Т(х) более пологим и уменьшает
изменение температуры.
12. РИВ и РИС-п
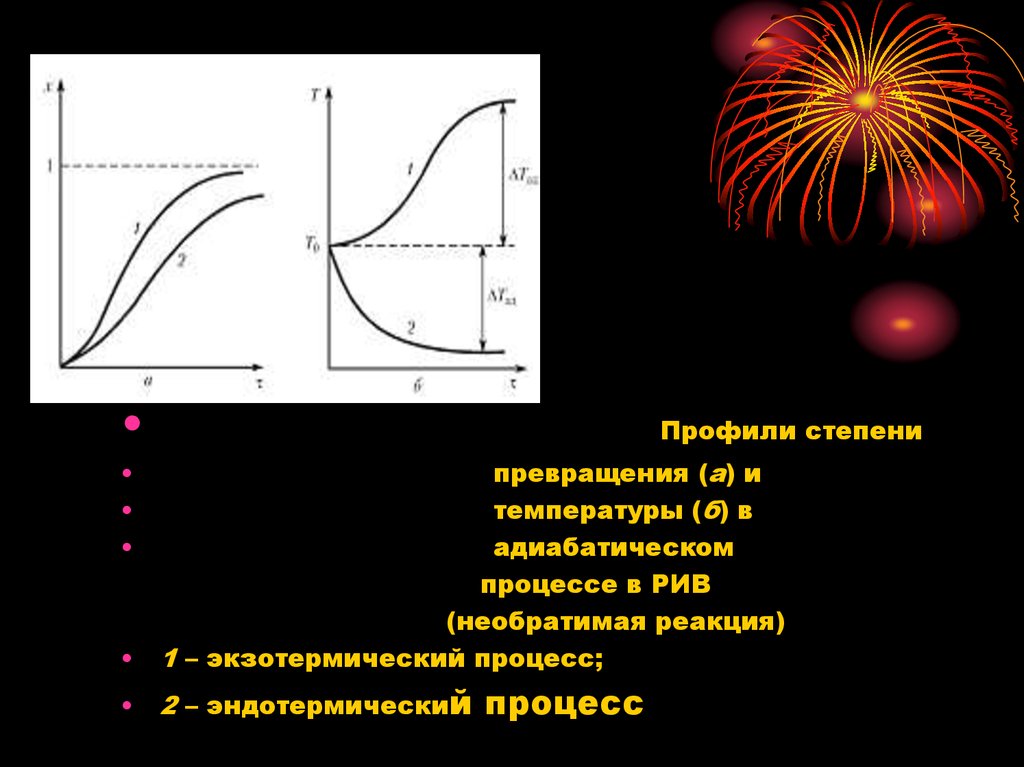
Профили степени
превращения (а) и
температуры (б) в
адиабатическом
процессе в РИВ
(необратимая реакция)
1 – экзотермический процесс;
2 – эндотермический
процесс
13. РИВ и РИС-п
• Для обратимой реакции общийхарактер зависимостей х(τ) и
Т(τ) сохраняется, но процесс
будет протекать только до
равновесия. Максимальный
разогрев в этом случае
составит
14. РИВ и РИС-п Сопоставление адиабатического и изотермического процесса
Если изотермический процесс будетосуществляться при
начальной
температуре адиабатического Т0, то
адиабатический процесс окажется
более
интенсивным
в
случае
экзотермического
процесса
(Т
реакции
повышается)
и
менее
интенсивным
в
случае
эндотермического
(Т
реакции
понижается).
15. РИВ и РИС-п Сопоставление адиабатического и изотермического процесса
Еслитемпература
изотермического
процесса будет Т > Т0, то вначале, до
достижения
в
адиабатическом
процессе температуры Т, процесс в
изотермическом
режиме
будет
протекать более интенсивно, после
достижения
Т
адиабатический
процесс станет более интенсивным. В
случае эндотермического процесса
повышение Т0 приводит к усилению
преимущества
изотермического
16. РИС-н
Математическая модель РИС-нпри = 0, С = С0, Т = Т0
Уравнение материального
баланса (для простой реакции, замены
С на х и введение ΔТад и В), при
Т = Т0
= 0, х = 0,
17. РИС-н
Модель адиабатическогопроцесса
(при В = 0)
Уравнение разогрева системы
18. РИС-н
Уравнение разогрева в РИС-нсовпадает с аналогичным
уравнением для РИВ и РИС-н.
Во всех режимах при одинаковой
степени превращения величина
разогрева совпадает, т.е. в
адиабатическом процессе
температура на выходе не зависит
от гидродинамического режима в
реакционном объеме
(концентрационного и
19. РИС-н
Зависимость x(τ), Т(τ) и Т(х)Получены для различных значений Vp при V0
= const или при разных V0 при Vр = const
20. РИС-н
Для реакции первого порядкаT T0
Получаем
уравнение,
увязывающее
k T
T
1устанавливающийся
k T
в процессе
температурный режим Т с
продолжительностью протекания
процесса (глубиной превращения
х) при определенных свойствах
системы Тад
ад
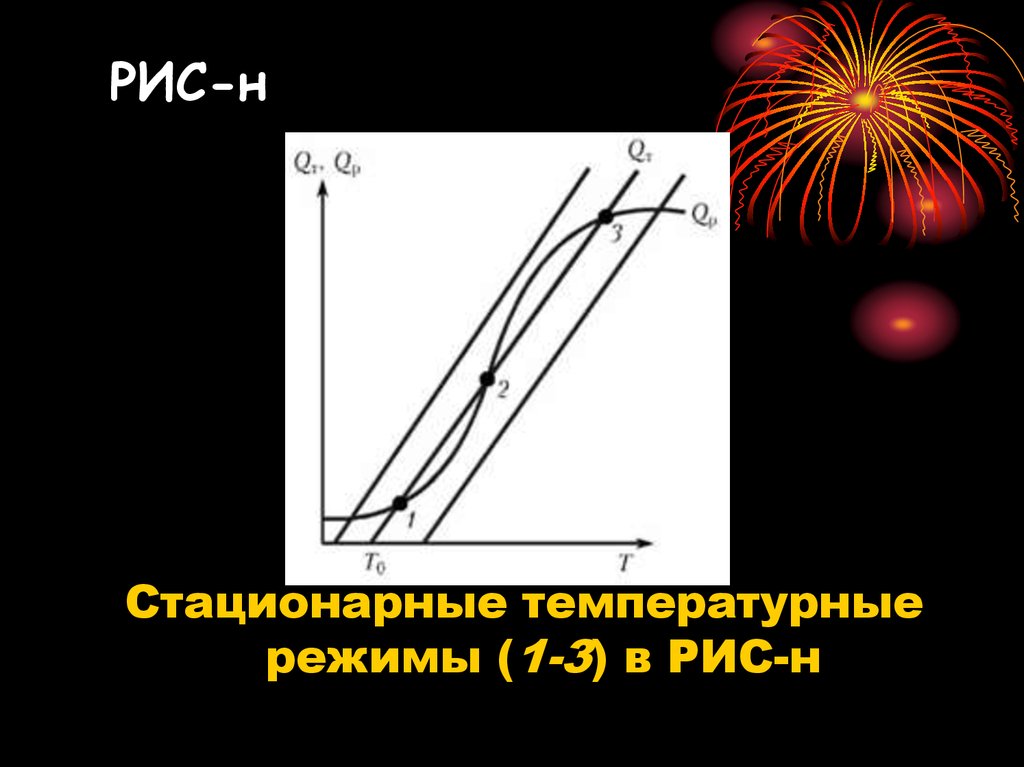
21. РИС-н
Стационарные температурныережимы (1-3) в РИС-н
22. РИС-н
При низких значениях Т0 будетреализоваться
низкотемпературный процесс,
при высоких —
высокотемпературный.
Предельные значения Т0
определяются свойствами
реагирующей смеси (qp, k, Е и
др.), проявляющимися в
конфигурации и температурном
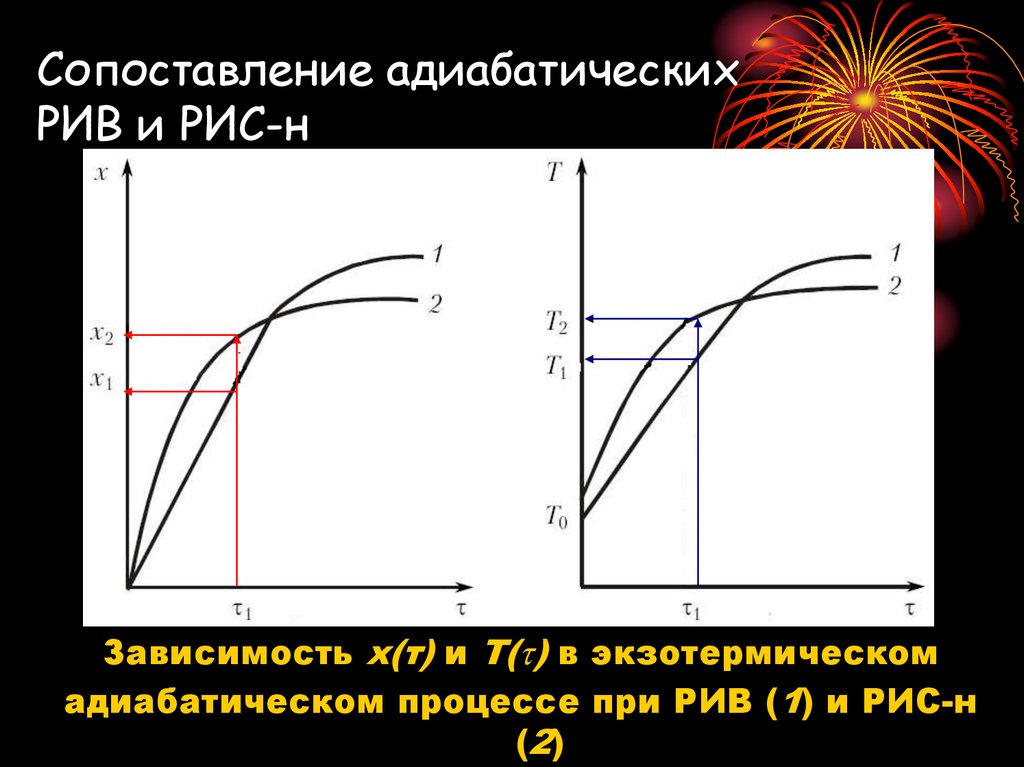
23. Сопоставление адиабатических РИВ и РИС-н
Зависимость x(τ) и Т( ) в экзотермическомадиабатическом процессе при РИВ (1) и РИС-н
(2)
24. Сопоставление адиабатических РИВ и РИС-н
В РИС-н процесс протекает припостоянных конечных условиях
(температура и концентрация), а
в РИВ эти условия переменны и
меняются от начальных до
конечных. Поэтому в РИВ
средняя концентрация исходных
веществ больше, а средняя
температура — меньше.
25. Сопоставление адиабатических РИВ и РИС-н
Экзотермический процесс:при одинаковом значении 1 (Vp = const) в РИС-н
достигается более высокая степень
превращения х2>х1, что указывает на более
высокую интенсивность процесса;
при одинаковой температуре входящего потока
Т0
в РИС-н поддерживается более высокая
температура Т2, чем в РИВ;
более высокая температура в РИС-н Т2 > Т1,
даже при более низкой концентрации реагента
(1 – х2)<(1 – х1), обеспечивает более высокую
скорость при РИС-н.
при достаточно больших степенях превращения,
когда процесс переходит в диффузионную
область и влияние концентрации на скорость
26. Сопоставление адиабатических РИВ и РИС-н
Эндотермический процесс:Средняя
температура в РИВ
выше, чем при РИС-н, поэтому
адиабатический
эндотермический
процесс
всегда
протекает
более
интенсивно в РИВ.
27. Критические тепловые явления в адиабатическом гетерогенном процессе
В адиабатических процессахтемпературный режим
устанавливается самопроизвольно,
как следствие протекания реакции
без внешнего регулирования.
Для практического осуществления
весьма существенна устойчивость
режима работы, независимость его
от различных возмущений.
28. Критические тепловые явления в адиабатическом гетерогенном процессе
Стационарный режим считаетсяустойчивым, если после устранения
источника внесенного возмущения
самопроизвольно восстанавливается
первоначальное стационарное
состояние процесса.
Неустойчивое стационарное состояние
- если после устранения источника
внесенного возмущения
самопроизвольно не
восстанавливается первоначальное
29. Критические тепловые явления в адиабатическом гетерогенном процессе
Внешнее возмущение(воздействие)
Стационарный
температурный
режим
Изменение
теплового баланса
Отклонение
от стационарного
режима
Расположение зависимостей
Qр(Т) и QТ(Т) в стационарном
режиме
30. Критические тепловые явления в адиабатическом гетерогенном процессе
• Вариант I• Если по каким-либо причинам температура процесса Т1
увеличится до Т'1 , то увеличится также тепловыделение Qp и
теплоотвод QT, но последний возрастет больше, чем
тепловыделение. Если источник возмущения будет устранен,
то превалирующий теплоотвод приведет к снижению
температуры процесса и режим самопроизвольно вернется в
первоначальное состояние с температурой Т1.
• Если температура процесса уменьшится до Т"1, то Qp станет
больше QT и после устранения источника возмущения
восстановится первоначальная температура Т1.
• В этом случае стационарное состояние является устойчивым.
• Следовательно, условием устойчивости стационарного режима
является dQp/dТ < dQT/dТ.
31. Критические тепловые явления в адиабатическом гетерогенном процессе
• Вариант II• Повышение температуры процесса от Т2 до Т‘2 приведет к
более сильному возрастанию тепловыделения Qp, нежели
теплоотвода QT.
• Поэтому температура процесса будет продолжать
увеличиваться и после устранения источника возмущения и
самопроизвольно первоначальный температурный режим не
восстановится.
• Понижение температуры до Т"2 приведет к состоянию, когда
Qp<QT, что приведет к дальнейшему остыванию процесса даже
при устранении источника возмущения.
• Следовательно, стационарное состояние является
неустойчивым и стационарный режим, даже при любых малых
изменениях Т0, не будет восстанавливаться самостоятельно.
• Показателем неустойчивости стационарного состояния
32. Критические тепловые явления в адиабатическом гетерогенном процессе
• Условие устойчивости (вариант I) характерно длянизкотемпературных и высокотемпературных
режимов (линии 1 и 3), тогда как промежуточный
режим (линия 2) является неустойчивым (вариант
II)
и
при
малейшем
отклонении
T0
самопроизвольно
не
восстанавливается,
и
процесс неизбежно охлаждается до режима 1 или
нагревается до режима 3.
• Экспериментально
подтверждено,
что
неустойчивые
стационарные
состояния
практически не реализуются.
33. Критические тепловые явления в адиабатическом гетерогенном процессе
Стационарные режимы экзотермическогоадиабатического РИС-н при повышении (а)
и понижении (б) температуры газового потока T0
34. Критические тепловые явления в адиабатическом гетерогенном процессе
Зависимость температуры адиабатического гетерогенногопроцесса в РИС-н TП от температуры входящего потока T0
TПН – Температура зажигания; TПВ – температура потухания
35. Критические тепловые явления в адиабатическом гетерогенном процессе
• Температуры зажигания ТПН и потухания ТПВ являютсякритическими
режимами
и
определяют
области
существования различных температурных режимов.
• Низкотемпературные режимы существуют при T0 < ТПН
• Высокотемпературные режимы существуют при T0 > ТПВ.
• Если T0 лежит в интервале ТПВ > T0 > ТПН, то система будет
находиться в одной из двух областей стационарных
режимов в зависимости от предыстории процесса, т.е. от
направления достижения T0.
• Температурные режимы процесса в интервале ТПВ > TП >
ТПН практически не реализуются.































 Физика
Физика Химия
Химия








