Похожие презентации:
Профилактика ВБИ. Санитарно-эпидемиологический режим
1. Профилактика ВБИ Санитарно-эпидемиологический режим
Профилактика ВБИСанитарноэпидемиологический
режим
2. Основные нормативно-правовые акты:
• ФЗ «О санитарно-эпидемиологическомблагополучии населения» № 52-ФЗ от 30.03.99г.
• ФЗ № 323-ФЗ от 21.11.2011г «Об основах охраны
здоровья граждан в РФ» (вступил в силу с
01.01.2012г)
• СанПиН 2.1.3.2630-10 «Санитарноэпидемиологические требования к организациям,
осуществляющим медицинскую деятельность».
• Национальная концепция профилактики инфекций,
связанных с оказанием медицинской помощи
(06.11.2011г)
3. Инфекции, связанные с оказанием медицинской помощи (ВБИ)
4. Инфекции, связанные с оказанием медицинской помощи (ВБИ) СанПиН 2.1.3.2630-10 «Санитарно-эпидемиологические требования к
организациям, осуществляющим медицинскую деятельность»глава 3 раздел 1 пункт 1.1
Любое клинически выраженное заболевание микробного
происхождения, которое поражает больного в результате
его поступления в больницу или обращения за
медицинской помощью вне зависимости от появления
симптомов заболевания у пациента во время пребывания в
стационаре или после его выписки, а также инфекционное
заболевание сотрудника лечебной организации вследствие
его инфицирования при работе в данной организации
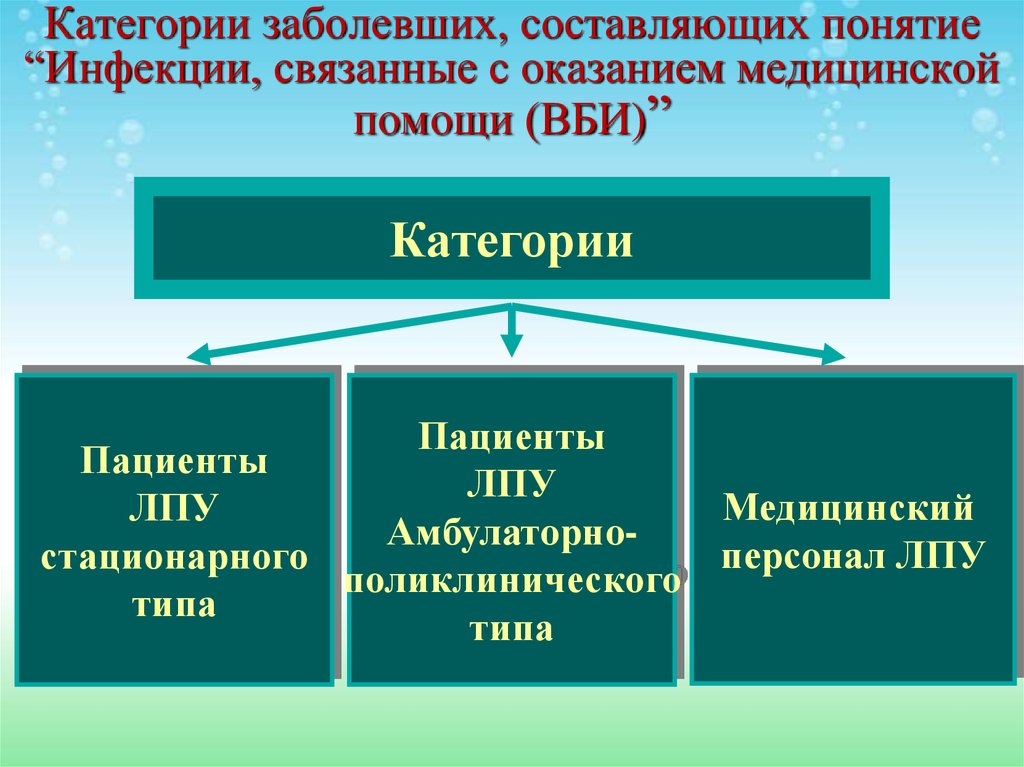
5. Категории заболевших, составляющих понятие “Инфекции, связанные с оказанием медицинской помощи (ВБИ)”
КатегорииПациенты
Пациенты
ЛПУ
Медицинский
ЛПУ
Амбулаторноперсонал ЛПУ
стационарного
поликлинического
типа
типа
6. Этиологическая структура ИСМП
• Условно-патогенные бактерии• Вирусы
• Грибы
• Простейшие
• Прионы
Всего более 300 различных возбудителей
инфекционных
и паразитарных болезней
7. Наиболее значимые возбудители ИСМП:
• Стафилококки• Грамотрицательные условнопатогенные бактерии
• Респираторные вирусы
8. Инфекции, связанные с оказанием медицинской помощи (ВБИ)
• Факторы передачи: инструментарий, мед аппаратура,белье, постельные принадлежности, кровати, предметы
ухода за больными, перевязочный и шовный материал,
эндопротезы и дренажи, трансплантанты, спецодежда,
обувь, волосы и руки персонала и больных..
• "Влажные объекты"- краны, раковины, контаминированные р-ры антисептиков, антибиотиков, дезинфектантов и
др., кремы для рук, вода в вазах для цветов, увлажнители
кондиционеров…
• Источник - мед персонал!!!
9. ИСПМ
• Инфекция мочевых путей• Инфекция нижних дыхательных путей
• Инфекция послеоперационной раны
• Сепсис
• Инфекция верхних дыхательных путей
• Инфекция ЖКТ, ЦНС, кожи, мягких тканей
и другие
10. Последствия ИСМП
• Такие пациенты находятся в стационаре в 2-3раза дольше
• в 3-4 раза возрастает стоимость лечения
• в 5-7 раз возрастает риск летального исхода
11. В мире нет ни одного стационара без ИСМП (ВБИ)
• Распространенность в Европе 3,5 – 14,8% (7,1%)• 4 100 000 пациентов с ВБИ в странах ЕС ежегодно
• Количество смертей, напрямую связанных с ВБИ –
37 000 в год
• 16миллионов «сверх»койко-дней в год
• Экономические потери – около 7 ТРИЛЛИОНОВ € в
год
“The global burden of HAI”. WHO, 2010
В Российской Федерации в 2010 году зарегистрировано
25 617 случаев внутрибольничных инфекций.
Показатель заболеваемости составил 0,8 на
1000 госпитализированных
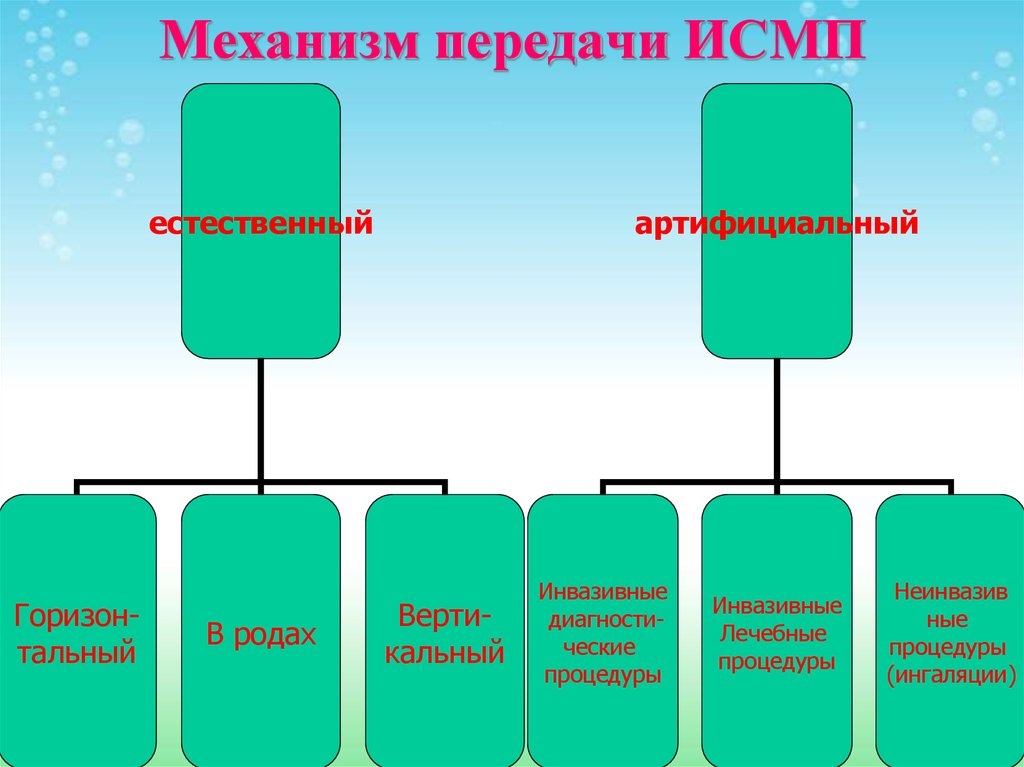
12. Механизм передачи ИСМП
естественныйГоризонтальный
В родах
артифициальный
Вертикальный
Инвазивные
диагностические
процедуры
Инвазивные
Лечебные
процедуры
Неинвазив
ные
процедуры
(ингаляции)
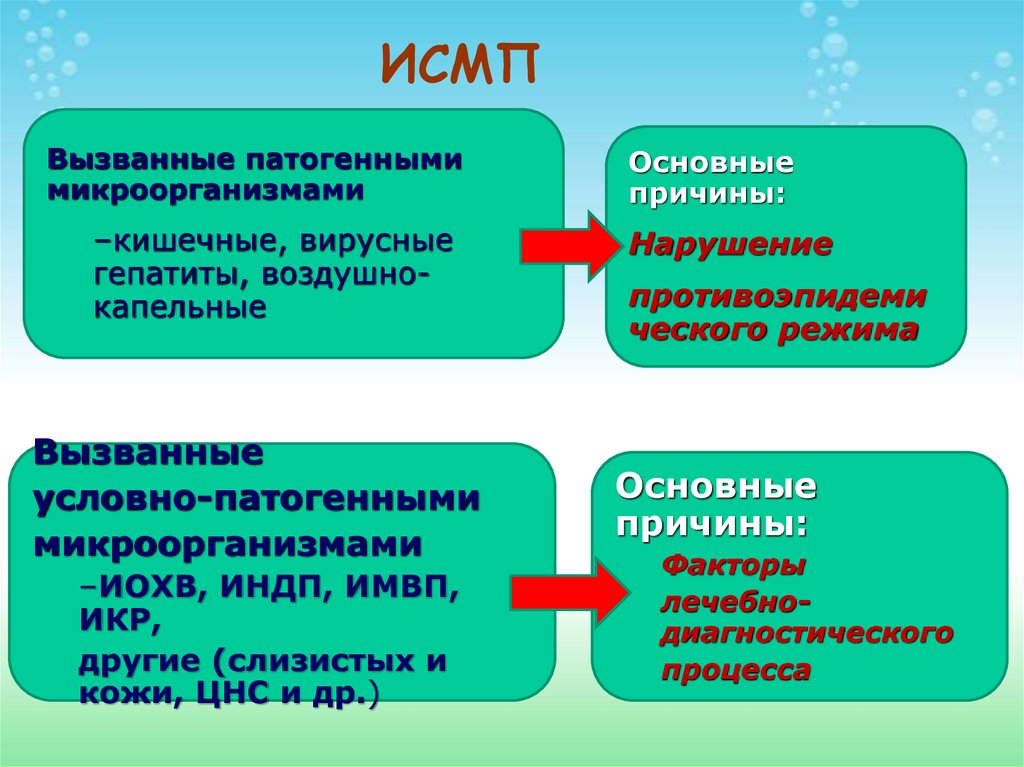
13. ИСМП
Вызванные патогеннымимикроорганизмами
–кишечные, вирусные
гепатиты, воздушнокапельные
Вызванные
условно-патогенными
микроорганизмами
–ИОХВ, ИНДП, ИМВП,
ИКР,
другие (слизистых и
кожи, ЦНС и др.)
Основные
причины:
Нарушение
противоэпидеми
ческого режима
Основные
причины:
Факторы
лечебнодиагностического
процесса
14. Артифициальный механизм передачи ИСМП
Забор кровидля исследований
Эндоскопические исследования
Эндохирургические вмешательства
Интубации
Зондирование желудка,
12-перстной кишки
Катетеризации сосудов,
мочевыводящих путей
Пункции люмбальные,
стернальные, органов и др.
Оперативные вмешательства
Роды, аборты
Трансплантация органов,
тканей, сосудов и др.
Артифициальный
(исскуственный)
механизм
передачи
Получение биоптата тканей,
органов
Мануальное обследование
Использование аппаратуры для
искусственного кровообращения
Инъекции
Гемодиализ, гемосорбция,
плазмафрез
Трансфузии крови, плазмы
Стоматологическое лечение
Е.П.Ковалева, 2004
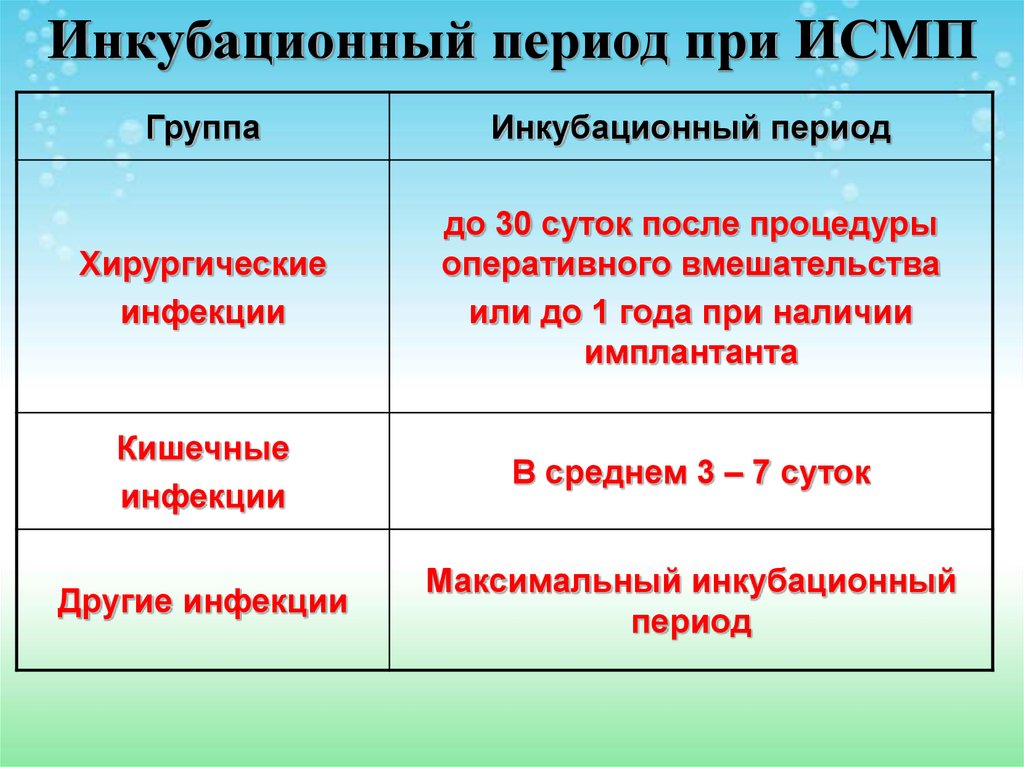
15. Инкубационный период при ИСМП
ГруппаИнкубационный период
Хирургические
инфекции
до 30 суток после процедуры
оперативного вмешательства
или до 1 года при наличии
имплантанта
Кишечные
инфекции
В среднем 3 – 7 суток
Другие инфекции
Максимальный инкубационный
период
16. «Сигнальные» признаки, свидетельствующие о надвигающейся эпидемиологической опасности для отделений хирургического профиля:
Доминирование 1-2 госпитальных штаммов с выраженнойантибиотикорезистентностью;
Ухудшение показателей бактериологического контроля
эффективности стерилизации изделий мед. назначения;
Выделение при санитарно-бактериологических
исследованиях объектов окружающей среды;
Появление 2-3 случаев ГСИ у пациентов одного
хирургического профиля с выделением идентичного по
свойствам штамма возбудителя с выраженной
антибиотикорезистентностью;
Появление 2-3 не связанных между собой случаев
кишечных заболеваний пациентов или сотрудников
17. «Сигнальные» признаки, свидетельствующие о надвигающейся эпидемиологической опасности в родильном доме:
Изменение соотношения легких и тяжелых форм патологиив сторону тяжелых;
Изменение в структуре заболеваемости по локализации
патологического процесса;
Преобладание одной из клинических форм в структуре ВБИ
новорожденных, появление генерализованных форм;
Возникновение 2-3 и более заболеваний, связанных между
собой;
Изменение этиологической структуры заболеваемости,
выделение преимущественно одного вида возбудителя;
Увеличение числа диагнозов «внутриутробная инфекция»
(сокрытие ВБИ)
18. Основные направления профилактики ИСМП:
1. Оптимизация системы эпидемиологического надзора за ВБИ.2. Совершенствование лабораторной диагностики и
мониторинга возбудителей ВБИ.
3. Повышение эффективности дезинфекционных мероприятий.
4. Повышение эффективности стерилизационных мероприятий.
5. Разработка стратегии и тактики применения антибиотиков и
химиопрепаратов.
6. Оптимизация мер борьбы и профилактики ВБИ с
различными путями передачи.
7. Рационализация основных принципов госпитальной гигиены.
8. Оптимизация принципов профилактики ВБИ медицинского
персонала
19. Мероприятия по контролю за ИСМП в ЛПУ
организация выявления, учета и регистрации внутрибольничныхинфекций в лечебно-профилактических учреждениях;
Контроль за состоянием санитарно-противоэпидемического
режима в структурных подразделениях ЛПУ, имеющих особое
эпидемиологическое значение;
внедрение в работу ЛПУ новые дезинфектанты и кожные
антисептики, допущенные к применению в установленном
порядке;
состояние стерилизующей аппаратуры и бактерицидных
облучателей и замене устаревшего оборудования;
соблюдение бельевого режима в ЛПУ, в том числе проведение
камерной обработки в соответствии с нормативной
документацией;
соответствие сбора, хранения и утилизации отходов в ЛПУ
действующей документации;
организация специфической профилактики групп риска против
ВГВ, соблюдение мер безопасности и т.д.
20. Документация по организации и контролю соблюдения санитарно-противоэпидемического режима в отделениях ( формы в приложении)
Документация по организации и контролю соблюдения санитарнопротивоэпидемического режима в отделениях( формы в приложении)
• Журнал регистрации прохождения персоналом медицинских
осмотров, лабораторных и инструментальных обследований
• Медицинские (санитарные) книжки на всех сотрудников
• Результаты производственного лабораторного контроля
• Журнал учета результатов контроля работы воздушных
стерилизаторов – при их наличии в отделении
• Журнал учета качества предстерилизационной обработки
ИМН
• Журнал регистрации контроля работы бактерицидных
облучателей
• Журнал (график) проведения генеральных уборок
21. Документация по организации и контролю соблюдения санитарно-противоэпидемического режима в отделениях - продолжение
Документация по организации и контролю соблюдения санитарнопротивоэпидемического режима в отделениях - продолжение• Список сотрудников отделения, подлежащих вакцинации
против вирусного гепатита В, краснухи, кори, дифтерии и
прошедших вакцинацию
• Журнал учета ВБИ среди пациентов и сотрудников
• Журнал учета проведения первичного на рабочем месте и
периодического инструктажей мед. Персонала по вопросам
охраны труда, техники безопасности и соблюдения
противоэпидемического режима
• Стандарты по профилактике ВИЧ-инфекции и
парентеральных вирусных гепатитов в клиникодиагностических отделениях
• Ответственными за правильное ведение данной
документации являются: старшая и процедурная м/с
22. Современные требования к дезинфицирующим средствам для эффективной организации дезинфекционных мероприятий в соответствии с
требованиями СанПиН 2.1.3.2630-10 «Санитарноэпидемиологические требования к организациям,осуществляющим медицинскую деятельность».
23. ДЕЗИНФЕКЦИОННЫЙ РЕЖИМ В ЛПУ
Виды дезинфекции:• Профилактическая (текущая) – при отсутствии очага инфекции –
проводится как предупредительная мера при отсутствии
выявленного источника инфекции для защиты человека от
возможного заражения.
• Очаговая – при наличии очага инфекции – противоэпидемическая,
проводится в случае возникновения инфекционного заболевания
или подозрении на него. В зависимости от времени проведения
подразделяется на текущую (проводится многократно) и
заключительную (проводится однократно поле выписки или смерти
пациента)
23
24. ДЕЗИНФЕКЦИОННЫЙ РЕЖИМ В ЛПУ
Методы дезинфекции:• механический – основан на удалении возбудителей инфекционных
болезней с предметов (встряхивание, мытье рук, выколачивание,
сквозное проветривание, протирание влажной ветошью, влажная
уборка, стирка, обмывание)
• физический- на воздействии физических факторов: кипячение,
пастеризация, применение огня, УФО.
• химический – применение химических средств (антисептиков и
дезинфектантов) способами орошения, протирания, погружения или
замачивания, засыпание сухим препаратом
• биологический – используются биологические процессы
(антагонистическое действие между микробами0
• комбинированный – сочетание методов, например – влажная уборка
с последующим УФО.
24
25. СанПиН 2.1.3.2630 – 10 «САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКИЕ ТРЕБОВАНИЯ К ОРГАНИЗАЦИЯМ, ОСУЩЕСТВЛЯЮЩИМ МЕДИЦИНСКУЮ ДЕЯТЕЛЬНОСТЬ» При
плановой профилактической дезинфекции вЛПО проводится:
обеззараживание всех видов поверхностей внутрибольничной среды,
обеспечивающее гибель санитарно-показательных бактерий и уменьшение
контаминации микроорганизмами различных объектов, в том числе воздуха,
предметов ухода за больными, посуды и других;
обеззараживание изделий медицинского назначения (поверхностей, каналов и
полостей) с целью умерщвления бактерий и вирусов (в том числе возбудителей
парентеральных вирусных гепатитов, ВИЧ-инфекции); обеззараживанию
подлежат все изделия медицинского назначения, включая эндоскопы и
инструменты к ним, после их использования у пациента;
дезинфекция высокого уровня эндоскопов (ДВУ), используемых в
диагностических целях (без нарушения целости тканей, то есть при
«нестерильных» эндоскопических манипуляциях), обеспечивающая гибель всех
вирусов, грибов рода Кандида, вегетативных форм бактерий и большинства
споровых форм микроорганизмов;
гигиеническая обработка рук медицинского персонала;
обработка рук хирургов и других лиц, участвующих в проведении оперативных
вмешательств и приеме родов;
обработка операционного и инъекционного полей;
полная или частичная санитарная обработка кожных покровов;
обеззараживание медицинских отходов классов Б и В;
26. II. Организация дезинфекционных и стерилизационных мероприятий в организациях, осуществляющих медицинскую деятельность 1. Общие
положения1.4.1 Плановая профилактическая дезинфекция
проводится систематически в ЛПО при отсутствии в
них ВБИ, когда источник возбудителя не выявлен и
возбудитель не выделен, с целью:
уменьшения микробной обсемененности объектов
внутрибольничной среды и предупреждения
возможности размножения микроорганизмов;
предупреждения распространения
микроорганизмов через изделия медицинского
назначения, руки и кожные покровы медицинского
персонала и больных;
27. Химический метод дезинфекции
• Классификация степени ингаляционнойопасности ДС
• 1 класс- высокоопасные и должны использоваться
только в экстремальных ситуациях, обученным
персоналом
• 2 класс опасности - рекомендуются для
использования в ЛПУ с обязательным
применением СИЗ и в отсутствии пациентов.
• 3 класс - могут использоваться персоналом без
СИЗ органов дыхания, но в отсутствии пациентов.
• 4 класс - относятся малоопасные средства, можно
использовать в присутствии больных.
28.
Эффективность дезинфекции зависит от:Устойчивости микроорганизмов к воздействию химических
факторов ;
Массивности микробного обсеменения;
Наличия на объектах органических веществ (кровь, фекалии,
мокрота и т.д.), которые могут нейтрализовать действие
химического агента;
Особенность обрабатываемого объекта;
Концентрации действующего вещества;
Времени воздействия и способа обработки (протирание,
орошение, погружение).
29. ПРИОНЫ ВИРОИДЫ СПОРЫ БАЦИЛЛ (Bacillus anthracis и др.) МИКОБАКТЕРИИ (M. tuberculosis) ВИРУСЫ, НЕ ИМЕЮЩИЕ СУПРАКАПСИДНОЙ
СРАВНИТЕЛЬНАЯ УСТОЙЧИВОСТЬ МИКРООРГАНИЗМОВК ХИМИЧЕСКИМ ДЕЗИНФИЦИРУЮЩИМ СРЕДСТВАМ
ВЫСОКАЯ
ПРИОНЫ
ВИРОИДЫ
СПОРЫ БАЦИЛЛ
(Bacillus anthracis и др.)
МИКОБАКТЕРИИ
(M. tuberculosis)
ВИРУСЫ, НЕ ИМЕЮЩИЕ
СУПРАКАПСИДНОЙ ОБОЛОЧКИ
(Polio, Coxsackie, Echo, Rhino, HBA и др.)
ГРИБЫ
(Trichophyton, Candida,)
ВЕГЕТАТИВНЫЕ ФОРМЫ БАКТЕРИЙ
(Ps.aeruginosa, S.aureus и др.)
НИЗКАЯ
ВИРУСЫ, ИМЕЮЩИЕ
СУПРАКАПСИДНУЮ ОБОЛОЧКУ
(HIV, HBV, influenza, herpes virusis, vaccinia, corona и др.)
30. Химический метод дезинфекции
1.
2.
3.
4.
5.
6.
7.
8.
Классификация химических
дезинфектантов (8 групп)
Галоидосодержащие
Кислородосодержащие
Надкислоты
Поверхностно-активные вещества
Альдегидосодержащие
Фенолсодержащие
Спиртосодержащие
Буанидины
31.
Характеристика основных химических соединенийАльдегиды
глутаровый альдегид, ортофталевый альдегид
Высокая антимикробная активность
(спороцидный эффект);
Токсичны (в концентрациях применяемых для
дезинфекции и особенно для стерилизации, не
безопасен для здоровья людей, работающих с
ним, т.к. оказывает раздражающее,
токсическое, наркологическое и
сенсибилизирующее действия;
В некоторых случаях могут взаимодействовать
с различными материалами;
Сложен в работе – при работе с концентратом
обязательно наличие отдельного хорошо
вентилируемого помещения – лучше
вытяжной шкаф;
Не обладают моющим эффектом;
Имеется фиксирующее действие.
32.
Характеристика основных химических соединенийГалоиды – хлорсодержащие средства
Широкий спектр антимикробной активности, включая споры
Обладают резким запахом; раздражают слизистые оболочки и
ВДП;
Оказывают разрушительное действие на обрабатываемые
материалы ( вызывают коррозию металлов, обесцвечивают
окрашенные изделия);
Низкая стабильность при хранении;
Инактивация органическими веществами;
Отсутствие моющих свойств
Кислородсодержащие: надкислоты и перекисные соединения
Широкий спектр антимикробной активности,
включая споры
Эффективны при низких концентрациях и
температурах
Эффективны в присутствии органических
материалов
Не требуют активации
Безопасны для окружающей среды
Не фиксируют кровь
Способствуют снятию органического загрязнения
33.
средства на основе ЧАС:ЧАС – низкая туберкулоцидная активность; некоторые ЧАС
относятся к ограниченным вируцидам, не обладают спороцидным
эффектом!!!!
Преимущества ЧАС:
Эффективны против вегетативных
м/организмов
Хороший моющий эффект
Не имеют запаха;
Совместимы с обрабатываемыми
поверхностями
Не обладают летучестью;
Не опасны при ингаляционном
воздействии и могут применяться у
постели больного.
Недостатки ЧАС:
• Сравнительно узкий спектр
противомикробной активности;
Неустойчивы в присутствии
органической нагрузки;
Неустойчивы при контакте с хлопком
и шерстью;
Быстрое формирование и
распространение
резистентных микроорганизмов
34. СанПиН 2.1.3.2630 – 10 «САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКИЕ ТРЕБОВАНИЯ К ОРГАНИЗАЦИЯМ, ОСУЩЕСТВЛЯЮЩИМ МЕДИЦИНСКУЮ ДЕЯТЕЛЬНОСТЬ» II.
Организация дезинфекционных и стерилизационных мероприятий в организациях,осуществляющих медицинскую деятельность
2. Требования к проведению дезинфекции, предстерилизационной очистки и стерилизации изделий
медицинского назначения
2.19 Химический метод стерилизации с применением растворов
химических средств, как правило применяют, для
стерилизации изделий, в конструкции которых использованы
термолабильные материалы, не позволяющие использовать
другие официально рекомендуемые, доступные методы
стерилизации.
Для химической стерилизации применяют растворы
альдегидсодержащих, кислородсодержащих и некоторых
хлорсодержащих средств, проявляющих спороцидное
действием.
Во избежание разбавления рабочих растворов, особенно
используемых многократно, погружаемые в них изделия
должны быть сухими.
35. СанПиН 2.1.3.2630 – 10 «САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКИЕ ТРЕБОВАНИЯ К ОРГАНИЗАЦИЯМ, ОСУЩЕСТВЛЯЮЩИМ МЕДИЦИНСКУЮ ДЕЯТЕЛЬНОСТЬ» II.
Организация дезинфекционных и стерилизационных мероприятий ворганизациях, осуществляющих медицинскую деятельность
1. Общие положения
1.9. В целях предупреждения возможного
формирования резистентных к дезинфектантам
штаммов микроорганизмов следует проводить
мониторинг устойчивости госпитальных
штаммов к применяемым дезинфицирующим
средствам с последующей их ротацией
(последовательная замена дезинфектанта из одной
химической группы на дезинфектант из другой
химической группы) при необходимости.
36. СанПиН 2.1.3.2630 – 10 «САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКИЕ ТРЕБОВАНИЯ К ОРГАНИЗАЦИЯМ, ОСУЩЕСТВЛЯЮЩИМ МЕДИЦИНСКУЮ ДЕЯТЕЛЬНОСТЬ» II.
Организация дезинфекционных и стерилизационных мероприятий в организациях,осуществляющих медицинскую деятельность
1. Общие положения
1.2. Для проведения дезинфекционных и
стерилизационных мероприятий ООМД должны
регулярно обеспечиваться моющими и
дезинфицирующими средствами различного
назначения, кожными антисептиками,
средствами для стерилизации изделий
медицинского назначения, а также
стерилизационными упаковочными материалами и
средствами контроля (в том числе химическими
индикаторами).
37. II. Организация дезинфекционных и стерилизационных мероприятий в организациях, осуществляющих медицинскую деятельность 1. Общие
положения1.10. В ООМД должен быть не менее чем
месячный запас разнообразных
дезинфицирующих средств (ДС) различного
химического состава и назначения в
соответствии с расчетной потребностью.
38. 1. Общие положения и область применения.
1.6. Медицинская техника, мебель,оборудование, дезинфекционные
средства, изделия медицинского
назначения, строительные и отделочные
материалы, а также используемые
медицинские технологии, должны быть
разрешены к применению на территории
Российской Федерации в установленном
порядке.
39. III. Профилактика внутрибольничных инфекций в стационарах (отделениях) хирургического профиля. 6. Дезинфекционные и
стерилизационныемероприятия
6.8 При проведении текущих уборок с применением растворов
ДС (профилактическая дезинфекция при отсутствии ВБИ или
текущая дезинфекции при наличии ВБИ) поверхности в
помещениях, приборов, оборудования и другого
дезинфицируют способом протирания.
Для этого целесообразно использовать дезинфицирующие
средства с моющими свойствами, что позволяет
объединить обеззараживание объекта с его мойкой.
При необходимости экстренной обработки
небольших по площади или труднодоступных
поверхностей возможно применение готовых форм ДС,
например, на основе спиртов с коротким временем
обеззараживания (способом орошения с помощью ручных
распылителей) или способом протирания растворами ДС, или
готовыми к применению дезинфицирующими
салфетками.
40.
СанПиН 2.1.3.2630 – 10«САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКИЕ ТРЕБОВАНИЯ К ОРГАНИЗАЦИЯМ,
ОСУЩЕСТВЛЯЮЩИМ МЕДИЦИНСКУЮ ДЕЯТЕЛЬНОСТЬ»
Текущую уборку в помещениях проводят по бактериальным
режимам;
при ВБИ по режиму, эффективному в отношении возбудителя ВБИ
инфекции.
При дезинфекции объектов, загрязненных кровью и др.
биосубстратами, опасными в отношении ВГ и ВИЧинфекции, по противовирусному режиму.
6.12 При использовании дезинфектантов в присутствии пациентов (профилактическая и
текущая дезинфекция) запрещается обеззараживание поверхностей растворами ДС
способом орошения, а также применение способом протирания ДС, обладающих
раздражающим действием, сенсибилизирующими свойствами.
4.3.2 Для дезинфекции кувезов не допускается применение хлорактивных средств, а также
средств, содержащих в своем составе альдегиды, фенол и его производные.
41. 11. Санитарное содержание помещений, оборудования, инвентаря
11.1. Все помещения, оборудование, медицинский идругой инвентарь должны содержаться в чистоте.
Влажная уборка помещений (обработка полов,
мебели, оборудования, подоконников, дверей)
должна осуществляться не менее 2 раз в сутки, с
использованием моющих и дезинфицирующих
средств, разрешенных к использованию в
установленном порядке. Администрация ЛПО
организует предварительный и периодический (не
реже 1 раза в год) инструктаж персонала,
осуществляющего уборку помещений по вопросам
санитарно -гигиенического режима и технологии
уборки.
42. II. Организация дезинфекционных и стерилизационных мероприятий в организациях, осуществляющих медицинскую деятельность 1. Общие
положения1.4.3. Генеральная уборка осуществляется с целью удаления
загрязнений и снижения микробной обсемененности в
помещениях организаций.
При генеральной уборке проводится мытье, очистка и
обеззараживание поверхностей помещений (в том числе
труднодоступных), дверей, мебели, оборудования (в том числе
осветительных приборов), аппаратуры с использованием
моющих и дезинфицирующих средств и последующим
обеззараживанием воздуха.
Генеральная уборка функциональных помещений, палат и
кабинетов проводится по графику не реже одного раза в месяц;
операционных блоков, перевязочных, родильных залов,
процедурных, манипуляционных, стерилизационных – один раз в
неделю.
При генеральной уборке режимы применения дезинфицирующих
средств определяются с учетом профиля стационара и
микробной контаминации объектов.
43. 11. Санитарное содержание помещений, оборудования, инвентаря (продолжение)
11.9. При проведении генеральной уборки дезинфицирующийраствор наносят на стены путем орошения или их протирания
на высоту не менее двух метров (в операционных блоках на
всю высоту стен), окна, подоконники, двери, мебель и
оборудование. По окончании времени обеззараживания
(персонал должен провести смену спецодежды) все
поверхности отмывают чистыми тканевыми
салфетками, смоченными водопроводной (питьевой)
водой, а затем проводят обеззараживание воздуха в
помещении.
ВАЖНО!!!
Для генеральной уборки целесообразно применять средства
на основе
ДВ, отличных от средств с ДВ для текущей уборки.
44. СанПиН 2.1.3.2630 – 10 «САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКИЕ ТРЕБОВАНИЯ К ОРГАНИЗАЦИЯМ, ОСУЩЕСТВЛЯЮЩИМ МЕДИЦИНСКУЮ ДЕЯТЕЛЬНОСТЬ»
Генеральные уборки в палатныхотделениях, врачебных кабинетах,
административно-хозяйственных помещениях,
отделениях и кабинетах физиотерапии и
функциональной диагностики и др. проводят
дезинфицирующими средствами по режимам,
рекомендованным для профилактики и борьбы с
бактериальными инфекциями.
45. СанПиН 2.1.3.2630 – 10 «САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКИЕ ТРЕБОВАНИЯ К ОРГАНИЗАЦИЯМ, ОСУЩЕСТВЛЯЮЩИМ МЕДИЦИНСКУЮ ДЕЯТЕЛЬНОСТЬ»
Генеральные уборки в операционных блоках, родильных залах,перевязочных, процедурных, манипуляционных,
стерилизационных проводят дезинфицирующими средствами с
широким спектром антимикробного действия по режимам,
обеспечивающим гибель
бактерий
вирусов
и грибов рода
Кандида
46. II. Организация дезинфекционных и стерилизационных мероприятий в организациях, осуществляющих медицинскую деятельность 2.
Требования к проведению дезинфекции, предстерилизационнойочистки и стерилизации изделий медицинского назначения
(продолжение)
2.6. в туберкулезных медицинских организациях
– по микобактериям туберкулеза;
в микологических стационарах
(кабинетах) – по режимам, эффективным в
отношении грибов рода
Трихофитон
47. II. Организация дезинфекционных и стерилизационных мероприятий в организациях, осуществляющих медицинскую деятельность 2.
Требования к проведению дезинфекции, предстерилизационнойочистки и стерилизации изделий медицинского назначения
2.6 Для дезинфекции изделий медицинского
назначения применяют дезинфицирующие средства,
обладающие широким спектром антимикробного
(вирулицидное, бактерицидное, фунгицидное с
активностью в отношении грибов рода Кандида)
действия. Выбор режимов дезинфекции проводят
по наиболее устойчивым микроорганизмам – между
вирусами
или
грибами рода Кандида
48.
Предстерилизационнаяочистка (ПСО)
49. Предстерилизационная очистка
Моющий комплекс используется до 6 раз и доизменения окраски
Температура раствора в процессе мойки не
поддерживается
Моющий раствор перекиси водорода с СМС, с
ингибиторами коррозии можно использовать в
течение суток с момента изготовления (в процессе
подогрева концентрация перекиси вожорода не
изменяется)
Раствор моющего средства Биолот используется
однократно, т.к. при повторном использовании
фермент в составе моющего раствора разрушается в
процессе очистки
50. Предстерилизационная очистка
Цель ПСО:– удаления белковых, жировых,
механических загрязнений
– удаления остаточных количеств
лекарственных препаратов
– повышения качества последующей
стерилизации
– уменьшение пирогенных реакций у
пациентов
51. Предстерилизационная очистка
• Последовательность ПСО:• Полное погружение в моющий раствор в
разобранном виде на 15-60 мин
• Механическая очистка – мойка в том же растворе в
течение 0,5-1 мин.
• Отмывка проточной водой – 0,5 10 мин
• Отмывка дистилированной водой – 0,5 – 10 мин
• Высушивание горячим паром (85°С) или открытым
способом
• Сборка и упаковка
Температура моющего раствора в процессе мойки
не поддерживается
52. Контроль качества ПСО
• После каждой ПСО для контроля ставитсяазопирамовая проба.
• Проверяется 1% от общего количества
инструментов (приказ 254), но не менее 3-4 предм.
• Срок хранения готового раствора азопирама (в
плотно закрытой таре, в темноте).
• - 2 месяца – в холодильнике (+4)
• - 1 месяц – вне холодильника (+18-+23)
• - 1-2 часа – срок хранения азопирама,
приготовленного в равных долях с 3% р-ром
перекиси водорода
53. Контроль качества ПСО (продолжение)
Раствор готовят смешивая в равных пропорциях азопирами перекись водорода.
• Проверка раствора на качество – наносим 2-3 капли
на кровяное пятно. Если не позже 1 минуты появляется
фиолетовое окрашивание, переходящее в фиолетовый
цвет, то реактив готов к употреблению. Если нет –
реактивом пользоваться нельзя.
• Исследуемые изделия должны иметь комнатную
температуру, не выше 25°С.
• При «+» пробе - фиолетовое окрашивание, переходящее в
розово-синее или буроватое. Окрашивание после 1
минуты не действительно.
• Буроватое окрашивание - наличие ржавчины и
хлорсодержащих окислителей.
54. Контроль качества ПСО - продолжение
Азопирамовая проба обнаруживает:– скрытую кровь
– кислоты
– окислители
– ржавчину
– растительные остатки
55.
СТЕРИЛИЗАЦИЯ–метод уничтожения вегетативных
и споровых форм патогенных и
условно-патогенных
микроорганизмов
56. Стерилизация
Согласно ОСТ 42-21-2-85 стерилизациидолжны подвергаться изделия :
• - соприкасающиеся с раневой поверхностью
• - контактирующие с кровью или инъекционными
препаратами
• - соприкасающиеся со слизистой оболочкой с
возможным ее повреждением
• выбор зависит от характера изделий
57. Стерилизация
• выбор зависит от:• материалов, из которых состоит
изделие
• конструктивного исполнения
изделий
• необходимости длительного
сохранения стерильности
• оперативности использования
58. Стерилизация
Способы стерилизацииI.
II.
III.
IV.
Физический
Паровой
Воздушный
Гласперленовый
Химический
Использование растворов химических препаратов
Газовый
Радиационный
59. Физический метод стерилизации - паровая
Стерилизующий агент - водяной насыщенный парпод избыточным давлением ( в паровых
стерилизаторах)
2 атм - 132ºС – 20 мин
Для изделий из коррозиестойкого металла, стекла,
текстильных и отдельных полимерных
материалов.
1,1 атм - 120ºС – 45 мин
Для изделий из резины, латекса, полиэтилена
(щадящий метод)
60. Физический метод стерилизации – воздушная стерилизация
Действующий агент - горячий сухой воздух.Проводится в воздушных стерилизаторах в двух режимах:
180ºС – 60 мин
160ºС – 150 мин
Рекомендуется для изделий из металла, стекла и силиконов резины
Условия:
Изделия укладывать равномерно (навалом нельзя)
Не допускается перекрытие продувочных окон и решетки вентиляции
Объемные предметы следует класть на верхнюю металлическую решетку,
чтобы не препятствовали потоку горячего воздуха
Загрузку проводят в предварительно прогретый стерилизатор, а выгрузку
производят из охлажденного до 40-50°С
Отсчет времени начинается с момента достижения необходимой
температуры.
61. Физический метод стерилизации –гласперленовая стерилизация
Физический метод стерилизации –гласперленовая стерилизация
Стерилизующим агентом является среда стеклянных
шариков, нагретых до 190-250°С.
Обязательное условие - инструмент должен быть сухим.
Режим указывается в инструкции по их эксплуатации.
230°С – 20 мин – мелкие инструменты, размер которых
не превышает 52 мм
230°С – 180 мин – инструменты, размер которых
превышает 52 мм (пинцеты, корнцанги, шипцы)
62. Физический метод стерилизации –гласперленовая стерилизация
Физический метод стерилизации –гласперленовая стерилизация
При стерилизации инструментарий погружается в
среду раскаленных кварцевых гранул на глубину
более 15 мм.
• Мелкие инструменты погружают целиком
• У инструментов, более 52 мм (щипцы, скальпели
и др.), погружается только рабочая часть.
• При стерилизации мелких инструментов в
гласперленовом стерилизаторе должны
использоваться специальные шприцы
63. Стерилизация – химический метод
Химический метод – более щадящий.• Осуществляется в двух вариантах:
1. С использованием химических веществ в
газообразном состоянии
2. Погружением стерилизуемых предметов в
растворы химических веществ
64. Стерилизация – химический метод
Стерилизация растворами химических препаратов.Недостатки:
• Создание особых асептических условий, проводятся в стерильной одежде и
перчатках
• Побочное действие стерилянтов на обслуживающий персонал
• Высокая стоимость препаратов
• Длительность процесса стерилизации
• Обязательное отмывание стерильной жидкостью простерилизованных
изделий от стерилянтов, для чего требуется запас стерильной жидкости
(питьевая вода, 0,9% раствор гипохлорида натрия).
• Потребность в стерильных емкостях для осуществления как процесса
стерилизации , так и отмыва изделий после стерилизации
• Короткий срок хранения простерилизованных изделий из-за высокой
вероятности вторичной контаминации
Преимущества:
• Современные виды стерилизации
65. Стерилизация – химический метод
• Все работы по стерилизации ИМН проводятся в асептических условиях.• Помещение для проведения готовится как операционный блок
(генеральная уборка, кварцевание)
• Персонал использует стерильную спец. одежду, перчатки.
• Для стерилизации и отмывания от остатков средств требуются
стерильные емкости, стерильная питьевая вода или 0,9% раствор натрия
хлорида и инструменты для захвата изделий, стерильные салфетки для
подсушки и упаковки.
• Температура горячих растворов для стерилизации в процессе
стерилизации не поддерживается. Ополаскивание проводится в 2-3
порциях стерильной воды по 5 минут в каждой.
Срок сохранности стерильности простерилизованных растворами ИМН:
• Без упаковки в асептических условиях – 6 часов, после окончания
обработки
• При упаковке в 2-х слойную стерильную х/б бязь, в стерильной
стерилизационной коробке, выложенной стерильной простыней на срок
не более 3-х суток
66. Одноразовые упаковочные материалы
• крепированная бумага• бумажные (касается только пакетов)
• комбинированные бумажно-пленочные
(существуют как пакеты, так и рулоны)
• пленочные (полиамидные рулоны)
67. Комбинированные пакеты и рулоны
68. Стерилизация – упаковка по ОСТу 42-21-2-85
Сроки хранения:
Биксы без фильтра (КСК), двойная бязь – 3 суток, крафтбумага
Биксы с бактериальным фильтром (КСКФ), крафт-пакеты
– 20 суток
Вскрытые биксы – 24 часа
Бумажные импортные пакеты, закрытые
термосшивателями, двухслойная упаковка из
крепированной бумаги – 21 сутки
Комбинированные прозрачные пакеты (ламинат+бумага)
– 1 год
Пакеты из полиэтиленовой пленки, пакет-футляр из
пленки «Стерикинг» - 5 лет.
69. Гигиена рук медицинского персонала – основа больничной гигиены.
70.
Любой вид медицинскойдеятельности сопровождается
контаминацией рук
медицинского персонала
71.
Уровень контаминациирук/перчаток
(кол-во бактерий на перчатку)
Смена повязки, инфицированные пролежни
Смена носового катетера
106-108
105-106
Отсос слизи у интубированного пациента
106-108
Опорожнение сосуда с инфицированной мочой
106-107
Подмывание промежности
108-1010
Jensen, Ugeskrift forLaeger, 1974;136:579-586
72.
Отпечаток перчатки после оказания медицинской помощи73.
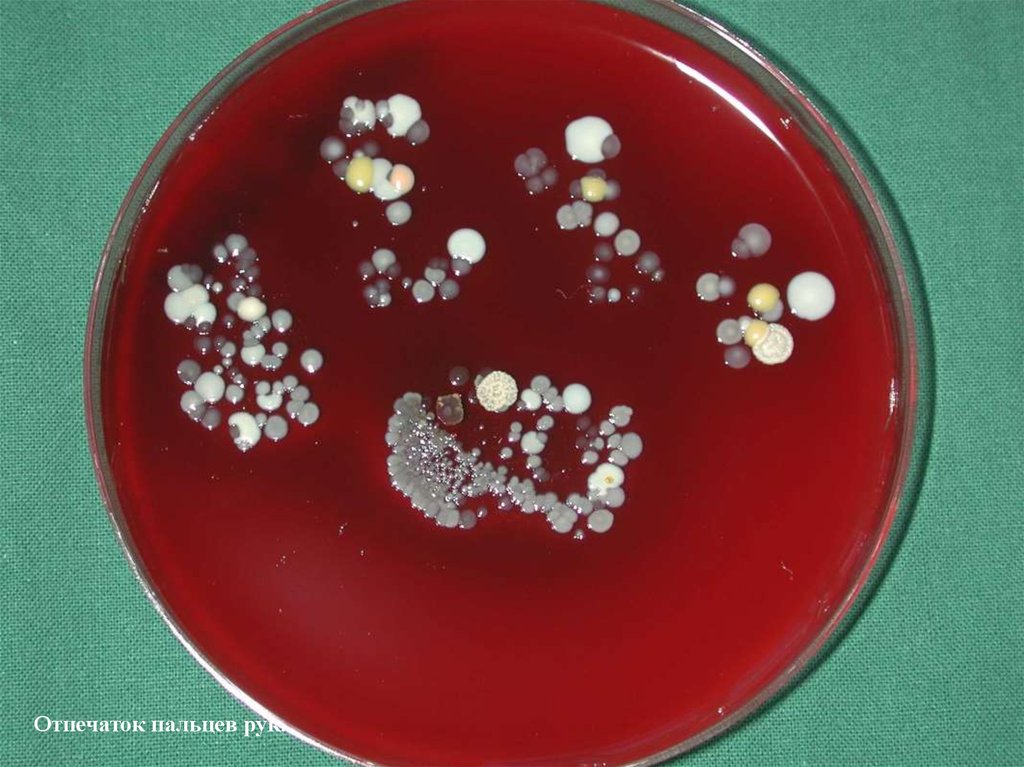
Отпечаток пальцев рук.74.
Отпечаток колец75.
5 мая – «Чистые руки спасут жизни»инициатива ВОЗ начата в 2005 г. в рамках проекта
«Всемирный альянс за безопасность пациента».
Ключевая акция в рамках пректа
«Чистота – залог безопасности пациента»,
на международном уровне и на уровне каждой страны явилось создание
«Руководства ВОЗ по гигиене рук в здравоохранении»
где указано: когда и как
мыть руки с мылом
протирать дезинфицирующим раствором на спиртовой основе.
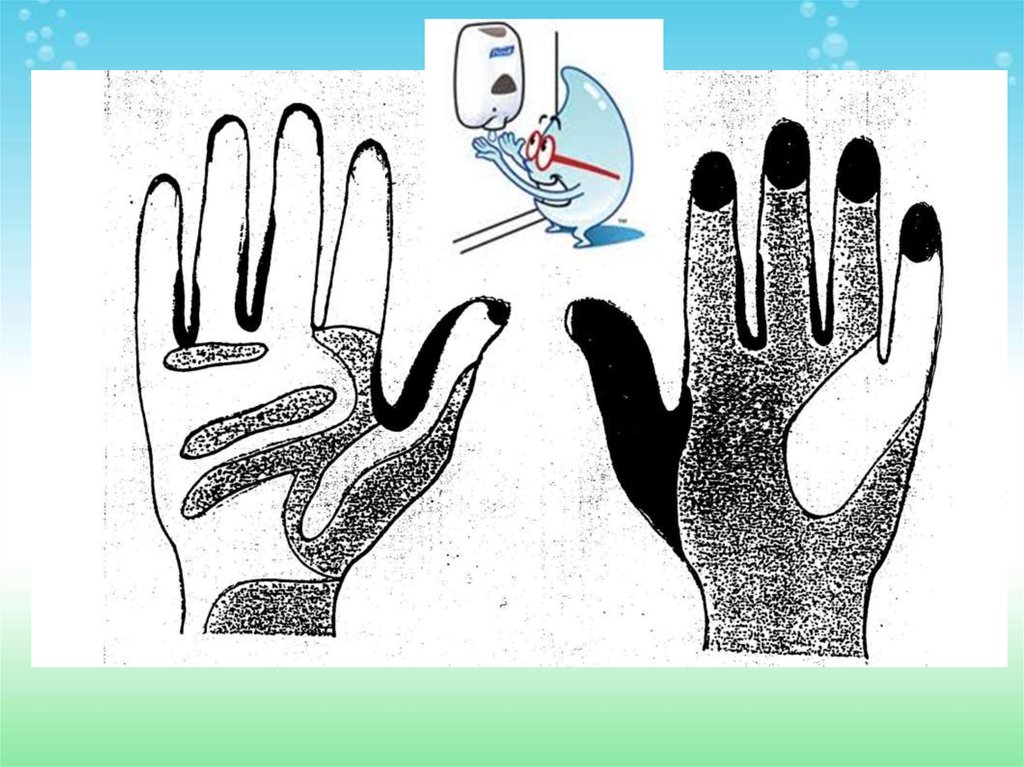
76.
Часто легко узнать, когда наши рукигрязные
Но всегда ли мы знаем, когда наши руки
чистые?
Наши руки могут выглядеть чистыми.
77.
ОБЕЗЗАРАЖИВАНИЕ РУКЗачем?
80% всех инфекций передается через
необеззараженные руки
78. ОБЕЗЗАРАЖИВАНИЕ РУК Зачем?
80% всех инфекций передается черезнеобеззараженные руки
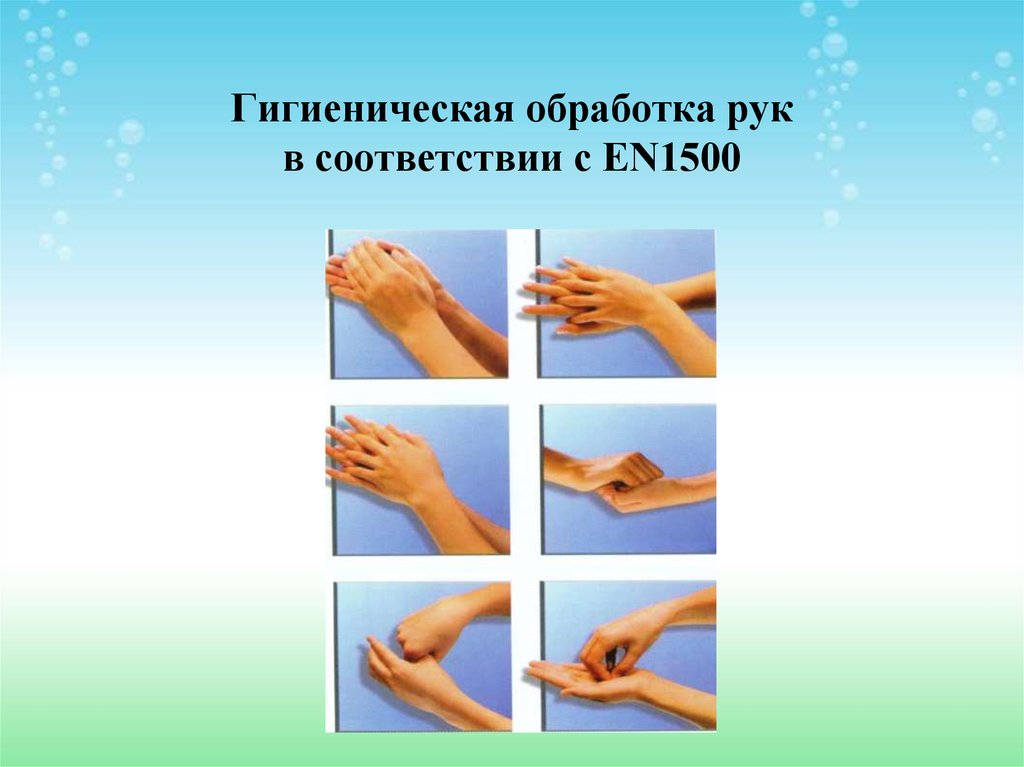
79. Гигиеническая обработка рук в соответствии с EN1500
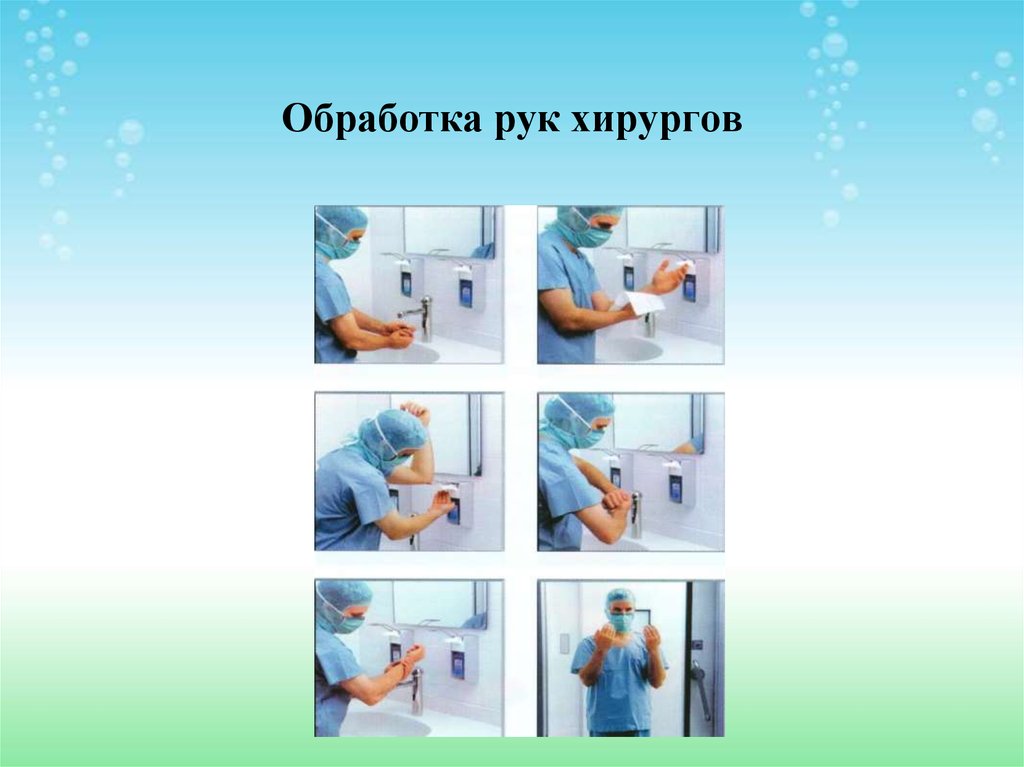
80. Обработка рук хирургов
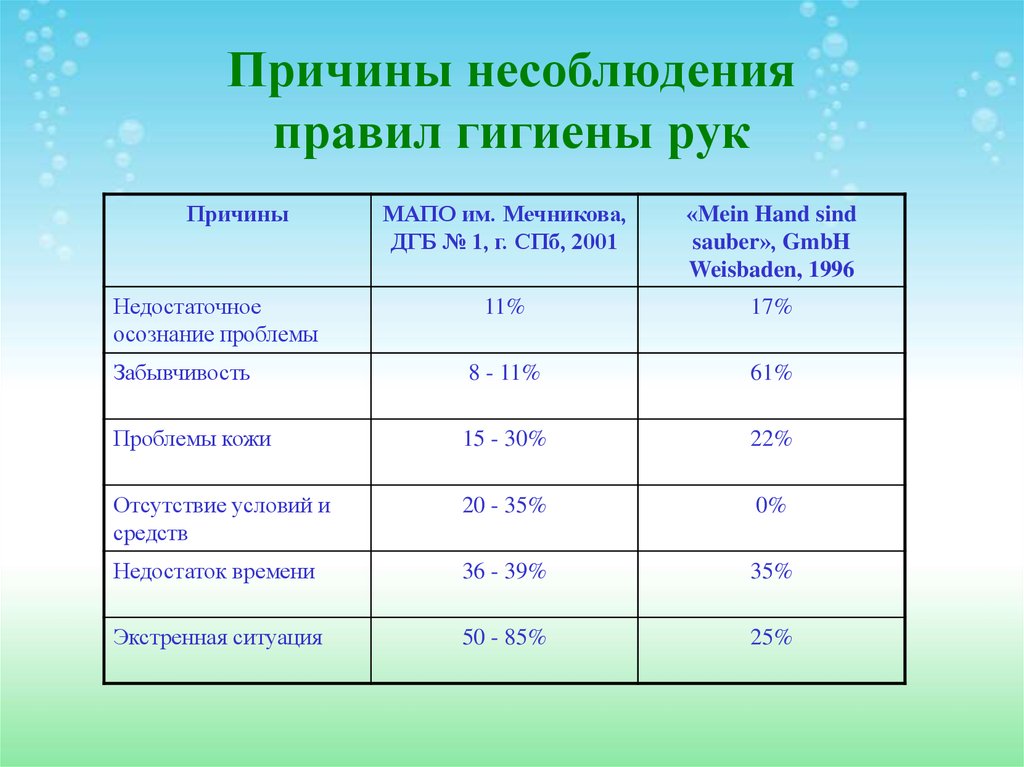
81. Причины несоблюдения правил гигиены рук
ПричиныМАПО им. Мечникова,
ДГБ № 1, г. СПб, 2001
«Mein Hand sind
sauber», GmbH
Weisbaden, 1996
11%
17%
Забывчивость
8 - 11%
61%
Проблемы кожи
15 - 30%
22%
Отсутствие условий и
средств
20 - 35%
0%
Недостаток времени
36 - 39%
35%
Экстренная ситуация
50 - 85%
25%
Недостаточное
осознание проблемы
82. Меры, направленные на снижение риска развития контактного дерматита, связанного с обработкой рук антисептиками:
уменьшение частоты использования раздражающихвеществ (особенно анионных моющих средств);
замена средств, обладающих сильным
раздражающим действием, на препараты,
повреждающие кожу в меньшей степени;
-обеспечение медицинского персонала
увлажняющими средствами ухода за кожей или
защитными кремами.
83. СанПиН 2.1.3.2630 – 10 «САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКИЕ ТРЕБОВАНИЯ К ОРГАНИЗАЦИЯМ, ОСУЩЕСТВЛЯЮЩИМ МЕДИЦИНСКУЮ ДЕЯТЕЛЬНОСТЬ»
12.6. Алгоритмы/стандарты всех эпидемиологическизначимых лечебных и диагностических
манипуляций должны включать в себя
рекомендуемые средства и способы обработки рук
при выполнении соответствующих манипуляций.
12.7. Необходимо осуществлять постоянный контроль
выполнения требований гигиены рук медицинскими
работниками и доводить эту информацию до
сведения персонала с целью повышения качества
медицинской помощи.
84.
Что мы втираем в кожу рук:2,4 % С4 – первомур
(смесь перекиси водорода и муравьиной кислоты)
- Использование щеток при мытье =>
травмирование эпидермиса кожи рук
- Раздражение кожи => химические ожоги рук
- Перчатки => формирование «перчаточного сока»
85. СанПиН 2.1.3.2630 – 10 «САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКИЕ ТРЕБОВАНИЯ К ОРГАНИЗАЦИЯМ, ОСУЩЕСТВЛЯЮЩИМ МЕДИЦИНСКУЮ ДЕЯТЕЛЬНОСТЬ»
12.3. Медицинский персонал должен бытьобеспечен в достаточном количестве
эффективными средствами для мытья и
обеззараживания рук, а также средствами для
ухода за кожей рук (кремы, лосьоны,
бальзамы и др.) для снижения риска
возникновения контактных дерматитов. При
выборе кожных антисептиков, моющих
средств и средств для ухода за кожей рук
следует учитывать индивидуальную
переносимость.
86.
СанПиН 2.1.3.2630 – 10«САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКИЕ ТРЕБОВАНИЯ К
ОРГАНИЗАЦИЯМ, ОСУЩЕСТВЛЯЮЩИМ МЕДИЦИНСКУЮ
ДЕЯТЕЛЬНОСТЬ»
12.8 Кожные антисептики для обработки рук должны быть
легко доступны на всех этапах лечебно-диагностического
процесса. В подразделениях с высокой интенсивностью ухода за
пациентами и нагрузкой на персонал (отделения реанимации и
интенсивной терапии и т. п.) дозаторы с кожными
антисептиками для обработки рук должны размещаться в
удобных для применения персоналом местах (у входа в палату,
у постели больного и др.). Следует также предусматривать
возможность
обеспечения
медицинских
работников
индивидуальными емкостями (флаконами) небольших объемов
(100—200 мл) с кожным антисептиком.
87. СанПиН 2.1.3.2630 – 10 «САНИТАРНО-ЭПИДЕМИОЛОГИЧЕСКИЕ ТРЕБОВАНИЯ К ОРГАНИЗАЦИЯМ, ОСУЩЕСТВЛЯЮЩИМ МЕДИЦИНСКУЮ ДЕЯТЕЛЬНОСТЬ»
12.9.3. Обработку операционного поля пациентаперед хирургическим вмешательством и
другими манипуляциями, связанными с
нарушением целостности кожных покровов
(пункции, биопсии), предпочтительно
проводить антисептиком, содержащим
краситель.
88. Условия качественного обеззараживания рук
- ухоженные руки;- отсутствие искусственных ногтей;
- коротко обрезанные ногти, не покрытые
лаком;
- отсутствие ювелирных украшений (колец,
браслетов, наручных часов);
- точное соблюдение техники обработки рук
89.
ОРГАНИЗАЦИЯ ИПРОВЕДЕНИЕ
МЕРОПРИЯТИЙ ПО
БОРЬБЕ С
ПЕДИКУЛЕЗОМ
89
90. ОРГАНИЗАЦИЯ И ПРОВЕДЕНИЕ МЕРО-ПРИЯТИЙ ПО БОРЬБЕ С ПЕДИКУЛЕЗОМ
ОРГАНИЗАЦИЯ И ПРОВЕДЕНИЕ МЕРОПРИЯТИЙ ПО БОРЬБЕ С ПЕДИКУЛЕЗОМНормативные документы
Приказ № 342 от 26.11.1998г МЗ РФ «Об
усилении мероприятий по профилактике
эпидемического сыпного тифа и борьбе с
педикулезом»
Педикулез или вшивость – специфическое
паразитирование на человеке вшей,
питающихся кровью
90
91. ОРГАНИЗАЦИЯ И ПРОВЕДЕНИЕ МЕРО-ПРИЯТИЙ ПО БОРЬБЕ С ПЕДИКУЛЕЗОМ
• Каждый выявленный случай головного,платяного и смешанного педикулеза
регистрируют в «Журнале учета
инфекционных заболеваний» (ф. 060у)
• Передача экстренного извещения в ФГУЗ
гигиены и эпидемиологии Архангельской
области.
• Учету подлежат лица, у которых при осмотре
выявлены вши в любой стадии развития
(яйцо-гнида, личинка, взрослое насекомое)
91
92. ОРГАНИЗАЦИЯ И ПРОВЕДЕНИЕ МЕРО-ПРИЯТИЙ ПО БОРЬБЕ С ПЕДИКУЛЕЗОМ
Кратность обследования для выявления вшей• Детские дошкольные учреждения – ежедневно
• Школы- 4 раза в год после каникул; ежемесячновыборочно
• Школы-интернаты, СПТУ – 1 раз в неделю
• Стационары –
при поступлении больных
1 раз в 10 дней
• Поликлиника – на поликлиническом приеме
92
93. ОРГАНИЗАЦИЯ И ПРОВЕДЕНИЕ МЕРО-ПРИЯТИЙ ПО БОРЬБЕ С ПЕДИКУЛЕЗОМ
• Основные симптомы педикулеза:• Зуд
• Огрубение кожи от массовых укусов вшей и воздействия
слюны насекомых
• Меланодермия
• Колтун
• На человеке паразитируют три вида вшей
• Платяная (нательное белье, верхняя одежда, постельное
белье, обувь)
• Головная (волосы головы, груди, подмышек, борода, усы,
брови, ресницы)
• Лобковая (волосы лобка, груди, подмышек, борода, усы,
брови, ресницы, голова у детей)
93
94. ОРГАНИЗАЦИЯ И ПРОВЕДЕНИЕ МЕРО-ПРИЯТИЙ ПО БОРЬБЕ С ПЕДИКУЛЕЗОМ
Методика проведения обработки лиц, пораженныхголовным педикулезом:
На волосистую часть головы наносят препарат (педикулицид),
затем голову плотно повязывают косынкой и выдерживают
экспозицию согласно МУ на данный препарат
0,15% водная эмульсия карбофоса (10-50 мл)
20% водно-мыльная суспензия бензилбензоната (10-30 мл)
Шампунь Веда
Препарат смывают теплой водой с применением моющего
средства
Волосы ополаскивают 5-10% теплым раствором уксусной
кислоты, что способствует снятию гнид, которые необходимо
тщательно вычесывать частым гребнем.
94
95. ОРГАНИЗАЦИЯ И ПРОВЕДЕНИЕ МЕРОПРИЯТИЙ ПО БОРЬБЕ С ПЕДИКУЛЕЗОМ
Обработка педикулицидами запрещается
беременных
кормящих женщин
людей с поврежденной кожей
дети
Для уничтожения всех видов вшей на нательном и постельном белье
рекомендуется кипячение в 1-2% содовом растворе в течении 15-20 мин
после закипания
• Вещи, не подлежащие кипячению, проглаживают горячим утюгом через
влажную ткань, а так же используют инсектицидные мыла
• Для дезинфекции помещений при платяном и смешанном педикулезе
применяют:0,15% р-р карбофоса, 0,5% водный р-р хлорофоса, средства
«Медифокс», ээрозольные баллоны типа «Прима», «Дихлофос»
• Дезинфекцию проводят при открытых окнах и форточках. По
окончании экспозиции проводят влажную уборку
95






















































































 Медицина
Медицина