Похожие презентации:
Токсикологични изследвания. Количествена оценка на токсичния отговор. Видове дози и методи за определяне. Лабораторна практика
1.
Токсикологични изследвания.Количествена оценка на токсичния
отговор. Видове дози и методи за
определяне. Добра лабораторна
практика
доц. М. Кондева-Бурдина
2.
ЕКСПОЗИЦИЯ И ДОЗАЕкспозиция – контакт, предоставящ възможност за
получаване на увреждаща доза.
Доза - количеството вещество, което постъпва в
организма при съответната експозиция.
Представя се като mg от веществото/kg телесна маса = mg/kg
Дозата е най-важният определящ фактор в токсичността.
Дозата зависи от:
* Концентрацията на веществото в околната среда
* Свойствата на веществото (токсиканта)
* Честота и продължителност на експозицията с токсиканта
* Пътища на експозицията с токсиканта – белодробен, дермален,
ГИТ, венозен
3.
ВИДОВЕ ДОЗИ (при in vivo експерименти) и КОНЦЕНТРАЦИИ (при invitro експерименти) – в зависимост от крайния ефект, който се цели
да се постигне:
ED: Ефективна доза
EC: Ефективна концентрация
ED50: Доза, при която у 50% от опитните животни се регистрира терапевтичен
ефект
EC50: Концентрация с 50% ефект
LD50: Доза, причиняваща 50% смъртност при опитните животни
LC50: Концентрация, причиняваща 50% смъртност
TD50: Доза, причиняваща проява на токсичен ефект при 50% от опитните
животни
TC50: Концентрация, причиняваща 50% токсичност
4.
Прагова доза (Threshold): Дозата, при която се появява токсичниятeфект, се нарича прагова доза
TI: Терапевтичен индекс TI=TD50(LD50)/ED50
MOS: Margin of Safety – Допустима граница на безопасност MOS=TD1/ED99
NOАEL: Доза, която се прилага многократно, без да предизвика нежелан
ефект. NOAEL се използва, за да се определят пределно допустимите
стойности за дневна доза на химични вещества, напр. адитиви в
храната
LOAЕL: Най-малката доза, при която се проявяват нежелани ефекти
Индекс (степен) на резорбция: LD50 p.o./LD50 i.v.
5.
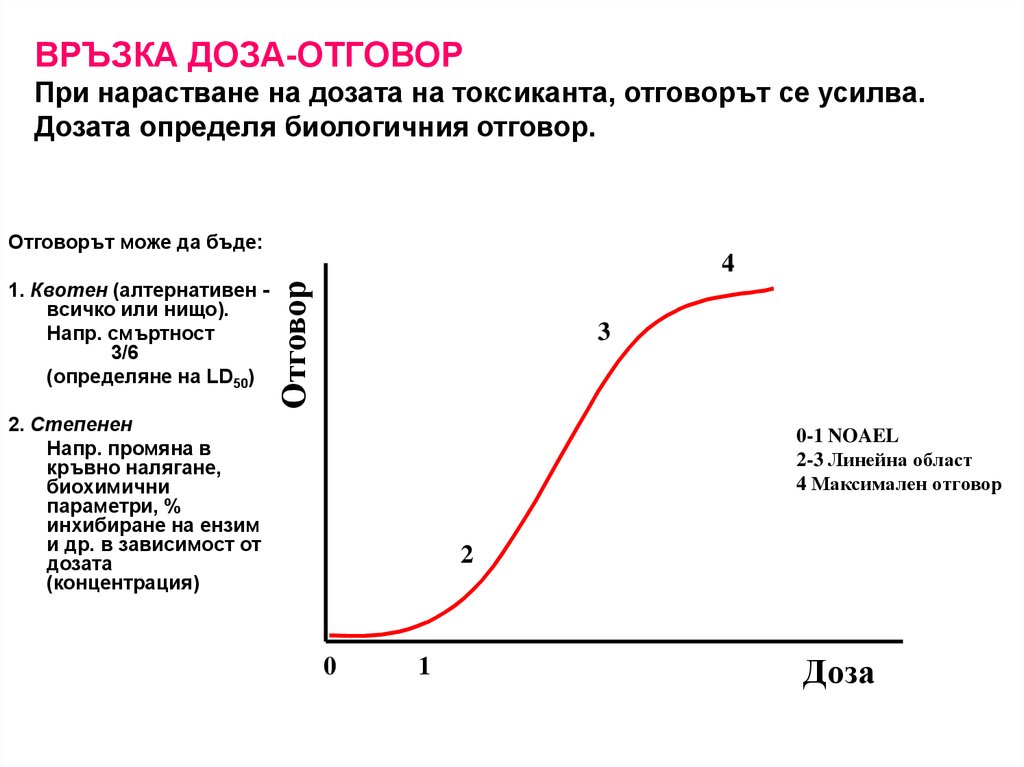
ВРЪЗКА ДОЗА-ОТГОВОРПри нарастване на дозата на токсиканта, отговорът се усилва.
Дозата определя биологичния отговор.
Отговорът може да бъде:
1. Квотен (алтернативен всичко или нищо).
Напр. смъртност
3/6
(определяне на LD50)
Отговор
4
3
2. Степенен
Напр. промяна в
кръвно налягане,
биохимични
параметри, %
инхибиране на ензим
и др. в зависимост от
дозата
(концентрация)
0-1 NOAEL
2-3 Линейна област
4 Максимален отговор
2
0
1
Доза
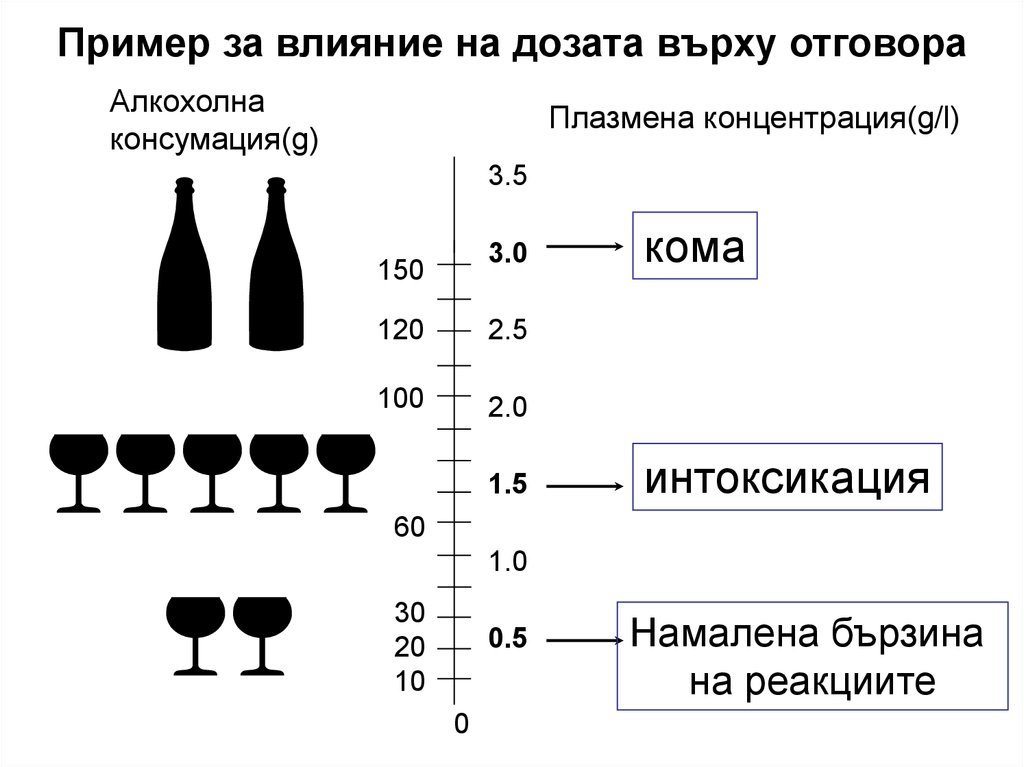
6.
Пример за влияние на дозата върху отговораАлкохолна
консумация(g)
Плазмена концентрация(g/l)
3.5
3.0
150
120
2.5
100
2.0
1.5
кома
интоксикация
60
1.0
30
20
10
0.5
0
Намалена бързина
на реакциите
7.
Ботулиновият токсин тип А е
невротиксин, продуциран от Gram (+)
бактерия Clostridium botulinum. Това е
най-мощният биологичен невротоксин,
инхибиращ освобождаването на
ацетилхолин.
Симптоми на ботулизъм: сухота в
устата, неясен говор, двойно виждане,
блокиране на дишането.
LD50 на ботулиновия токсин:
0,0001mg/kg.
Влиза в състава на продукт използван
е клиниката – пластичната хирургия
(много ниски дози – pg/kg) – BOTOX®
(i.m.)
8.
ТОКСИКОЛОГИЧНИ ИЗСЛЕДВАНИЯ, чрезизползване на in vivo методи
• Определяне на токсичност при еднократно
третиране – остра токсичност (LD50)
• Определяне на токсичност при многократно
третиране – подостра, субхронична и хронична
9.
ОСТРА ТОКСИЧНОСТ – ОПРЕДЕЛЯНЕ НА LD50Острата токсичност е качествено и количествено изследване на токсичния
ефект в резултат на еднократно прилагане на активно действащо
вещество (субстанция) или вещества в определени съотношения.
Острата токсичност е способността на една химическа субстанция да
предизвика токсични ефекти и смърт за “относително кратък период от
време”, след еднократно прилагане.
“Относително кратък период” – няколко минути, часове (24 часа) или дни
(14), но не повече.
Тестуват се чисти субстанции и по-рядко смеси от две или повече
вещества.
Използват се животни (бозайници) от най-малко два различни вида.
Експериментите най-често се провеждат на гризачи.
Път на въвеждане – перорален (p.o.), парентерален (i.v.; i.p.), инхалаторен,
дермален. Най-често се прилагат два пътя на въвеждане, като единият
задължително е i.v.(i.p.), а другият – този, по който веществото ще се
прилага в клиничната практика (p.o.; инхалаторен; дермален).
10.
Най-широко застъпено е определянето на перорална остра токсичност
(LD50 p.o.), тъй като по този начин се прилагат повечето лекарства,
могат да постъпят отрови и битови вещества.
Стойностите на LD50 зависят от:
- вид и възраст на животните
- път на въвеждане – p.o.; i.v.(i.p.); дермален
Например: За веществото А са установени различни стойности на LD50
в зависимост от пътя на въвеждане:
- LD50 (i.p., плъх) – 15mg/kg
- LD50 (p.o., плъх) – 56mg/kg
- LD50 (дермално, плъх) – 75mg/kg
Приложение на LD50:
- Определяне на терапевтичен индекс
- Определяне степен на резорбция
- Сравняване на различни вещества – потенциални лекарства. Като
правило, колкото по-ниска е стойността на LD50, толкова по-токсично е
даденото вещество.
Например: Вещество с LD50 = 5mg/kg е много по токсично от вещество
с LD50 = 200mg/kg.
- При сравняване на нови вещества със съответен стандарт.
11.
КЛАСИФИКАЦИИ ЗА ТОКСИЧНОСТ НА ВЕЩЕСТВАТА – взависимост от стойностите на LD50
Hodge&Sterner
Stallard&Whitehead, J Drug Inf, 1997
LD50
ОПРЕДЕЛЕНИЕ
LD50
ОПРЕДЕЛЕНИЕ
< 1mg/kg
Изключително
токсично
< 25 mg/kg
Силно токсично
1-50 mg/kg
Високо токсично
25-200 mg/kg
Токсично
50-500 mg/kg
Умерено токсично
200-2000 mg/kg
Вредно
500-5000 mg/kg
Слабо токсично
> 2000 mg/kg
Неопределена
токсичност
5000-15000 mg/kg Практически
нетоксично
> 15000 mg/kg
Относително
безвредно
12.
Принципи при определяне на остратоксичност
• Избор на животински видове
Най-подходящи са тези животински видове, които метаболизират
веществото, както при човека – това позволява да се екстраполират
данните. Това рядко може да се реалзира.
Друг подход е острата токсичност да се провежда върху различни
животински видове, като се предполага, че токсичният отговор, проявил
се в животинските видове може да се прояви и при човека. Най-често –
мишки, плъхове, морски свинчета, зайци (млади, здрави, полово зрели
животни).
Условия за отглеждане на експерименталните животни
- температура 22 ± 3°С.
- относителна влажност – 30-70%
- цикъл – светлина/тъмнина – 12/12 часа
- храна и вода - стандартизирани
Животните могат да се разделят по пол или да са в индивидуални кафези.
Гризачите – на групи, обикновено не повече от 3 животни в кафез. Поголеми животни (като кучета и зайци) – индивидуално.
13.
• Подготовка на животнитеПреди началото на опита, животните трябва да се аклиматизират
поне 5 дни в лабораторни условия. Преди прилагане на
веществото, храната се отнема. За плъхове – едно денонощие
преди опита, за мишки – 3-4 часа преди опита.
• Подготовка на дозите
Тест-субстанцията се разтваря или суспендира, за предпочитане във
вода. Ако веществото не е разтворимо във вода, се предпочита
маслен разтвор или емулсия, ако и това не е възможно се
използва органичен разтворител. В този случай трябва да се
изследва токсичността на разтворителя.
• Прилагане на веществото
Съобразен с пътя на прилагане, който се предвижда при хора –
перорален, парентерален, инхалаторен, дермален.
14.
• Наблюдения по време на експериментаПри определяне на остра токсичност, животните се наблюдават от 24
часа до 14 дни. При летален изход в рамките на този период, както
и на животните преживели периода, са прави аутопсия и
хистопатология. По време на периода се отчитат всички промени
в поведението, физиологичното (телесна маса) и здравословното
им състояние.
Опитите с ескперименталните животни се провеждат в съответствие
с Наредба №15 за минимални изисквания, за защита и хуманно
отношение към опитните животни (ДВ бр.17, 2006) и Европейската
наредба за работа с експериментални животни.
15.
МЕТОДИ ЗА ОПРЕДЕЛЯНЕ НА ОСТРА ТОКСИЧНОСТ• Метод на Личфийлд-Уилкоксон
Използват се плъхове и мишки, от двата пола, разделени в групи по 10
животни.
Изследваното вещество се прилага по два пътя – i.v. (i.p.) и пътя, по който
ще бъде прилагано – p.o.; дермален; инхалаторен.
Избор на дозите – включва очаквани стойности на LD50. Тези стойности
могат да се вземат от изследвания на остра токсичност на вещества с
близка структура, или да се определят след пилотни изследвания.
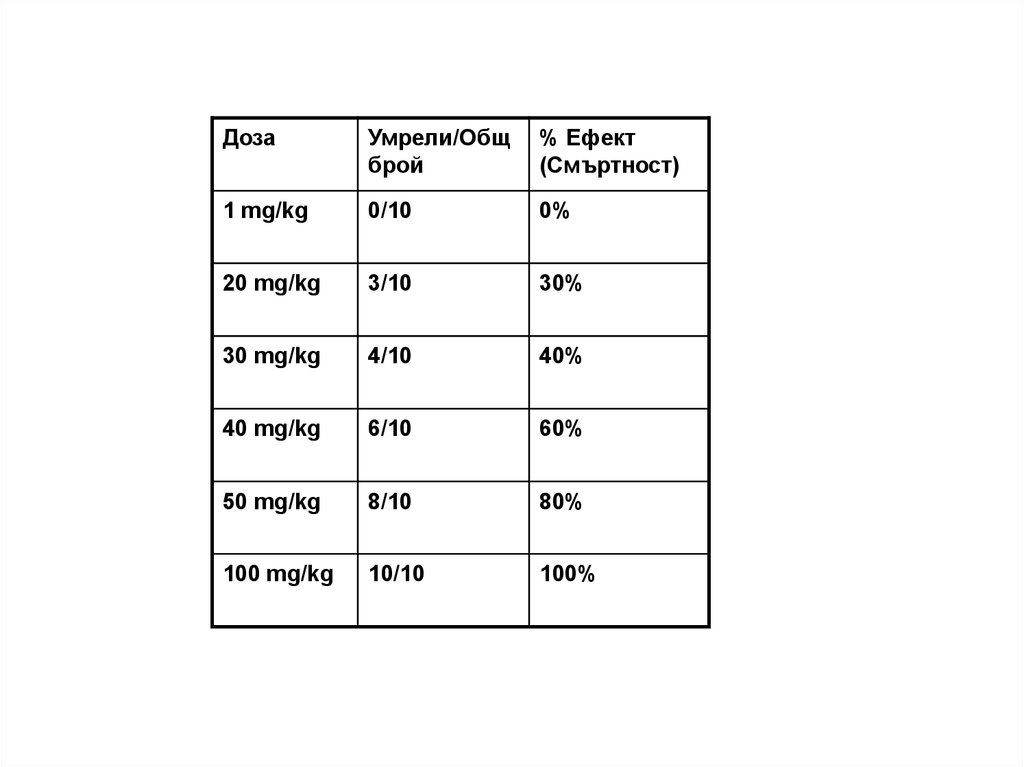
Например: Провежда се пилотно изследване с 3 животни и две дози
1mg/kg и 100mg/kg. Установява се при първата доза не се наблюдава
летален ефект (0/3), а при втората доза и трите животни умират (3/3). В
този случай се очакват стойности на LD50 в границата между 1mg/kg и
100mg/kg. Избират се 6 дозови нива в този интервал (1, 20, 30, 40, 50,
100mg/kg).
16.
ДозаУмрели/Общ
брой
% Eфект
(Смъртност)
1 mg/kg
0/10
0%
20 mg/kg
3/10
30%
30 mg/kg
4/10
40%
40 mg/kg
6/10
60%
50 mg/kg
8/10
80%
100 mg/kg
10/10
100%
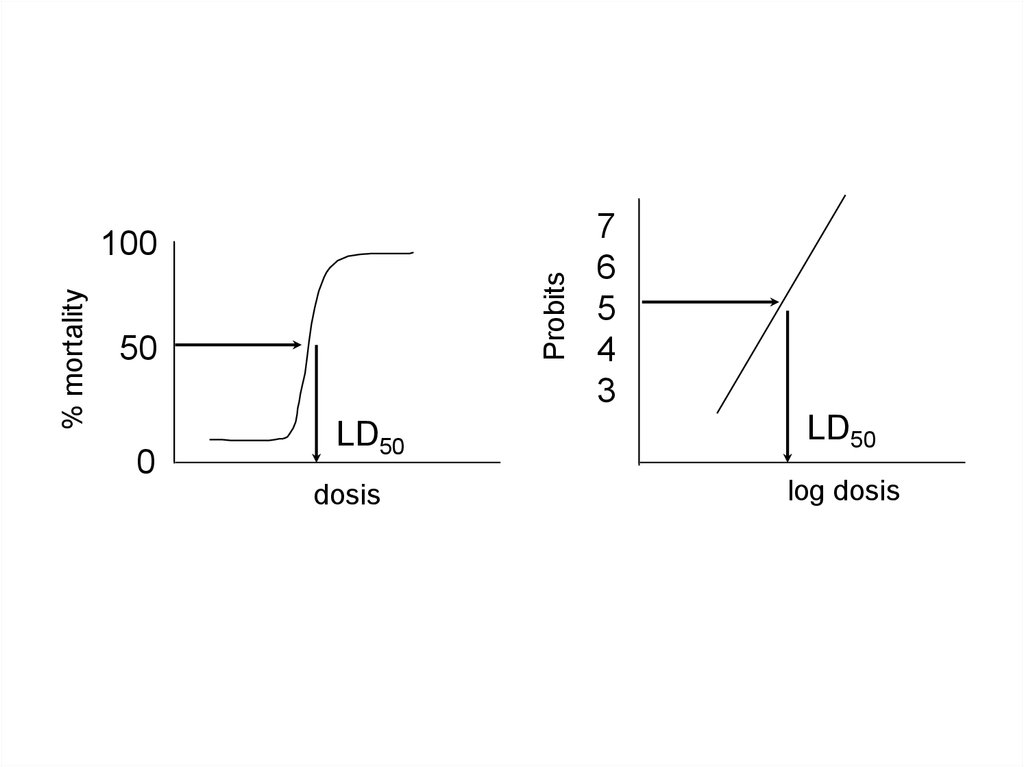
17.
Probits% mortality
100
50
0
LD50
dosis
7
6
5
4
3
LD50
log dosis
18.
Определяне на LD50 на комбинация от вещества по метода на
Финей
При оценка на токсичността при лекарствени комбинации се използва
методът на Финей. Съгласно този метод се определя LD50 на
комбинацията и поотделно на компонентите, влизащи в нея.
1
LD50 (А+B+C)
Е
=
fA
LD50 (А)
+
fB
LD50 (B)
+
fc
LD50 (C)
F
където:
LD50 (A+B+C) – средна летална доза на комбинацята от вещества ABC,
определена експериментално
LD50 (A); LD50 (B); LD50 (C) – средни летални дози на веществата А, В, С –
определени експериментално
fA; fB; fC – са частите на отделните вещества от комбинацията АВС.
Лявата страна на уравнението (Е) представлява експериментално
определената стойност на LD50 на комбинацията от вещества.
Дясната страна на уравнението (F) представлява теоритично
изчислената по Финей стойност на LD50.
19.
Съотношението Е/F дава възможност да се определивзаимодействието между отделните компоненти на комбинацията
от вещества.
Е/F = 1 – адитивен ефект (1+1=2)
Например: Сулфаметоксазол+Триметоприм (Co-trimoxazole Biseptol)
самостоятелно двете лекарства – бактериостатичен ефект
в комбинация – бактерициден
E/F < 0.57 – антагонизъм (антидоти)
- функционален – Кофеин и Фенобарбитал
- химичен – Димеркапрол и As
- рецепторен – Атропин и ФОС
- антагонизъм на кинетично ниво – тетрациклини и Ca2+ йони (на
ниво резорбция)
E/F > 1.75 – потенциране (синергизъм) (1+1=10) – самостоятелно не се
наблюдава токсичен ефект, а в комбинация
Например: Дисулфирам + Алкохол
Дисулфирам приложен самостоятелно няма изразен токсичен
ефект. В комбинация с алкохол (малка доза) се наблюдава изразен
токсичен ефект – хипертонична криза, главоболие, световъртеж,
повръщане, колапс.
20.
• Метод на фиксираните дозиОсновава се на въвеждането на ограничен брой дози на малък брой
опитни животни. Подборът на дозите се извършва така, че да се
получат видими токсични ефекти (но не смъртност). Животните се
наблюдават след прилагането на няколко дози, като се
регистрират проявените токсични ефекти.
Предимства на метода:
- Използват се по-малък брой опитни животни
- Не се цели летален изход
- Животните се предпазват от прекомерен стрес и болка
- Осигурява се възможност за класифициране на веществата по
риска от предизвикване на остри токсични ефекти
- Получава се информация необходима за оценка на токсичните
ефекти при хора.
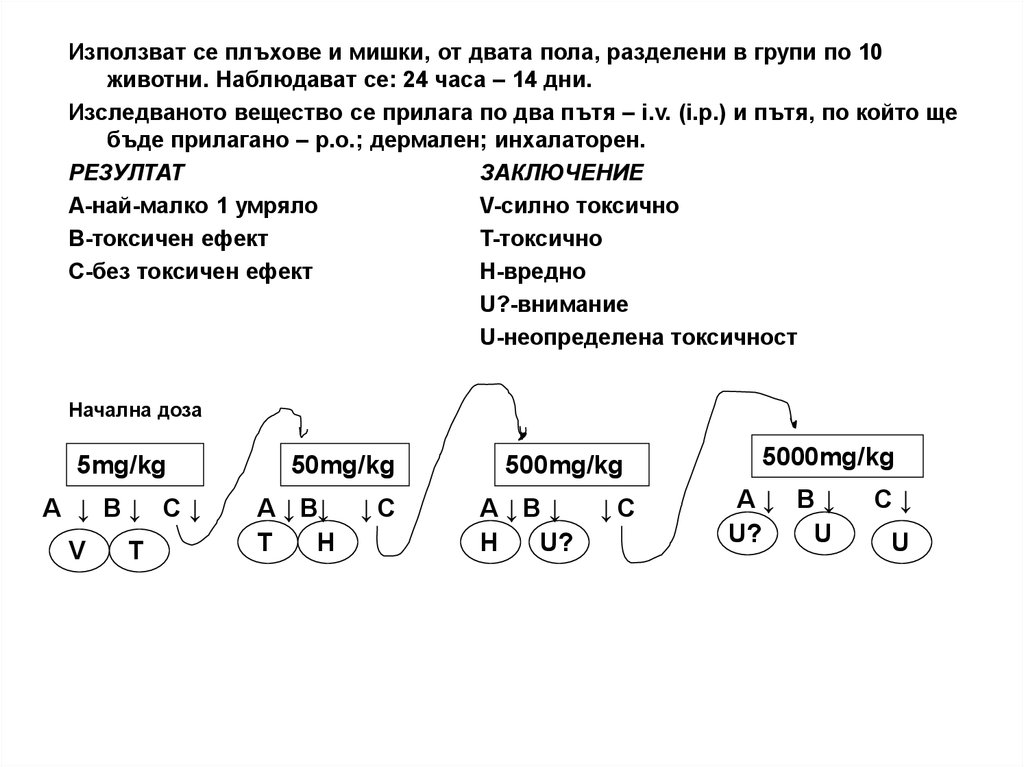
21.
Използват се плъхове и мишки, от двата пола, разделени в групи по 10животни. Наблюдават се: 24 часа – 14 дни.
Изследваното вещество се прилага по два пътя – i.v. (i.p.) и пътя, по който ще
бъде прилагано – p.o.; дермален; инхалаторен.
РЕЗУЛТАТ
ЗАКЛЮЧЕНИЕ
А-най-малко 1 умряло
V-силно токсично
В-токсичен ефект
T-токсично
С-без токсичен ефект
H-вредно
U?-внимание
U-неопределена токсичност
Начална доза
5mg/kg
А ↓ В↓ С↓
V
T
50mg/kg
А ↓ В↓ ↓ С
T
H
500mg/kg
А ↓В ↓
H
U?
↓С
5000mg/kg
А↓ В↓
U?
U
С↓
U
22.
Определяне на LD50 – Up and Down процедура (UDP) (Guideline 425,
1998 на EMEA)
Основен принцип – намаляване броя на животните. Използват се животни от
един пол. Установено е, че средният брой животни, които се използват е 69.
Избор на начална доза – базира се на цялата налична информация за
веществото, на изследвания на вещества с подобна структура, на
установена връзка структура-действие.
Ако няма информация за веществото, че не проявява токсичен ефект, се
провежда лимитиращ тест – въвежда се максимална доза 2000mg/kg или
5000mg/kg и ако животните не умрат или не се наблюдава токсичен ефект –
веществото се определя като нетоксично.
Когато няма никаква информация за веществото се започва с по-ниски дози
(напр. 5mg/kg).
Използват се плъхове или мишки, разделени в групи по 2 животни.
Наблюдават се: 24 часа – 14 дни.
Изследваното вещество се прилага по два пътя – i.v. (i.p.) и пътя, по който ще
бъде прилагано веществото – p.o.; дермален; инхалаторен.
В зависимост от изхода (преживяемост/токсичен ефект/смърт), дозата за
следващото животно се повишава или намалява. Резултатът се въвежда и
компютърната програма определя следващата доза и максималната
използвана доза.
Последните два метода са подходящи за вещества – замърсители на околната
среда, използвани консерванти и др. и по-рядко за вещества – потенциални
лекарства.
23.
ТОКСИЧНОСТ ПРИ МНОГОКРАТНО ПРИЛАГАНЕ• ПОДОСТРА
Цели да се проследят токсичните ефекти, в резултата на многократна експозиция
на организма към по-ниски дози от изследваното вещество. Обикновено
изследването продължава 2 седмици.
• СУБХРОНИЧНА
Цели да се проследят токсичните ефекти на веществото, в резултата на
многократното му прилагане в рамките на 90 дни.
• Един вид – плъхове, двата пола
• Три дози
• 10 плъха от всеки пол за доза
• Опитната група се сравнява с контролна
• Отчита се смъртност, телесно тегло, консумация на храна, хематология и
биохимия.
• Макроскопско и микроскопско охарактеризиране на органите и тъканите.
Използва се, за да се определи NOAEL, т.е. дава възможност да се определят
дозовите нива, при които не се проявяват токсични ефекти. Резултатите от
такова изследване може да предоставят информация , която ще е полезна при
подбора на дозови нива при хронична токсичност, репродуктивна токсичност
и канцерогенеза.
24.
• ХРОНИЧНАЦели да се проследят токсичните ефекти на изследваното вещество,
които не се проявяват веднага, но които в резултата на попродължителното му прилагане, могат да доведат до появата на
нежелани ефекти. Тя дава информация за кумулативната токсичност
на веществото, таргетните органи и за проявата на толерантност на
веществото при продължителна експозиция на по-ниски дози.
• Нови вещества – потенциални лекарства, след проведени
фармакологични изследвания и определяне на остра токсичност;
хранителни добавки, консерванти, стабилизатори и др.
• Продължителност на изследването – 6 месеца до 2 години
• Прилага се поне три дози
• Животни поне 2 вида, от които единият задължително - плъхове или
мишки, вторият е друг вид (може да са кучета – 4-6 месечни, не
повече от 9 месечни).
• Животните да са от двата пола, половозрели.
• Опитната група се сравняна с контролната.
• Брой животни: 10-20 мъжки + 10-20 женски – за гризачи
6-8 мъжки + 6-8 женски – други
Изследваното вещество се прилага по два пътя – i.v. (i.p.) и пътя, по
който ще бъде прилагано – p.o.; дермален; инхалаторен
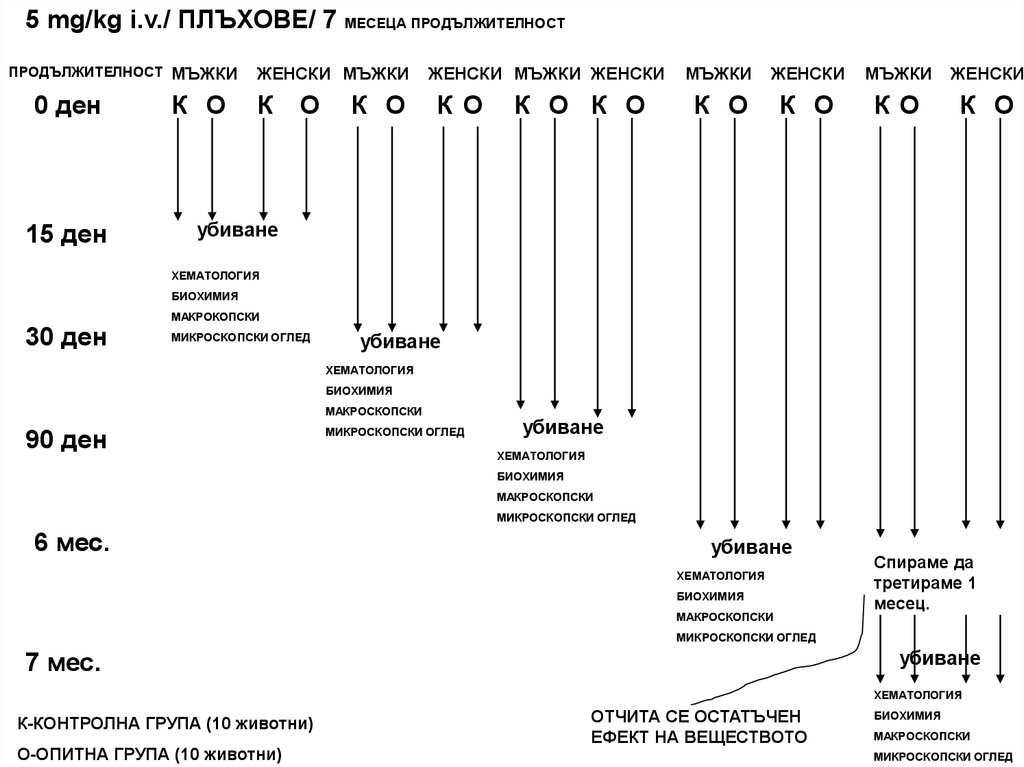
25.
5 mg/kg i.v./ ПЛЪХОВЕ/ 7 МЕСЕЦА ПРОДЪЛЖИТЕЛНОСТПРОДЪЛЖИТЕЛНОСТ
0 ден
15 ден
МЪЖКИ
ЖЕНСКИ МЪЖКИ
К О
К
О
К О
ЖЕНСКИ МЪЖКИ ЖЕНСКИ
КО
К О К О
МЪЖКИ
ЖЕНСКИ
МЪЖКИ
ЖЕНСКИ
К О
К О
КО
К О
убиване
ХЕМАТОЛОГИЯ
БИОХИМИЯ
30 ден
МАКРОКОПСКИ
МИКРОСКОПСКИ ОГЛЕД
убиване
ХЕМАТОЛОГИЯ
БИОХИМИЯ
МАКРОСКОПСКИ
90 ден
МИКРОСКОПСКИ ОГЛЕД
убиване
ХЕМАТОЛОГИЯ
БИОХИМИЯ
МАКРОСКОПСКИ
МИКРОСКОПСКИ ОГЛЕД
6 мес.
убиване
ХЕМАТОЛОГИЯ
БИОХИМИЯ
МАКРОСКОПСКИ
Спираме да
третираме 1
месец.
МИКРОСКОПСКИ ОГЛЕД
убиване
7 мес.
ХЕМАТОЛОГИЯ
К-КОНТРОЛНА ГРУПА (10 животни)
О-ОПИТНА ГРУПА (10 животни)
ОТЧИТА СЕ ОСТАТЪЧЕН
ЕФЕКТ НА ВЕЩЕСТВОТО
БИОХИМИЯ
МАКРОСКОПСКИ
МИКРОСКОПСКИ ОГЛЕД
26.
ТОКСИКОЛОГИЧНИ ИЗСЛЕДВАНИЯ НА ВЕЩЕСТВАТА ЗАОЧНА И КОЖНА ПОНОСИМОСТ
Кожната поносимост на веществата обикновено се определя върху зайци. Козината се бръсне,
като се внимава да няма наранявания, които да компрометират резултатите.
-Веществото се прилага върху кожата и се оставя за период от 60 min, 24 часа, 48 часа и 72 часа.
-Степента на кожното дразнещо действие се отчита чрез:
- определяне степен на зачервяване, образуване на едем.
Тест за кожна поносимост
Кожно дразнещо действие
Кожна реакция
Точки
Зачервяване
няма зачервяване
слабо зачервяване
добре изразено зачервяване
умерено към тежко зачервяване
тежко зачервяване
0
1
2
3
4 (max)
Образуване на едем
няма отток (едем)
слабо изразен отток
добре изразен отток
умерен отток
тежък отток
0
1
2
3
4
Draize JH&Kelley EA. Toxicology, 1; 1959: pp 267
27.
Класификация на веществата по тяхното локално дразнещо действиевърху кожата
Липса на дразнещо действие
Незначително дразнещо действие
Меко дразнещо действие
Умерено дразнещо действие
Силно дразнещо действие
0 точки
0-0,5 точки
0,5-2,5 точки
2,5-5,0 точки
5,0-8,0 точки
Auletta CS. Basic Clin Pharmacol Toxicol, 95; 2004: pp 201
Очната поносимост на веществата също се определя върху зайци.
Използва се очен тест на Draize, за отчитане локалното дразнещо
действие на веществата върху окото.
При този тест изследваното вещество се поставя в конюнктивалният
сак в окото на зайци. При този тест се използва точкова система,
която отчита промените, които настъпват в корнеата, конюнгтивата
и ириса в резултат на действието на веществото.
За да се намали броя на експерименталните животни и болката са
въведени in vitro алтернативни методи на метода на Draize.
28.
ОПРЕДЕЛЯНЕ НА ОТДАЛЕЧЕНИ ТОКСИЧНИ ЕФЕКТИИзследвания за токсичност върху репродуктивната функция, ембриофетална и
перинатална токсичност, мутагенност, канцерогенност, чрез използването на in vivo
методи.
Специализираните токсикологични изследвания включват три вида експерименти:
- Определяне тератогенният потенциал на веществата – да се изясни влиянието на
веществата върху репродуктивния цикъл при лабораторни условия.
In vivo метод: върху бременни плъхове, порода Wistar.
In vitro метод: ембрионални Stem клетки – получени от миши и заешки ембриони, в
стадий на морула и бластула. Те се характеризират с неограничена и
недиференцирана пролиферация.
- Специализирани изследвания за мутагенност – да се определи потенциала на
лекарството да индуцира мутации в клетките, т.е. увреждане на генетичния материал.
Използват се цитогенетични методи.
In vitro метод: използване на бактериални клетъчни системи (тест на Ames).
- Определяне потенциала за карциногенност – в случаите, когато лекарственото
средство е предназначено за продължителна терапия или се отличава с химична
структура с дефинирани вече увреждащи ефекти върху клетките.
29.
ТОКСИКОЛОГИЧНИ ИЗСЛЕДВАНИЯ, чрезизползване на in vitro методи
Съгласно ECVAM (European Center for the Validation of Alternative
Methods) с оглед намаляване броя на експерименталните животни са
разработени алтернативни in vitro методи за оценка токсичният
потенциал на веществата и механизмите на токсичност.
- субклетъчни фракции (S9 фракция, съдържаща цитозол и
микрозоми; микрозомална фракция; изолирани синаптозоми)
- клетъчна суспензия (изолирани плъши хепатоцити)
- първични клетъчни култури (първични култури от плъши
хепатоцити)
- ко-култури (например: хепатоцити + Купферови клетки)
- клетъчни линии (безсмъртни – HepG2)
- тъканни срезове (чернодробни)
- изолирани и перфузирани органи (черен дроб, око, бъбрек)
30.
G.L.P. (Добра лабораторна практика)Система от правила и общопризнати стандарти за планиране,
организиране, провеждане, контролиране, документиране и отчет на
лабораторните изследвания, която има за цел да осигури висок
стандарт на изследванията
Организация
Водещ изследовател – лице, отговорно за цялостният процес на
проучването в научно-изследователската лаборатория
Екип от квалифицирани специалисти (аналитици,
експериментатори - фармаколози, токсиколози,
патоморфолози и др.), координиращи своята дейност съобразно
целите на проекта и отговарящи за представянето и анализа на
резултатите
Лаборатория, отговаряща на изискванията на GLP – апаратура,
персонал, методични възможности, експериментални животни,
манипулационна, тест-субстанции, тегловна, компютърна техника
и системи, осигуряващи провеждането на експеримента.
31.
G.L.P.• Планиране
Протоколи
Стандартно действащи процедури, осигуряващи
точност и качество на получените данни
• Изпълнение
Изисквания към експерименталните животни,
съобразени с регулаторните изисквания и
използваните материали (вкл. тест-субстанция и
референтна субстанция – пълна информация за
тяхната идентичност, характеристика и съхранение)
Колекциониране и документиране на данни
Обработка, обобщаване и подготовка на отчетен доклад
























 Медицина
Медицина








