Похожие презентации:
Биологически важные поли- и гетерофункциональные соединения
1. Биологически важные поли- и гетерофункциональные соединения
Биологически важные полии гетерофункциональныесоединения
2. Поли- и гетерофункциональные соединения обладают типичной реакционной способностью
Взаимное влияние функ. группприводит к появлению
специфических свойств
3. Полифункциональные соединения
Многоатомные спиртыДвухатомные фенолы
Двухосновные кислоты
Полиамины
4.
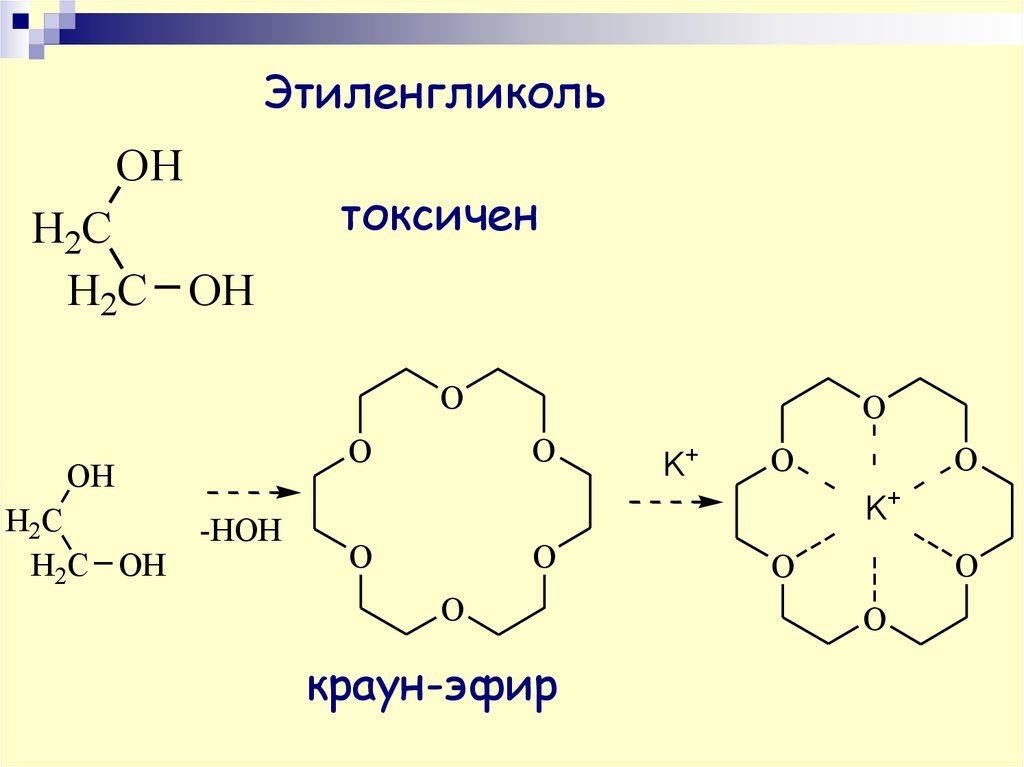
ЭтиленгликольOH
H2C
H2C OH
токсичен
O
H2C
H2C OH
O
O
OH
-HOH
O
K+
O
O
K+
O
O
O
краун-эфир
O
O
O
5.
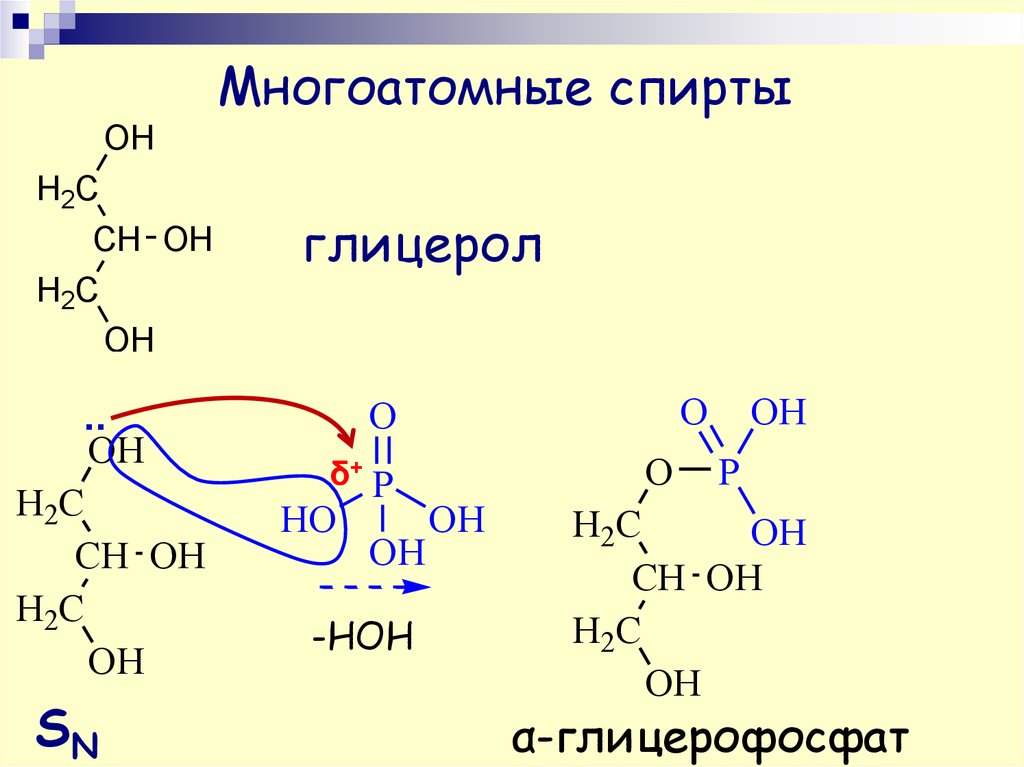
Многоатомные спиртыOH
H 2C
CH OH
H 2C
OH
..
OH
H2C
CH OH
H2C
OH
SN
глицерол
O
O
δ+ P
HO
OH
-НОН
O
OH
OH
P
H2C
OH
CH OH
H2C
OH
α-глицерофосфат
6.
..OH
H2C
CH OH
H2C
OH
O
O
δ+ C R
CoAS
-СoASH
O
C
R
H2C
CH OH
H2C
OH
моноацилглицерол
SN
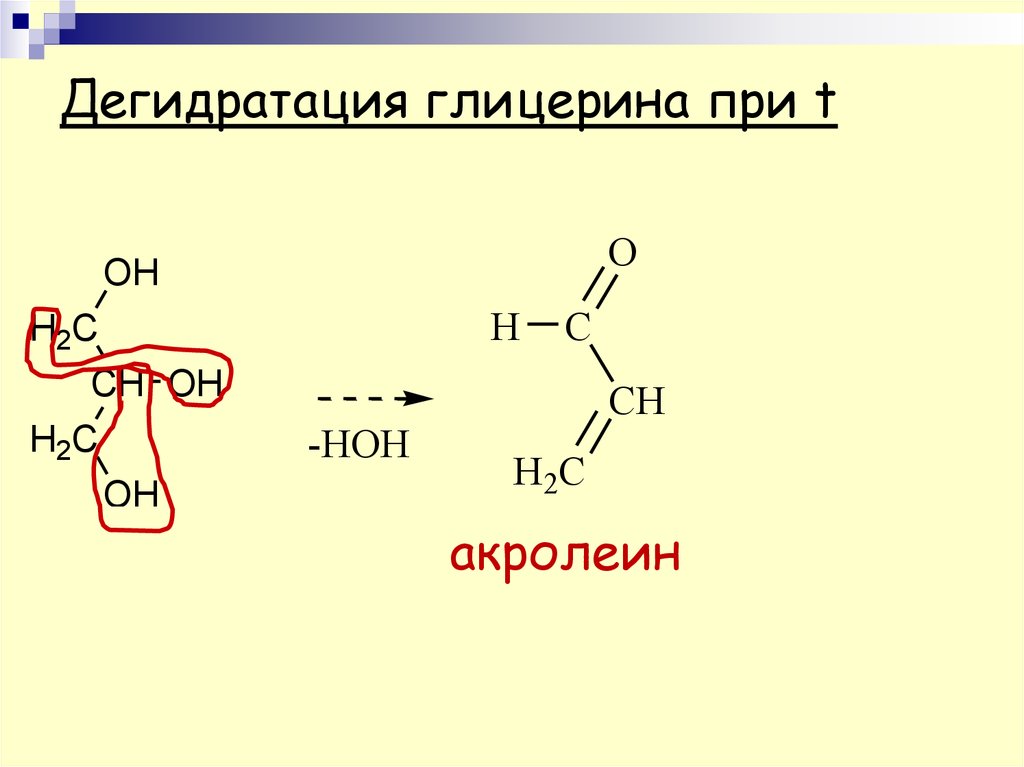
7. Дегидратация глицерина при t
OOH
H 2C
CH OH
H 2C
OH
H
-HOH
C
CH
H 2C
акролеин
8.
..O
OH
H 2C
CH OH
H 2C
OH
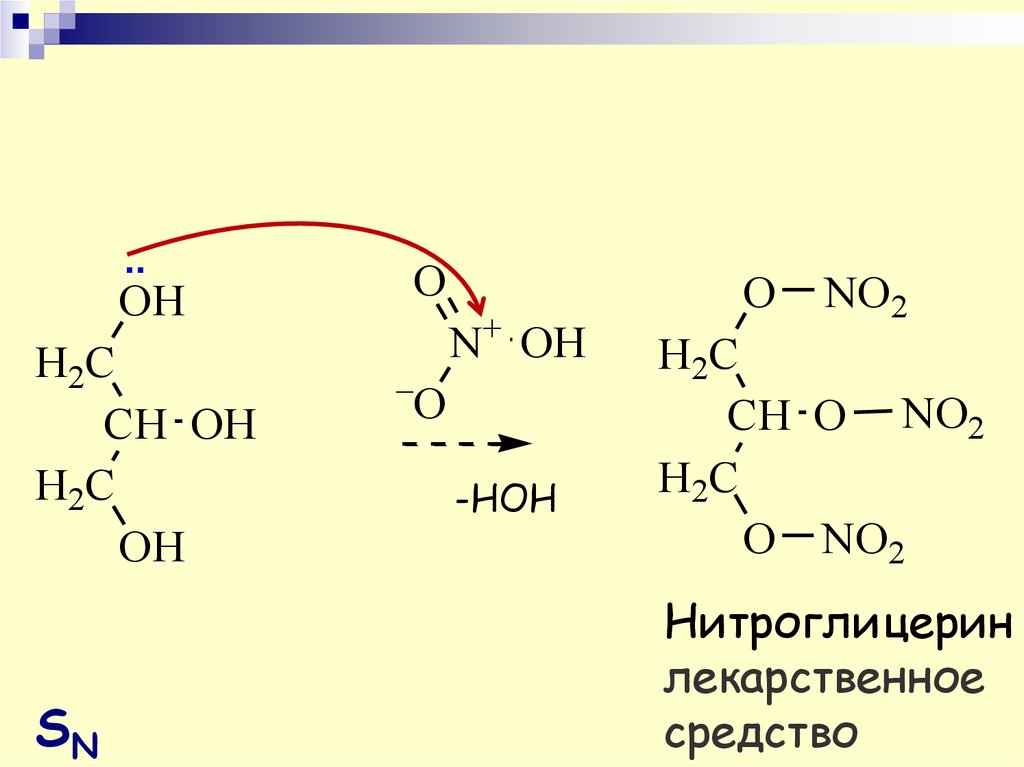
SN
N+ OH
–
O
-НОН
O
NO2
H 2C
CH O NO2
H 2C
O NO2
Нитроглицерин
лекарственное
средство
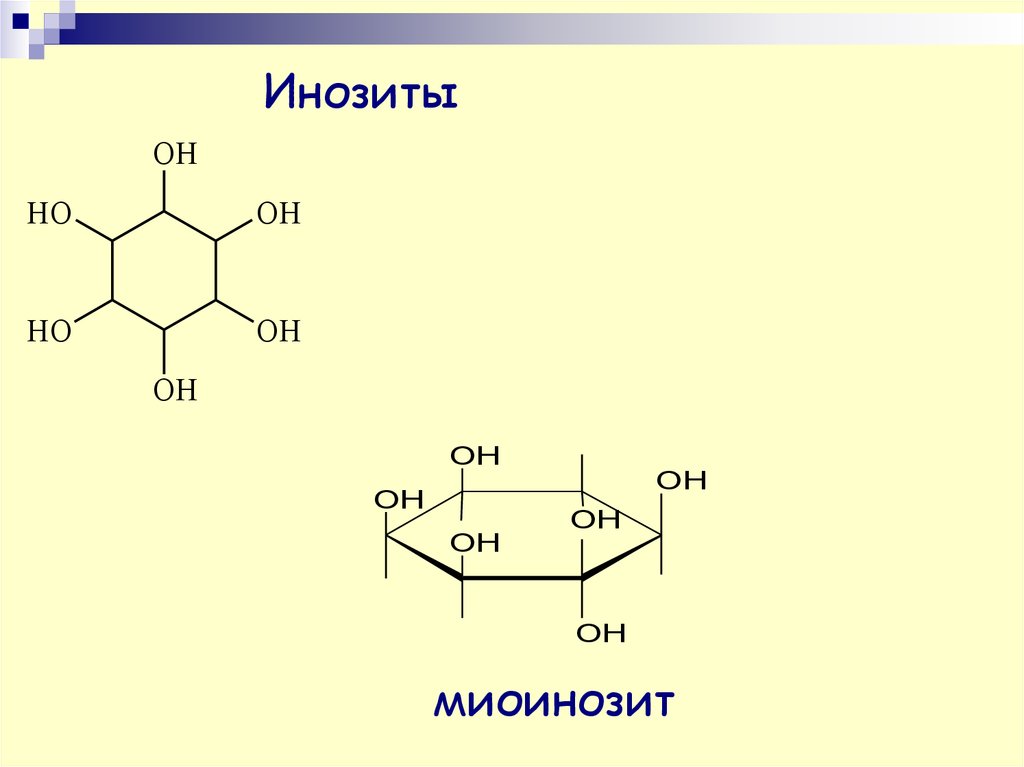
9.
ИнозитыOH
HO
OH
HO
OH
OH
OH
OH
OH
OH
OH
OH
миоинозит
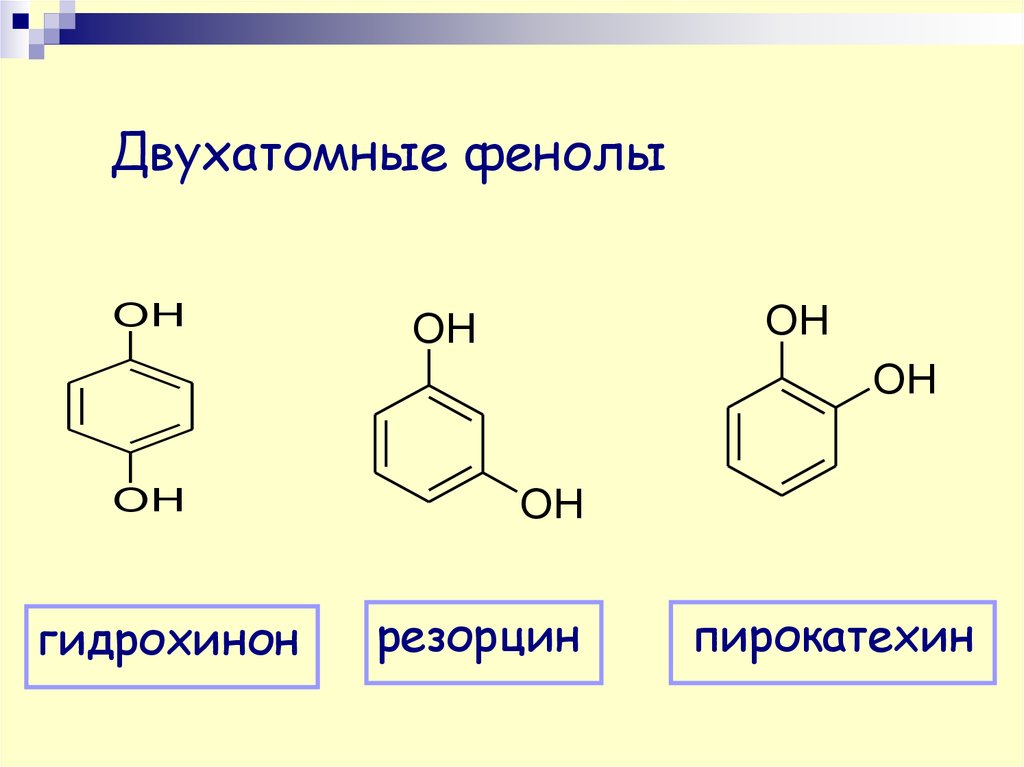
10.
Двухатомные фенолыOH
OH
OH
OH
OH
гидрохинон
OH
резорцин
пирокатехин
11.
БВС, содержащие фенольныйгидроксил, могут играть роль
антиоксидантов
Витамин Е (токоферол)
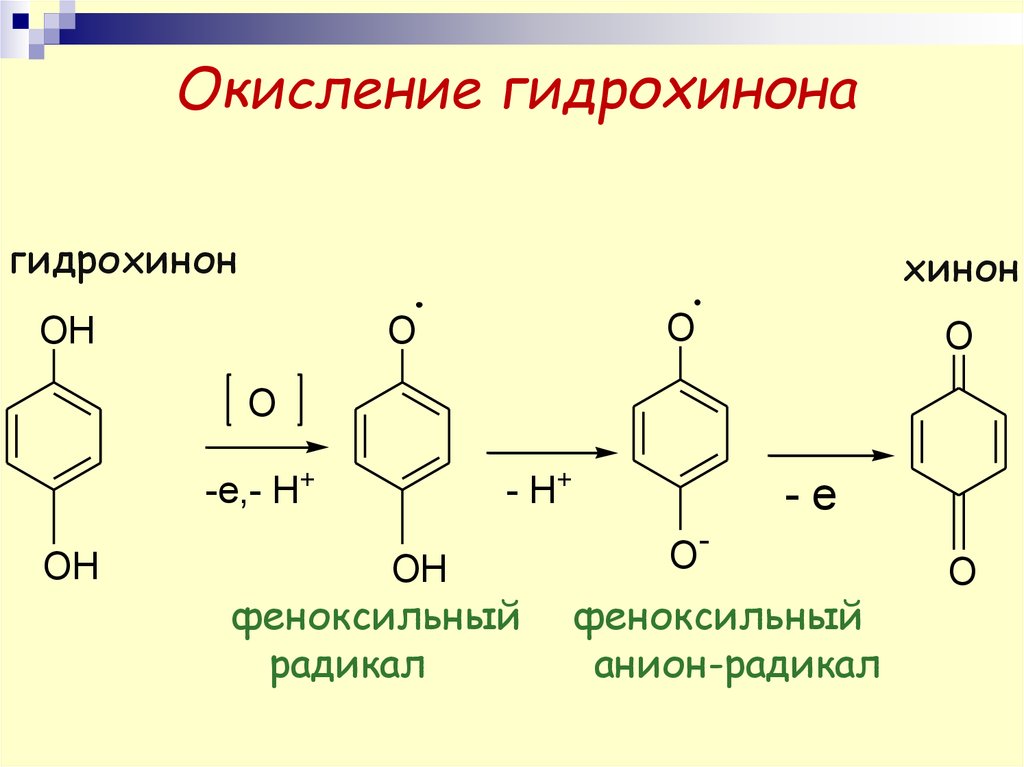
12. Окисление гидрохинона
гидрохинонхинон
OH
O
O
O
O
-e,- H+
OH
- H+
OH
феноксильный
радикал
-e
O-
феноксильный
анион-радикал
O
13.
Убихиноны участвуют в переносеэлектронов в дыхательной цепи
OH
O
O
[O]
O
CH3
H3C
CH3
H3C
[H]
H3C
H3C
O
H
OH
CH3
10
O
H
O
CH3
10
14.
HOHO
CH2
NH2
CH
COOH
тирозин
HO
CH2
CH2
-CO2
HO
дофамин
HO
OH
NH2 метили- HO
CH
рование
CH2
HO
HO
норадреналин
NH2
гидроксилирование
OH
CH
CH2
адреналин
Катехоламины –
дофамин,норадреналин, адреналин
CH3
NH
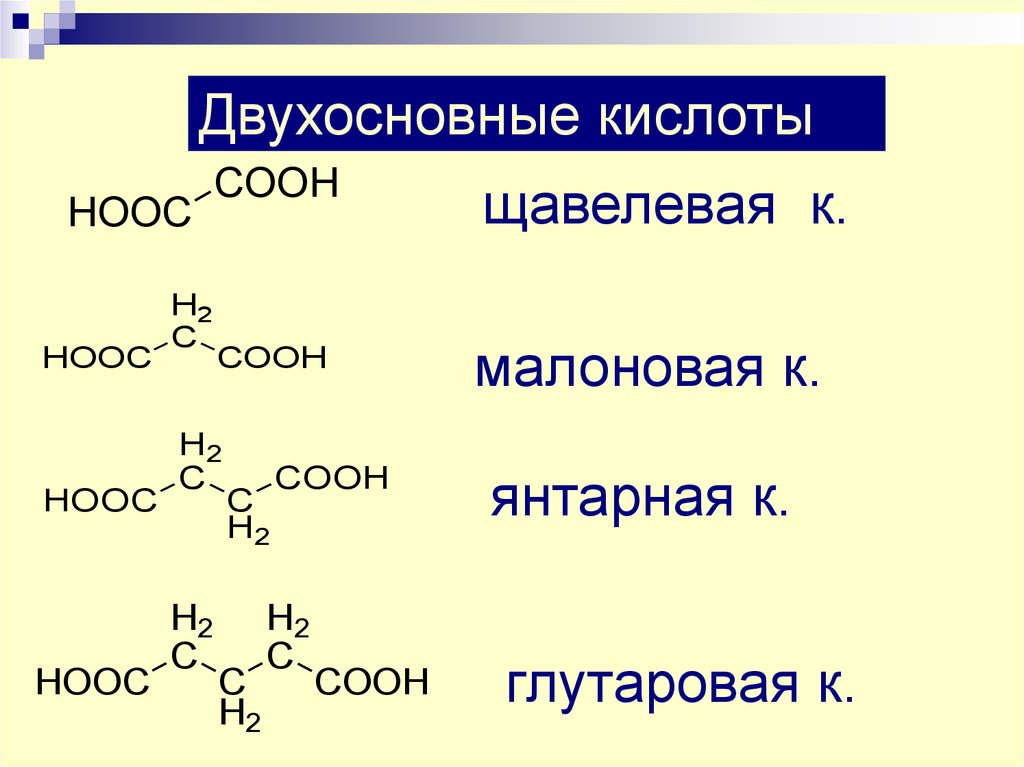
15. Двухосновные кислоты
HOOCHOOC
HOOC
HOOC
H2
C
COOH
щавелевая к.
COOH
малоновая к.
H2
C
H2
C
C
H2
C
H2
COOH
H2
C
COOH
янтарная к.
глутаровая к.
16.
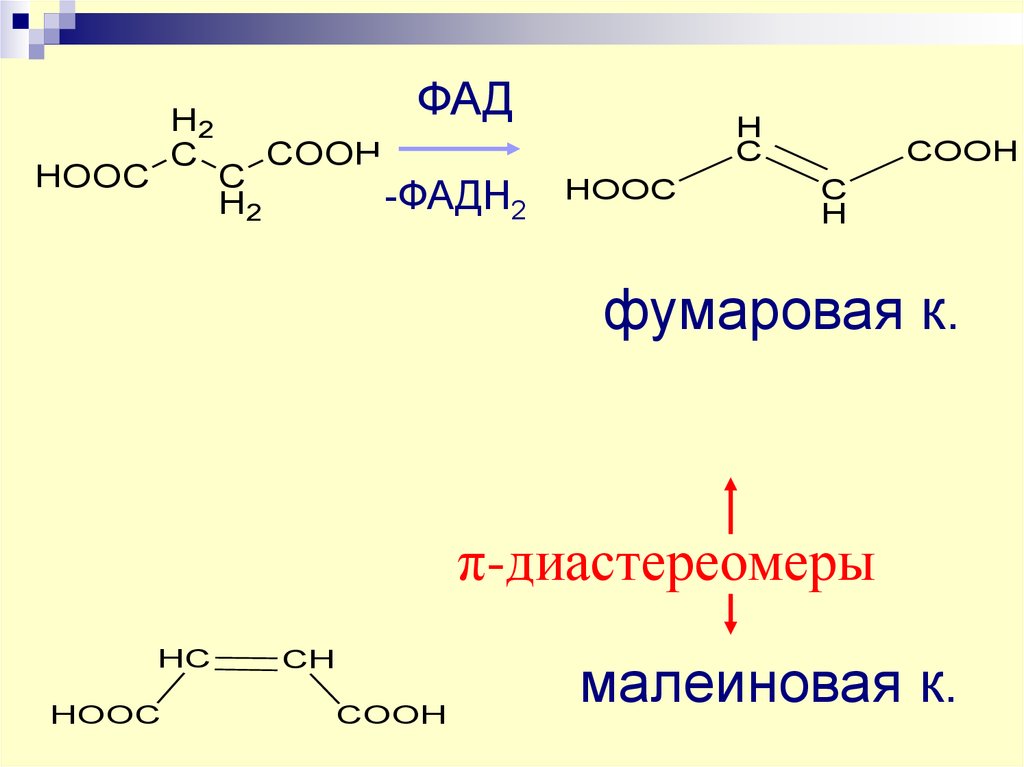
H2C
HOOC
ФАД
C
H2
H
C
COOH
-ФАДН2
HOOC
COOH
C
H
фумаровая к.
π-диастереомеры
HC
HOOC
CH
COOH
малеиновая к.
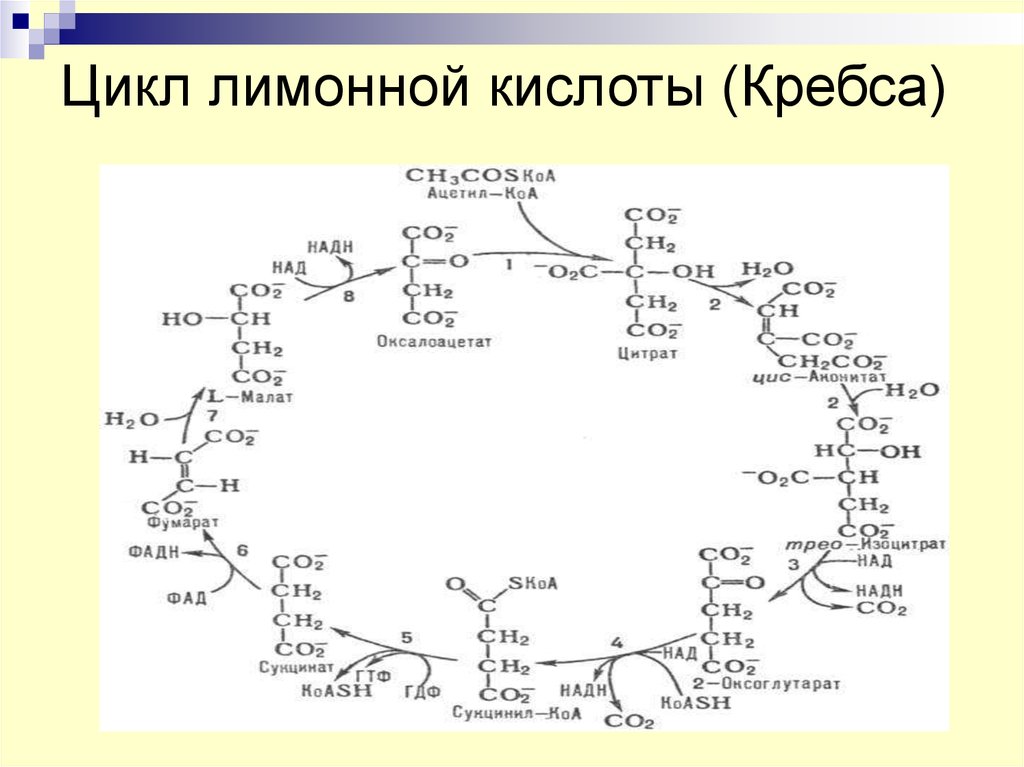
17. Цикл лимонной кислоты (Кребса)
18. Гетерофункциональные соединения
аминоспирты-ОН
-NH2
гидроксикислоты
-ОН
-COOH
оксокислоты
аминокислоты
-C═О
-COOH
-NH2
-COOH
19.
АминоспиртыHO
CH2
CH2
NH2
этаноламин
HO
CH2
CH2
CH3
N
H3 C
CH3
холин
20.
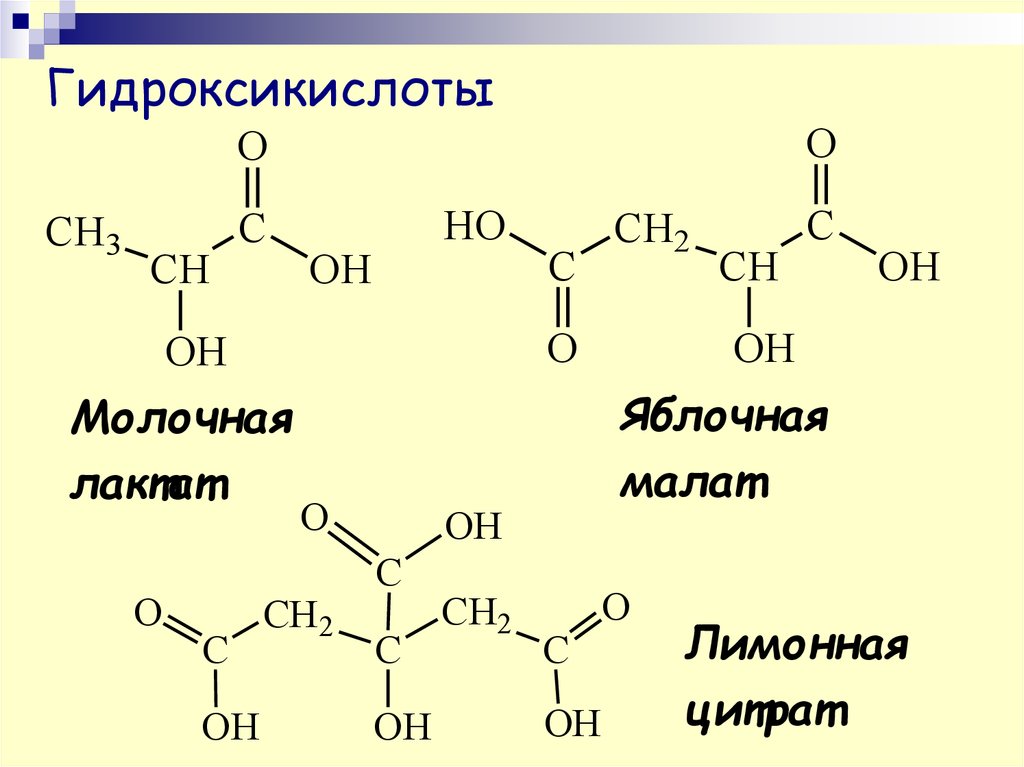
ГидроксикислотыO
O
CH3
CH
C
HO
OH
O
OH
Молочная
лактат
O
C
OH
C
CH2
O
CH2
C
OH
CH2
OH
OH
Яблочная
малат
OH
C
CH
C
O
C
OH
Лимонная
цитрат
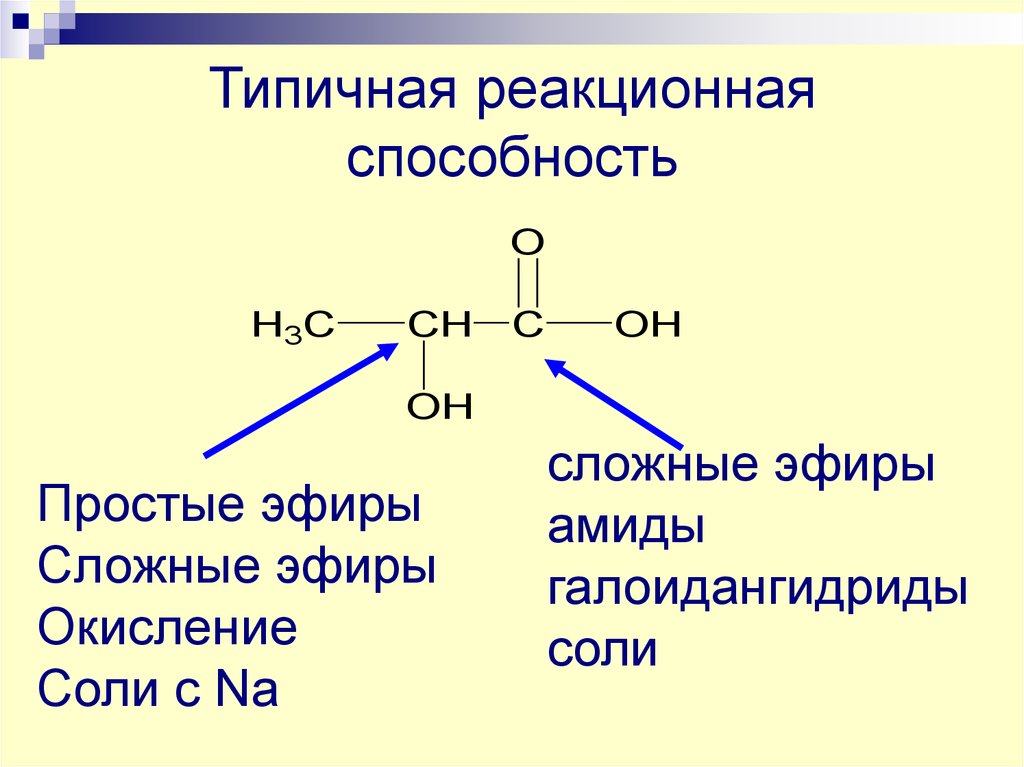
21. Типичная реакционная способность
OH3C
CH
C
OH
OH
Простые эфиры
Сложные эфиры
Окисление
Соли с Na
сложные эфиры
амиды
галоидангидриды
соли
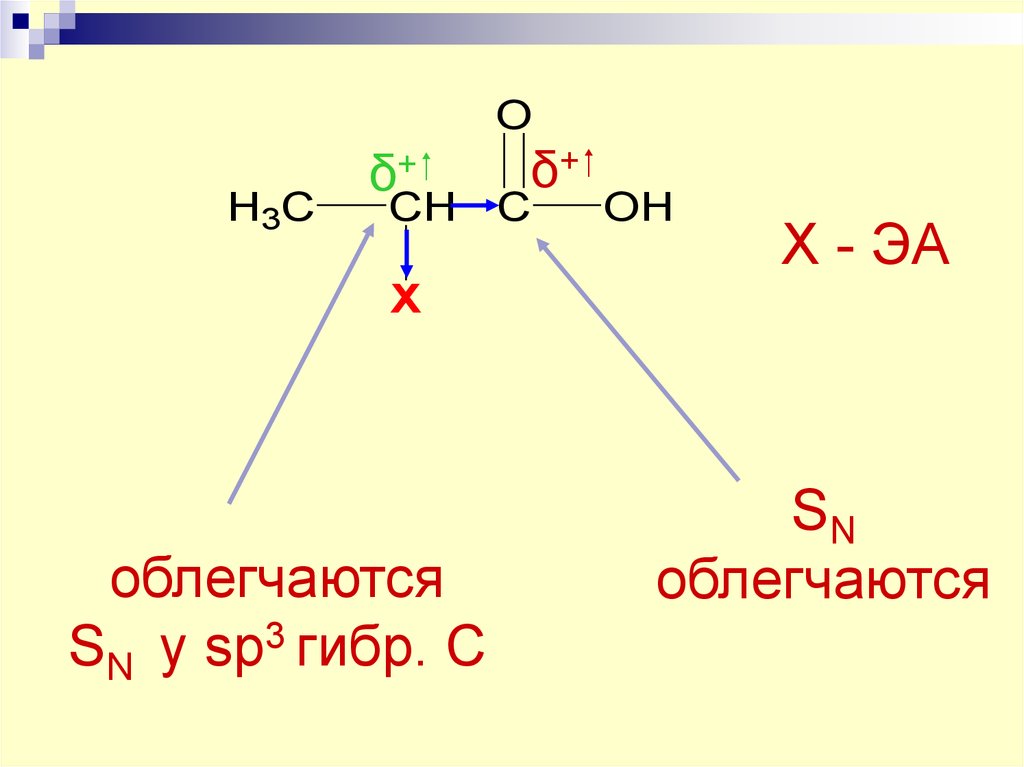
22. Х - ЭА
OH3C
δ+
δ+
CH C
OH
Х - ЭА
X
облегчаются
SN у sp3 гибр. С
SN
облегчаются
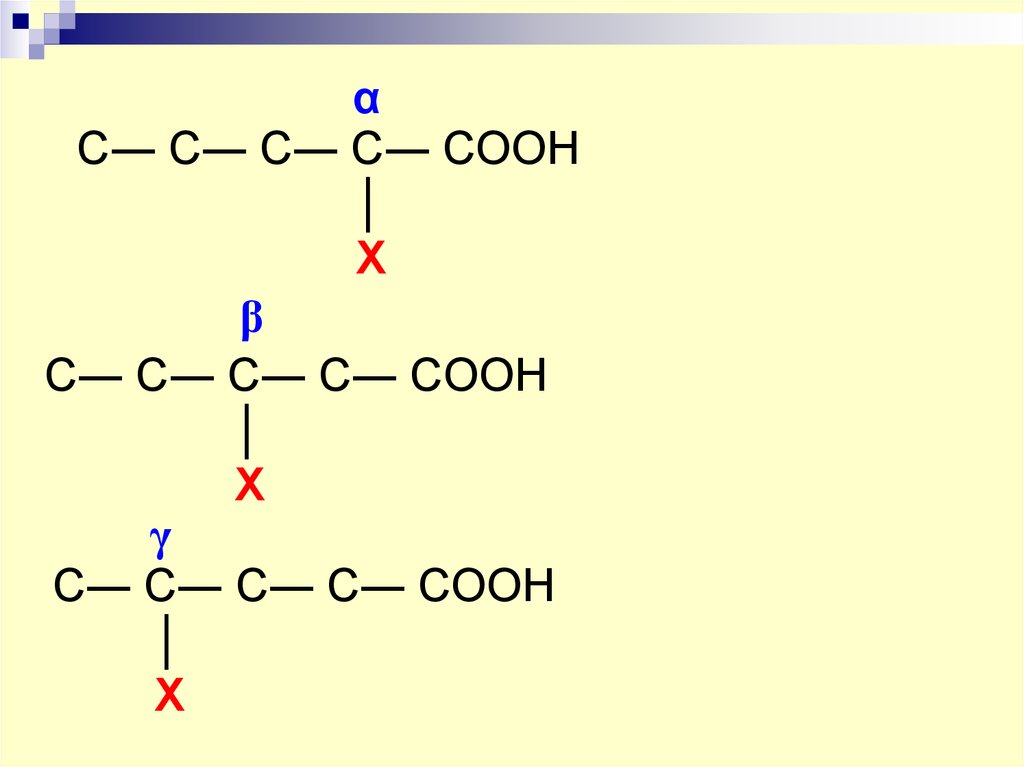
23. С― С― С― С― СOOH │ X
αС― С― С― С― СOOH
│
X
β
С― С― С― С― СOOH
│
X
γ
С― С― С― С― СOOH
│
X
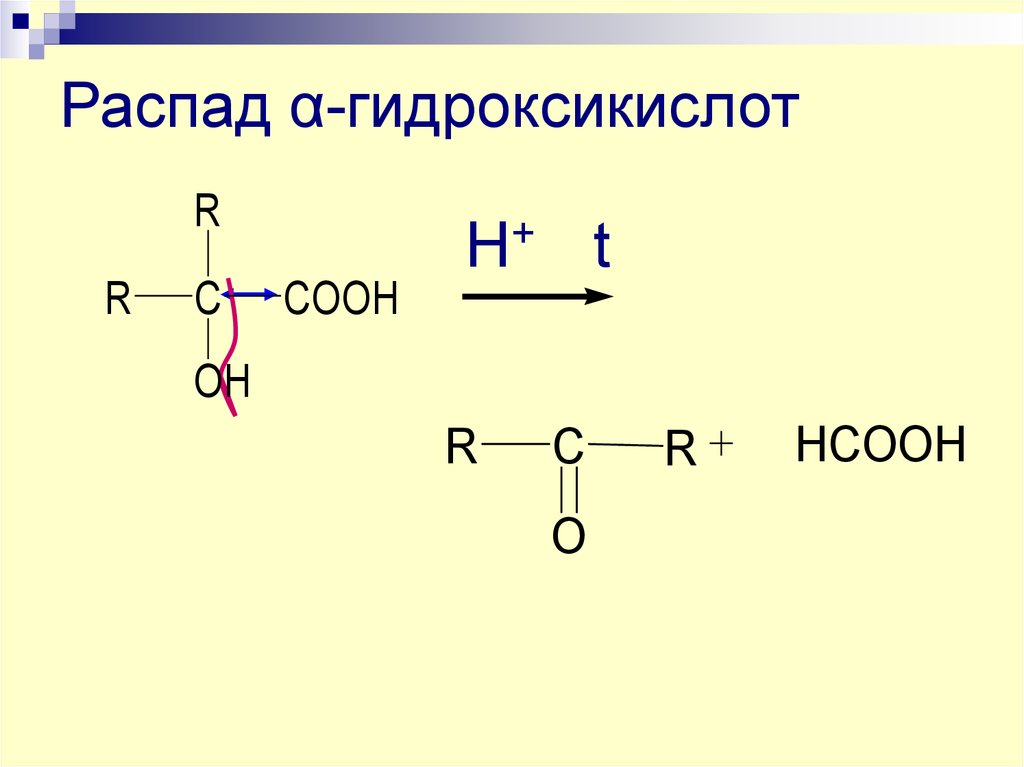
24. Распад α-гидроксикислот
RR
C
Н+ t
COOH
OH
R
C
O
R
HCOOH
25. Распад молочной кислоты
HH3C
C
Н+ t
COOH
OH
лактат
H3C
C
O
H
HCOOH
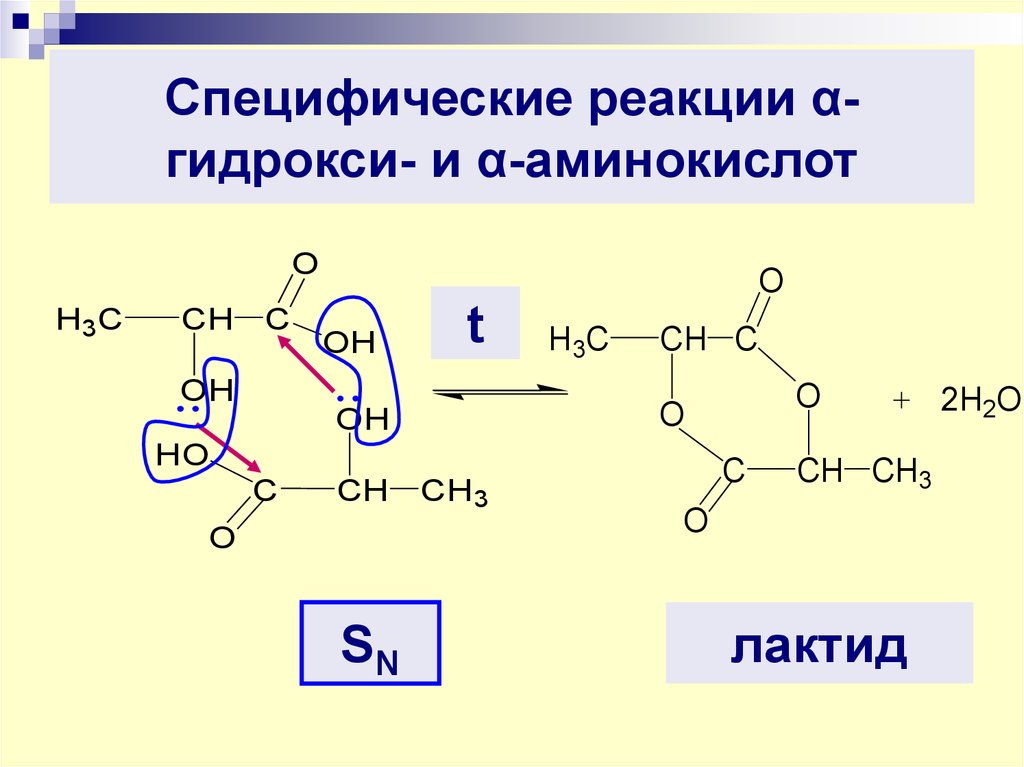
26. Специфические реакции α-гидрокси- и α-аминокислот
Специфические реакции αгидрокси- и α-аминокислотO
H3 C
CH C
OH
O
OH
t
H3 C
CH C
OH
HO
C
CH
O
SN
O
O
CH3
C
CH CH3
O
лактид
2H2O
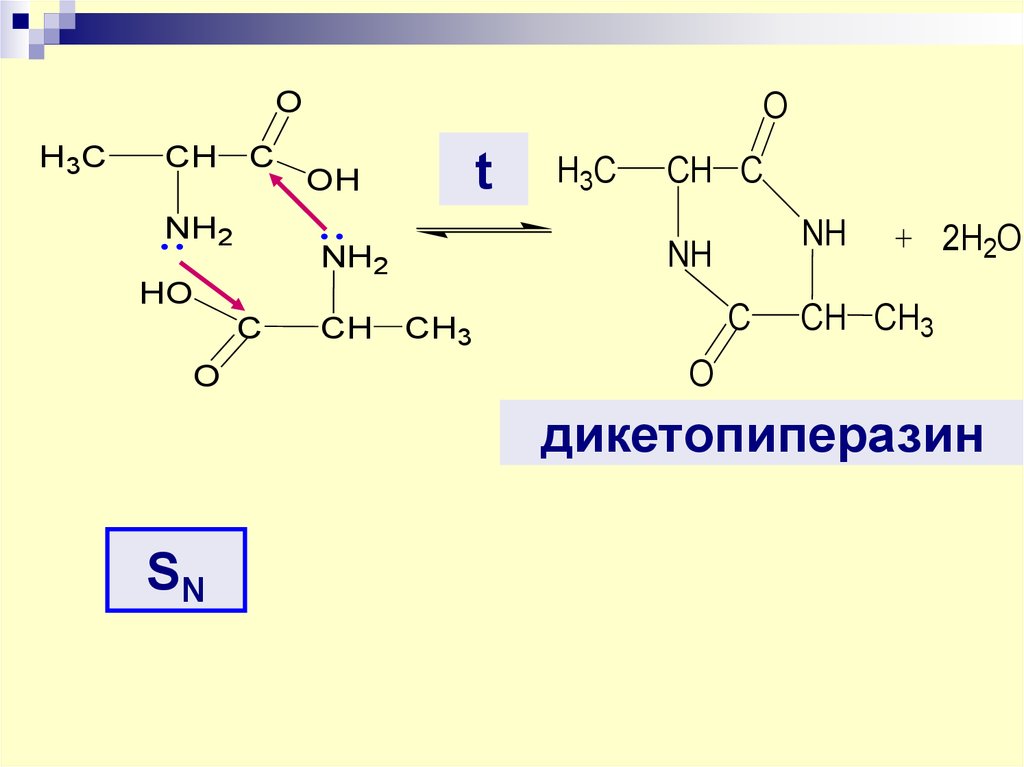
27.
OH3C
CH C
NH2
O
OH
NH2
t
H3C
CH C
NH
HO
C
O
NH
C
CH CH3
2H2O
CH CH3
O
дикетопиперазин
SN
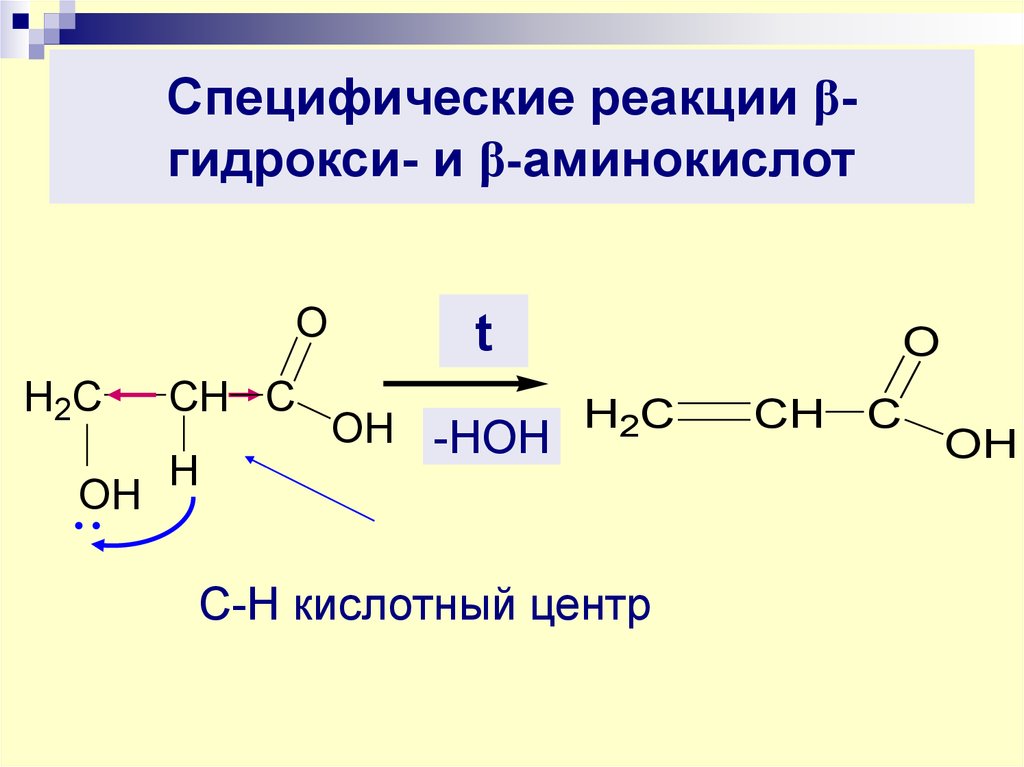
28. Специфические реакции β-гидрокси- и β-аминокислот
Специфические реакции βгидрокси- и β-аминокислотO
H2C
OH
CH C
H
t
OH -НОН H2C
С-Н кислотный центр
O
CH
C
OH
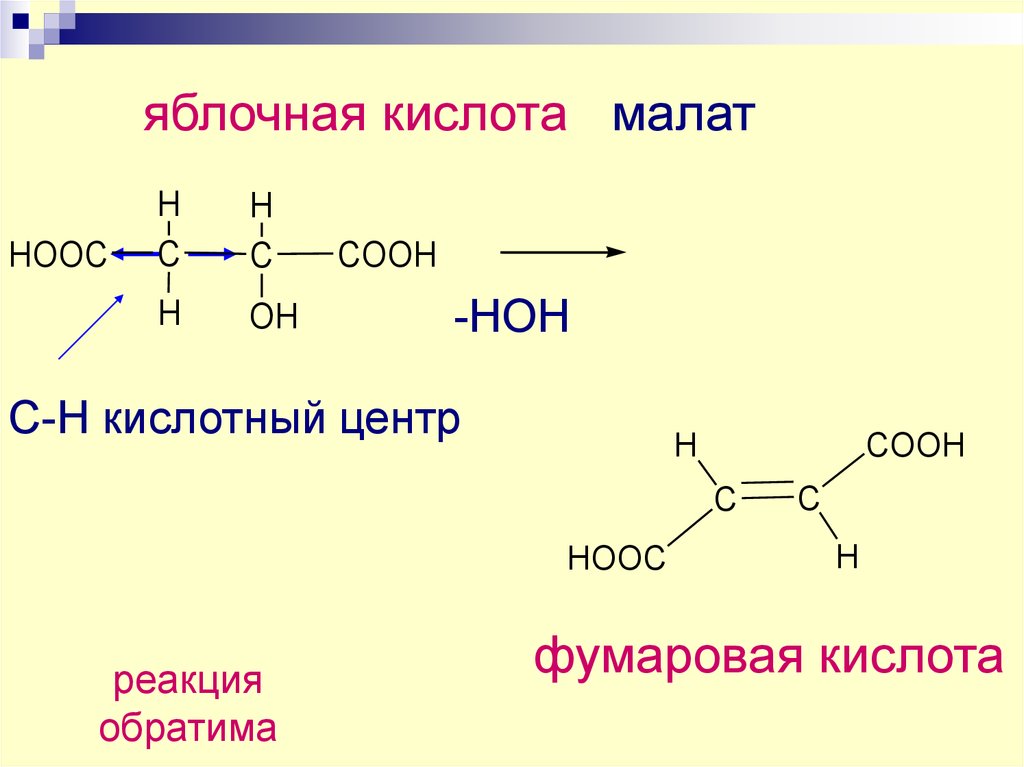
29.
яблочная кислота малатHOOC
H
C
H
C
H
OH
COOH
-НОН
С-Н кислотный центр
H
COOH
C
HOOC
реакция
обратима
C
H
фумаровая кислота
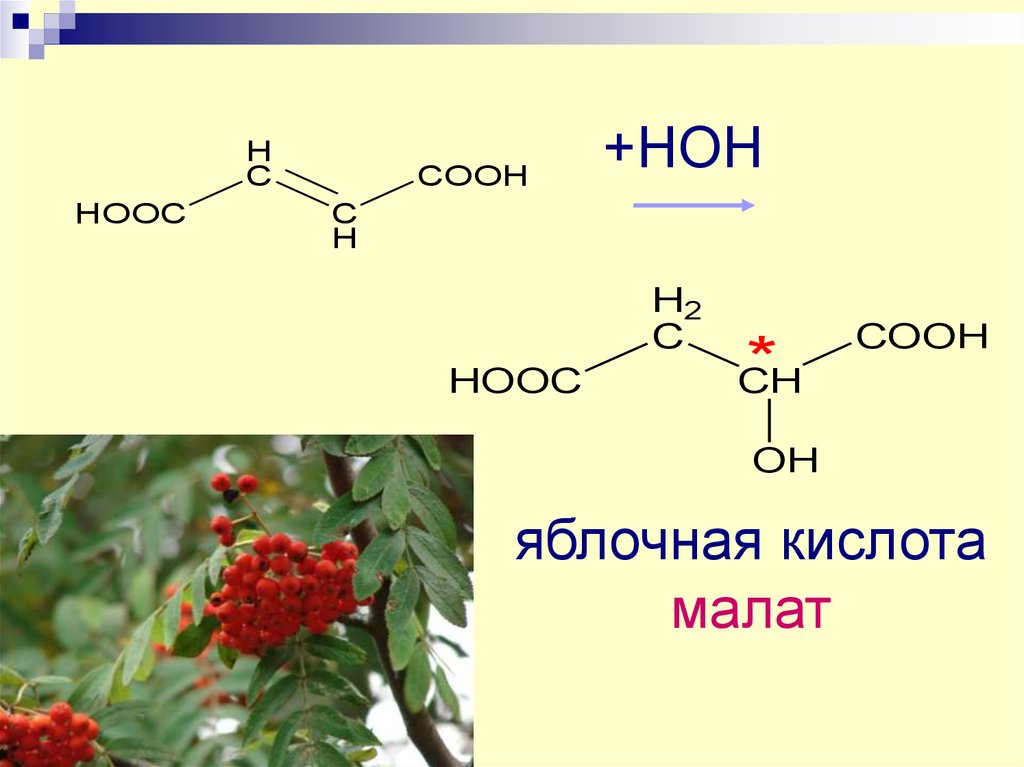
30.
HC
HOOC
COOH
+HOH
C
H
H2
C
HOOC
*
COOH
CH
OH
яблочная кислота
малат
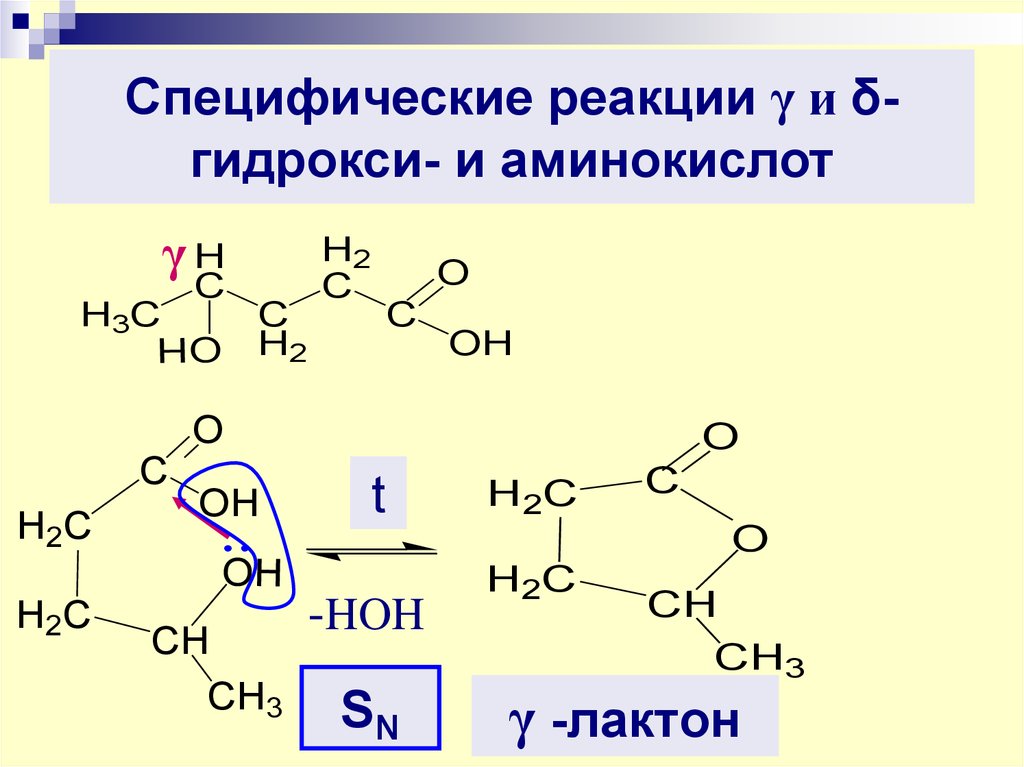
31. Специфические реакции γ и δ-гидрокси- и аминокислот
Специфические реакции γ и δгидрокси- и аминокислотγH
H3C
C
C
H2
H2
C
O
C
OH
OH
O
C
H2C
OH
O
t
CH
CH3
C
O
OH
H2 C
H2 C
-HOH
SN
H2 C
CH
CH3
γ -лактон
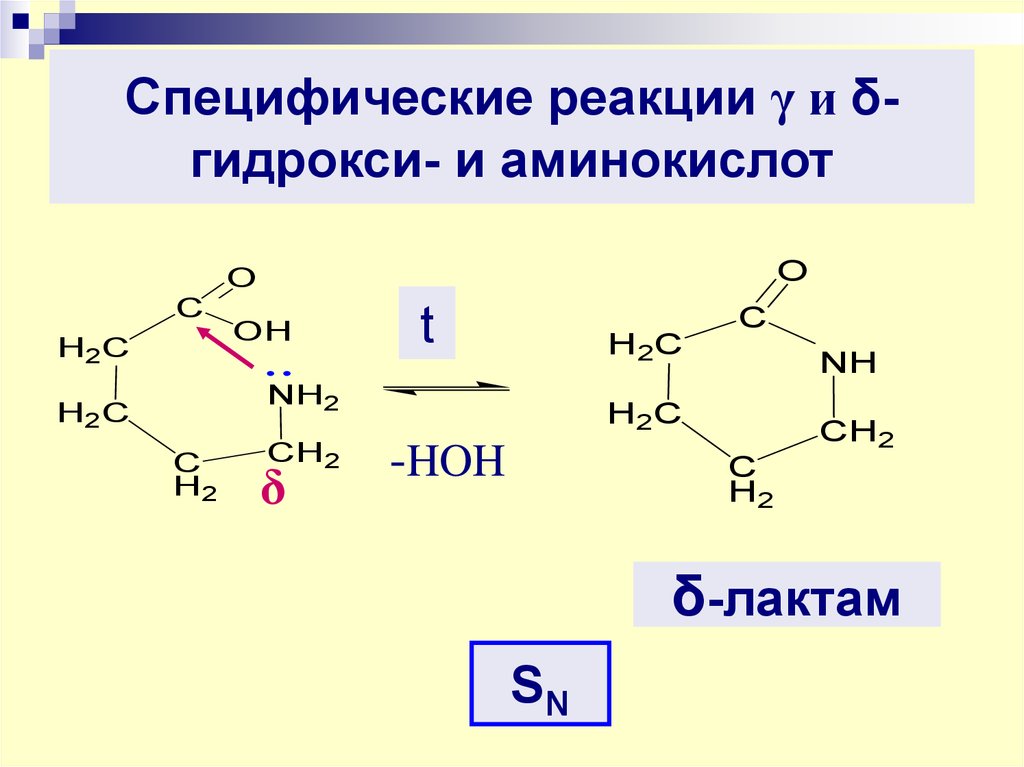
32. Специфические реакции γ и δ-гидрокси- и аминокислот
Специфические реакции γ и δгидрокси- и аминокислотO
O
C
H2C
OH
t
C
H2C
NH2
H2C
C
H2
CH2
δ
NH
H2 C
-HOH
CH2
C
H2
δ-лактам
SN
33.
Реакции внутримолекулярнойциклизации характерны для γ- и δгидрокси- и аминокислот,
дикарбоновых кислот,
гидроксикарбонильных соединений
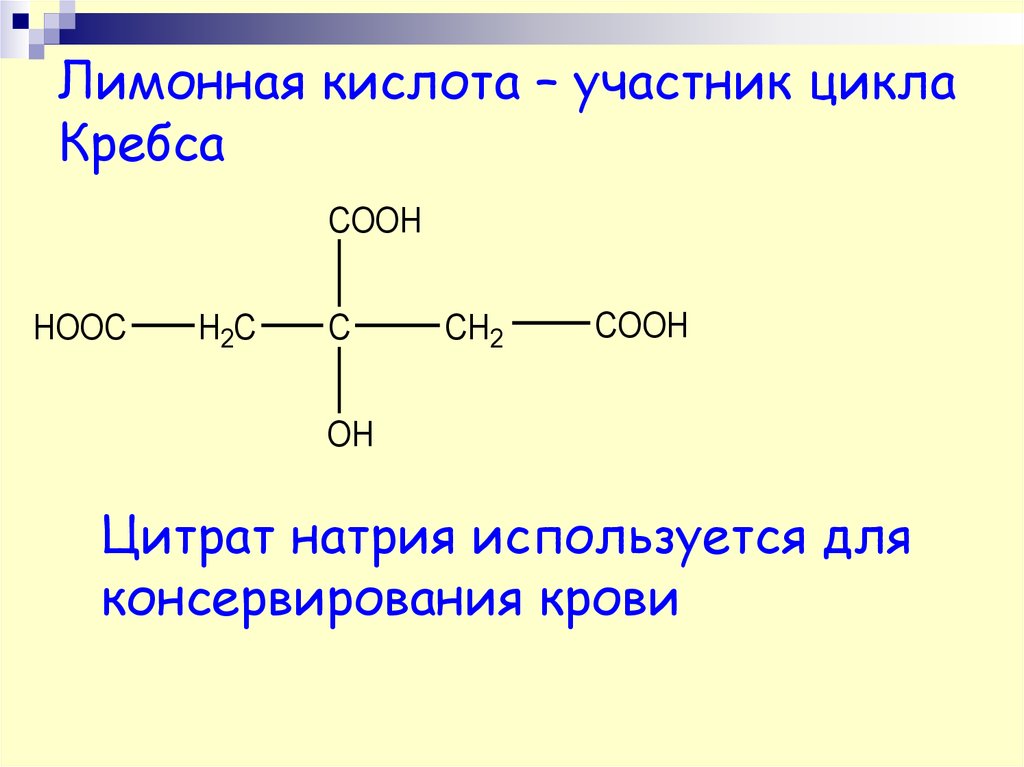
34.
Лимонная кислота – участник циклаКребса
COOH
HOOC
H2C
C
CH2
COOH
OH
Цитрат натрия используется для
консервирования крови
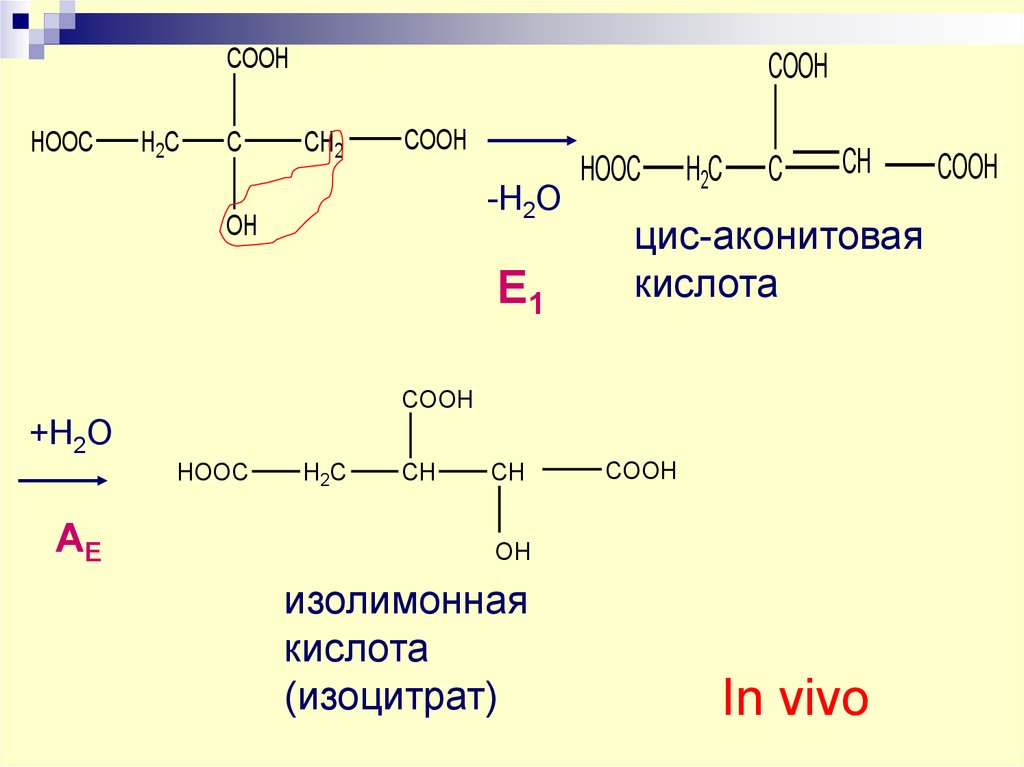
35. -H2O
COOHHOOC
H2C
C
COOH
CH2
COOH
-H2O
OH
E1
HOOC
H2C
C
CH
цис-аконитовая
кислота
COOH
+H2O
HOOC
AE
H2C
CH
CH
COOH
OH
изолимонная
кислота
(изоцитрат)
In vivo
COOH
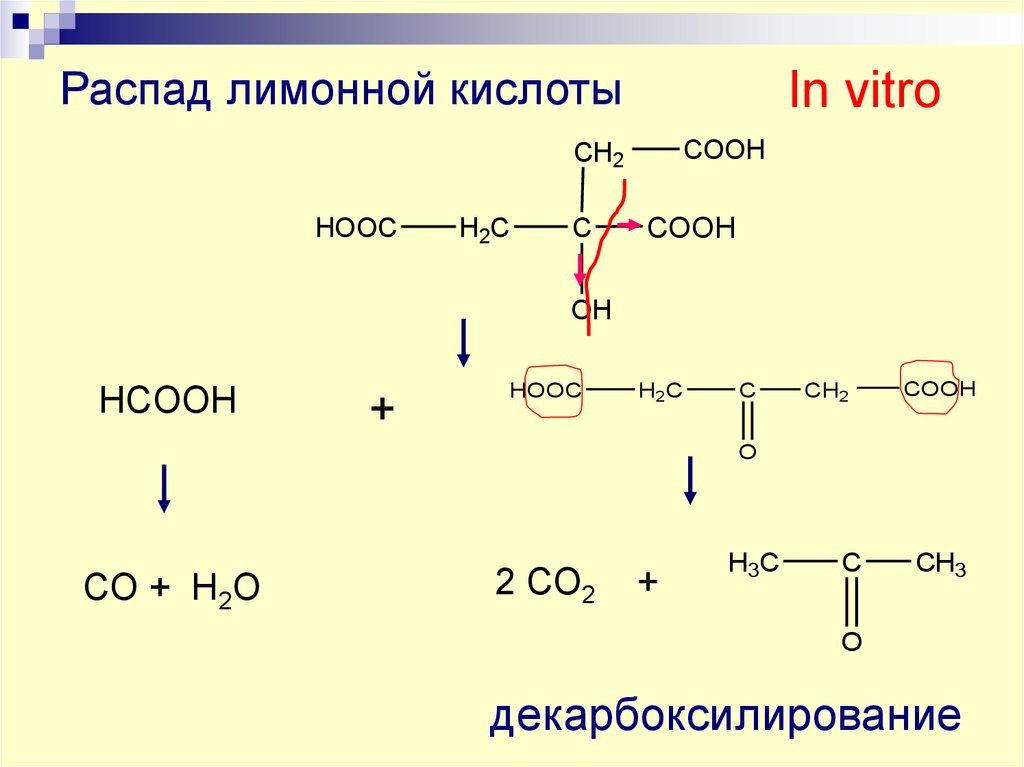
36. Распад лимонной кислоты
In vitroCOOH
CH2
HOOC
H2C
C
COOH
OH
HCOOH
+
HOOC
H2C
C
CH2
COOH
O
CO + H2O
2 CO2
+
H3C
C
CH3
O
декарбоксилирование
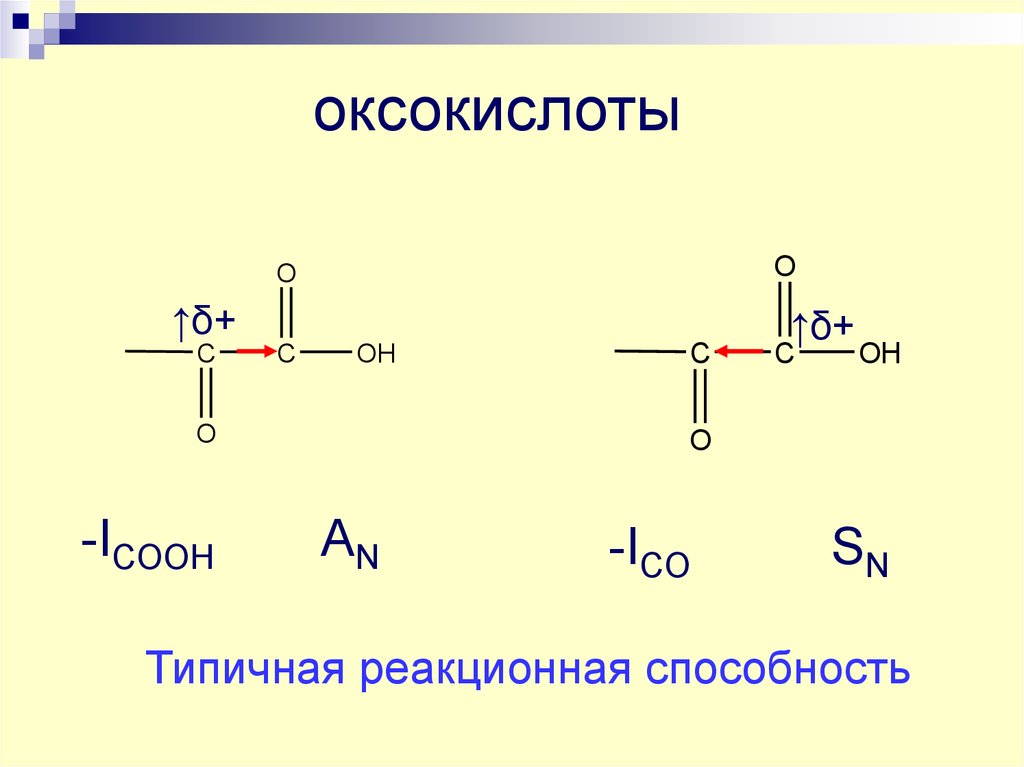
37. оксокислоты
OO
↑δ+
C
C
OH
O
-ICOOH
C
↑δ+
C
OH
O
AN
-ICO
SN
Типичная реакционная способность
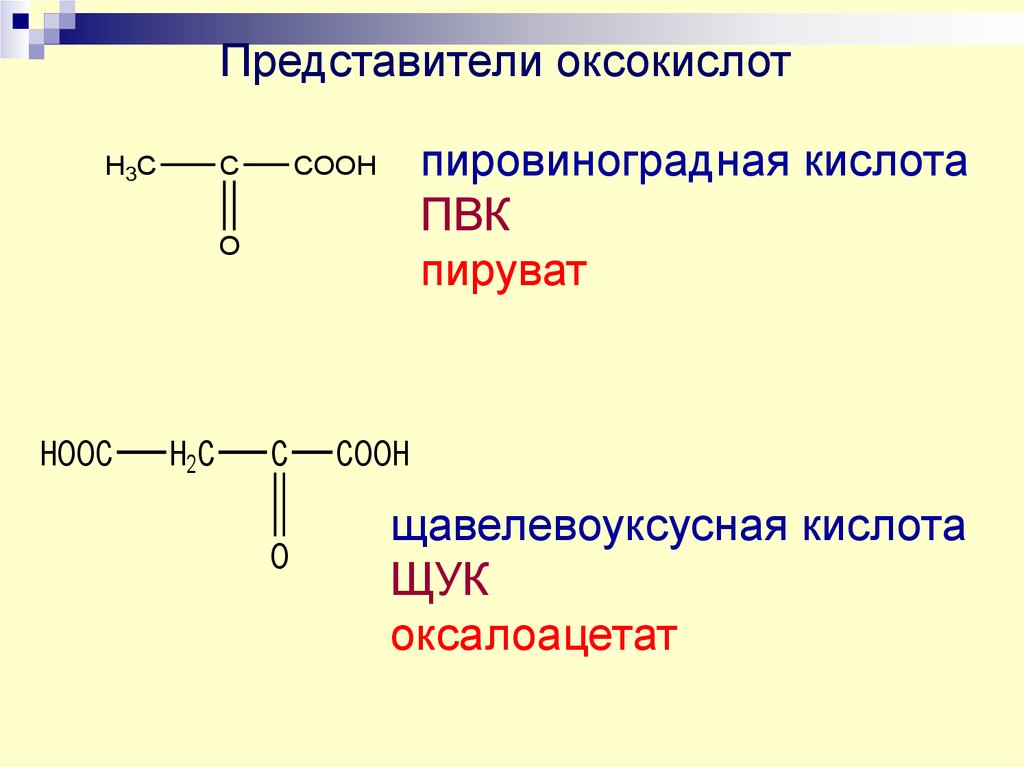
38.
Представители оксокислотH3C
C
пировиноградная кислота
ПВК
пируват
COOH
O
HOOC
H2C
C
O
COOH
щавелевоуксусная кислота
ЩУК
оксалоацетат
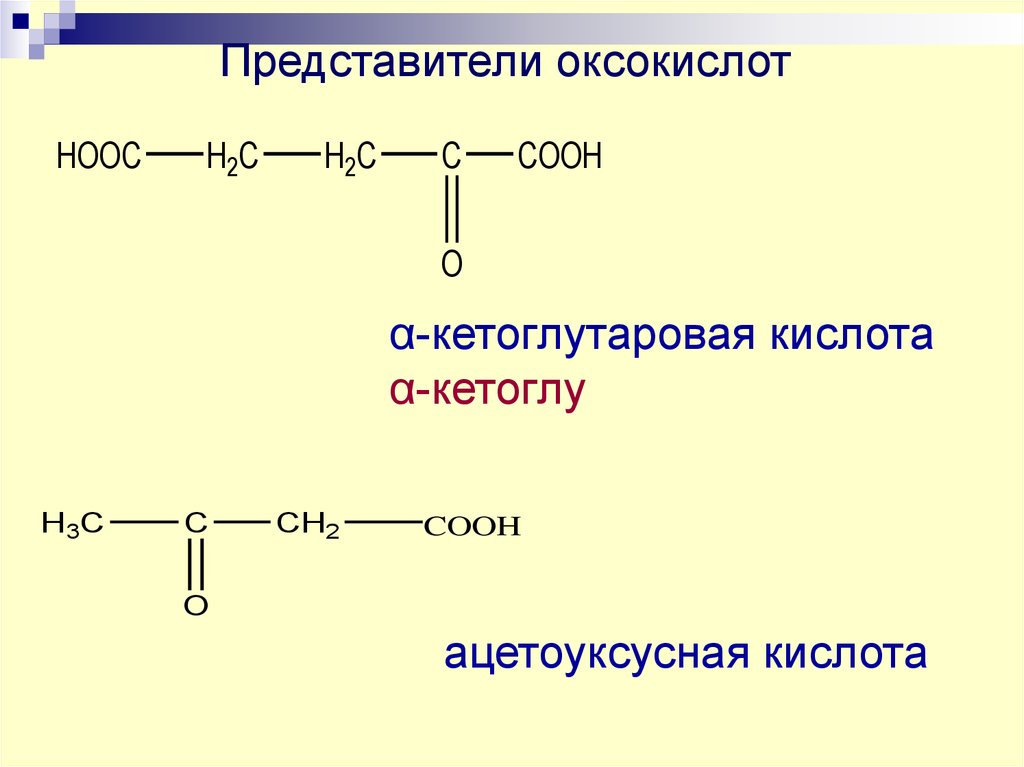
39.
Представители оксокислотHOOC
H2C
H2C
C
COOH
O
α-кетоглутаровая кислота
α-кетоглу
H3C
C
CH2
COOH
O
ацетоуксусная кислота
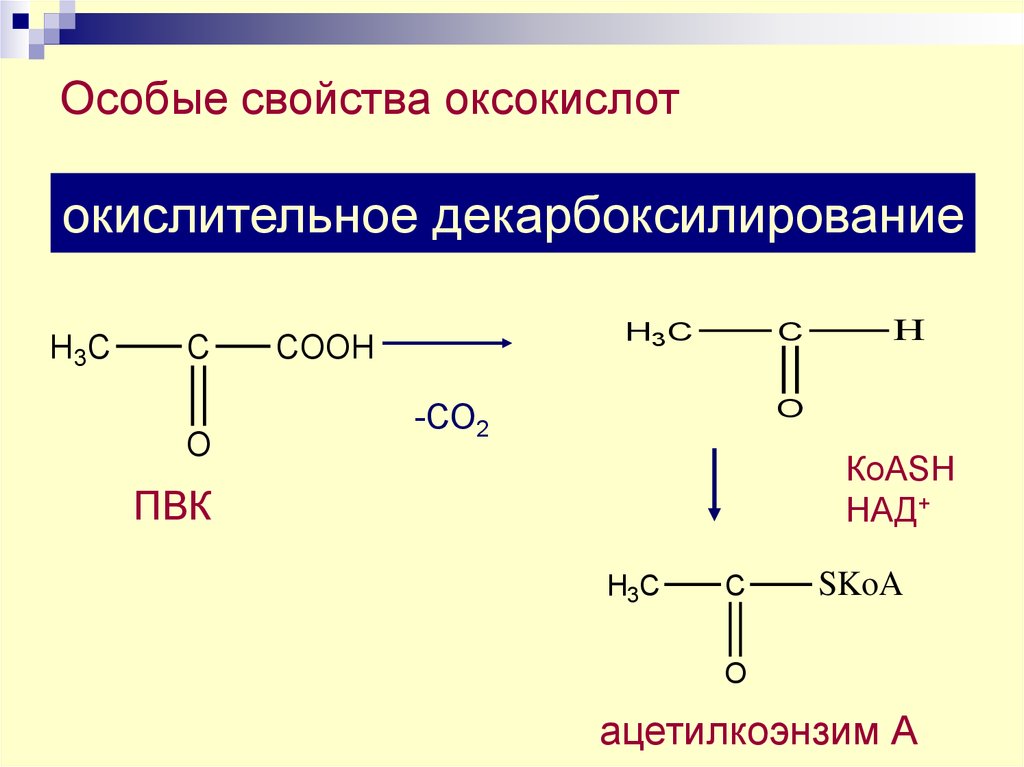
40. Особые свойства оксокислот
неокислительноедекарбоксилированиедекарбоксилирование
окислительное
H3C
C
O
H3C
COOH
C
H
O
-СО2
КоАSH
НАД+
ПВК
H3C
C
SKoA
O
ацетилкоэнзим А
41.
Реакция трансаминированияHOOC
H2C
ЩУК
C
COOH
+
HOOC
H2C
H2C
O
CH COOH
NH2
глутаминовая кислота
пиридоксаль
фосфат
HOOC
H2C
CH
COOH
HOOC
NH2
аспарагиновая
кислота
H2C
H2C
C
α-кетоглу
O
+
COOH
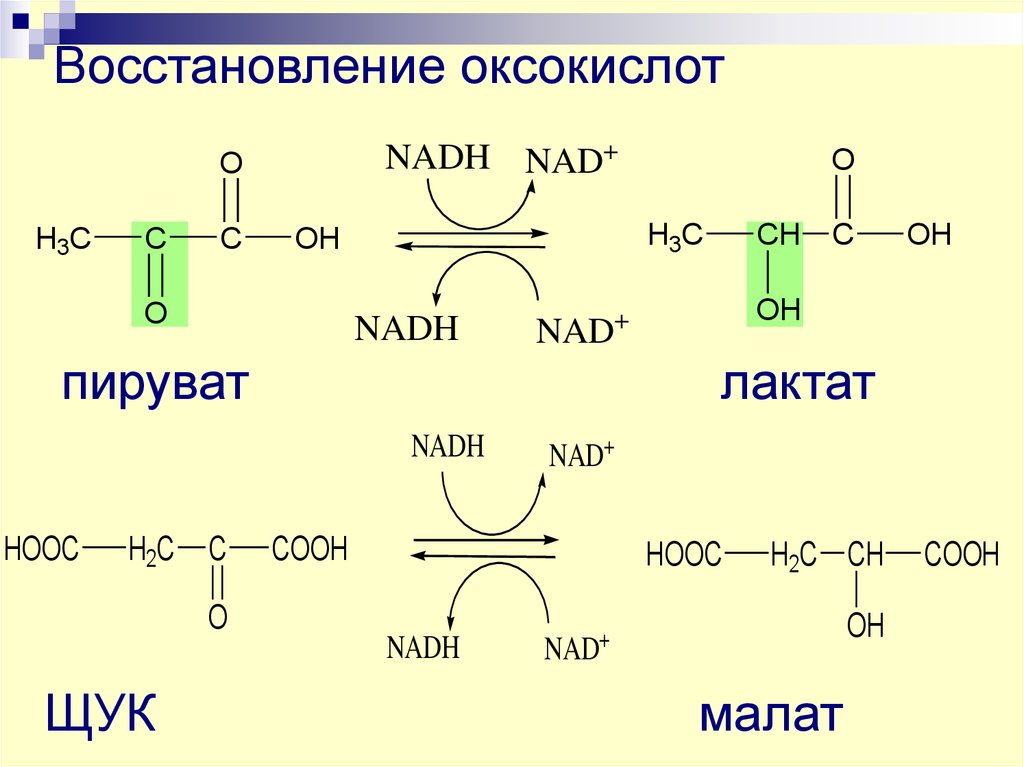
42. Восстановление оксокислот
NADH NAD+O
H3C
C
C
H3C
OH
O
NADH
C
O
ЩУК
C
OH
OH
NAD
лактат
NADH
H2C
CH
+
пируват
HOOC
O
NAD+
COOH
HOOC
NADH
H2C CH
OH
+
NAD
малат
COOH
43. Таутомерия
динамическая изомерия, при которойизомеры могут переходить друг в
друга, находясь в растворе в
состоянии подвижного равновесия
Прото-тропная таутомерия связана с
переносом протона
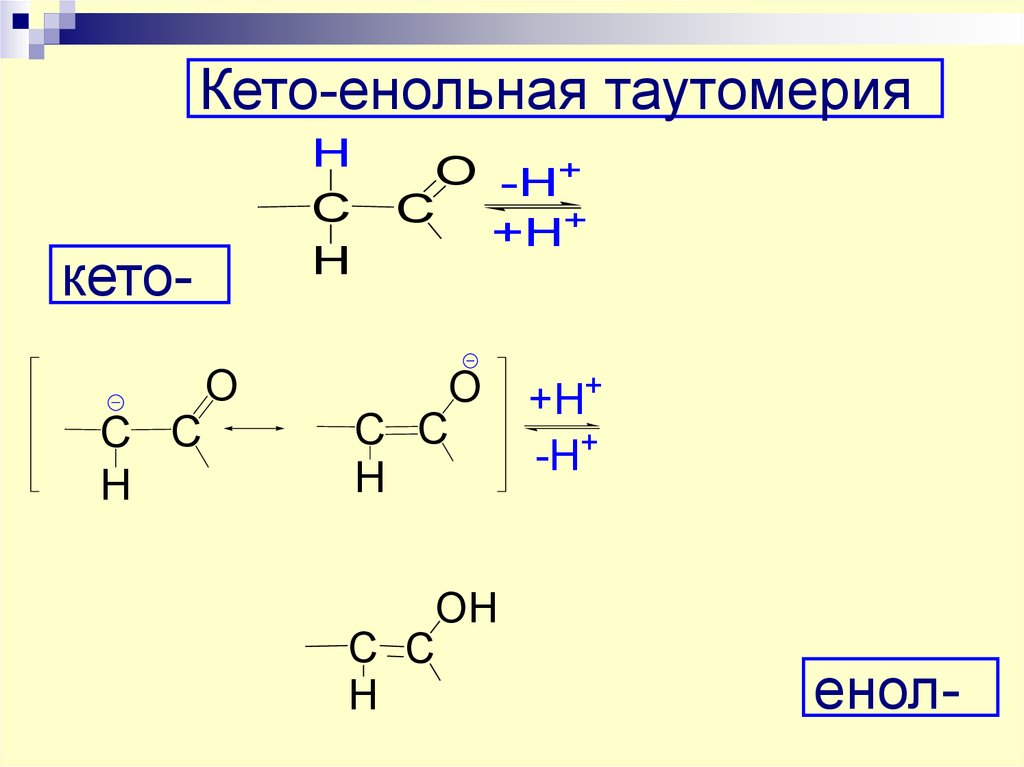
44. Кето-енольная таутомерия
HC
H
кетоO
C C
H
O -H+
C
+H+
O
C C
H
OH
C C
H
+H+
-H+
енол-
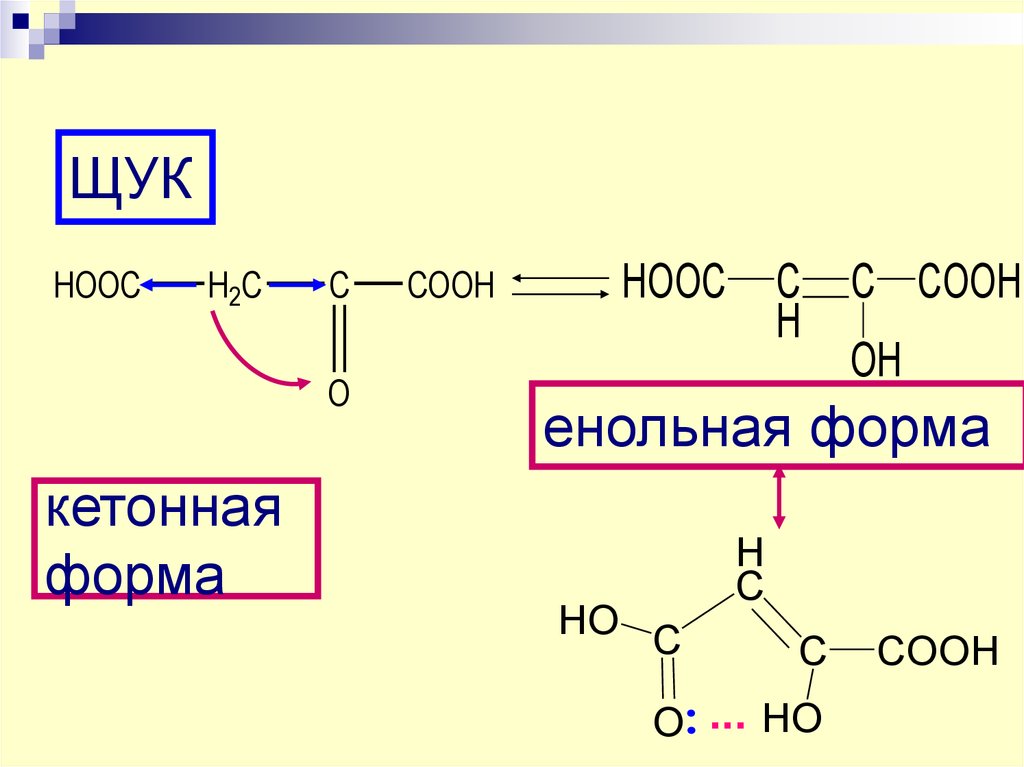
45.
ЩУКHOOC
H2C
C
O
кетонная
форма
COOH
HOOC
C
H
C COOH
OH
енольная форма
HO C
H
C
C
O ... HO
COOH
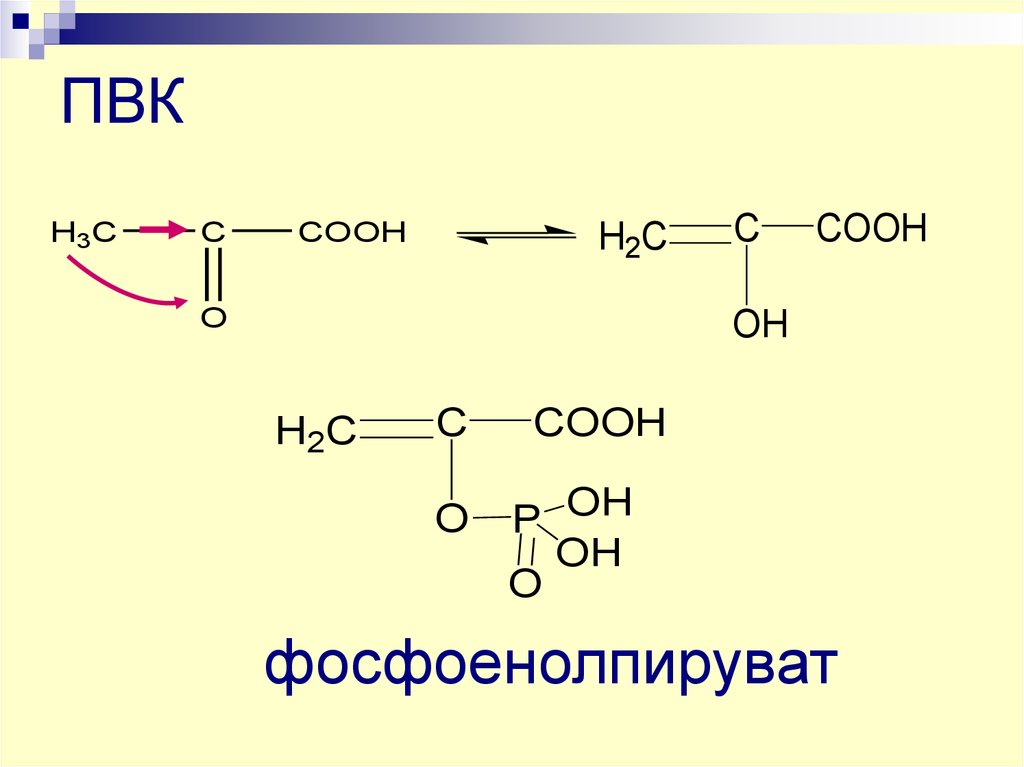
46. ПВК
H3CC
COOH
H2C
O
C
COOH
OH
H2C
C
O
COOH
P OH
OH
O
фосфоенолпируват
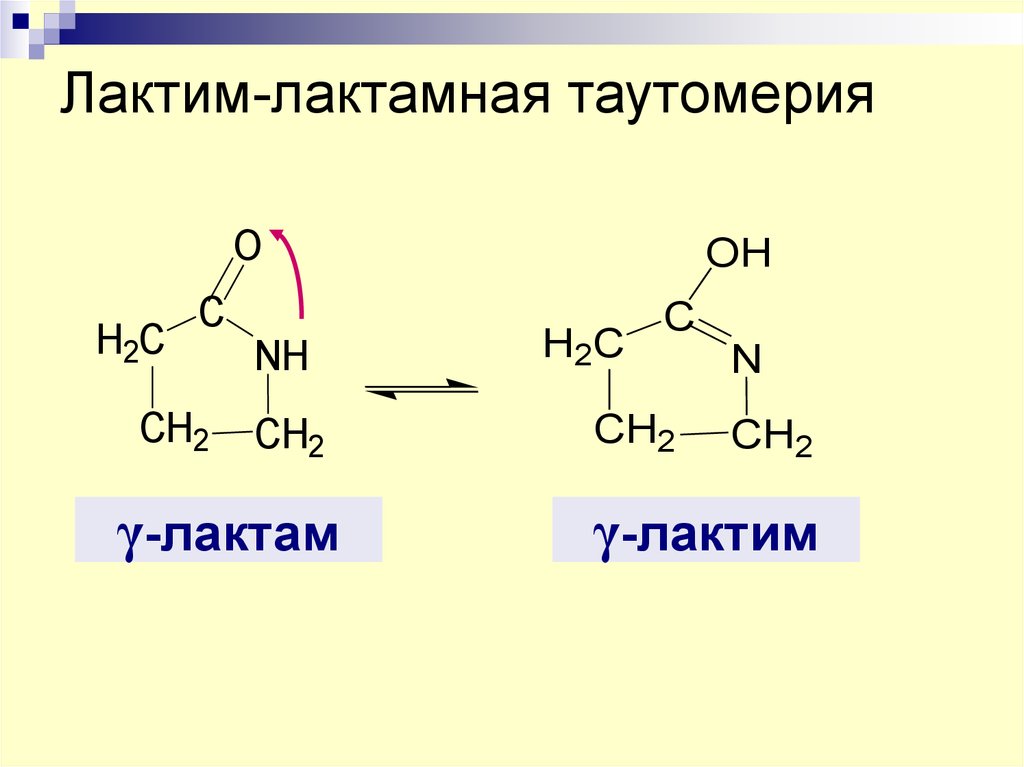
47. Лактим-лактамная таутомерия
OH2C
C
CH2
NH
CH2
γ-лактам
OH
H2C
C
CH2
N
CH2
γ-лактим
48.
Таутомерия расширяетреакционную способность
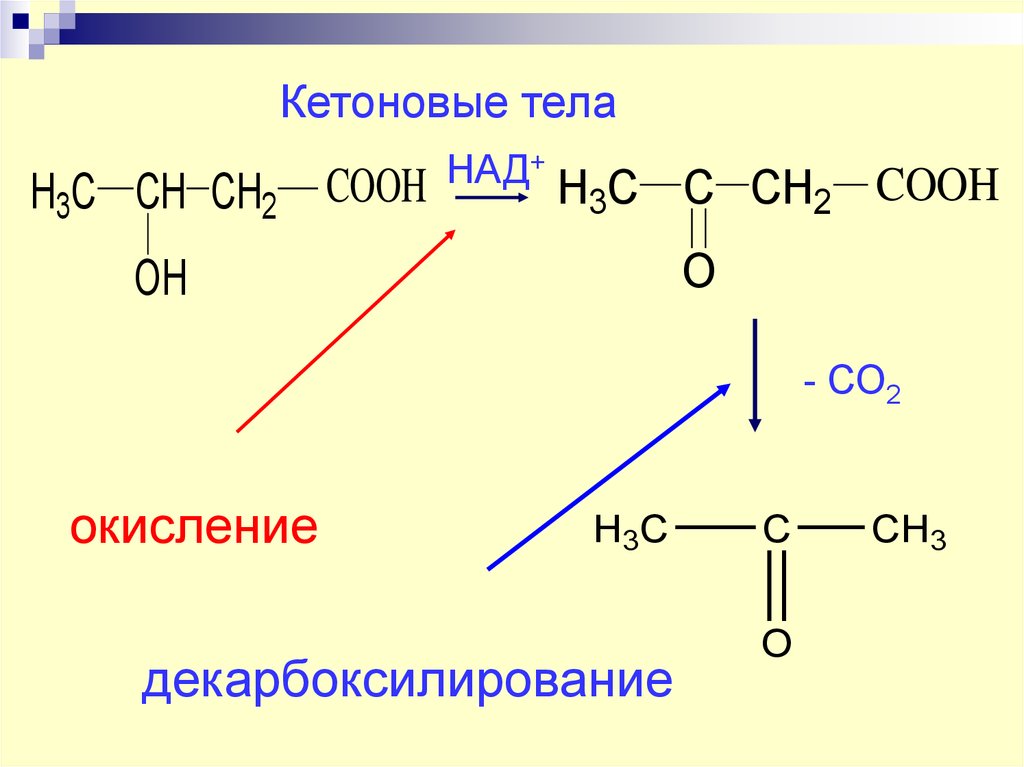
49. Кетоновые тела
H3C CH CH2COOH
НАД+
H3C C CH2 COOH
O
OH
- СО2
окисление
H3C
декарбоксилирование
C
O
CH3
50.
• Кетоновые тела образуются ворганизме в незначительных
количествах в норме
• В значительных количествах – при
декомпенсации сахарного диабета и
длительном голодании
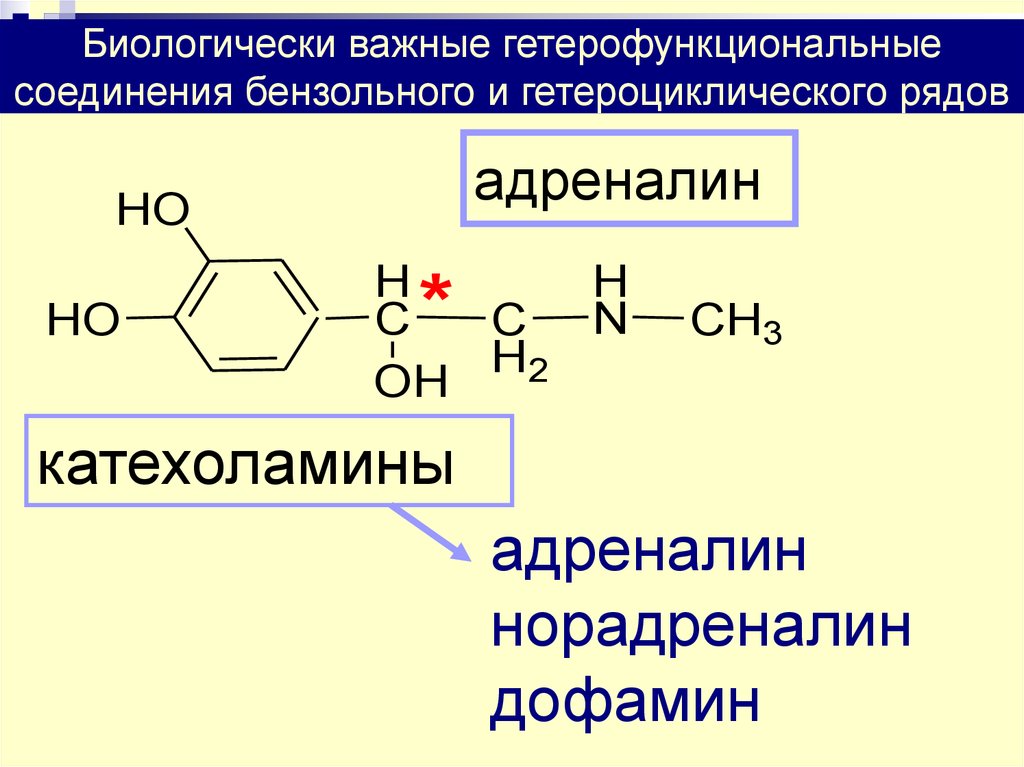
51. адреналин
Биологически важные гетерофункциональныесоединения бензольного и гетероциклического рядов
адреналин
HO
HO
H
H
C
C N
H2
OH
*
CH3
катехоламины
адреналин
норадреналин
дофамин
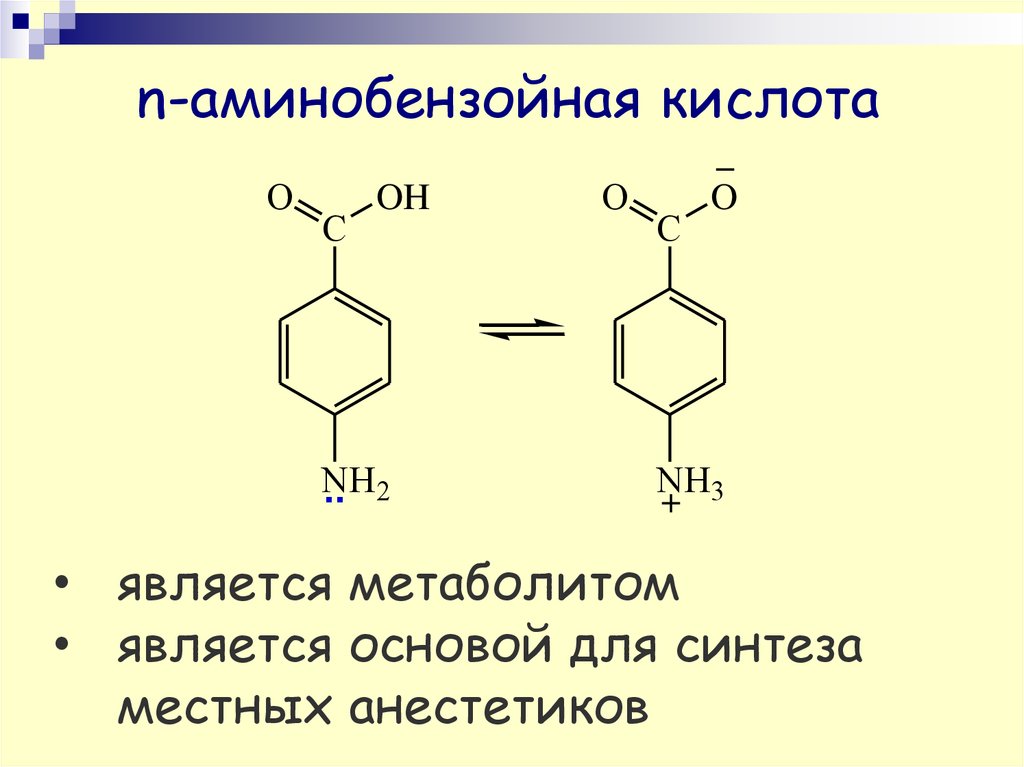
52. n-аминобензойная кислота
OC
OH
NH
.. 2
O
C
O
NH3
• является метаболитом
• является основой для синтеза
местных анестетиков
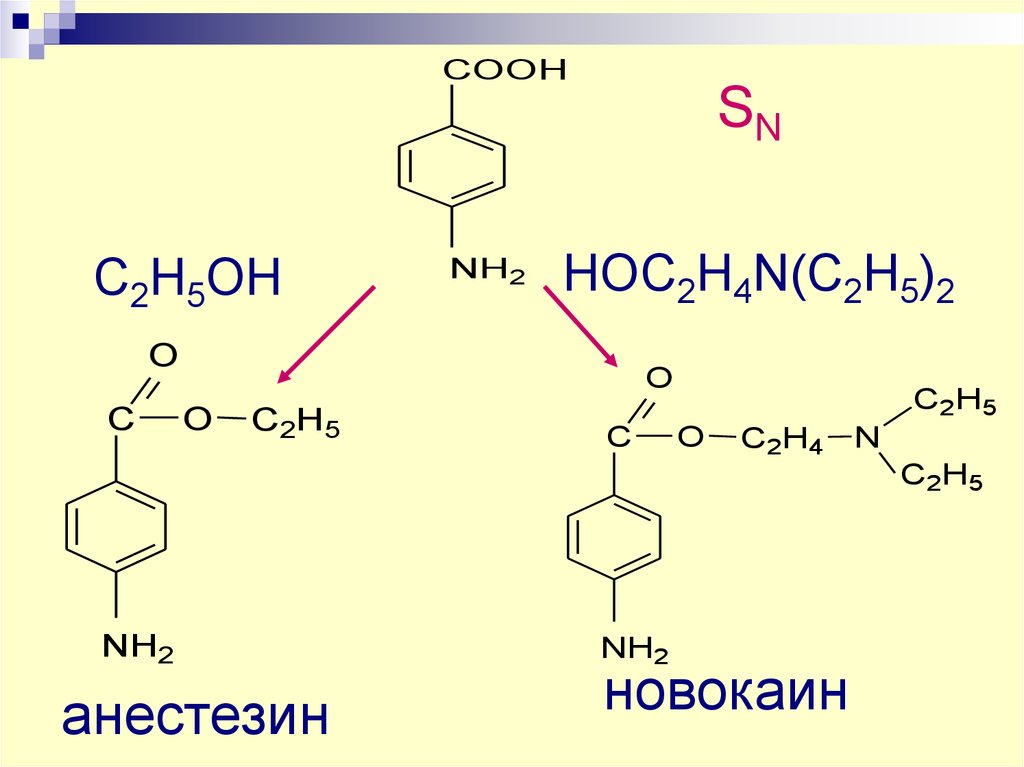
53. С2Н5ОН
COOHSN
С2Н5ОН
NH2
НОС2Н4N(C2H5)2
O
C
O
O
C2H5
C
C2H5
O
C2H4
N
C2H5
NH2
анестезин
NH2
новокаин
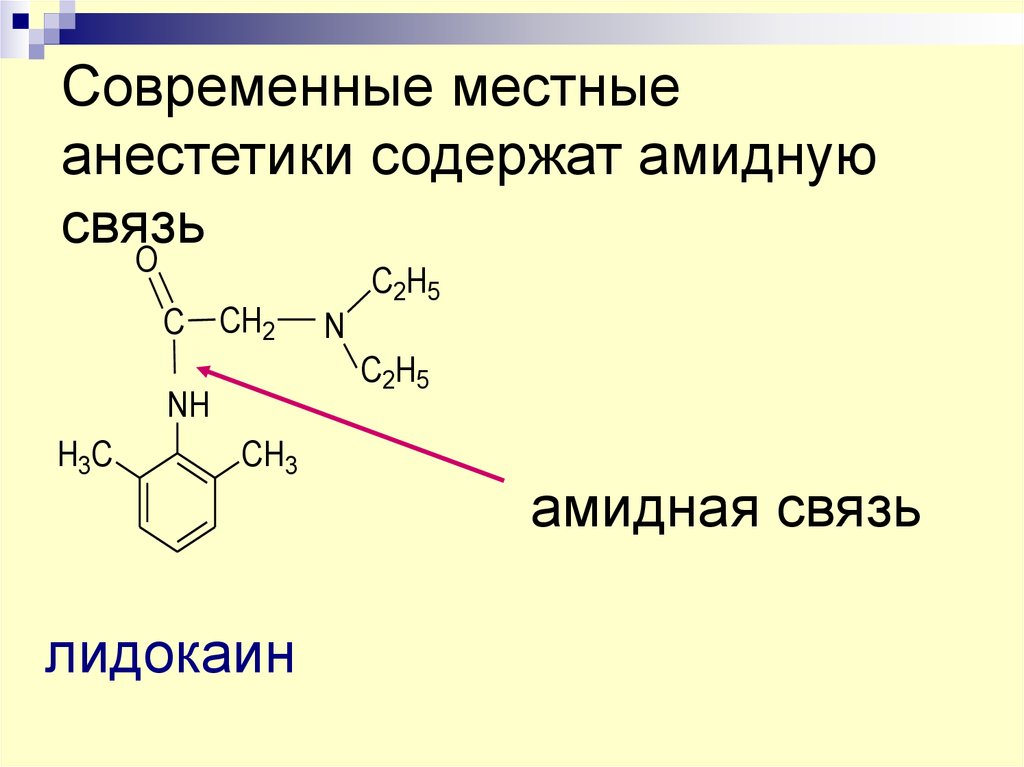
54. Современные местные анестетики содержат амидную связь
OC2H5
C CH2
C2H5
NH
H3C
N
CH3
лидокаин
амидная связь
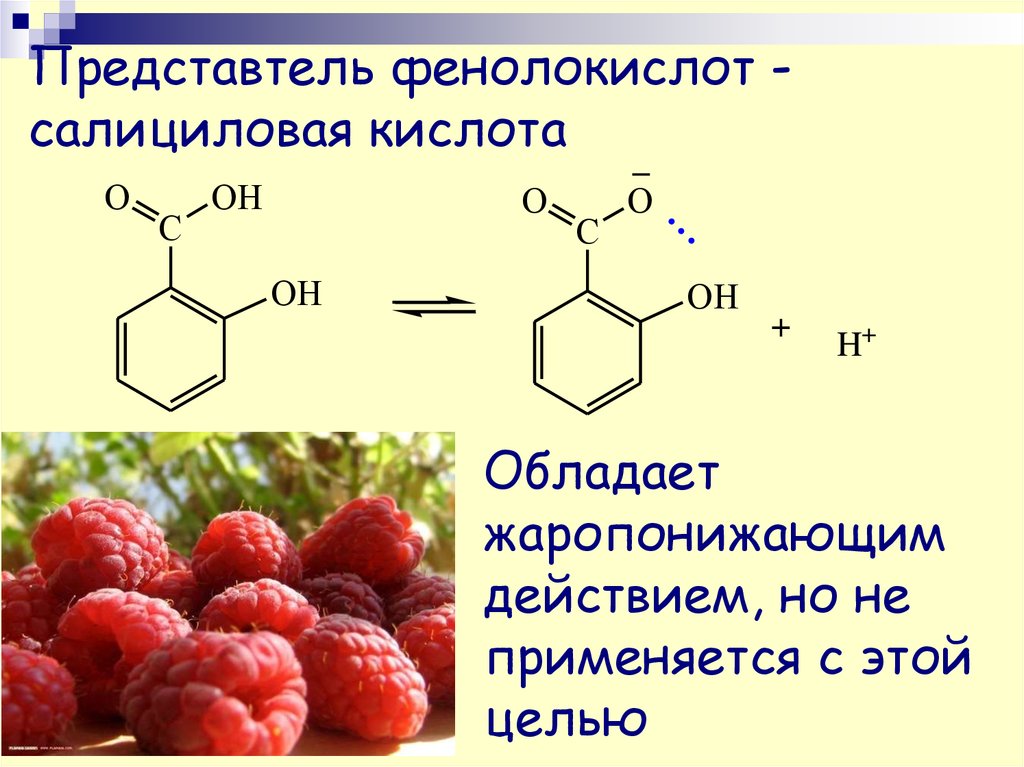
55. Представтель фенолокислот - салициловая кислота
Представтель фенолокислот салициловая кислотаO
C
OH
O
OH
C
O
...
OH
H+
Обладает
жаропонижающим
действием, но не
применяется с этой
целью
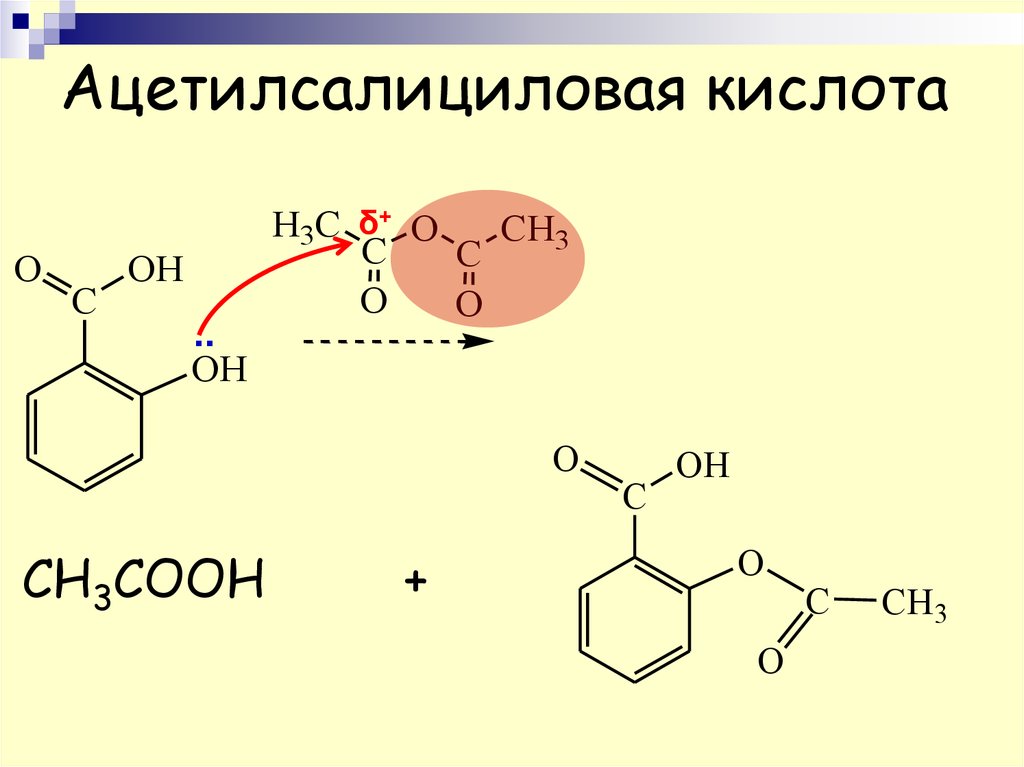
56. Ацетилсалициловая кислота
OC
OH
..
H3C δ+ O
CH3
C
C
O
O
OH
O
СН3СООН
+
C
OH
O
O
C
CH3
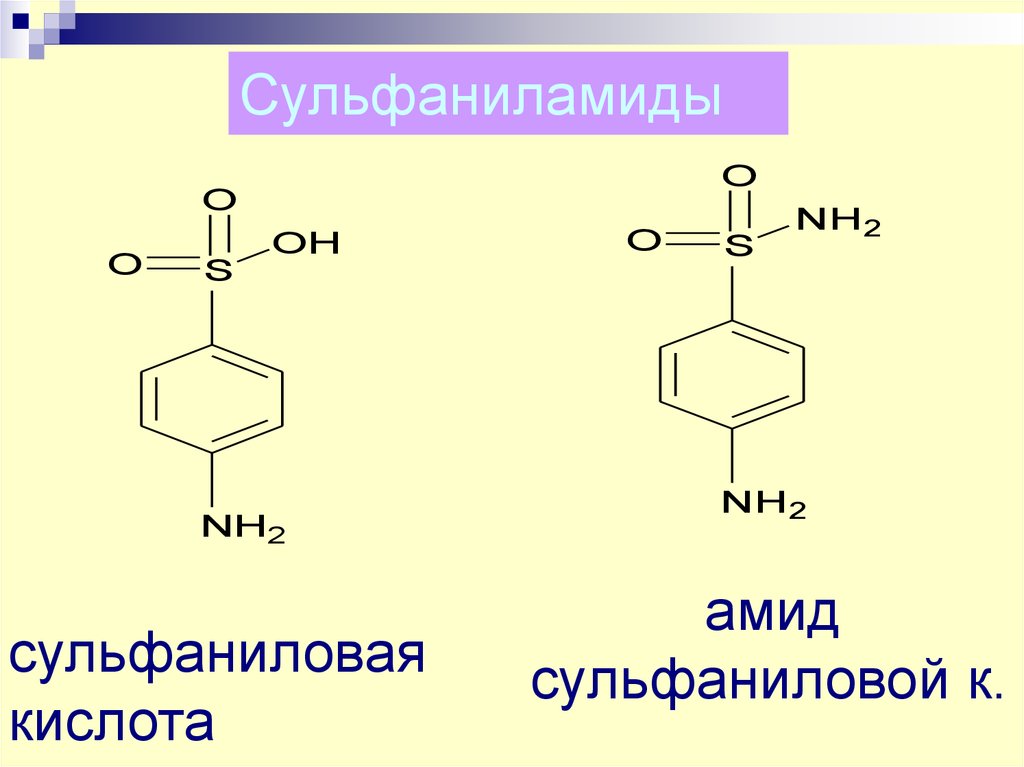
57. Сульфаниламиды
OO
O
S
OH
NH2
сульфаниловая
кислота
O
S
NH2
NH2
амид
сульфаниловой к.
58.
СульфаниламидыO
O
S
O
NHR
NH2
C
OH
NH2
ПАБК
Сульфаниламиды обладают
антибактериальным действием
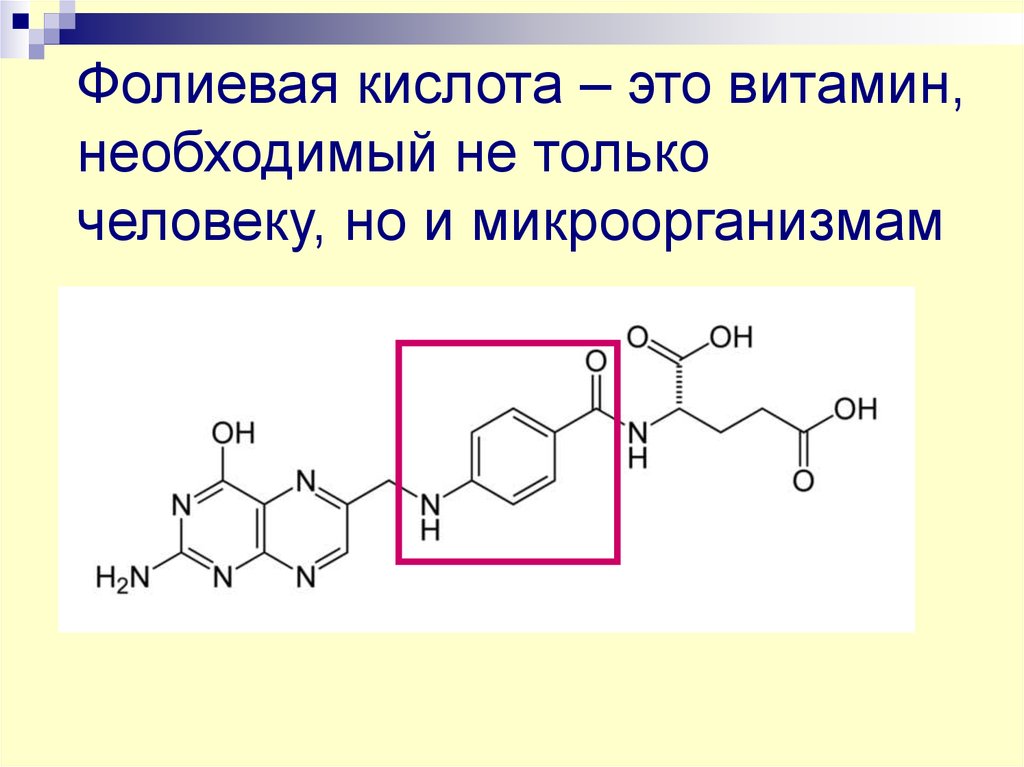
59. Фолиевая кислота – это витамин, необходимый не только человеку, но и микроорганизмам
60. Механизм действия сульфаниламидов основан на конкуренции между СА и ПАБК
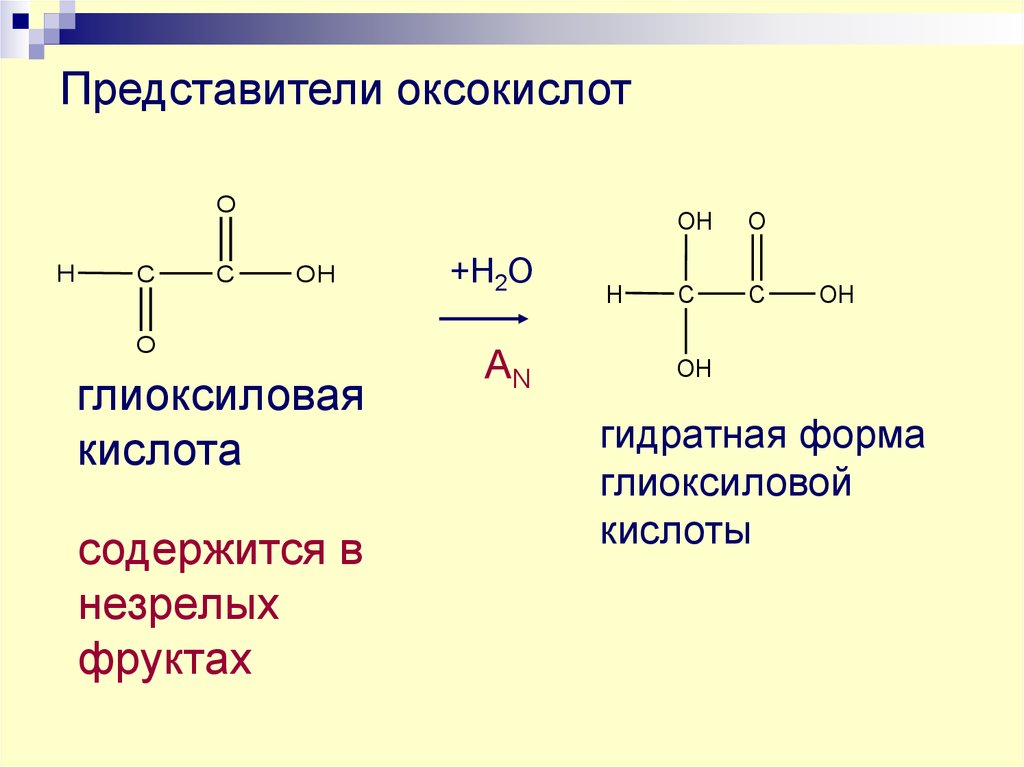
61. Представители оксокислот
OH
C
C
OH
O
глиоксиловая
кислота
содержится в
незрелых
фруктах
+H2O
AN
H
OH
O
C
C
OH
OH
гидратная форма
глиоксиловой
кислоты
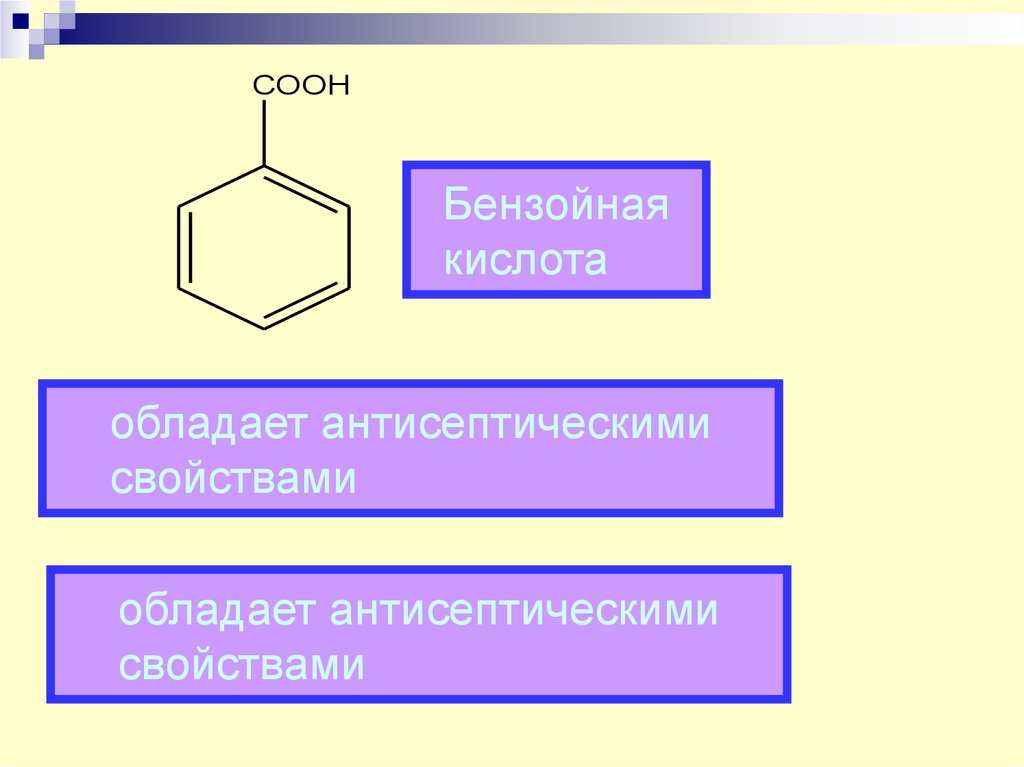
62. Бензойная кислота
COOHБензойная
кислота
обладает антисептическими
свойствами
обладает антисептическими
свойствами
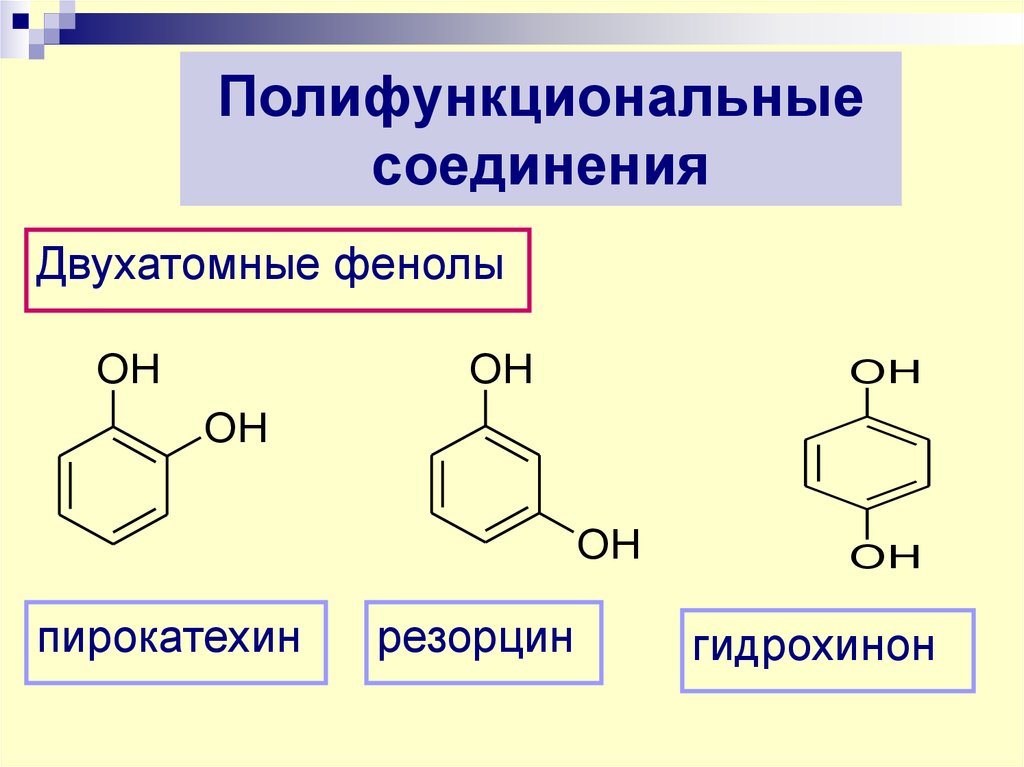
63. Полифункциональные соединения
Двухатомные фенолыOH
OH
OH
OH
OH
пирокатехин
резорцин
OH
гидрохинон
64.
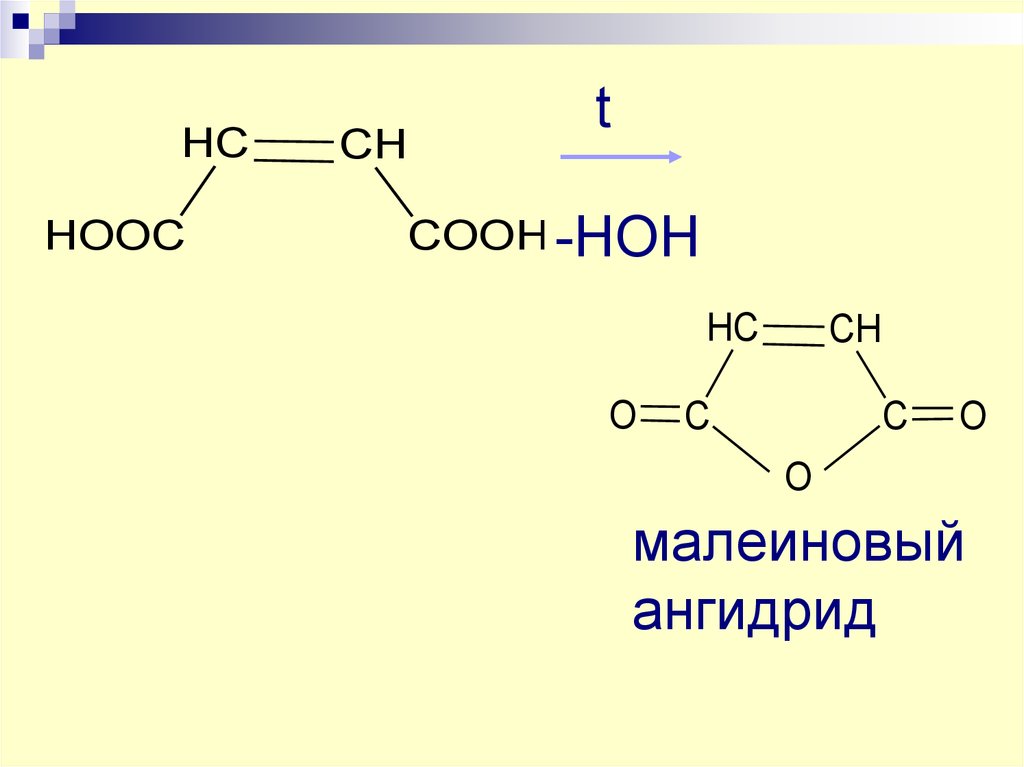
HCHOOC
CH
t
COOH -HOH
HC
O
CH
C
C
O
O
малеиновый
ангидрид
65. Гетерофункциональные соединения обладают типичной реакционной способностью
Взаимное влияние разных функ.групп приводит к появлению
специфических свойств
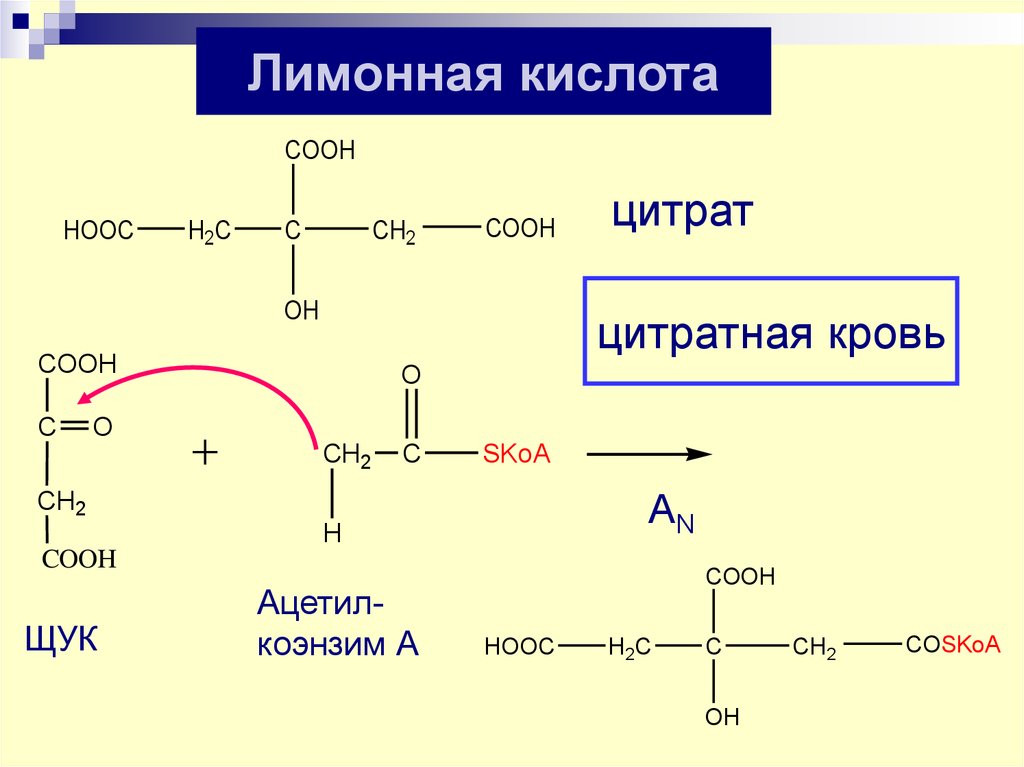
66.
Лимонная кислотаCOOH
HOOC
H2C
C
CH2
COOH
OH
цитратная кровь
COOH
C
цитрат
O
O
CH2
C
SKoA
CH2
AN
H
COOH
ЩУК
Ацетилкоэнзим А
COOH
HOOC
H2C
C
OH
CH2
COSKoA


















 Химия
Химия








