Похожие презентации:
Коллоидная химия. Введение
1. Коллоидная химия. Введение
12.
Коллоидная химия (от греч. κόλλα — клей)- физическая химия поверхностных явлений и
дисперсных систем.
Предметом изучения коллоидной химии
являются гетерогенные
смеси
веществ
(дисперсные системы), их свойства, процессы,
протекающие в этих системах.
Задачи
коллоидной
химии
–
прогнозирование направления и изучение
особенностей протекания физико-химических
процессов в дисперсных системах.
3.
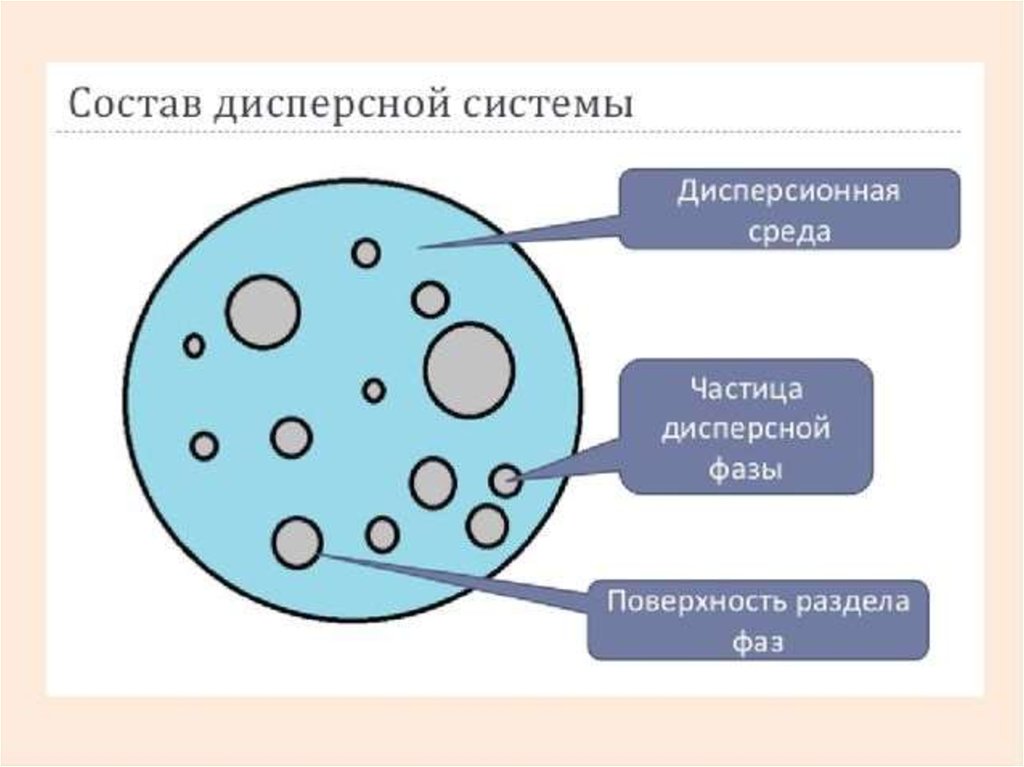
Основные понятия в коллоидной химииДисперсные системы – это двух- или в общем случае
многофазные гетерогенные системы, в которых одно
вещество (или несколько) находится в состоянии более
или менее высокой степени раздробленности и
распределено в сплошной среде другого вещества.
Дисперсная система состоит из дисперсной фазы и
дисперсионной среды.
Дисперсная фаза – это та часть дисперсной системы,
которая раздроблена и распределена в дисперсионной
среде.
Дисперсионная среда – это сплошная фаза, в которой
распределено раздробленное вещество дисперсной фазы.
3
4.
45.
Признаками дисперсных систем являются:- гетерогенность, т. е. наличие поверхности раздела
между частицами дисперсной фазы и дисперсионной
средой;
- дисперсность, т. е. раздробленность.
Различия дисперсных систем и истинных растворов
Размер частиц, м Гетерогенность
Дисперсные
> 10-9
Гетерогенные
системы
системы
Истинные
< 10-9
Гомогенные
растворы
системы
5
6.
Степень раздробленности дисперснойфазы характеризуется дисперсностью D.
Дисперсность
–
это
величина,
обратная линейным размерам частиц l.
6
7.
Классификация дисперсных систем1а. Классификация дисперсных систем по степени
дисперсности
- грубодисперсные системы с
размером частиц более10-5 м;
- тонкодисперсные (коллоидные
системы) с размером частиц 10-9–10-5 м;
- молекулярно-дисперсные
(истинные растворы) с размером
частиц менее 10-9 м.
7
8.
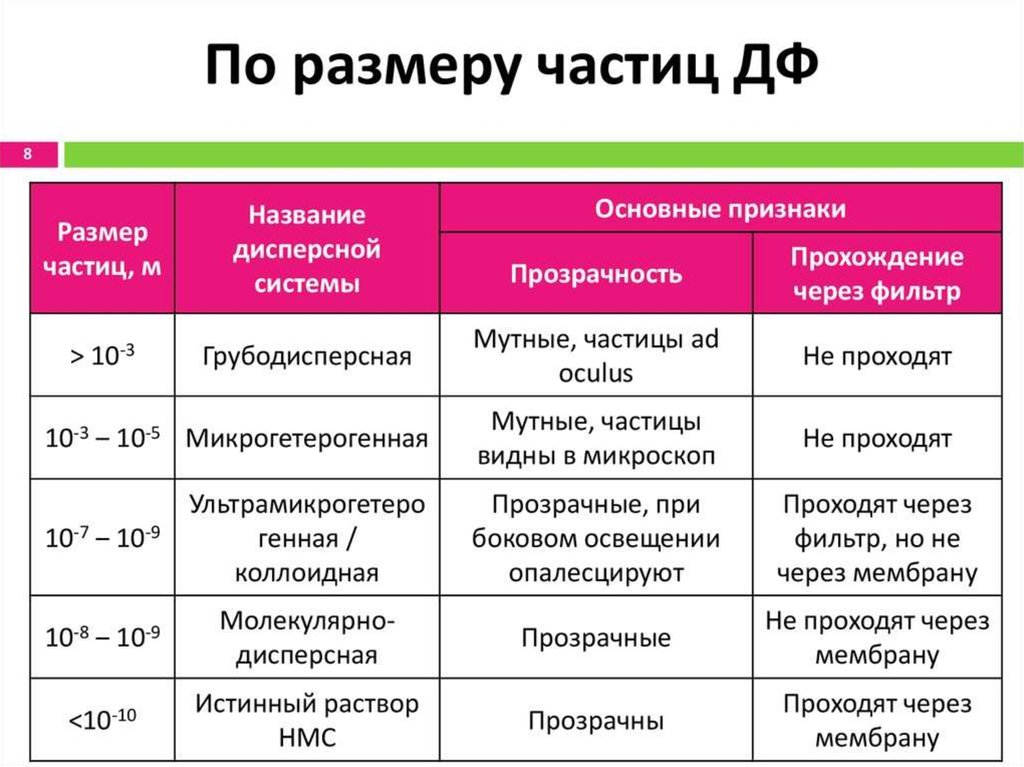
1б. Классификация дисперсных систем по размерамВиды систем
Размер
частиц
или пор, м
Грубодисперсные
(суспензии, > 10-5
эмульсии, пены, пористые тела)
Микрогетерогенные
или 10-5 – 10-7
тонкодисперсные (дымы, аэрозоли,
пористые тела)
Ультрамикрогетерогенные
или 10-7 – 10-9
коллоидно-дисперсные (золи или
коллоидные растворы)
Истинные растворы
< 10-9
8
9.
910.
1011.
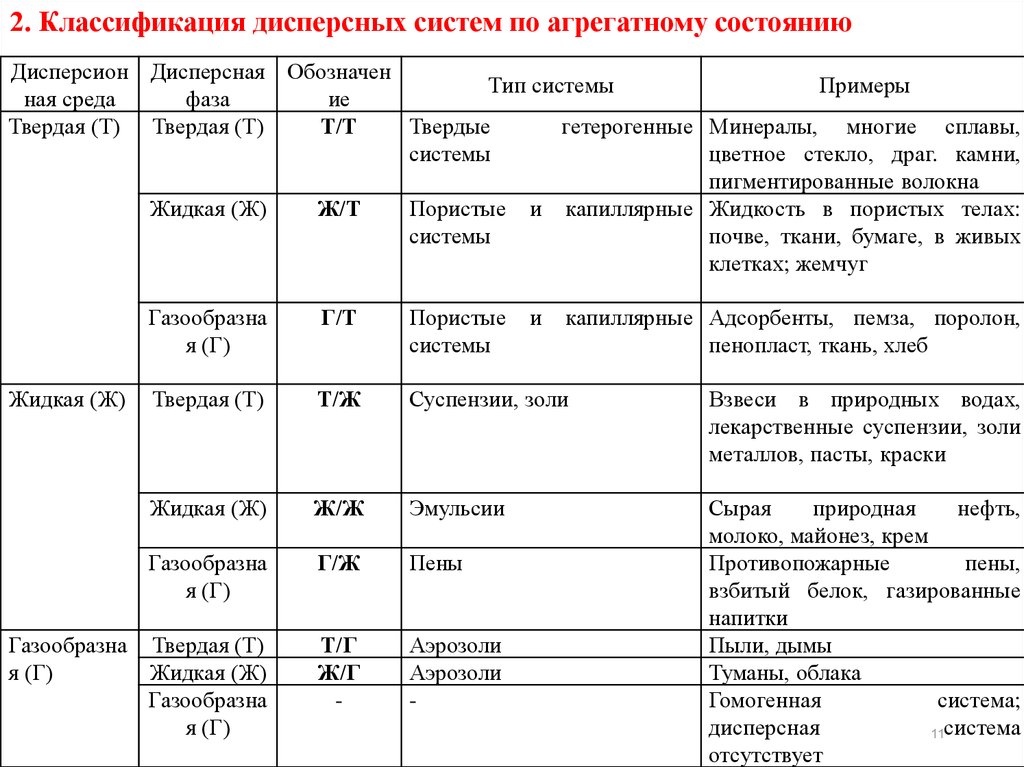
2. Классификация дисперсных систем по агрегатному состояниюДисперсион Дисперсная Обозначен
Тип системы
Примеры
ная среда
фаза
ие
Твердая (Т) Твердая (Т)
Т/Т
Твердые
гетерогенные Минералы, многие сплавы,
системы
цветное стекло, драг. камни,
пигментированные волокна
Жидкая (Ж)
Ж/Т
Пористые и капиллярные Жидкость в пористых телах:
системы
почве, ткани, бумаге, в живых
клетках; жемчуг
Газообразна
я (Г)
Г/Т
Пористые
системы
Твердая (Т)
Т/Ж
Суспензии, золи
Взвеси в природных водах,
лекарственные суспензии, золи
металлов, пасты, краски
Жидкая (Ж)
Ж/Ж
Эмульсии
Газообразна
я (Г)
Г/Ж
Пены
Газообразна Твердая (Т)
я (Г)
Жидкая (Ж)
Газообразна
я (Г)
Т/Г
Ж/Г
-
Аэрозоли
Аэрозоли
-
Сырая
природная
нефть,
молоко, майонез, крем
Противопожарные
пены,
взбитый белок, газированные
напитки
Пыли, дымы
Туманы, облака
Гомогенная
система;
дисперсная
11система
отсутствует
Жидкая (Ж)
и
капиллярные Адсорбенты, пемза, поролон,
пенопласт, ткань, хлеб
12.
3. Классификация по характеру взаимодействия частицсо средой
Лиофильные системы характеризуются тем, что молекулы
дисперсионной среды в значительной степени взаимодействуют с
частицами дисперсной фазы (сольватируются), образуя вокруг нее
оболочку. Эти системы характеризуются низким значением
поверхностного натяжения и имеют предельно высокую
дисперсность. К таким системам относятся растворы ВМС
(например, желатин, целлюлоза, крахмал и т.д.).
Лиофобные системы не образуют сольватной оболочки из
дисперсионной среды вокруг частиц дисперсной фазы. В таких
системах взаимодействие между частицами различных фаз
значительно слабее. Значение межфазного поверхностного
натяжения велико, вследствие чего система проявляет тенденции к
самопроизвольному укрупнению частиц дисперсной фазы. Такие
системы образуют неорганические и органические вещества плохо
растворимые в данной среде.
13









 Химия
Химия