Похожие презентации:
Физиология растений. Фотоиндуцированное окисление воды
1.
Физиология растенийДемидчик Вадим
Викторович
(д.б.н., зав. каф. физиологии
и биохимии растений)
Copyrights of Vadim Demidchik
2.
ФС II и ФС I размещаются последовательно в цепитранспорта электронов от Н2О до НАДФ+.
Для восстановления одной молекулы НАДФ+ в
процессе фотосинтеза необходимо два электрона и
два протона, при этом донором электронов является
вода.
Фотоиндуцированное окисление воды происходит в
ФС II, восстановление НАДФ+ – ФС I.
Таким образом, фотосистемы должны
функционировать во взаимодействии для
восстановления углерода до сахаров и выделения
кислорода.
Современная «квантовая теория» передачи энергии в ранних
стадиях фотосинтеза (теория Флемминга):
http://www.physorg.com/news95605211.html
3.
Поток электронов в фотосинтезе начинается с ФС II:(компоненты расположены очень близко - на расстоянии всего
около 10 ангстрем, что повышает вероятность перехода по
компонентам цепи, а не на молекулы раствора)
1. Электрон от
первичного донора ФСII –
возбужденного Р680 (Р680* или Р680-)
(Р680 – один из специальных димеров хл. а - всего их два димера приобретает более позитивное значение потенциала
вследствие присоединения электронов от свето-собирающего
комплекса фотосистемы 2 - ССКII)
переходит на
феофитин – первичный акцептор ФСII
это молекула хл., лишенная иона магния
после принятия электрона она возбуждается, приобретает
отрицательный заряд и становится радикалом –
.феофитин
4.
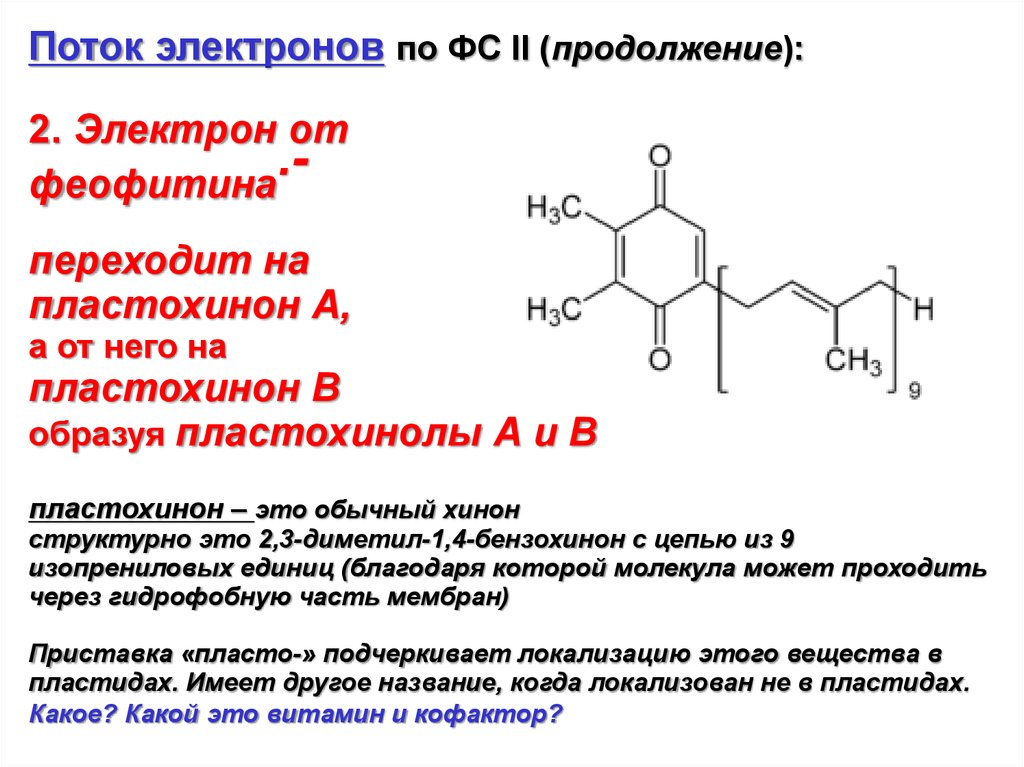
Поток электронов по ФС II (продолжение):2. Электрон от
.феофитина
переходит на
пластохинон А,
а от него на
пластохинон B
образуя пластохинолы А и B
пластохинон – это обычный хинон
структурно это 2,3-диметил-1,4-бензохинон с цепью из 9
изопрениловых единиц (благодаря которой молекула может проходить
через гидрофобную часть мембран)
Приставка «пласто-» подчеркивает локализацию этого вещества в
пластидах. Имеет другое название, когда локализован не в пластидах.
Какое? Какой это витамин и кофактор?
5.
Поток электронов по ФС II (продолжение):3. Восстановление Р680
электрон от воды
переходит на «окисленный Р680» (Р680+),
восстанавлиявая его обратно до Р680
это происходит в результате работы
The oxygen-evolving complex (OEC) – «кислород-выделяющий
комплекс» также известного под другим названием - water-splitting
complex – «водоразлогающий
комплекс»
Это фермент, окисляющий воду . Процесс, катализируемый им, называют фотоокислением
воды . Теория Кока (1970 г.) – фермент ОЕС может существовать в 5 состояниях S0, S1, S2, S3 и
S4. При взаимодействии с окисленным Р680 фермент постепенно переходит в состояние S4,
теряя 4 электрона, которые он забирает от 2 молекул воды . На Р680 электроны передаются
через боковую ветвь тирозина D1-Y161.
OEC – сложно-устроенный металлопротеин , содержащий 4 атома марганца, 1 атом кальция и как
минимум один атом хлора (возможно 2) + карбонат ионы - Mn4Ca1OxCl1–2(HCO3)y.
Предполагается, что ОЕС эволюционно возник, благодаря большой концентрации марганецсодержащих минералов ранцита и холандита в ранних океанах, из которых этот металл был
утилизирован примитивными Cyanobacteria в качестве активного центра своих ферментов.
6.
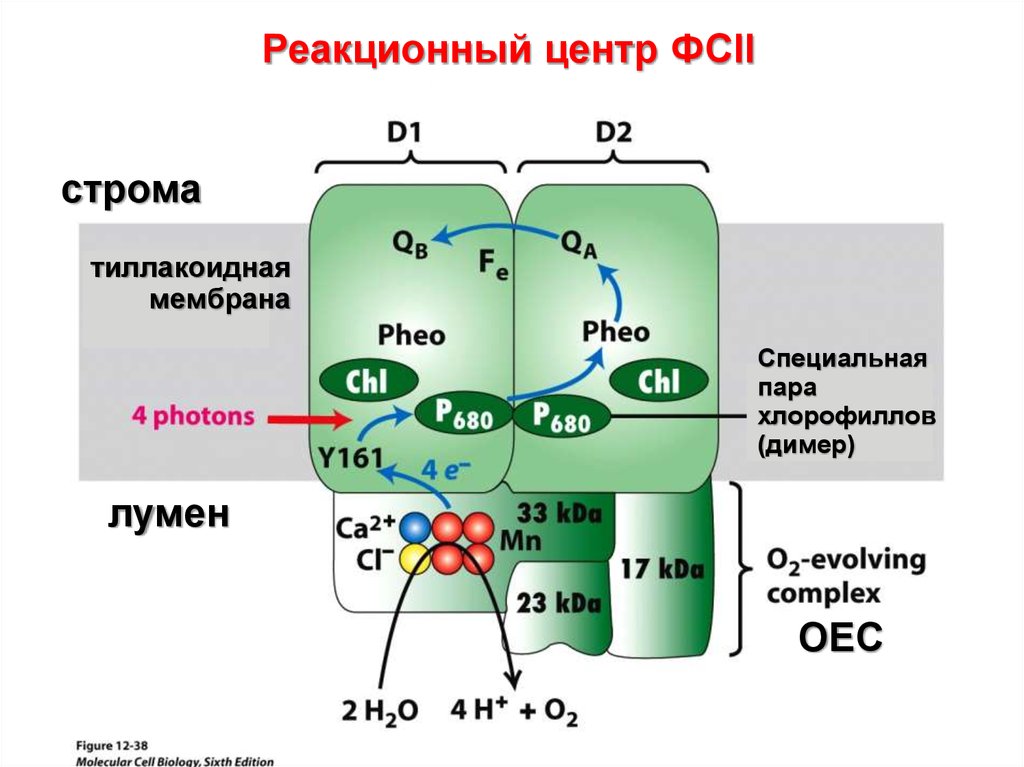
Реакционный центр ФСIIстрома
тиллакоидная
мембрана
Специальная
пара
хлорофиллов
(димер)
лумен
ОЕС
7.
Субъединицы белков (только те, длякоторых установлена функция)
Субъединица
Функция
D1
Реакционный центр белка, связывает P680,
феофитин, бета-каротин, хинон и Mn-центр
D2
CP43
PsbO
Реакционный центр белка, связывает P680,
феофитин
Связывает Mn-центр
Стабилизирует Mn-центр
Коэнзимы/кофакторы
Хлорофилл
Бета-каротин
Гем b559
Феофитин
Пластохиноны
Mn-центр
Поглощает свет
Поглощает свет, гасит избыточное
возбуждение
Участвует в передаче электронов от
пласитохинона В на пул свободных
пластохинонов
Первичный акцептор электронов
Мобильные внутритиллакоидные
переносчики электронов
OEC (Oxygen-Evolving Complex)
8.
ФС II и ФС I размещаются последовательно в цепи транспортаэлектронов от Н2О до НАДФ+:
Хиноновый
цикл:
дополн.
транспорт
протонов
строма
Тилакоидная
мембрана
2 фотона
2 фотона
лумен
Реакционный
центр
ФСII
Комплекс
цит-в bf
Пластоционины
Реакционный
центр
ФСI
АТФ-синтаза
Q - quinone – «хинон»
9.
Поток электронов (продолжение):4. Работа комплекса цитохромов b6f
электрон от пластохинола (QH2)
переходит на пластоцианин
b6f - димер, каждый из мономеров которого состоит
из 8 субъединиц:
4 большие субъединицы –
(1) цит. f (32 кДа),
(2) цит. b6 (25 кДа) с «высоко-» и «низко-энергетическими»
гемовыми группами,
(3) комплекс Риске (19 кДа) – железосерный белок – содержит [2Fe2S]-кластер,
(4) субъединица IV (17 кДа)
4 малые субъединицы – (все по 3-4 кДа) - PetG, PetL, PetM и PetN.
Общий молекулярный вес комплекса b6f – 217 кДа.
10.
Поток электронов (продолжение):4. Работа комплекса цитохромов b6f «хиноновый цикл»
Первая часть Q-цикла
высокоэнергетический перенос:
- QH2 связывается с положительной стороной 'p‘ (лумен) комплекса b6f
- QH2 отдает электроны железосерному центру (Fe-Sцентру) и превращается в семихинон (SQ) и также выделяет 2
протона (Н+) в тилакоидный лумен.
- восстановленный железо-серный центр переносит электроны через
цитохром f до пластоцианина
В случае так-называемого низкоэнергетического переноса:
- семихинон транспортирует электроны на гем bp цитохрома b6
- гем bp переносит электроны на гем bn
- гем bn восстанавливает Q до SQ.
11.
Поток электронов (продолжение):4. Работа комплекса цитохромов b6f «хиноновый цикл»
Вторая часть Q-цикла
- второй QH2 связывается с комплексом.
- в высокоэнергетическом переносе один электрон
восстанавливает вторую молекулу пластоцианина
- в низкоэнергетическом переносе электрон от гема bn
переносится на SQ, образуя Q2- - полностью восстановленную
форму хинона, которая может принимать 2 протона из стромы
и формировать QH2.
Регенерируемые окисленные Q и восстановленные QH2 могут
передвигаться внутри мембраны в противоположные стороны.
12.
4. Работа комплекса цитохромов b6f - «хиноновый цикл»Первая часть
Q-цикла
лумен
строма
Вторая часть
Q-цикла
13.
Поток электронов (продолжение):5. Работа пластоцианинов (ПЦ)
Перенос электронов на ПЦ
Медь-содержащий (потому голубой) белок фотосинтетической ЭТЦ.
Имеет мономерную структуру (10,5 кДа), всего 99 аминокислот.
ПЦ-Cu2+ может восстанавливаться цитохромом f до ПЦ-Cu+
ПЦ-Cu+ диффундирует внутри лумена и связывается с P700+.
P700+ окисляет ПЦ-Cu+ обратно до ПЦ-Cu2+.
14.
Обзор механизмов регуляции потоков электронов при фотосинтезе:http://www.pnas.org/content/early/2011/07/21/1110189108.full.pdf














 Биология
Биология








