Похожие презентации:
Основания. Классификация оснований
1. ОСНОВАНИЯ
2.
BaOP2O5 KOH HCl Mg(OH)2
LiOH
H2SO4
Ca(OH)2
Fe(OH)3
NaCl H2O
Ba(OH)2
MgOHCl
K 2O
Al(OH)3
NO AgNO3 CaO Al2O3
3.
Основания- это сложные вещества, состоящие из
атомов металлов и гидроксильных
групп ОН.
Me(OH)n
n = валентность металла
4.
Названия основанийКОН
Mg(OH)2
LiOH
Fe(OH)3
Ca(OH)2
Al(OH)3
гидроксид
гидроксид
гидроксид
гидроксид
гидроксид
гидроксид
калия
магния
лития
железа (III)
кальция
алюминия
5.
Классификация основанийОснования
Растворимые
(Щелочи)
Нерастворимые
6.
BaOP2O5 KOH HCl Mg(OH)2
LiOH
H2SO4
Ca(OH)2
Fe(OH)3
NaCl H2O
Ba(OH)2
MgOHCl
K 2O
Al(OH)3
NO AgNO3 CaO Al2O3
7.
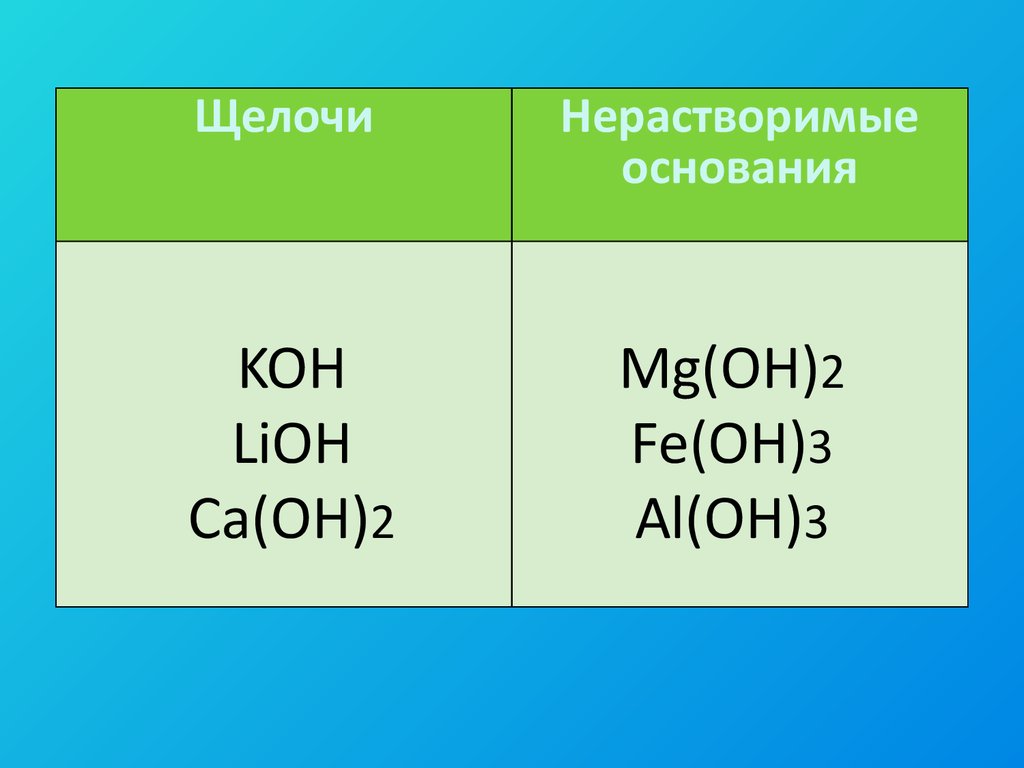
ЩелочиНерастворимые
основания
KOH
LiOH
Ca(OH)2
Mg(OH)2
Fe(OH)3
Al(OH)3
8.
Физические свойстваоснований
Ba(OH)2
Ca(OH)2
LiOH
NaOH
Cu(OH)2
Co(OH)2
9.
Получение основанийПолучение
оснований
растворимых
1. Активный металл + вода =
= щелочь + водород
нерастворимых
1. Соль (в растворе)+ щелочь =
= нерастворимое основание +
+ другая соль
2Na + 2H2O = 2NaOH + H2
2. Оксид активного металла +
+ вода = щелочь
CaO + H2O = Ca(OH)2
FeCl3 + 3NaOH = Fe(OH)3 +
+ 3NaCl
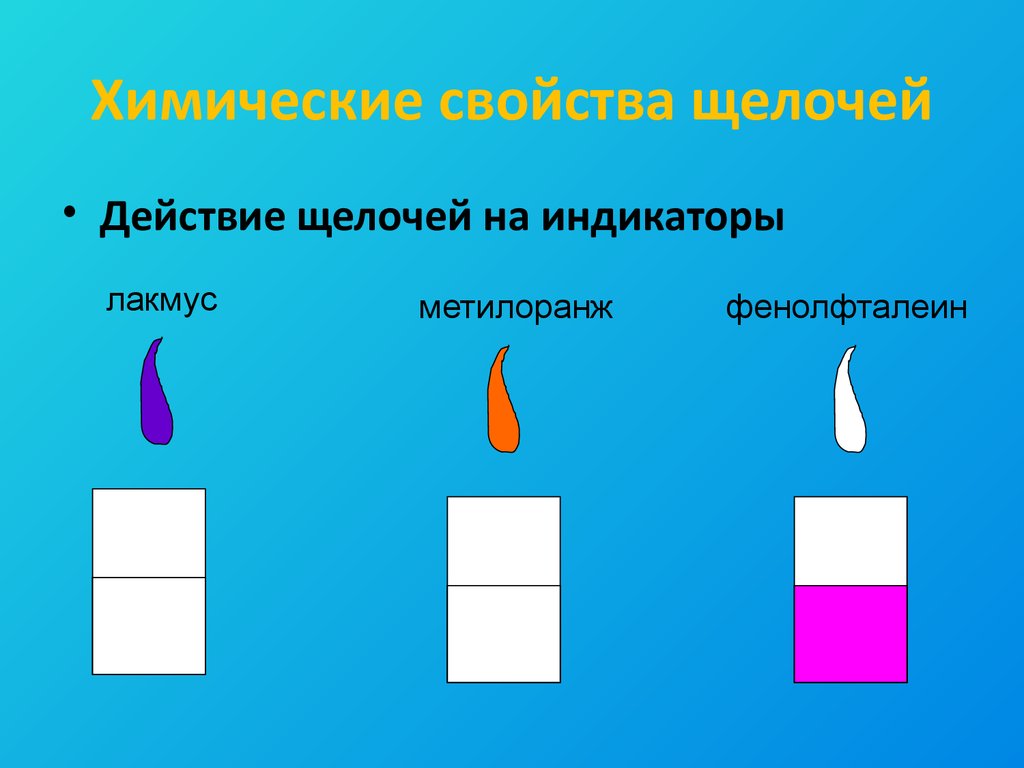
10. Химические свойства щелочей
• Действие щелочей на индикаторылакмус
метилоранж
фенолфталеин
11.
Химические свойстваоснований
1. Взаимодействие с кислотами:
NaOH + HCl = NaCl +H2O
2. Взаимодействие щелочей с кислотными
оксидами:
2NaOH + SO3 = Na2SO4 + H2O
3. Разложение нерастворимых оснований при
нагревании:
12.
ПрименениеФормула
основания
NaOH
КОН
Са(ОН)2
Mg(OH)2
Al(OH)3
Применение








 Химия
Химия