Похожие презентации:
Алкины. Номенклатура и изомерия
1. Алкины
АЛКИНЫАлкинами называются соединения, молекулы
которых содержат углеродный атом, имеющий
тройную связь с другим атомом углерода
СН ≡ СН - ацетилен
Формула для алкинов записывается в следующем
виде:
CnH2n-2
2. i. Номенклатура и изомерия
I. НОМЕНКЛАТУРА И ИЗОМЕРИЯрациональная
систематическая
номенклатура
номенклатура
СН ≡ НС
ацетилен
СН3 – С ≡ СН
метилацетилен
СН3 – С ≡ С – СН3
диметилацетилен
СН ≡ С – СН2 – СН2 – СН3 пропилацетилен
этин
пропин
бутин – 2
пентин – 1
СН ≡ С – СН – СН3
|
СН3
З – метил бутин – 1
изопропилацетилен
3. II.Способы получения алкинов
II.СПОСОБЫ ПОЛУЧЕНИЯ АЛКИНОВ1. Промышленные способы получения ацетилена
1) из карбида кальция:
t
CaCO3
CaO + CO2
t
CaO + 3C
CaC2 + 2H2O
CaC2 + CO
Ca(OH)2 + C2H2
2) окисление метана:
O2,1000°
2CН4
С2Н2 + ЗН2
4.
5.
2. Лабораторные способы получения1) получение из дигалогенопроизводных
углеводородов:
Cl
|
NaNH2
NaOH(спирт.р-р)
CH3 – CH
CH2 = CH
CH ≡ CH
-NaCl
- NaCl
|
|
-H O
Cl
Cl
-NH3
2
Если избыток NaOH, значит реакция идет до конца
CH2 – CH2
|
|
Cl
Cl
NaOH(спирт.р-р)
-NaCl
-H O
2
CH = CH2
|
Cl
NaNH2
CH ≡ CH
- NaCl
-NH3
6.
2) из тетрагалогенидов:Cl Cl
|
|
CH – CH + 2 Zn
|
|
пыль
Cl Cl
CH ≡ CH + 2 ZnCl2
З) дегидрирование алканов и алкенов:
CH3 – CH3
Pt;Pd,Ni
Pt;Pd,Ni
CH2 = CH2
CH ≡ CH
200-300°
4) Из ацетиленидов щелочных металлов:
HC ≡ CNa + CH3Cl
ацетиленид
натрия
HC ≡ C – CH3 + NaCl
необходимо учитывать реакционную способность
галогеналкила
7.
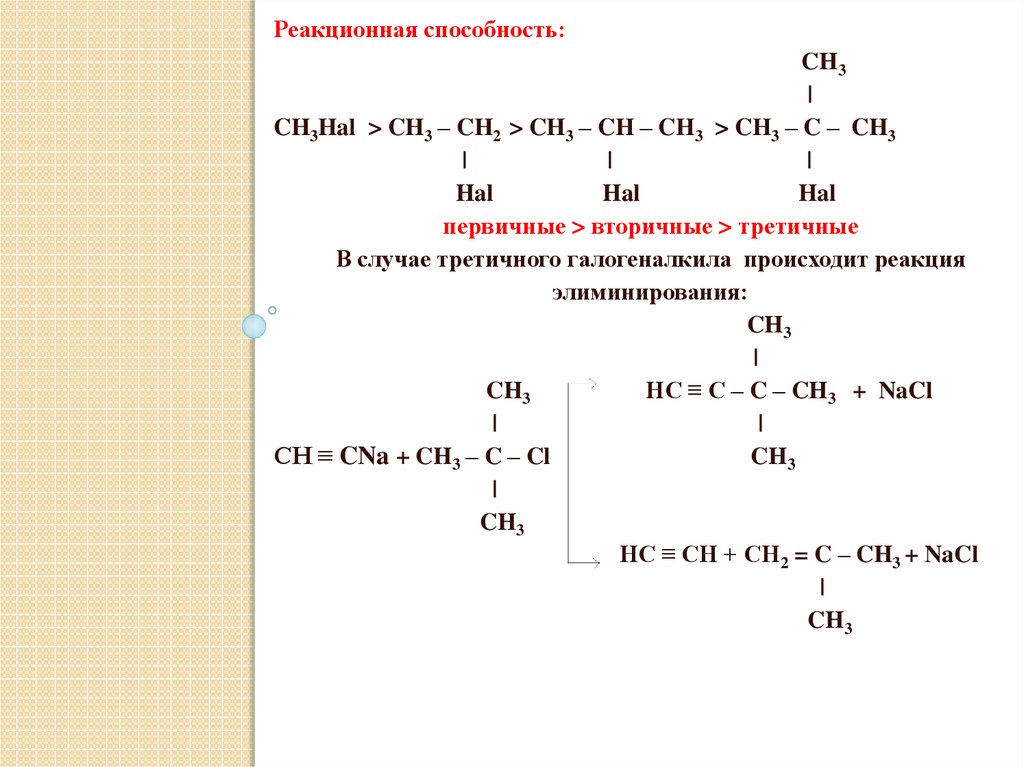
Реакционная способность:CH3
|
CH3Hal > CH3 – CH2 > CH3 – CH – CH3 > CH3 – C – CH3
|
|
|
Hal
Hal
Hal
первичные > вторичные > третичные
В случае третичного галогеналкила происходит реакция
элиминирования:
CH3
|
CH3
HC ≡ C – C – CH3 + NaCl
|
|
CH ≡ CNa + CH3 – C – Cl
CH3
|
CH3
HC ≡ CH + CH2 = C – CH3 + NaCl
|
CH3
8.
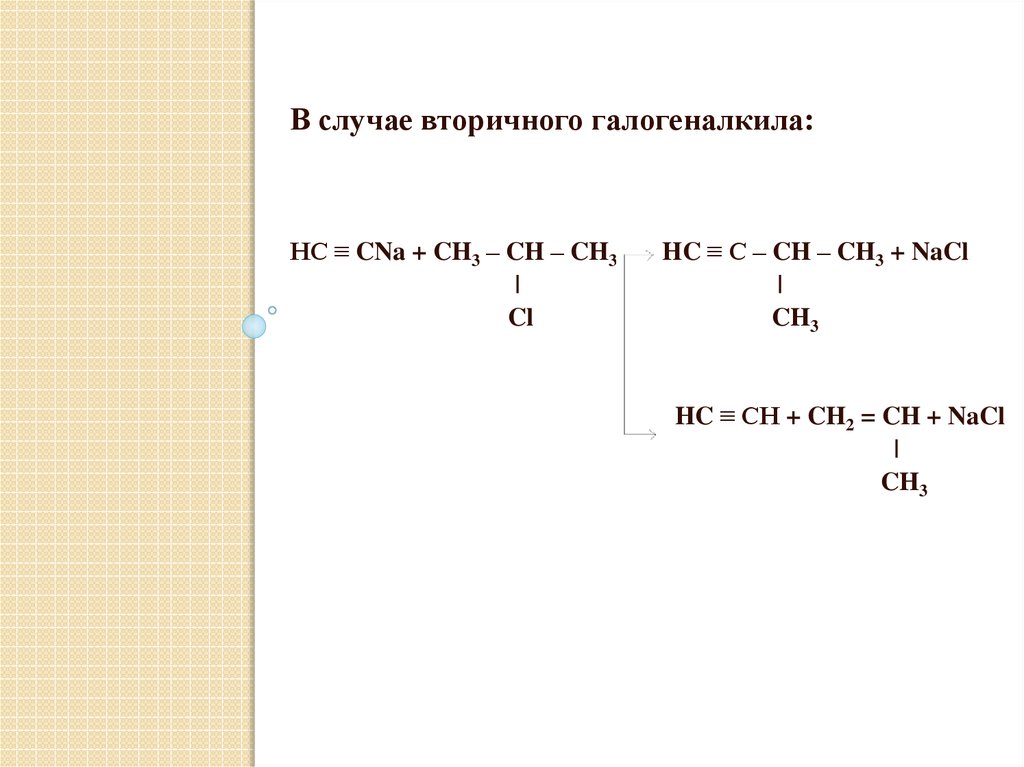
В случае вторичного галогеналкила:HC ≡ CNa + CH3 – CH – CH3
|
Cl
HC ≡ C – CH – CH3 + NaCl
|
CH3
HC ≡ CH + CH2 = CH + NaCl
|
CH3
9. III. Строение алкинов
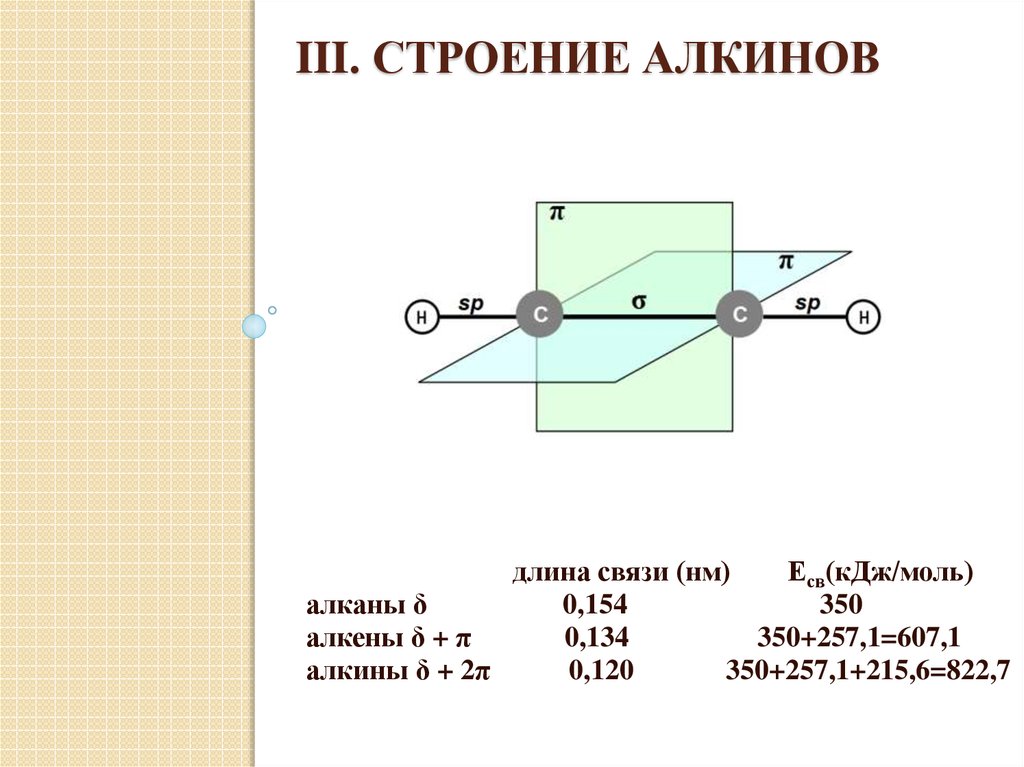
III. СТРОЕНИЕ АЛКИНОВдлина связи (нм)
Есв(кДж/моль)
алканы δ
0,154
350
алкены δ + π
0,134
350+257,1=607,1
алкины δ + 2π
0,120
350+257,1+215,6=822,7
10. IV. Химические свойства алкинов
IV. ХИМИЧЕСКИЕ СВОЙСТВА АЛКИНОВ1. Кислотные свойства (получение ацетиленидов
щелочных и тяжелых металлов):
HC ≡ CH +
NaOH
HC ≡ CH
+
NaNH2
HC ≡ CH
+ AgNO3
HC ≡ CNa + H2O
ацетиленид натрия
HC ≡ CNa + NH3
HC ≡ CAg + HNO3
ацетиленид серебра
качественная реакция на концевую тройную связь
CH ≡ C – CH2 – CH3+AgNО3
Ag – C ≡ C – CH2 – CH3↓+HNO3
CH3 – C ≡ C – CH3 + AgNO3
нет водорода при тройной
связи.
11.
Получение ацетиленида серебраСH ≡ CH
ацетилен
+ 2[Ag(NH3)2]OH
аммиачный раствор оксида
серебра
AgC ≡ CAg + 2H2O + 4NH3
ацетиленид серебра
12.
13.
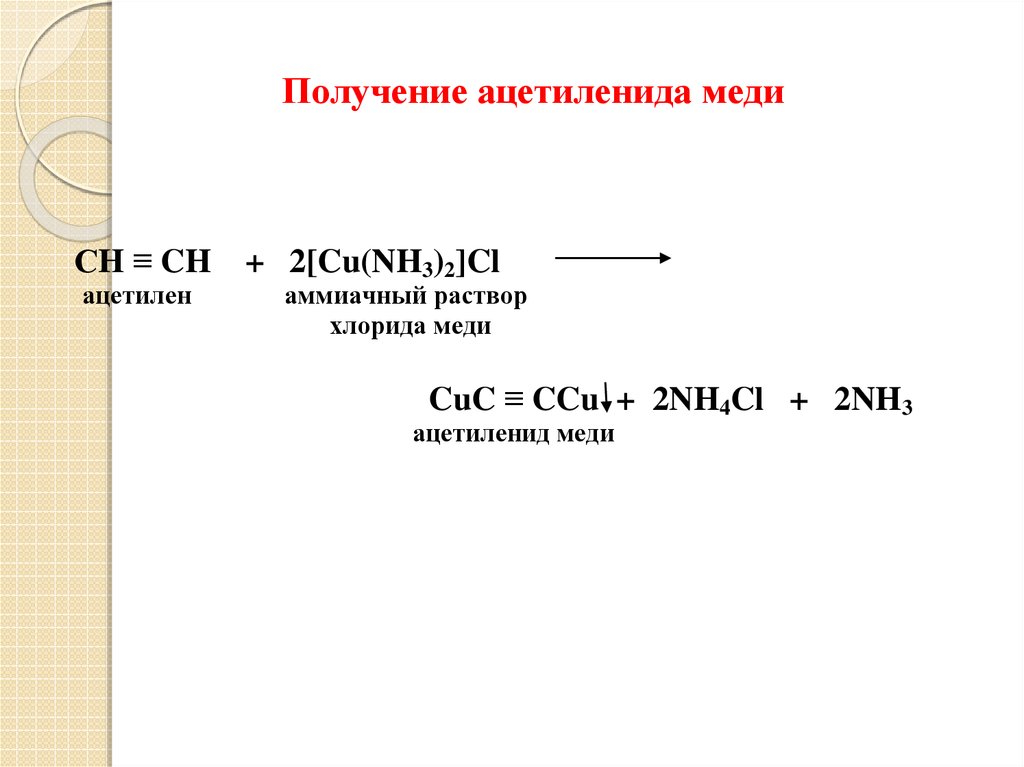
Получение ацетиленида медиСH ≡ CH
ацетилен
+ 2[Cu(NH3)2]Cl
аммиачный раствор
хлорида меди
CuC ≡ CCu + 2NH4Cl + 2NH3
ацетиленид меди
14.
15.
Неустойчивость ацетиленидов металловt
1. AgC ≡ CAg
+ 2O2
2CO2
t
2. AgC ≡ CAg
2C
+
2Ag
+
2Ag
16.
17.
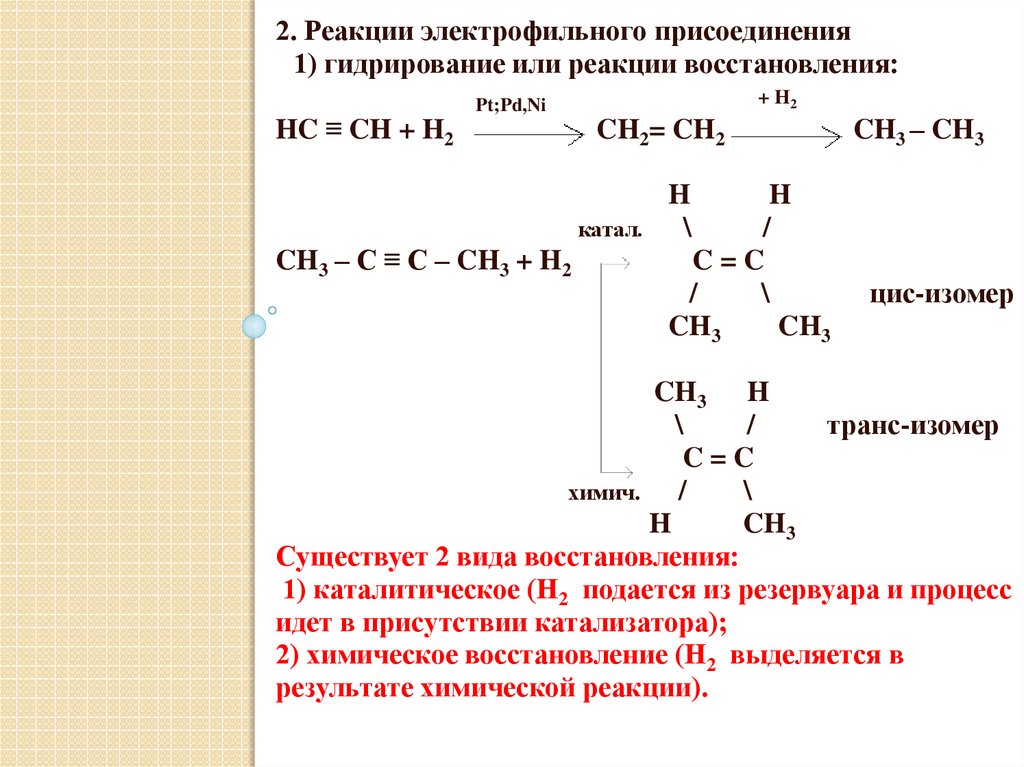
2. Реакции электрофильного присоединения1) гидрирование или реакции восстановления:
HC ≡ CH + H2
+ H2
Pt;Pd,Ni
CH2= CH2
катал.
CH3 – C ≡ C – CH3 + H2
H
/
C=C
/
\
CH3
CH3
CH3 – CH3
H
\
цис-изомер
CH3 H
\
/
транс-изомер
C=C
химич.
/
\
H
CH3
Существует 2 вида восстановления:
1) каталитическое (Н2 подается из резервуара и процесс
идет в присутствии катализатора);
2) химическое восстановление (Н2 выделяется в
результате химической реакции).
18.
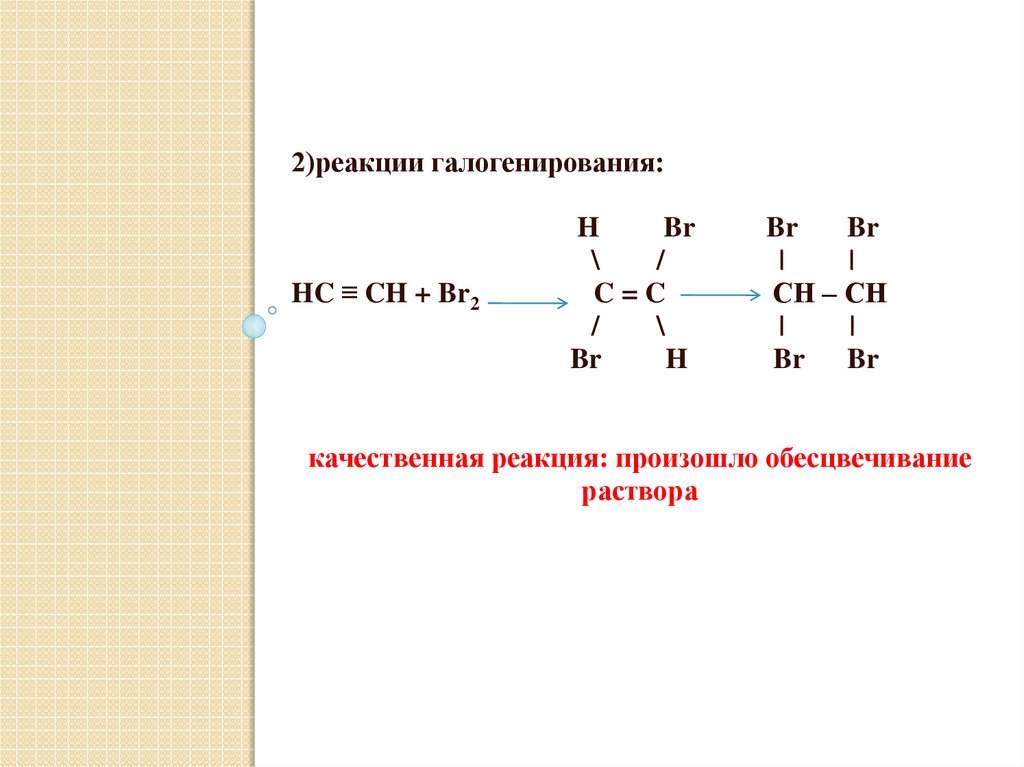
2)реакции галогенирования:HC ≡ CH + Br2
H
Br
\
/
C=C
/
\
Br
H
Br
Br
|
|
СН – СН
|
|
Br Br
качественная реакция: произошло обесцвечивание
раствора
19.
20.
Взаимодействие ацетилена с хлором1. CaC2 + 2HCl
2. 2 KMnO4 + 16HCl
3. Cl2 +
HC ≡ CH
HC ≡ CH
+ CaCl2
5Cl2 + 2MnCl2 + 2KCl + 8H2O
2C + 2 HCl
взрыв
21.
22.
3) реакции гидрогалогенирования:HC ≡ CH + HCl
CH3 – C ≡ CH + HCl
CH2 = CH
|
Cl
CH3 – C = CH2
|
Cl
Реакция идёт по правилу Марковникова
23.
3. Реакции нуклеофильного присоединения:1) реакции гидратации (реакция Кучерова):
HgSO4
HC ≡ CH + H2O
CH3 – C = O
CH2 = CH
|
\
OH
H
енол
По пр.Эльтекова при образовании енола происходит кетоенольная таутомерия
+H2O
HC ≡ CH + Hg2+
HC = +CH
HC = CH
|
|
Hg+
|
Hg+ H-O+-H
CH3 – C = O
CH2 = CH
|
\
OH
H
альдегид
HgSO4
CH3 – C ≡ CH + H2O
CH3 – C = CH2
CH3 – C – CH3
|
║
OH
O
кетон
24.
2) реакции со спиртом:+H+
CH3 – C ≡ CH + (C2H5O)-H+
CH3 – C = CH -
CH3 – C = CH2
|
|
O – C2H5
O – C2H5
3) реакции с карбоновыми кислотами:
+H+
CH3 – C ≡ CH + (CH3 – C = O)-H+
CH3 – C = CH -
CH3 – C = CH2
\
|
|
О
O–C=O
O – C =O
\
\
CH3
CH3
реакции идут по правилу Марковникова
25.
4. Реакции конденсации с карбонильнымисоединениями (альдегидами и кетонами):
HC ≡ CH + CH3 – C = O
\
H
CH3 – CH – C ≡ CH
|
OH бутин-3-ол-2
CH3
|
CH3 – C – C ≡ CH
|
ОH
HC ≡ CH + CH3 – C – CH3
||
O
2-метилбутин-3-ол-2
CH3 – C ≡ C – CH3 + CH3 – C = O
\
H
26.
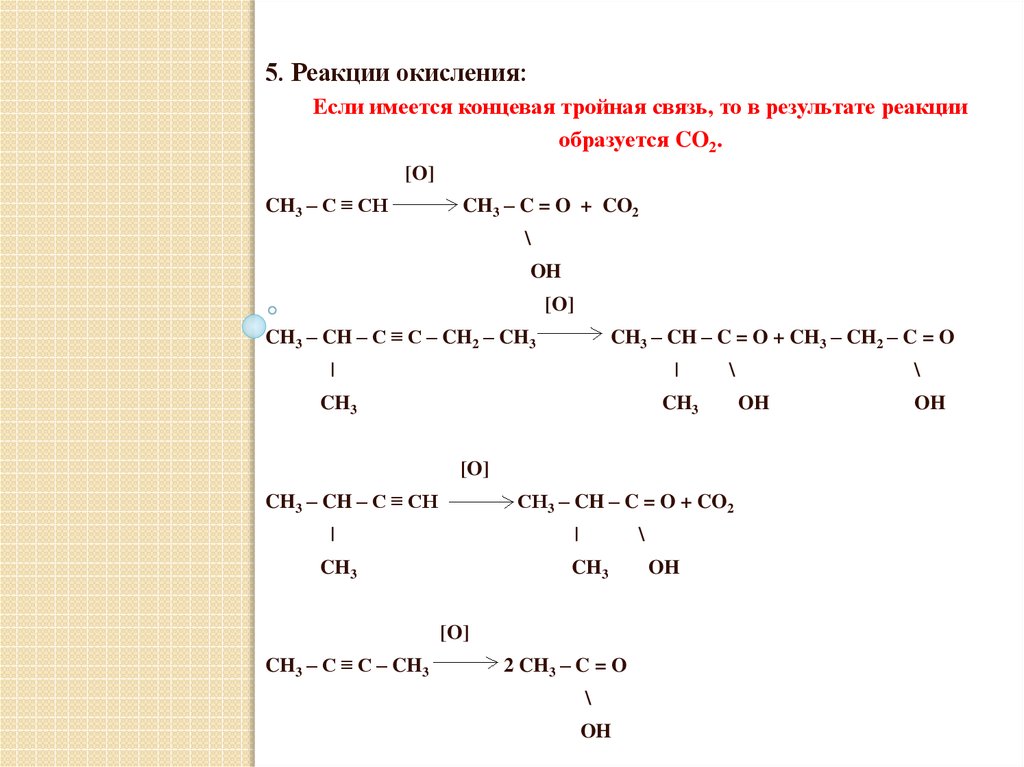
5. Реакции окисления:Если имеется концевая тройная связь, то в результате реакции
образуется CO2.
[O]
CH3 – C ≡ CH
CH3 – C = O + CO2
\
OH
[O]
CH3 – CH – C ≡ C – CH2 – CH3
CH3 – CH – C = O + CH3 – CH2 – C = O
|
|
CH3
\
CH3
[O]
CH3 – CH – C ≡ CH
CH3 – CH – C = O + CO2
|
|
CH3
\
CH3
[O]
CH3 – C ≡ C – CH3
2 CH3 – C = O
\
OH
OH
\
OH
OH
27.
28.
Взрыв смеси ацетилена с кислородом1. 2Н2О2
2. СаС2
2Н2О
+ 2Н2О
+
О2
CH ≡ CH
3. 2CH ≡ CH + 5O2
4. CH ≡ CH
+
О2
4CO2
С
+
+
Са(ОН)2
+ 2H2O
СО
+
Н2О
29.
30.
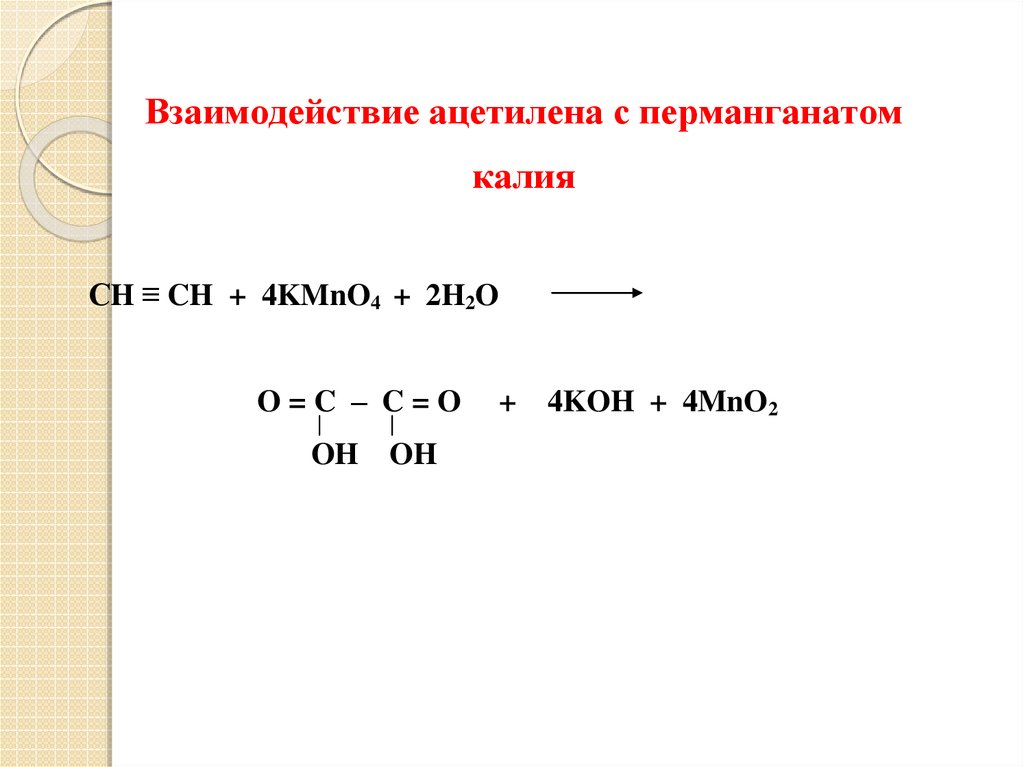
Взаимодействие ацетилена с перманганатомкалия
СH ≡ CH + 4KMnO4 + 2H2O
O=C – C=O
OH OH
+ 4KOH + 4MnO2
31.
32.
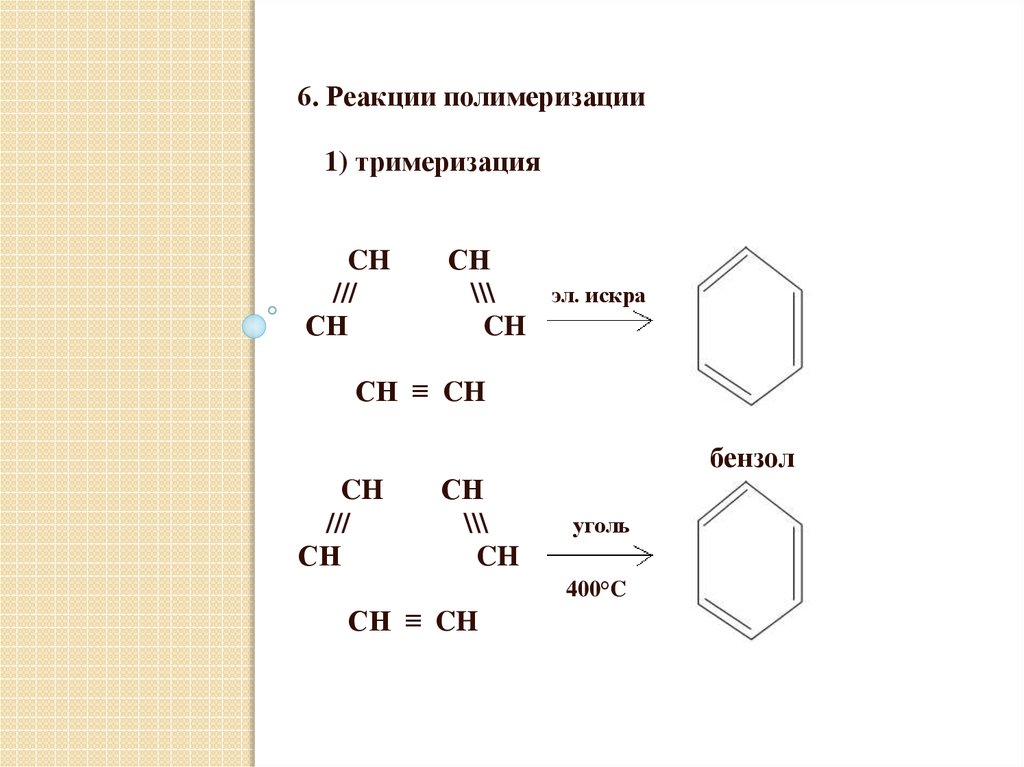
6. Реакции полимеризации1) тримеризация
CH
///
СН
СН
\\\
CH
эл. искра
СН ≡ CH
бензол
CH
///
СН
СН
\\\
CH
уголь
400°C
СН ≡ CH
33.
2) димеризация с последующей полимеризацией:HCl
HC ≡ CH + HC ≡ CH
CH2 = CH – C ≡ CH
n CH2 = CH – C= CH2
|
Cl
CH2 = CH – C =CH2
|
хлоропрен Cl
[ – CH2 – C = CH – CH2 – ] n
|
Cl
хлоропреновый каучук
CH2 = CH – C= CH + HC ≡ CH
CH2 = CH – C ≡ C – CH = CH2
дивинилацетилен
3) полимеризация в присутствии катализатора Cu:
Cu
HC ≡ CH
[ – CH = CH – ] n
купрен
























 Химия
Химия








