Похожие презентации:
Кислоты: классификация, реакции, применение
1. Кислоты
Презентацию приготовилСтудент группы 33 АМС
Аброськин Константин
Преподаватель: Дячук Мария
Владимировна
2. Кислоты
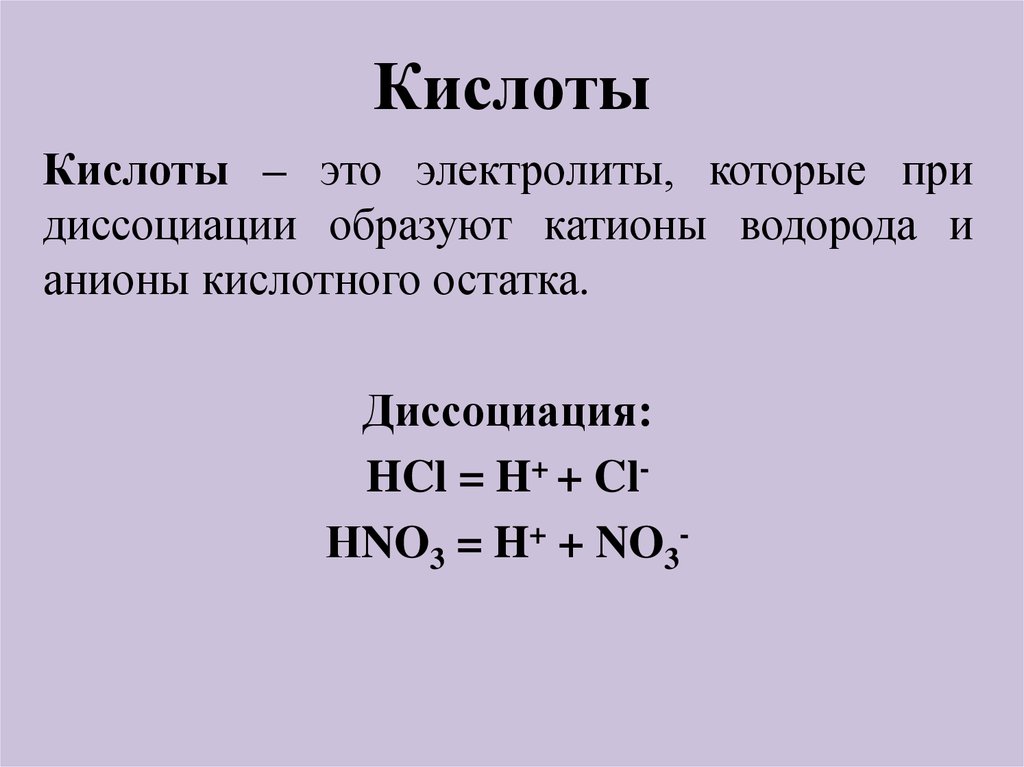
Кислоты – это электролиты, которые придиссоциации образуют катионы водорода и
анионы кислотного остатка.
Диссоциация:
HCl = H+ + ClНNO3 = H+ + NO3-
3. Классификация кислот
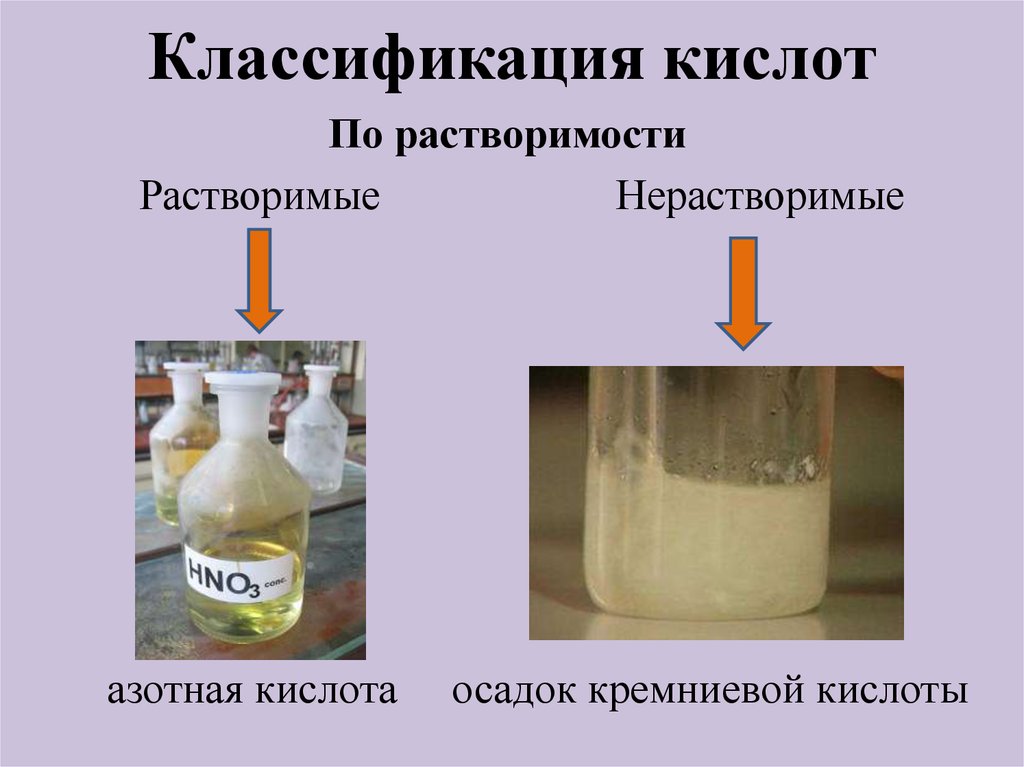
По растворимостиРастворимые
Нерастворимые
азотная кислота
осадок кремниевой кислоты
4. Классификация кислот
По наличию кислородаКислородсодержащие
Бескислородные
уксусная кислота
соляная кислота
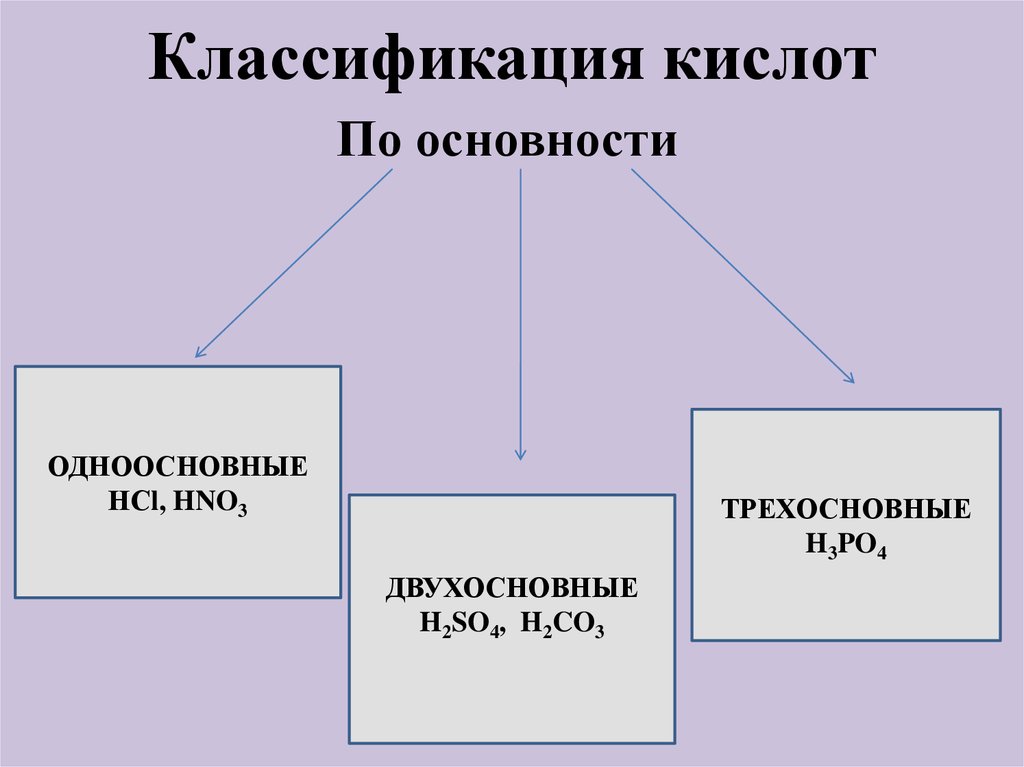
5. Классификация кислот
По основностиОДНООСНОВНЫЕ
НСl, HNO3
ТРЕХОСНОВНЫЕ
H3PO4
ДВУХОСНОВНЫЕ
H2SO4, H2CO3
6. Классификация кислот
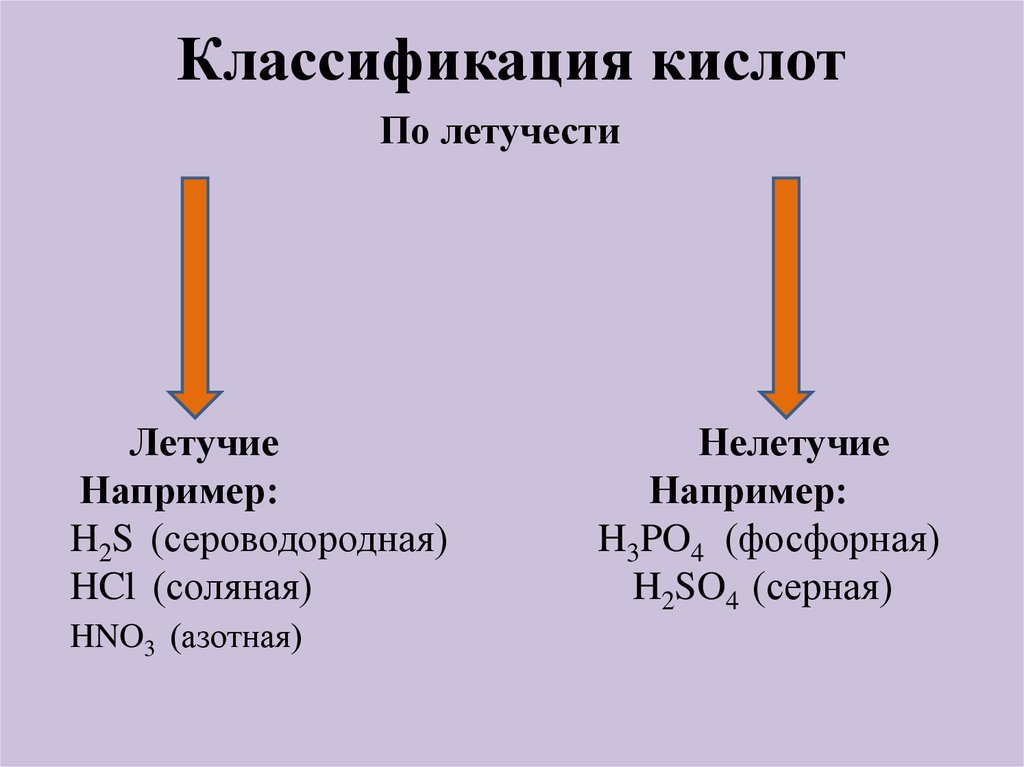
По летучестиЛетучие
Например:
H2S (сероводородная)
HCl (соляная)
HNO3 (азотная)
Нелетучие
Например:
H3PO4 (фосфорная)
H2SO4 (серная)
7. Типичные реакции кислот
1) Кислота + основание = соль + вода2) Кислота + оксид металла = соль + вода
3) Кислота + металл = соль + водород
4) Кислота + соль = новая кислота + новая соль
8. Типичные реакции кислот
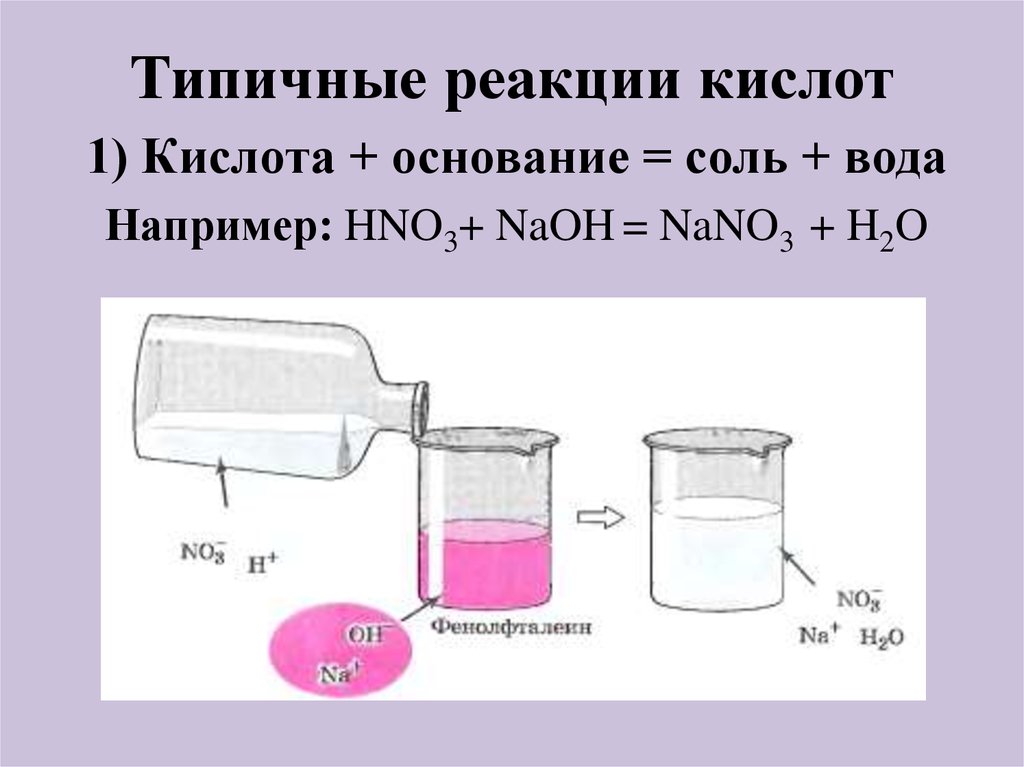
1) Кислота + основание = соль + водаНапример: HNO3+ NaOH = NaNO3 + H2O
9. Типичные реакции кислот
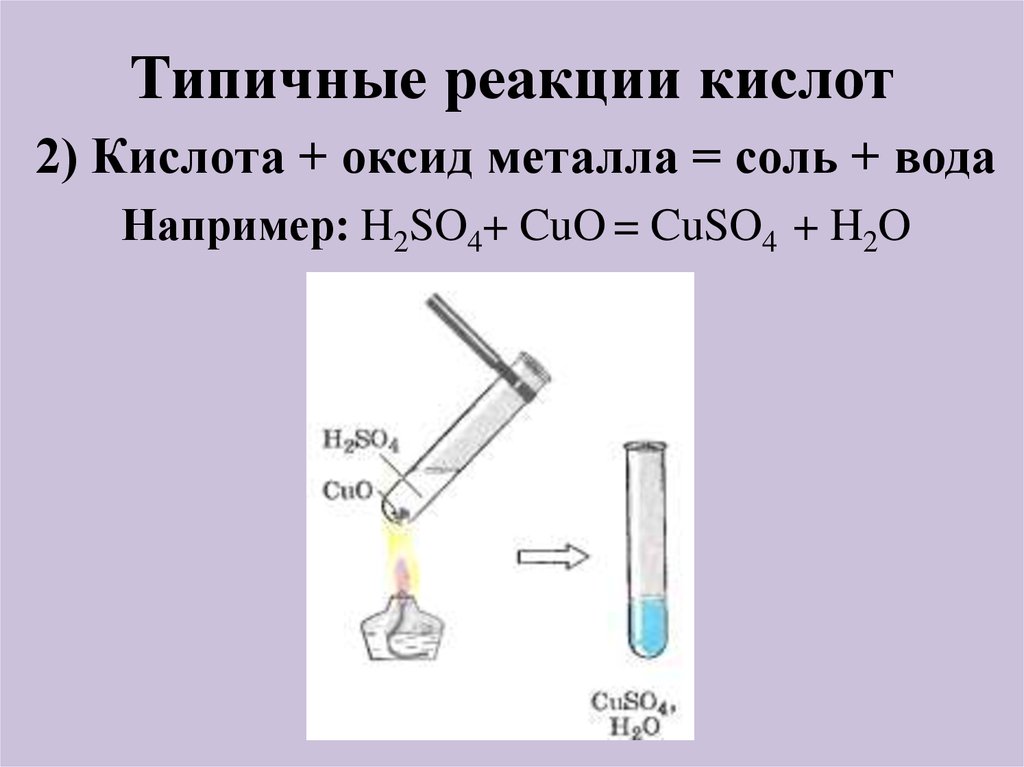
2) Кислота + оксид металла = соль + водаНапример: H2SO4+ CuO = CuSO4 + H2O
10. Типичные реакции кислот
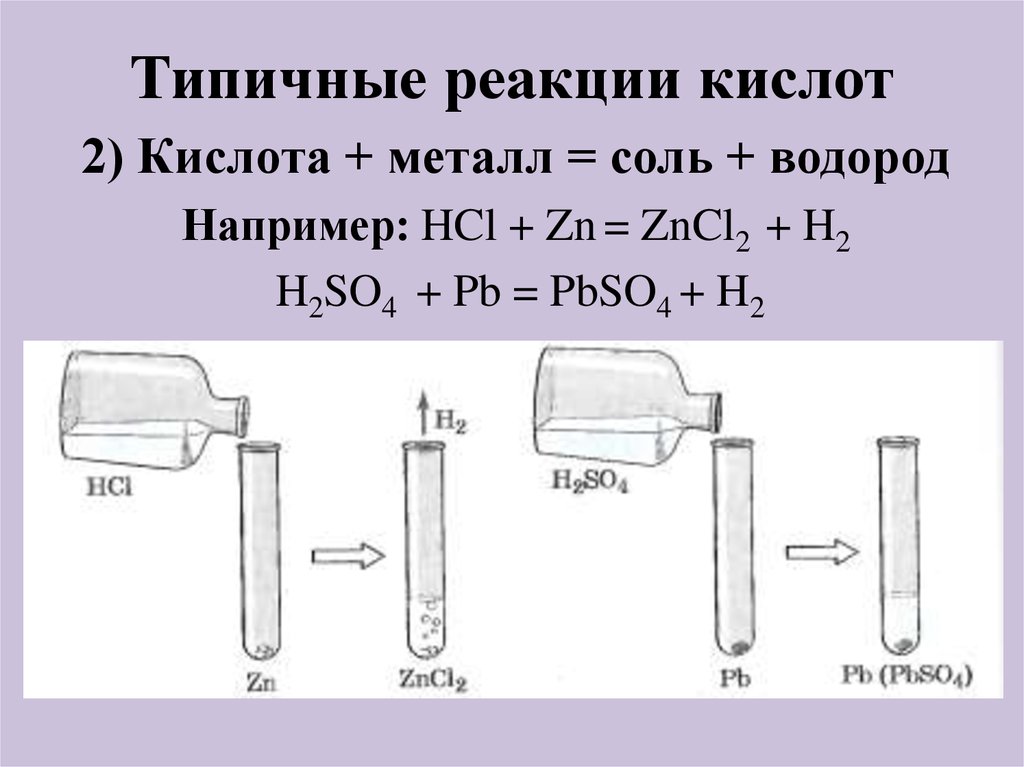
2) Кислота + металл = соль + водородНапример: HCl + Zn = ZnCl2 + H2
H2SO4 + Pb = PbSO4 + H2
11. Типичные реакции средних солей
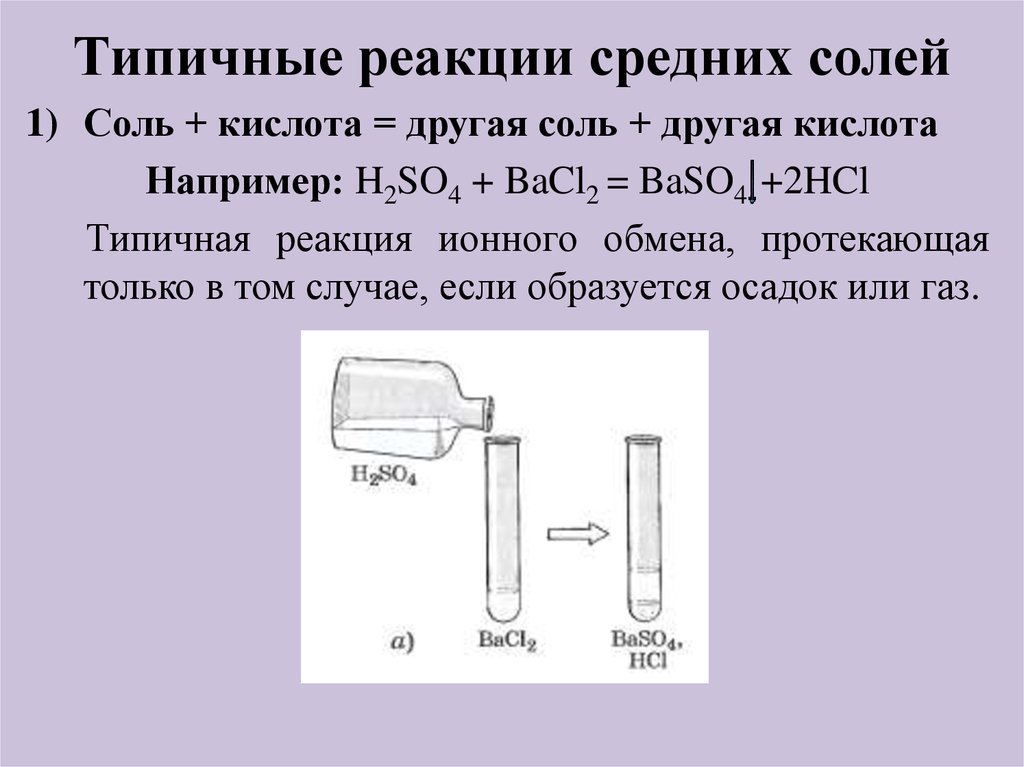
1) Соль + кислота = другая соль + другая кислотаНапример: H2SO4 + BaCl2 = BaSO4 +2HCl
Типичная реакция ионного обмена, протекающая
только в том случае, если образуется осадок или газ.
12. Практическое применение кислот
1) Производство лекарств;2) химических продуктов и товаров;
3) минеральных удобрений;
4) красок;
5) пластмасс и т.д.;
13. Обобщение темы:
Тест: «Проверь себя»1) Серная кислота – это кислота:
а) одноосновная
б) трехосновная
в) двухосновная
г) это не кислота
2) Кислоты – это электролиты, состоящие из
катионов:
а) металла
б) кислорода
в) серы
г) водорода
3) Реакцией замещения будет взаимодействие
кислоты с:
а) металлом
б) солью
в) основанием
г) оксидом





 Химия
Химия








