Похожие презентации:
Алкены. Гомологический ряд и изомерия
1. Алкены
АЛКЕНЫ2. Алкены -
АЛКЕНЫ это ациклическиеуглеводороды, содержащие в
молекуле, помимо одинарных
связей, одну двойную связь
между атомами углерода и
соответствующие общей
формуле CnH2n олефины
3.
4. Гомологический ряд и изомерия:
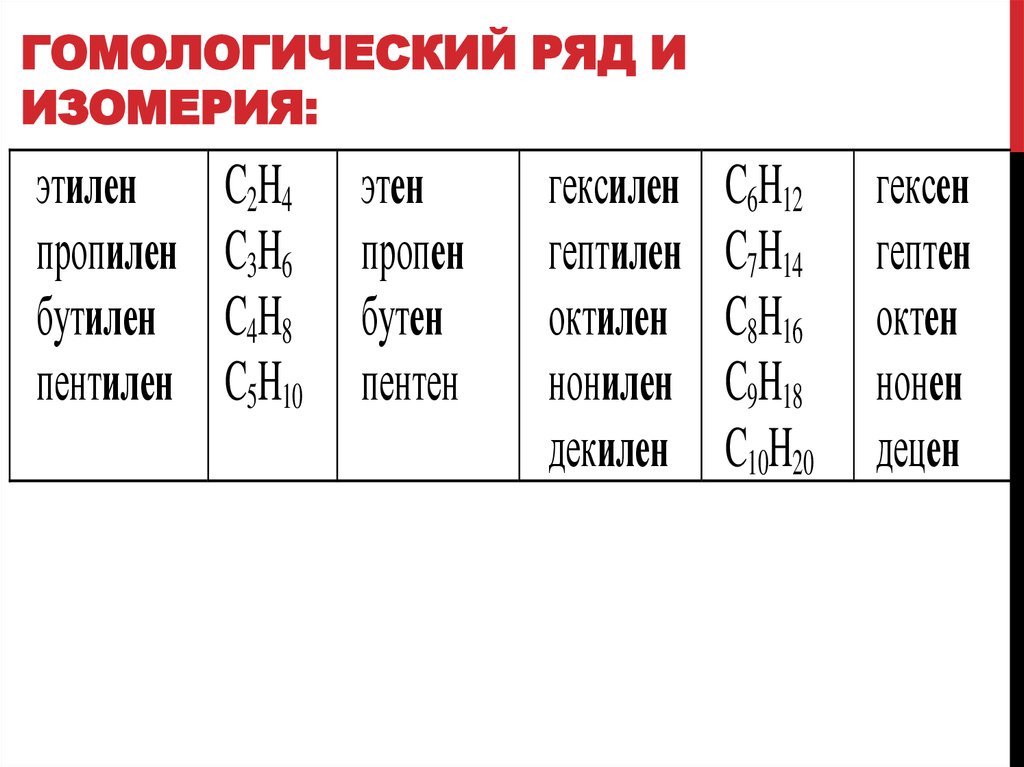
ГОМОЛОГИЧЕСКИЙ РЯД ИИЗОМЕРИЯ:
этилен
пропилен
бутилен
пентилен
C2H4
C3H6
C4H8
C5H10
этен
пропен
бутен
пентен
гексилен
гептилен
октилен
нонилен
декилен
C6H12
C7H14
C8H16
C9H18
C10H20
гексен
гептен
октен
нонен
децен
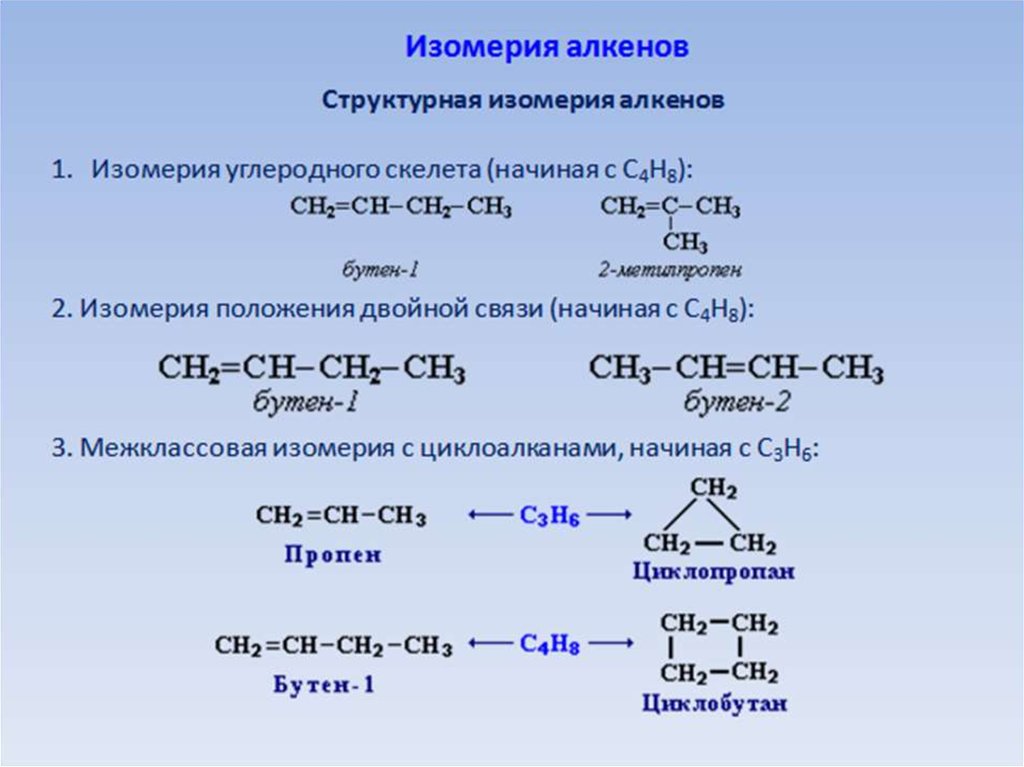
5. Изомерия:
ИЗОМЕРИЯ:6. Физические свойства:
ФИЗИЧЕСКИЕ СВОЙСТВА:• 2-4 – газы (без цвета, вкуса,
запаха)
• 5-16 – жидкости,
• 17 – твердые вещества
• t кипения и плавления
увеличивается с увеличением
цепи
7. химические свойства:
ХИМИЧЕСКИЕ СВОЙСТВА:1. р-ция присоединения (электрофильное
присоединения)
1) гидрирование (+Н, в присутствии Ni, Pt,
Pd) экзотермическая
СН3-СН2-СН=СН2+Н2→ СН3-СН2-СН2-СН3
(при повышение t идет обратная р-ия)
2) галогенирование (присоединение
галогенов)
СН2=СН2+Br2→ СН2Br -СН2Br 1,2-дибромэтан
8.
3) гидрогалогенирование (прис.галогеноводорода)
СН3-СН=СН2+НBr→ СН3-СНBr-СН3
2-бромпропан
правила Марковникова
При присоединении галогенводорода к
алкену водород присоединяется к более
гидрированному атому углерода, т. е.
атому, при котором находится больше
атомов водорода, а галоген – к менее
гидрированному.
9.
4) гидратация (присоединение воды) –спирты
СН2=СН2+Н2О→t,H3PO4→ СН3 -СН2OH
этен
этанол (первичный спирт)
СН3-СН=СН2+Н2ОH3PO4 СН3 –СН(ОН)-СН3
пропен
пропанол-2 (вторичный)
5) полимеризация
nСН2=СН2 →УФ-свет, R→ (…-СН2 -СН2-…)n
этен
полиэтилен
10.
2. Реакция окислениягорят с образованием CO2 и H2O
СН2=СН2+3О2→ СО2 +2Н2O
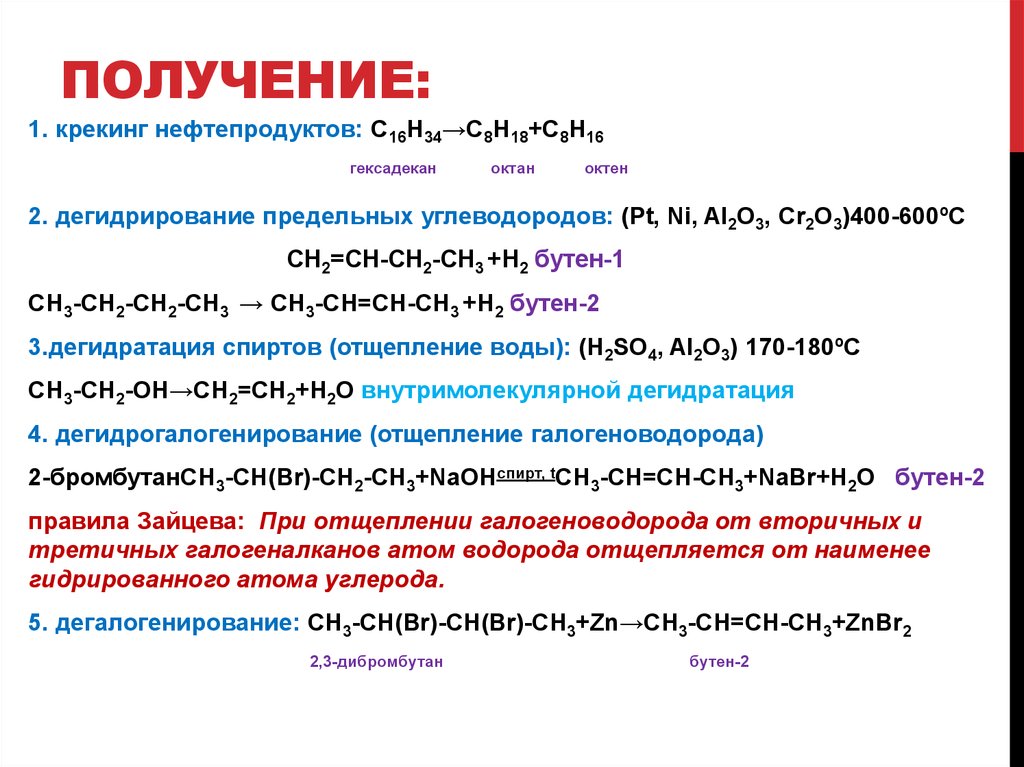
11. Получение:
ПОЛУЧЕНИЕ:1. крекинг нефтепродуктов: С16Н34→С8Н18+С8Н16
гексадекан
октан
октен
2. дегидрирование предельных углеводородов: (Pt, Ni, Al2O3, Cr2O3)400-600ºC
СН2=СН-СН2-СН3 +Н2 бутен-1
СН3-СН2-СН2-СН3 → СН3-СН=СН-СН3 +Н2 бутен-2
3.дегидратация спиртов (отщепление воды): (H2SO4, Al2O3) 170-180ºC
СН3-СН2-ОН→СН2=СН2+Н2О внутримолекулярной дегидратация
4. дегидрогалогенирование (отщепление галогеноводорода)
2-бромбутанСН3-СН(Br)-СН2-СН3+NaOHспирт, tСН3-СН=СН-СН3+NaBr+Н2О бутен-2
правила Зайцева: При отщеплении галогеноводорода от вторичных и
третичных галогеналканов атом водорода отщепляется от наименее
гидрированного атома углерода.
5. дегалогенирование: СН3-СН(Br)-CH(Br)-CH3+Zn→CH3-CH=CH-CH3+ZnBr2
2,3-дибромбутан
бутен-2
12. Применение:
ПРИМЕНЕНИЕ:1. в химической промышленности,
2. упаковочная пленка, посуда, трубы,
электроизоляционные материалы









 Химия
Химия








