Похожие презентации:
Методика изучения периодического закона, периодической системы Д.И. Менделеева и строения атома
1. Методика изучения периодического закона, периодической системы Д. И. Менделеева и строения атома
Береснева Е. В.к.п.н., профессор кафедры фундаментальной
химии и методики обучения химии ВятГУ
2. План лекции
1.2.
3.
4.
Значение изучения периодического
закона и теории строения атома в
школьном курсе химии
Место данной темы в школьном курсе
химии и методические подходы к ее
изучению
Методы и средства изучения темы
Методика изучения темы в школьном
курсе химии
3. Литература
1. Агафошин Н.П. Периодический закон ипериодическая система элементов Д.И.
Менделеева: пособ. для учащихся. М.:
Просвещение, 1982, 1973
2. Астахов К.В. Современное состояние
периодической системы Д.И. Менделеева: Серия
Химия №12. М.: Знание, 1969
3. Биографии великих химиков / ред. К. Хайниг,
пер. с нем. В.А. Крицмана, под ред. Г.В. Быкова и
С.А. Погодина. М.: Изд. Мир, 1981
4. Волков В.А., Вонский Е.В., Кузнецова Г.И.
Выдающиеся химики мира: биографический
справочник. М.: Высшая школа, 1991
4. Литература
5. Кедров Б.М. Прогнозы Д.И. Менделеева ватомистике. Неизвестные элементы. М.:
Атомиздат, 1977
6. Кедров В.М., Трифонов Д.Н. Закон
периодичности и химические элементы. М.: Наука,
1969
7. Курбатов В. Менделеев: детгиз в помощь
школьнику. Москва, Ленинград, 1950
8. Макареня А.А., Рысев Ю.В. Менделеев Д.И.:
серия «Люди науки». М.: Просвещение, 1983
9. Макареня А.А. Д.И. Менделеев и физикохимические науки. М.: Энергоиздат, 1982
5. Литература
10. Макареня А.А., Трифонов Д.Н. Периодическийзакон Д.И. Менделеева: пособие для учителей. М.:
Просвещение, 1969
11. Манолов К. Великие химики. М.: Мир, 1985, т. 2
12. Семишин В.И. Периодическая система
химических элементов Д.И. Менделеева. М.: Химия,
1972
13. Соловьев Ю.И. История химии. М.:
Просвещение, 1976
14. Фигуровский Н.А. История химии. М.:
Просвещение,1979
6.
1. Значение изучения периодическогозакона и теории строения атома в
школьном курсе химии
«Периодический закон и система
Д.И.Менделеева – предельно краткая и
четкая физико-химическая энциклопедия,
уникальное обобщение основного
содержания химии, взаимосвязи всех
химических элементов, основной закон
развития общества, отражающий
поступательное развитие материи»
М. Х. Карапетьянц
7.
Образовательное значение темыТема имеет большое образовательное значение:
- позволяет раскрыть смысл периодического закона
- вскрыть природу периодичности свойств элементов,
определяемую строением атомов
- выявить закономерности периодической системы
- сформировать представления об амфотерных
соединениях
- привить знания о качественных и количественных
характеристиках атомов, которые в дальнейшем
обеспечат глубокое понимание природы связи,
структуры веществ, закономерностей протекания
химических реакций
8.
Воспитательное значение темы-
-
Учебный материал темы позволяет
раскрыть идею материального единства веществ
благодаря общности в строении их атомов
рассмотреть изотопию как одну из причин многообразия
веществ
развить знания о внутренней двойственности веществ на
материале об амфотерных соединениях и строении
атомов
показать на конкретных примерах значение
теоретических знаний для развития науки и техники
подтвердить основные законы диалектики
провести патриотическое воспитание
9. Д. И. Менделеев (1834-1907)
Памятник и мозаичное панно в сквере ВНИИМ им. Д. И. Менделеева10.
Развивающее значение темыМатериал этой темы курса химии позволяет
- совершенствовать умения анализировать, сравнивать
свойства химических элементов и характер
соответствующих им оксидов и гидроксидов
- устанавливать причинно-следственные связи
- применять теоретические знания для объяснения и
предсказания свойств простых и сложных веществ на
основе знаний о строении атомов химических
элементов
- прогнозировать свойства неоткрытых элементов и
образуемых ими соединений
11.
2. Место темы в школьном курсе химии иметодические подходы к ее изучению
Периодический закон выполняет в школьном курсе химии
две функции:
является целью изучения (периодический закон
изучается в конце курса и рассматривается как
обобщение)
является средством обучения (периодический
закон изучается в начале курса и рассматривается
как средство усиления (углубления) далее
получаемых знаний)
12. Функции периодического закона
Эти функции нельзя рассматривать без ихвзаимного сочетания, так как 1-ая
функция не ведет к углублению знаний
учащихся, а для реализации 2-ой функции
на начальном этапе изучения химии
необходим минимум знаний (основных
законов и понятий химии), поэтому
изучение темы переносится на середину
8-го класса
13. Содержание темы состоит из двух тесно переплетающихся крупных блоков информации
Сведения опериодическом
законе и
периодическом
изменении свойств
химических
элементов и веществ
в зависимости от
возрастания атомных
масс элементов
Сведения о строении
атомов элементов
14. Методические подходы к изучению данной темы
ИсторическийУчащиеся как бы повторяют
путь, пройденный Д. И.
Менделеевым. Подход
позволяет показать
школьникам диалектику
познания; раскрыть
своеобразие стиля
мышления, характерного
для данного периода
времени в развитии
познания; проникнуть в
лабораторию ученого,
увидеть, какая работа в ней
происходит, как
совершаются открытия
Логический
Изучение строения атомов
первых 20 элементов
периодической системы
должно проводиться до
ознакомления учащихся с
периодическим законом.
Такой подход экономит
время, но игнорирует
принцип историзма, что
ведет к недооценке
воспитывающей функции
обучения. Критикуется
многими методистами
15.
Методические подходы к изучениюданной темы
Историко-логический подход: сначала показывается
обнаруженная Д. И. Менделеевым периодическая
зависимость свойств элементов и веществ от атомных
масс элементов, а затем выявляется ее причина на основе
строения атомов элементов
Изложить полностью процесс открытия периодического
закона, сравнительный метод Д. И. Менделеева, который
лежал в основе открытия, нет возможности в курсе химии
средней школы, так как ряд понятий, таких, как
изоморфизм, атомные объемы, атоманалогия и некоторые
другие, не изучаются в школе (этот материал выносится
на внеурочную деятельность)
16. Последовательность изучения темы при историко-логическом подходе
анализ сложившихся к середине XIX века знаний о составевеществ, их структуре и химическом процессе
классификация веществ, взаимосвязь классификаций
элементов, простых веществ по физическим свойствам,
сложных веществ по составу и химическим свойствам
формирование естественных групп элементов
сравнение свойств несходных элементов, формирование
понятия о форме соединения
выяснение характера взаимосвязи между свойствами и
атомными массами элементов, «выведение» периодического
закона в менделеевской формулировке
изучение строения атома и установление связей
приобретенных знаний с явлением периодичности
глубокий синтез знаний на материале изучения структуры
периодической системы, формирование умений пользоваться
ею
17.
Историко-логический подход позволяет:1.
2.
3.
4.
Правильно оценить роль периодического закона как
научной основы школьного курса химии
Отобрать материал, относящийся к истории открытия,
раскрытию сущности периодического закона,
преобразованию его в учение о периодичности, и на
основе этого полнее раскрыть объяснительную и
предсказательную функции периодического закона и
системы
Определить целесообразность и последовательность
выбора соответствующих форм, методов и средств
обучения по данной теме
Понять роль периодического закона как высшей формы
обобщения химических знаний, сформировать ряд
положений о научной картине мира
18.
3. Методы и средства изучения темыТрудности у учеников:
1. Большая информативность материала (большой
объем теоретических знаний)
2. Высокая степень абстрактности понятий
3. Концентрический способ изложения материала,
при котором существует необходимость
«переучивания» закона на основе электронных
представлений
19.
Причины трудностей учащихсяМетафизический характер мышления школьников,
которому чужды противоречия, переходы одних понятий
в другие. Знания представляются им как нечто
неизменное, раз и навсегда данное
Переход к электронному объяснению периодического
закона осуществляется несколько поспешно, так что
учащиеся не успевают осмыслить сущность закона и
понять, зачем шла речь об атомной массе
Преимущественное применение информационных
методов при изучении данной темы
20.
Методические принципы для устраненияпричин, порождающих трудности в
изучении данной темы
1.
2.
3.
4.
5.
Тесная связь с физикой
Использование проблемного подхода
Доказательное объяснение абстрактных
вопросов
Историко-логический подход к построению
материала
Комплексное использование средств обучения
21.
Комплекс средств наглядностиК важнейшим средствам обучения относятся:
1.
2.
3.
4.
Экранные пособия
Модельная и символическая
наглядность
Химический эксперимент
Изобразительные средства
наглядности
22.
Проблемно-поисковая деятельностьучащихся
Использование комплекса средств наглядности должно
сочетаться с проблемным подходом в обучении.
Этот подход должен доминировать на всех этапах
изучения темы
Проблемное обучение можно сочетать с
самостоятельной поисковой работой самих
учащихся в ходе решения проблемы
В процессе изучения Периодического закона
постоянно используется работа с карточками, что
позволяет эффективно организовать
самостоятельную работу
23. 4. Методика изучения темы в школьном курсе химии
Подготовка учащихся к усвоению периодического законасостоит из нескольких этапов:
Формирование знаний учащихся о существовании
естественных семейств химических элементов
Доказательство существования химических элементов с
промежуточными свойствами
Подведение учащихся к выводу об отсутствии резкой
границы между элементами – металлами и элементами
– неметаллами
Раскрытие содержания понятия «амфотерность»
24. Вывод периодического закона
В основу классификации Д. И. Менделеев положилглавную количественную характеристику элементов –
атомную массу (атомный вес)
В отличие от своих предшественников он сопоставил
между собой несходные семейства элементов. Он
сравнил их, располагая элементы в порядке
возрастания атомных масс, и обнаружил, что свойства
меняются не монотонно (линейно), а периодически, т.е.
сходные элементы встречаются через определенное
число элементов. Эту закономерность Д. И. Менделеев
назвал периодическим законом
25.
Связь периодического закона ипериодической системы
Периодический закон – реально существующий
(объективный) закон природы, он действует
независимо от человеческого сознания.
Периодический закон выражает сущность
взаимосвязи между химическими элементами
Периодическая система - это графическое
выражение Периодического закона и отражение
естественной системы химических элементов
Система – это совокупность элементов,
находящихся в отношениях и связях между собой
и образующих определенную целостность,
единство
26.
Периодическая системаСтруктура Периодической системы
рассматривается на основе строения атома и
знаний о периодическом изменении свойств
химических элементов
Периодическая система – единое целое,
включающее в себя все химические элементы
Форма периодической системы может быть
различна, но сущность их одна – Периодический
закон
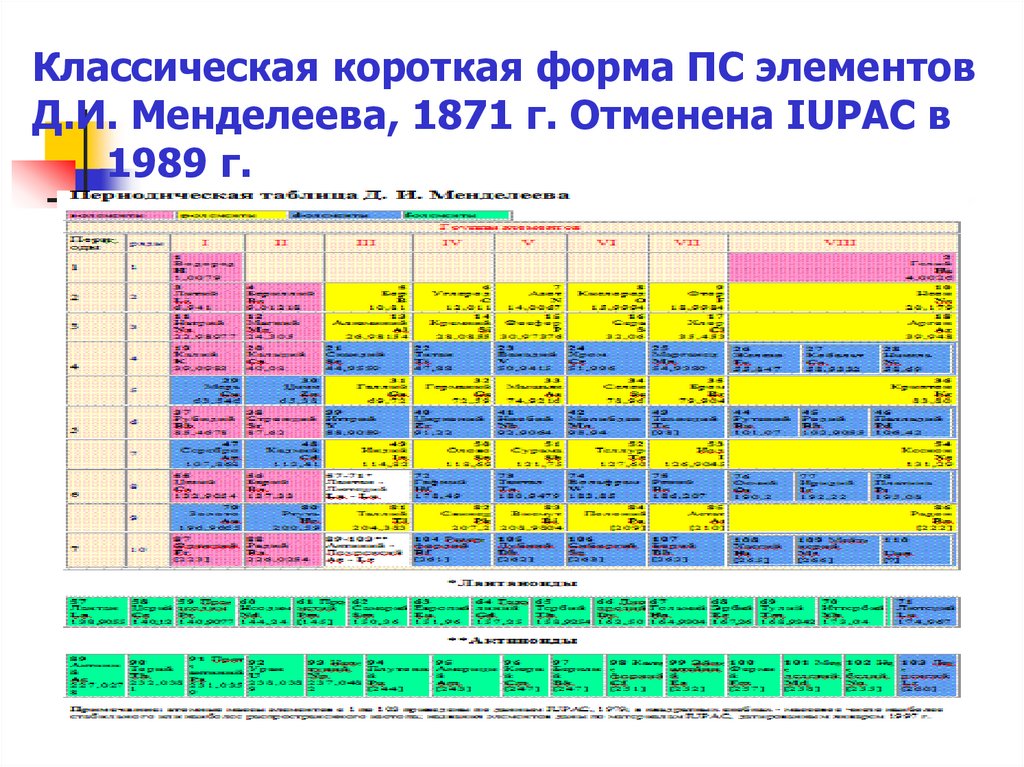
27. Классическая короткая форма ПС элементов Д.И. Менделеева, 1871 г. Отменена IUPAC в 1989 г.
28. Периодическая система длинной формы, утверждена IUPAC в 1989 г.
29. Расширенная форма ПС элементов Гленна Теодора Сиборга, 1969г.
30. Спиралевидная ПС Г. Баумгауэра (H. Baumhaur), 1870 г.
31. Типичная спиралевидная периодическая система многих авторов
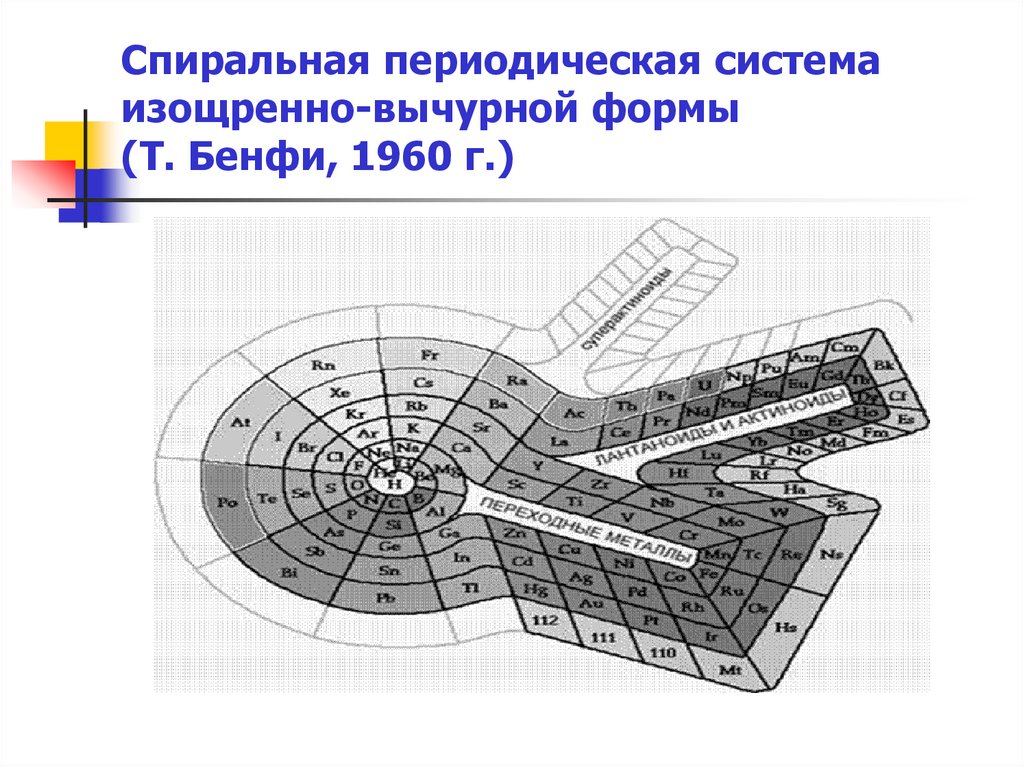
32. Спиральная периодическая система изощренно-вычурной формы (T. Бенфи, 1960 г.)
33. Лестничная форма периодической системы Ю.Томсена, 1895 год
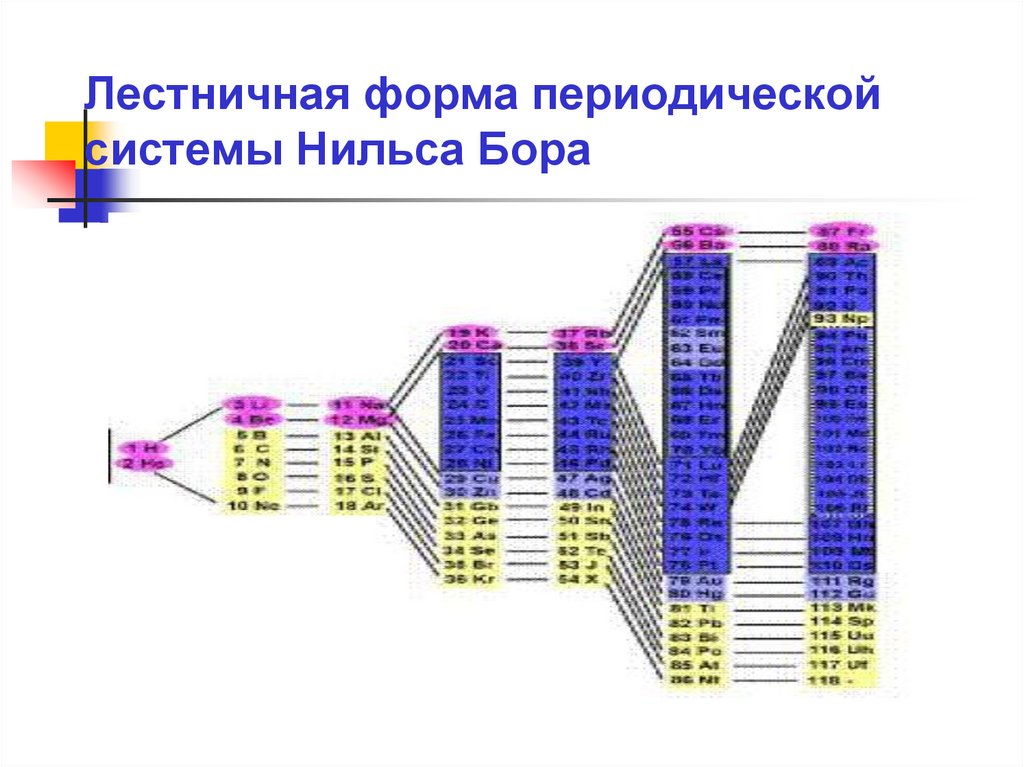
34. Лестничная форма периодической системы Нильса Бора
35. Сравните два определения периода
- горизонтальный рядэлементов Периодической
системы, начинающийся
щелочными металлами и
заканчивающийся
инертными элементами
- совокупность химических
элементов с одинаковым
числом электронных слоев в
атомах, в пределах которого
происходит увеличение
зарядов ядер атомов и
постепенное накопление
электронов во внешнем слое
или в предвнешних слоях,
обуславливающее ослабление
металличности и нарастание
неметалличности
36. Сравните два определения группы
- вертикальный столбец втаблице, включающий
элементы со сходными
свойствами
- совокупность химических
элементов, имеющих сходное
строение электронных
оболочек, число которых и
радиус атомов возрастают с
увеличением зарядов их ядер,
что приводит к усилению
металлических свойств и
ослаблению неметаллических
37. План характеристики химического элемента (базовый уровень)
1.2.
3.
4.
5.
6.
7.
8.
9.
Название
Порядковый номер
Положение в группе и подгруппе
Положение в периоде и ряду
Состав ядра атома
Общее число электронов в атоме, число электронов на
каждом уровне (для элементов малых периодов)
Металлические или неметаллические свойства
характерны для элемента
Формулы оксидов, гидроксидов, водородных
соединений и характер их свойств
Сравнение свойств элемента с соседними по периоду и
группе элементами
38. План характеристики химического элемента (профильный уровень)
1. Строение атома:заряд ядра атома
состав ядра атома
характеристика электронной оболочки
электронная формула
валентные электроны
сравнение основных характеристик атомов соседних
элементов
2. Свойства простых и сложных веществ:
состав (формула)
агрегатное состояние
химические свойства
применение
получение
39.
Выводы1.
2.
3.
4.
5.
Открытие ПЗ способствовало развитию химической науки
и вместе с другими открытиями привело к созданию
теории строения атома. В свою очередь, теория строения
атома глубже раскрыла природу химических элементов и
объяснила закономерности ПС
Открытый Д. И. Менделеевым ПЗ – всеобщий,
естественный закон развития природы. ПС наглядно
иллюстрирует взаимосвязь между химическими
элементами и их порядок, существующий в природе
ПЗ и ПС позволяют предвидеть свойства открытых и
неоткрытых элементов и их соединений
На основе ПЗ успешно развивается атомная и ядерная
физика, геохимия, минералогия и другие науки
ПЗ является наглядным подтверждением материальности,
единства и познаваемости окружающего нас мира
40.
Благодарюза внимание!





































 Химия
Химия








