Похожие презентации:
Гексамидин Hexamidinum. Примидон Primidone
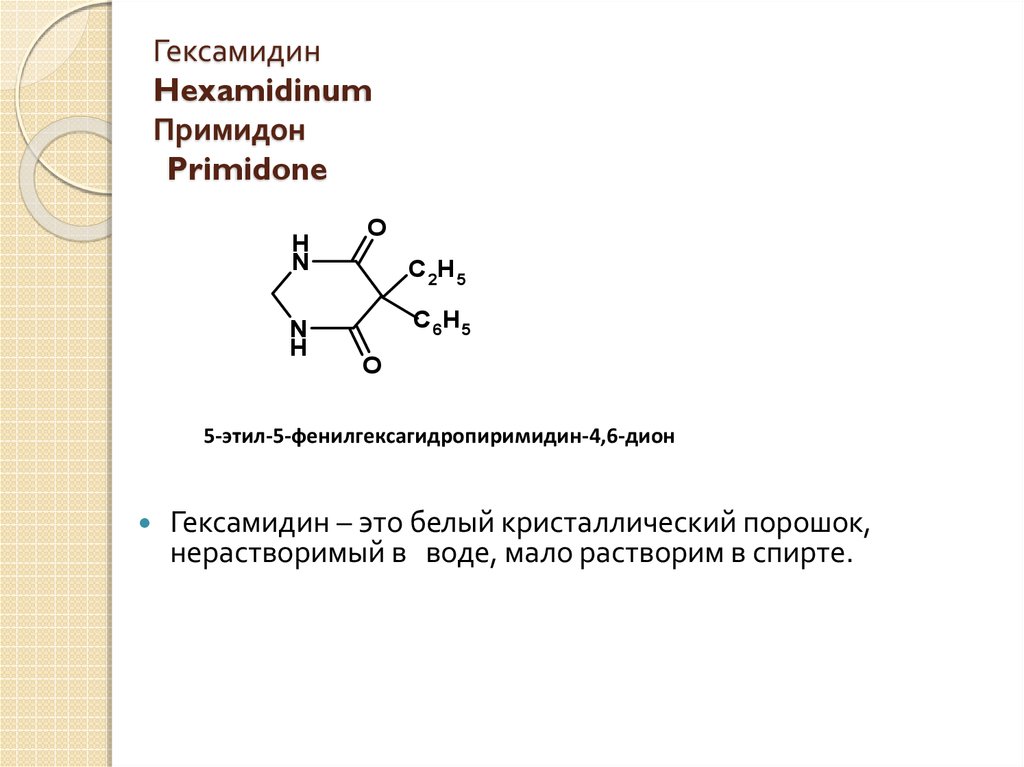
1. Гексамидин Hexamidinum Примидон Primidone
HN
N
H
O
C 2H 5
C 6H 5
O
5-этил-5-фенилгексагидропиримидин-4,6-дион
Гексамидин – это белый кристаллический порошок,
нерастворимый в воде, мало растворим в спирте.
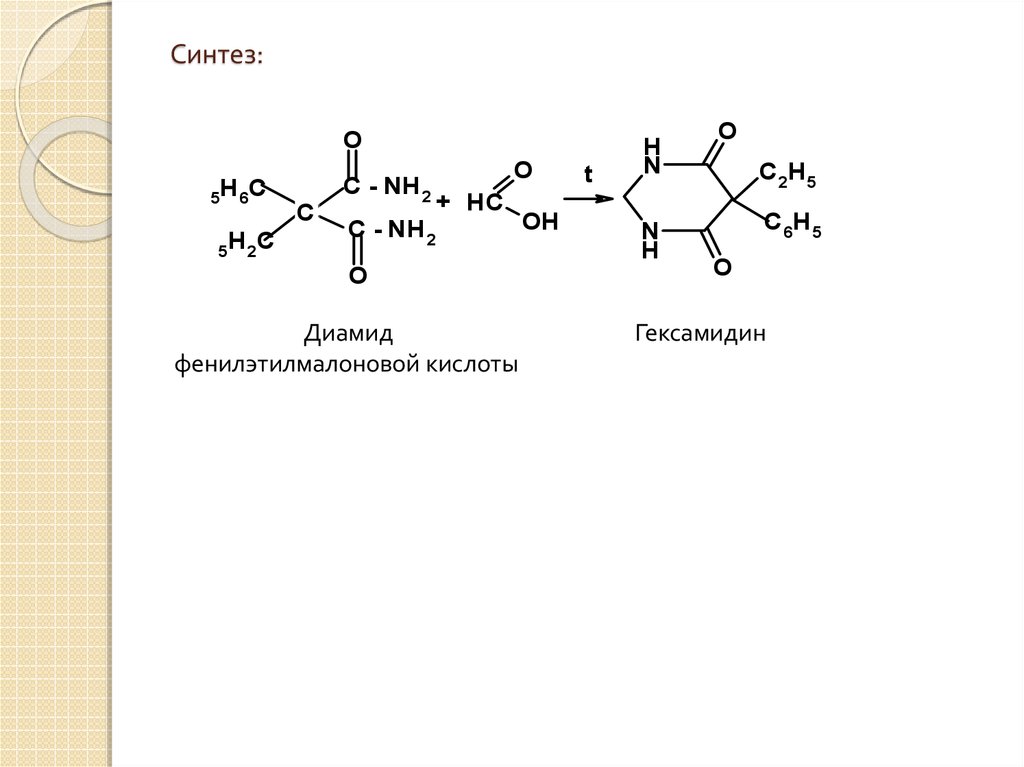
2. Синтез:
OH C
5 6
H C
5 2
C
C - NH 2
O
+ HC
C - NH 2
O
Диамид
фенилэтилмалоновой кислоты
OH
t
H
N
N
H
O
C 2H 5
C 6H 5
O
Гексамидин
3.
Для идентификации гексамидина используют УФ- и ИК–спектроскопию.
УФ-спектр гексамидина в этанольном растворе имеет
три полосы поглощения с максимумами при 252, 258 и
264 нм.
ИК-спектр гексамидина должен соответствовать
спектру поглощения, прилагаемому к НД.
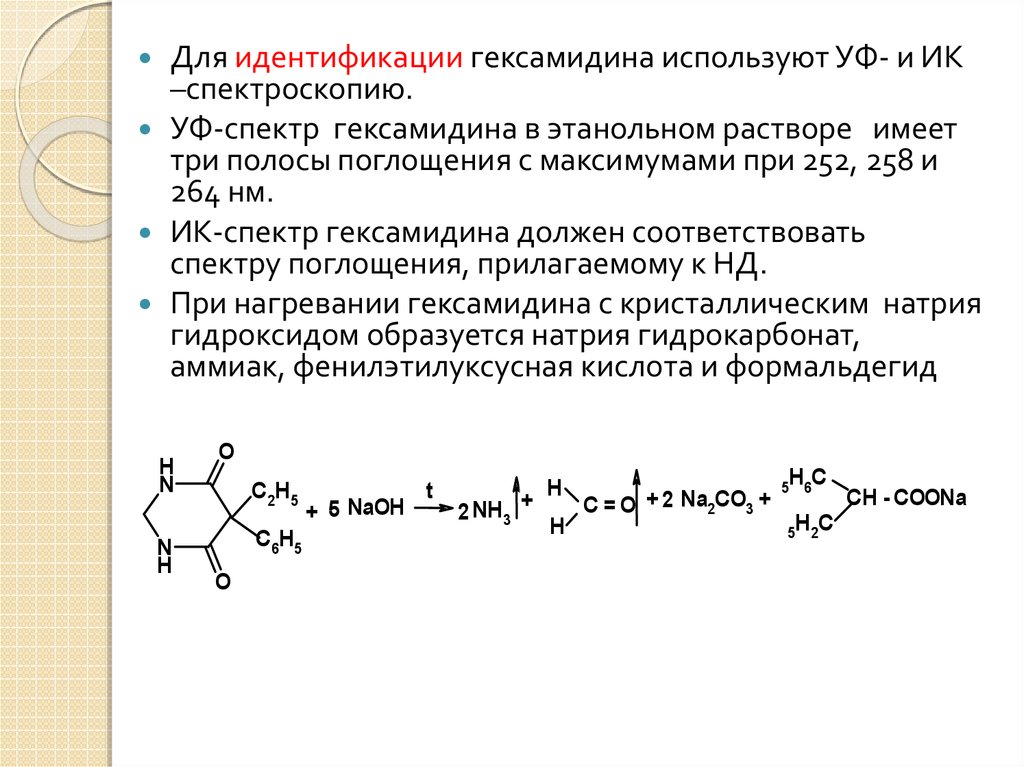
При нагревании гексамидина с кристаллическим натрия
гидроксидом образуется натрия гидрокарбонат,
аммиак, фенилэтилуксусная кислота и формальдегид
H
N
N
H
O
C 2H 5
C 6H 5
O
+ 5 NaOH
t
2 NH 3
+
H
H
C = O + 2 Na2CO3 +
H 6C
5
H 2C
5
CH - COONa
4.
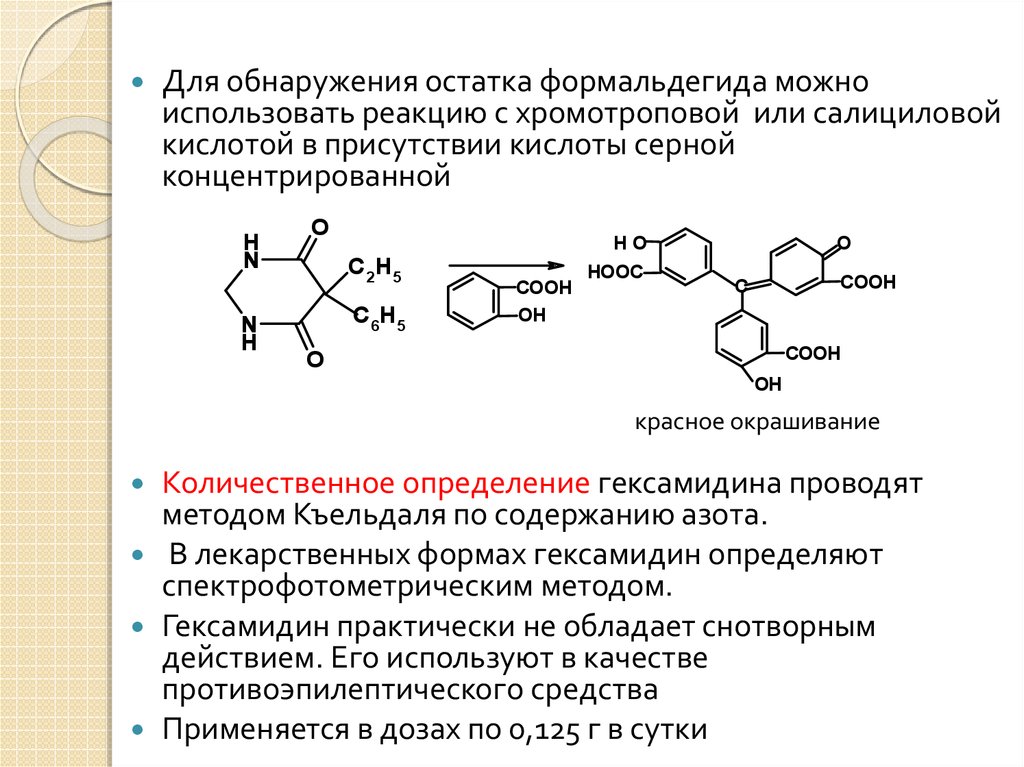
Для обнаружения остатка формальдегида можноиспользовать реакцию с хромотроповой или салициловой
кислотой в присутствии кислоты серной
концентрированной
H
N
N
H
O
HO
C 2H 5
C 6H 5
COOH
OH
HOOC
O
COOH
C
COOH
O
OH
красное окрашивание
Количественное определение гексамидина проводят
методом Къельдаля по содержанию азота.
В лекарственных формах гексамидин определяют
спектрофотометрическим методом.
Гексамидин практически не обладает снотворным
действием. Его используют в качестве
противоэпилептического средства
Применяется в дозах по 0,125 г в сутки
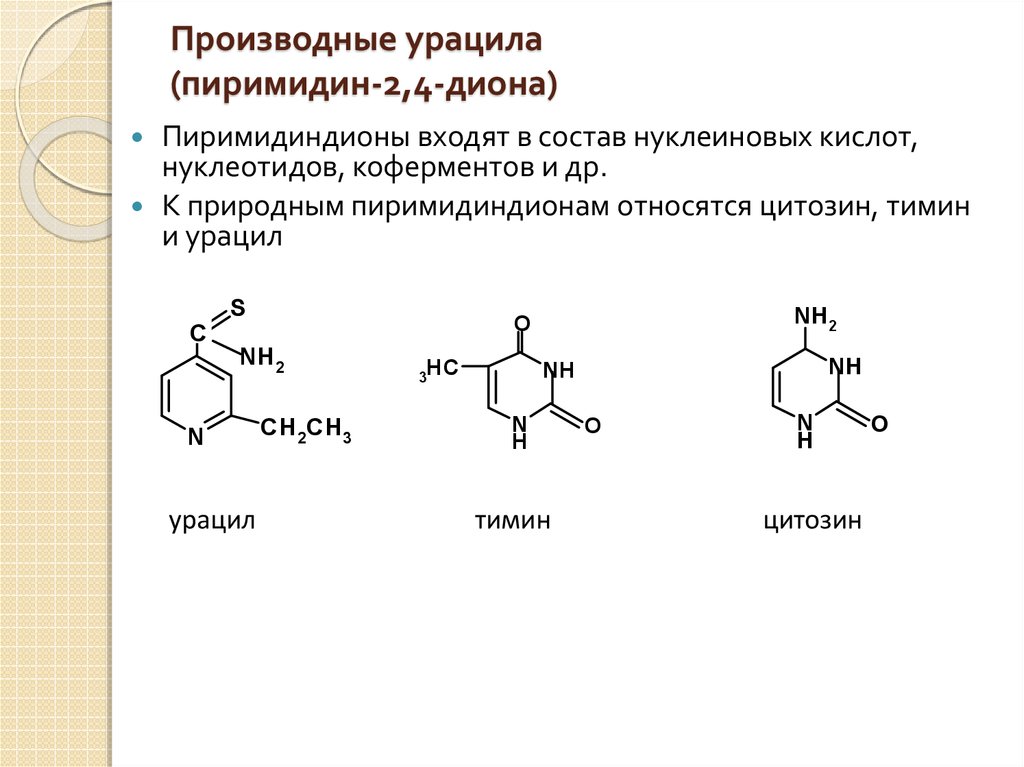
5. Производные урацила (пиримидин-2,4-диона)
Пиримидиндионы входят в состав нуклеиновых кислот,нуклеотидов, коферментов и др.
К природным пиримидиндионам относятся цитозин, тимин
и урацил
S
C
NH 2
N
урацил
NH 2
O
CH 2CH 3
HC
NH
NH
3
N
H
тимин
O
N
H
цитозин
O
6.
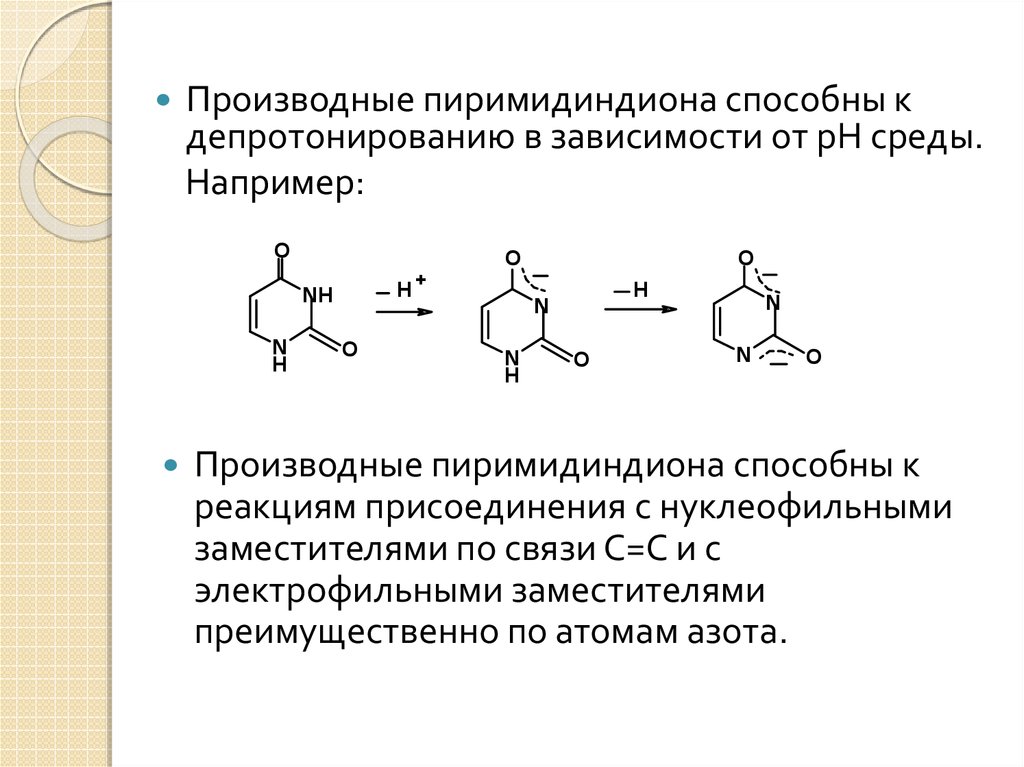
Производные пиримидиндиона способны кдепротонированию в зависимости от рН среды.
Например:
O
O
H+
NH
N
H
O
O
H
N
N
H
O
N
N
O
Производные пиримидиндиона способны к
реакциям присоединения с нуклеофильными
заместителями по связи С=С и с
электрофильными заместителями
преимущественно по атомам азота.
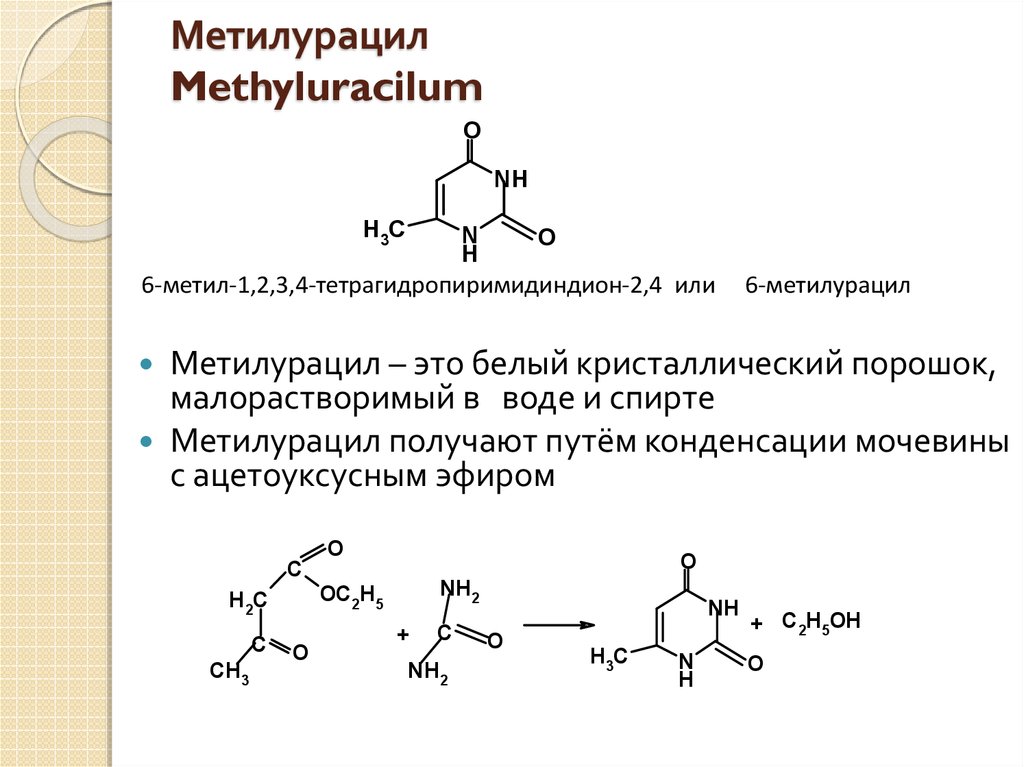
7. Метилурацил Methyluracilum
ONH
H 3C
N
H
O
6-метил-1,2,3,4-тетрагидропиримидиндион-2,4 или
6-метилурацил
Метилурацил – это белый кристаллический порошок,
малорастворимый в воде и спирте
Метилурацил получают путём конденсации мочевины
с ацетоуксусным эфиром
O
O
C
C
CH 3
NH 2
OC 2H 5
H 2C
O
+
C
NH 2
NH
O
H 3C
N
H
+ C 2H 5OH
O
8.
Идентификацию метилурацила проводят с помощьюУФ- и ИК –спектроскопии.
УФ-спектр метилурацила в растворе 0,1 М кислоте
хлористоводородной имеет полосу поглощения с
максимумом при 266 нм.
ИК-спектр метилурацила должен соответствовать ИКспектру стандартного образца.
Метилурацил образует осадки с солями серебра
нитрата, ртути дихлорида,
И комплексную соль фиолетового цвета с кобальта
хлоридом. Реакции проводятся также, как с
барбитуратами.
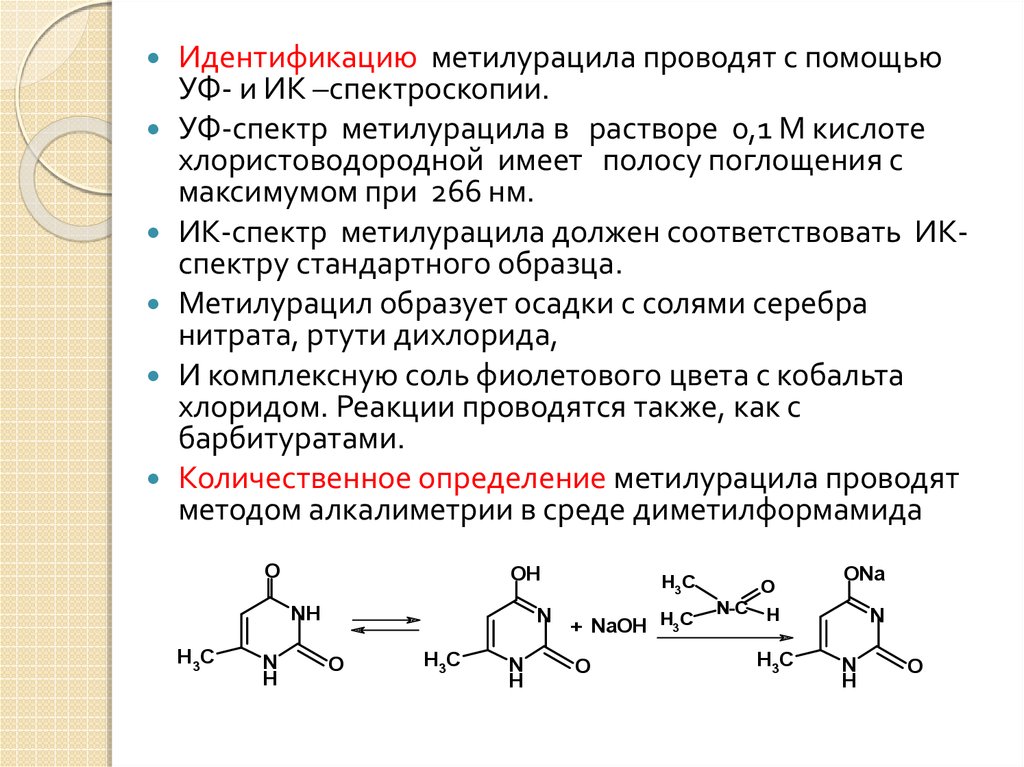
Количественное определение метилурацила проводят
методом алкалиметрии в среде диметилформамида
O
OH
NH
H 3C
N
H
N
O
H 3C
N
H
H3 C
+ NaOH H3 C
O
O
ONa
N-C H
H 3C
N
N
H
O
9.
Метилурацил обладает способностьюстимулировать процессы лейкопоэза, клеточных и
гуморальных факторов иммунитета. Он
способствует заживлению ран, оказывает
противовоспалительное действие.
Назначают метилурацил при лейкопении
различной этиологии, в том числе при
химиотерапии, при бензольном отравлении. Его
применяют при вялозаживающих ранах, при
заболеваниях ЖКТ. Обычные дозы внутрь в
пределах 0,25-0,5 г. Местно применяют
метилурацил в виде 10% мази.
Выпускают метилурацил в таблетках по 0,5г и
мази 10% в тубах или банках по 25, 40 и 80 г.
10.
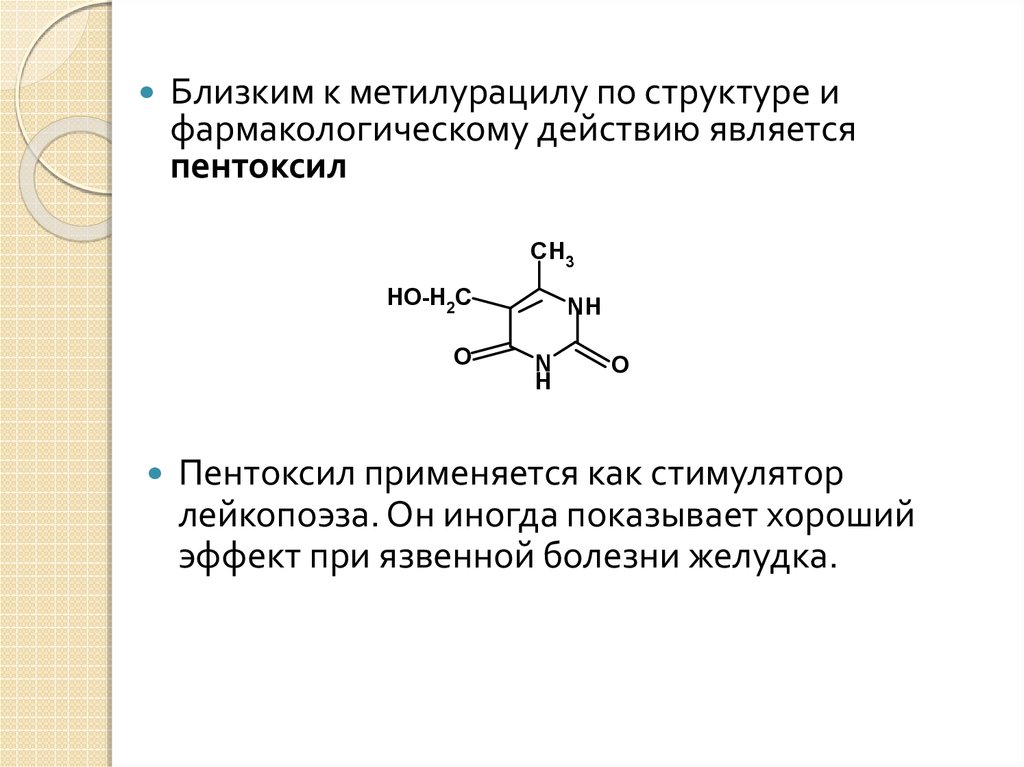
Близким к метилурацилу по структуре ифармакологическому действию является
пентоксил
CH 3
HO-H 2C
O
NH
N
H
O
Пентоксил применяется как стимулятор
лейкопоэза. Он иногда показывает хороший
эффект при язвенной болезни желудка.
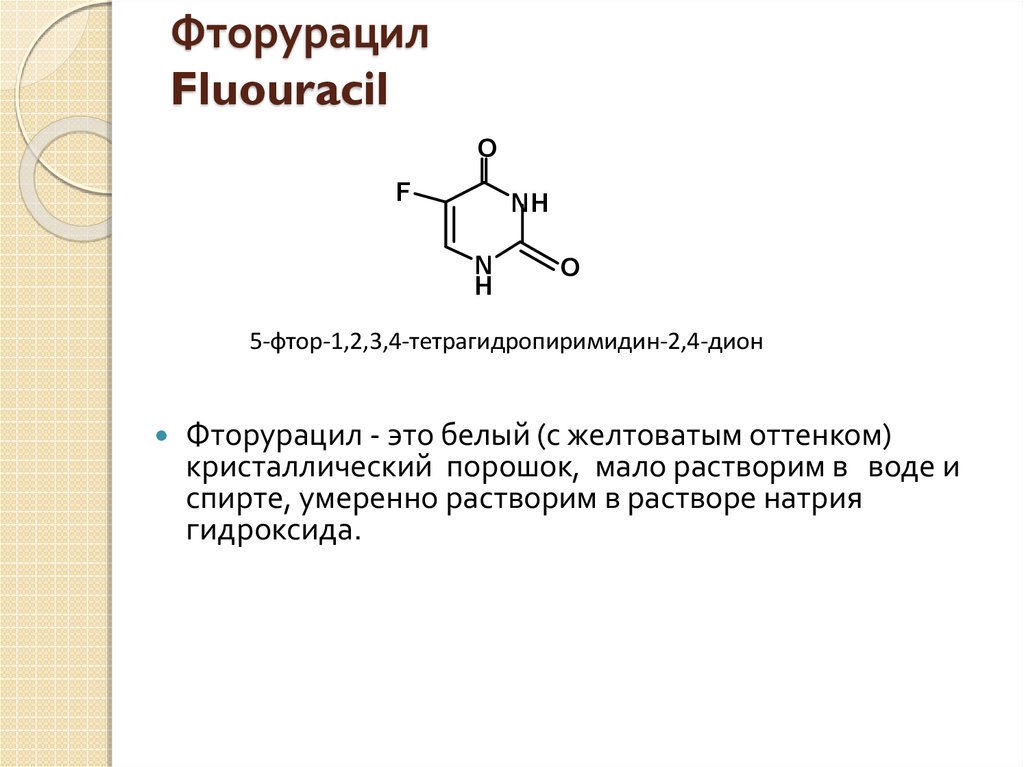
11. Фторурацил Fluouracil
OF
NH
N
H
O
5-фтор-1,2,3,4-тетрагидропиримидин-2,4-дион
Фторурацил - это белый (с желтоватым оттенком)
кристаллический порошок, мало растворим в воде и
спирте, умеренно растворим в растворе натрия
гидроксида.
12.
Идентификацию фторурацила проводят с помощьюУФ- и ИК –спектроскопии.
УФ-спектр фторурацила в 0,1 М растворе натрия
гидроксида имеет полосу поглощения с максимумом
при 265 нм.
ИК-спектр фторурацила должен соответствовать ИКспектру стандартного образца.
Наличие фтора в структуре фторурацил определяют
после минерализации путём сплавления со смесью
натрия карбоната и натрия нитрата. Фторид-ионы
определяют по обесцвечиванию красного комплекса
железа с тиоцианатом или по появлению белого
осадка с кальция хлоридом
Fe(NCS)3 + 6NaF → Na3[FeF6] + 3 NaNCS
CaCl2 + 2 NaF → CaF2↓ + 2 NaCl
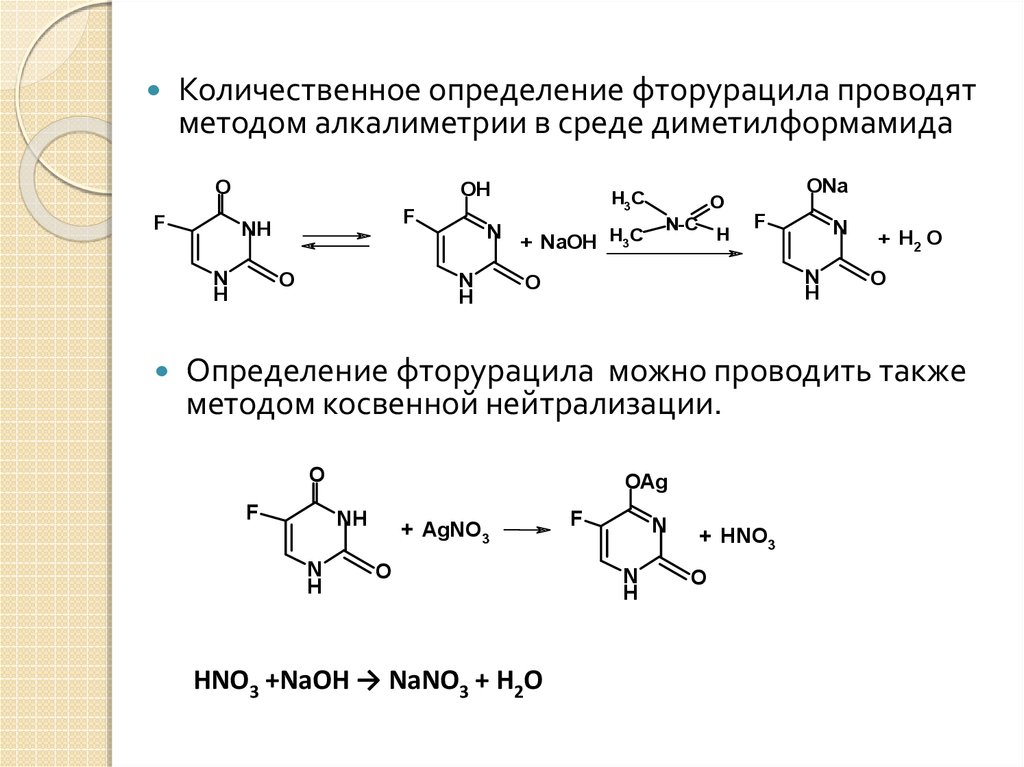
13.
Количественное определение фторурацила проводятметодом алкалиметрии в среде диметилформамида
O
F
OH
N
H
F
NH
O
N
N
H
H3 C
+ NaOH H3 C
ONa
O
N-C
H
F
N
N
H
O
+ H2 O
O
Определение фторурацила можно проводить также
методом косвенной нейтрализации.
O
F
OAg
NH
N
H
+ AgNO3
O
HNO3 +NaOH → NaNO3 + H2O
F
N
N
H
+ HNO3
O
14. Производные пиримидино-тиазола
В этом разделе будут рассмотрены лекарственныевещества, содержащие в своей структуре два
гетероцикла: пиримидин и тиазол.
Изучение производных пиримидино-тиазолового
ряда связано с изучением витамина В1.
Само понятие «витамин» было введено в
медицинскую литературу в 1912 г польским учёным
Функом, который выделил из рисовых отрубей
фракцию, с выраженными основными свойствами и
обладающую способностью оказывать лечебное
действие при полиневрите (vita amine– амин жизни).
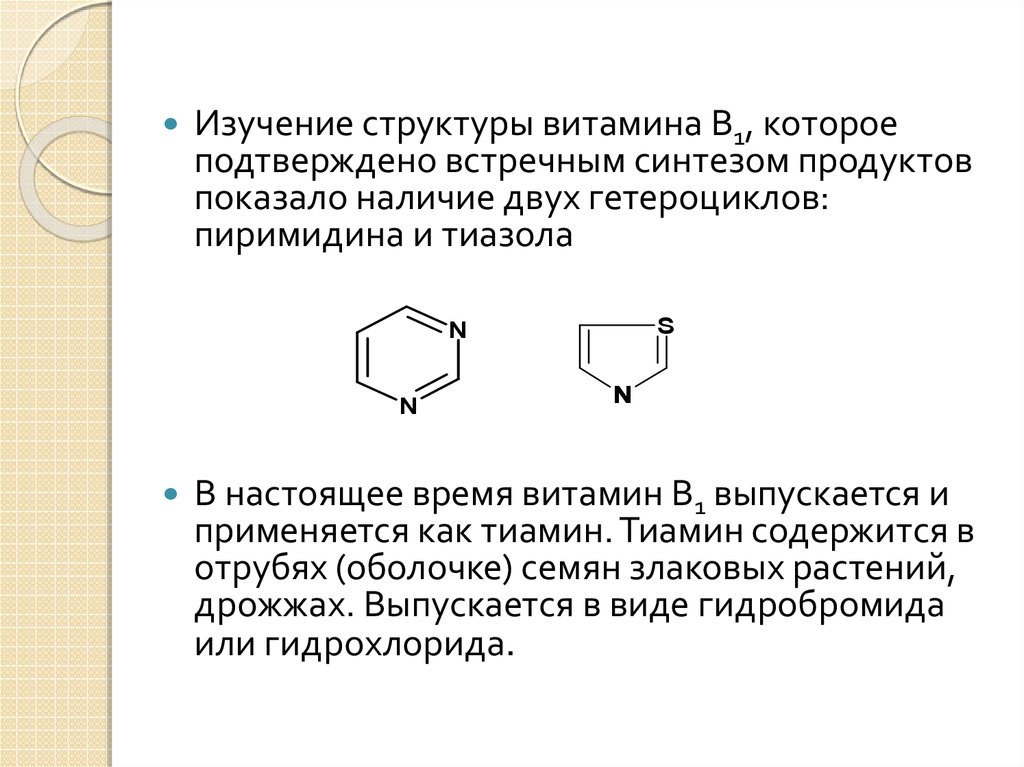
15.
Изучение структуры витамина В1, котороеподтверждено встречным синтезом продуктов
показало наличие двух гетероциклов:
пиримидина и тиазола
S
N
N
N
В настоящее время витамин В1 выпускается и
применяется как тиамин. Тиамин содержится в
отрубях (оболочке) семян злаковых растений,
дрожжах. Выпускается в виде гидробромида
или гидрохлорида.
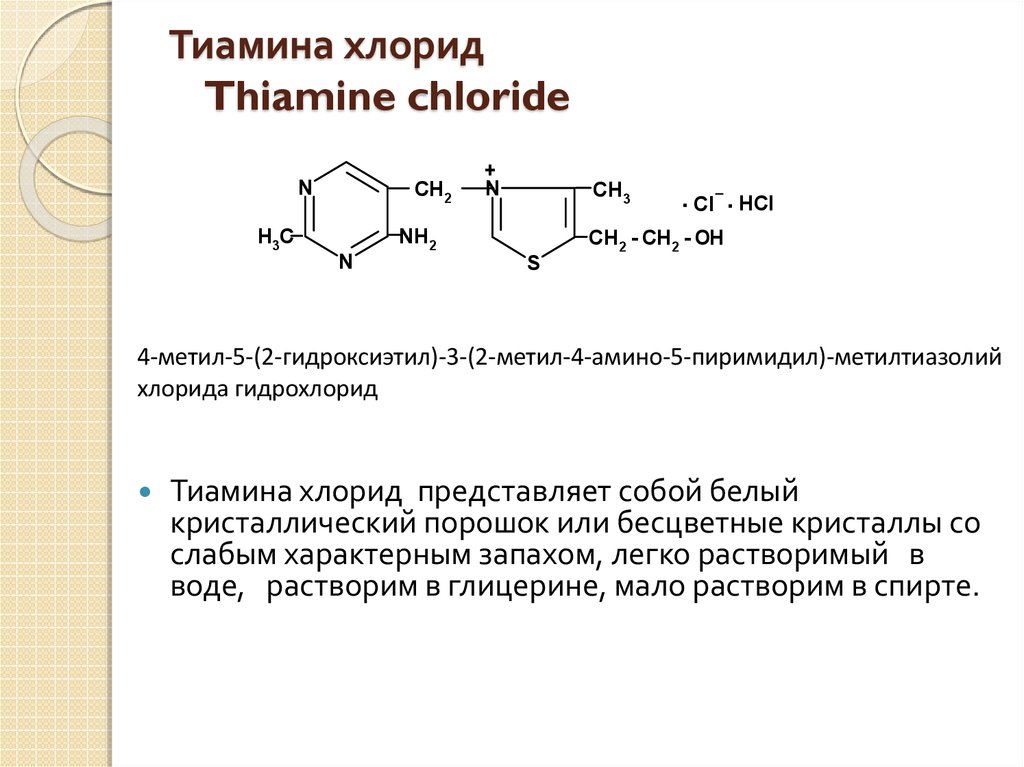
16. Тиамина хлорид Thiamine chloride
NCH 2
H 3C
+
N
CH 3
NH 2
N
. Cl . HCl
CH 2 - CH 2 - OH
S
4-метил-5-(2-гидроксиэтил)-3-(2-метил-4-амино-5-пиримидил)-метилтиазолий
хлорида гидрохлорид
Тиамина хлорид представляет собой белый
кристаллический порошок или бесцветные кристаллы со
слабым характерным запахом, легко растворимый в
воде, растворим в глицерине, мало растворим в спирте.
17.
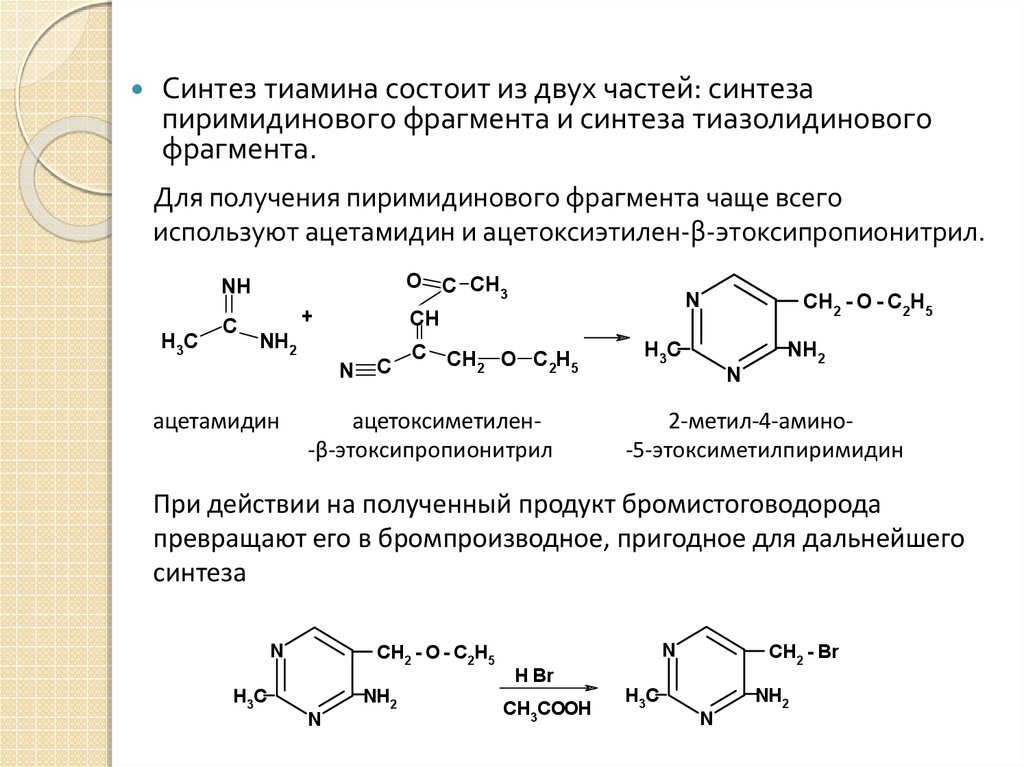
Синтез тиамина состоит из двух частей: синтезапиримидинового фрагмента и синтеза тиазолидинового
фрагмента.
Для получения пиримидинового фрагмента чаще всего
используют ацетамидин и ацетоксиэтилен-β-этоксипропионитрил.
O C CH
3
NH
H 3C
C
+
NH 2
N
ацетамидин
N
CH
C
C
CH 2 O C 2H 5
ацетоксиметилен-β-этоксипропионитрил
CH 2 - O - C 2H 5
H 3C
NH 2
N
2-метил-4-амино-5-этоксиметилпиримидин
При действии на полученный продукт бромистоговодорода
превращают его в бромпроизводное, пригодное для дальнейшего
синтеза
N
N
CH 2 - O - C 2H5
CH 2 - Br
H Br
H 3C
NH 2
N
CH 3COOH
H 3C
NH 2
N
18.
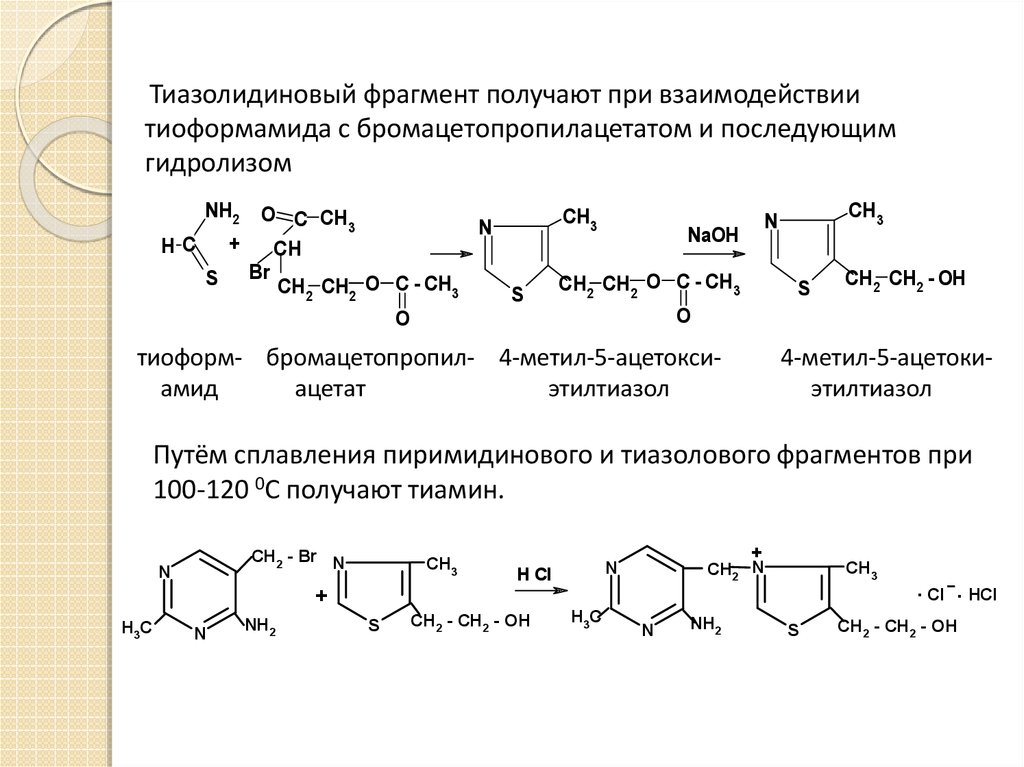
Тиазолидиновый фрагмент получают при взаимодействиитиоформамида с бромацетопропилацетатом и последующим
гидролизом
NH 2
O C CH
3
N
+
HC
CH
S Br CH CH O C - CH
3
2
2
S
O
CH 3
NaOH
CH 2 CH 2 O C - CH 3
CH 3
N
S
CH 2 CH 2 - OH
O
тиоформ- бромацетопропил- 4-метил-5-ацетоксиамид
ацетат
этилтиазол
4-метил-5-ацетокиэтилтиазол
Путём сплавления пиримидинового и тиазолового фрагментов при
100-120 0С получают тиамин.
CH2 - Br N
N
CH3
+
CH2 N
N
H Cl
CH3
. Cl . HCl
+
H3C
N
NH2
S
CH2 - CH2 - OH
H3C
N
NH2
S
CH2 - CH2 - OH
19.
Идентификацию тиамина хлорида проводят по реакцииобразования тиохрома. К раствору препарата добавляют
щелочной раствор калия гексоцианоферрата (III) и
бутанол, встряхивают – наблюдается синяя
флюоресценция бутанольного слоя при действии
ультрафиолетового излучения
+
CH2 N
N
CH3
CH2
[O]
N
CH3
N
H2 O
H3C
N
NH2
S
CH2 - CH2 - OH
H3C
N
N
S
CH2 - CH2 - OH
тиохром
Тиамина хлорид даёт положительную реакцию на хлоридионы, а также образует осадки с кремневольфрамовой,
фосфорновольфрамовой, пикриновой кислотами и другими
осадительными реактивами.
ИК-спектр тиамина хлорида должен иметь полосы
поглощения, совпадающие с полосами поглощения
спектра, прилагаемого к НД.
Уф-спектр поглощения тиамина хлорида в 0,1 М растворе
кислоты хлористоводородной должен иметь полосу
поглощения с максимумом при 246 нм, в 0,1 М растворе
натрия гидроксида – при 232 нм.
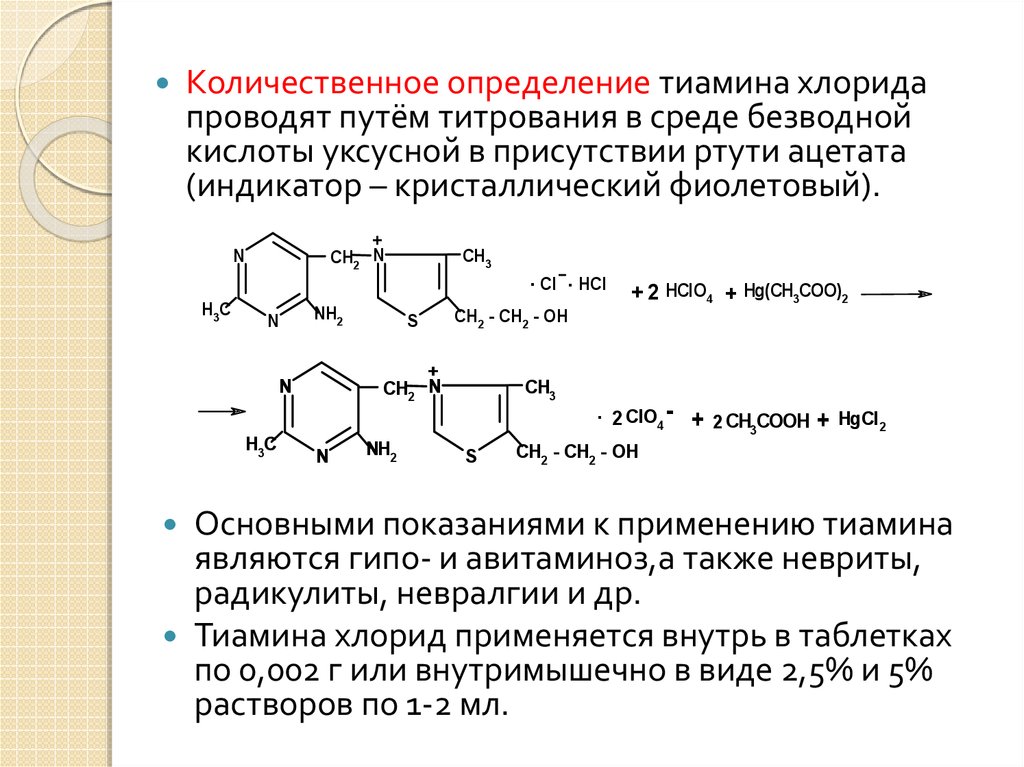
20.
Количественное определение тиамина хлоридапроводят путём титрования в среде безводной
кислоты уксусной в присутствии ртути ацетата
(индикатор – кристаллический фиолетовый).
+
CH2 N
N
H3C
N
NH2
. Cl . HCl
S
N
NH2
+ 2 HClO4 + Hg(CH3COO)2
CH2 - CH2 - OH
+
CH2 N
N
H3C
CH3
CH3
S
. 2 ClO - + 2 CH COOH + HgCl
4
2
3
CH2 - CH2 - OH
Основными показаниями к применению тиамина
являются гипо- и авитаминоз,а также невриты,
радикулиты, невралгии и др.
Тиамина хлорид применяется внутрь в таблетках
по 0,002 г или внутримышечно в виде 2,5% и 5%
растворов по 1-2 мл.
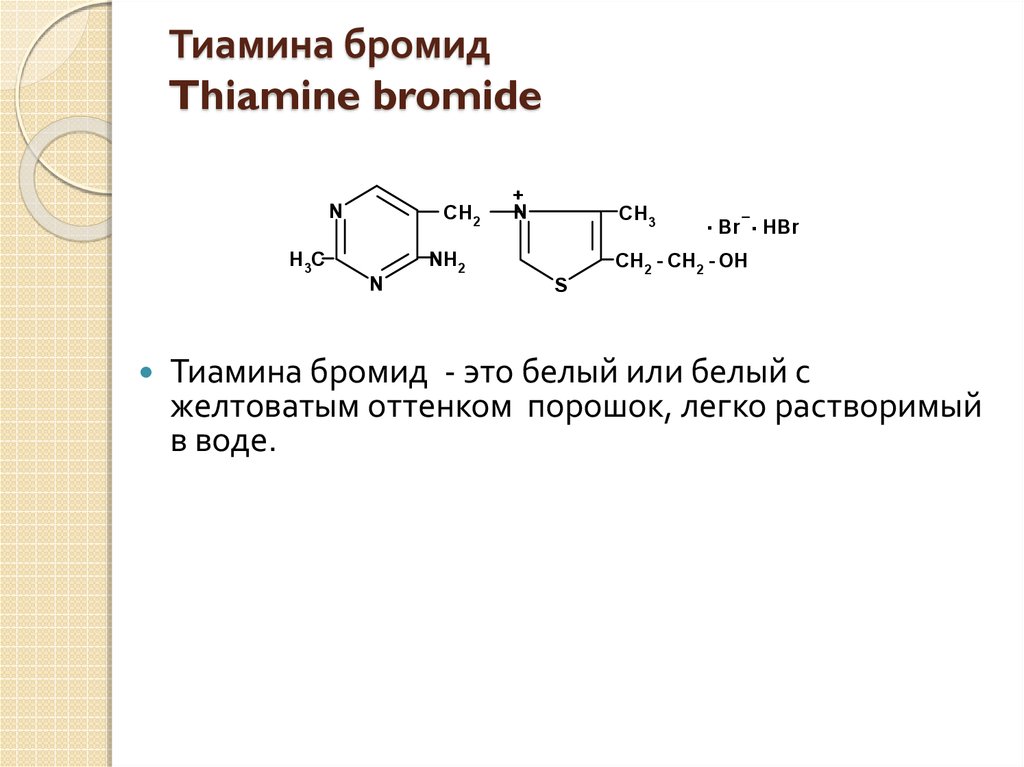
21. Тиамина бромид Thiamine bromide
NCH 2
H 3C
CH 3
NH 2
N
+
N
. Br . HBr
CH 2 - CH 2 - OH
S
Тиамина бромид - это белый или белый с
желтоватым оттенком порошок, легко растворимый
в воде.
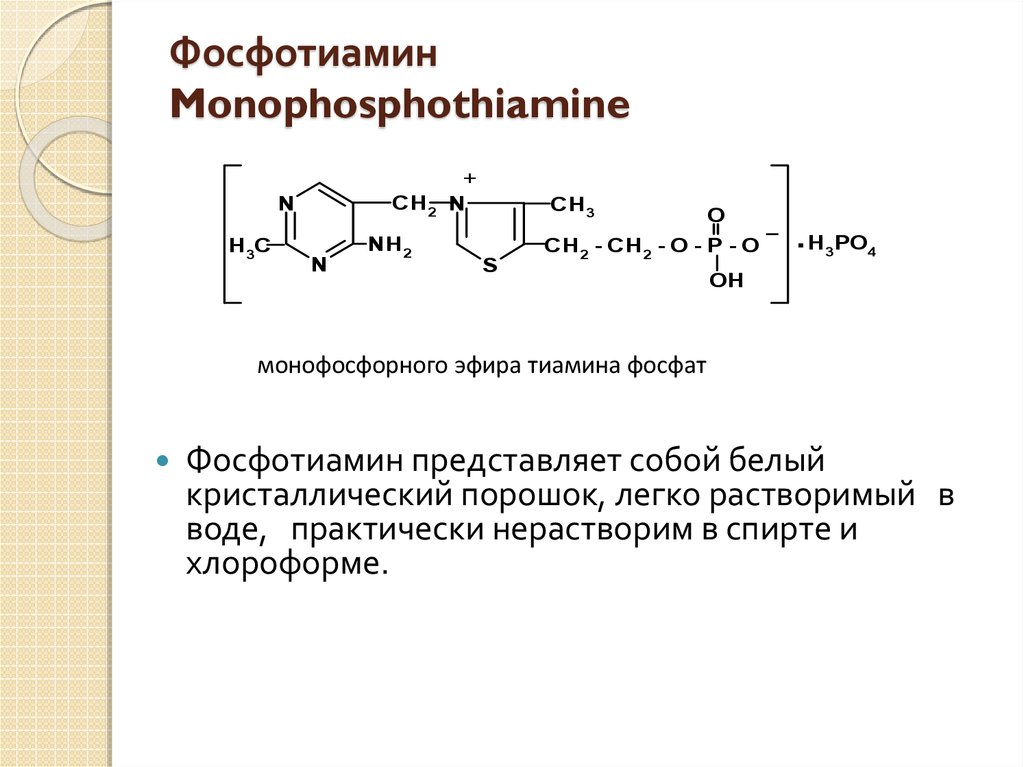
22. Фосфотиамин Monophosphothiamine
CH 2N
H 3C
N
NH 2
+
N
CH 3
S
O
CH 2 - CH 2 - O - P - O
. H3PO4
OH
монофосфорного эфира тиамина фосфат
Фосфотиамин представляет собой белый
кристаллический порошок, легко растворимый в
воде, практически нерастворим в спирте и
хлороформе.
23.
Подлинность фосфотиамина устанавливают пореакции образования тиохрома. К раствору
препарата добавляют 1мл раствора калия
гексоцианоферрата (III) и 1 мл раствора натрия
гидроксида, 5 мл бутилового или изоамилового
спирта, встряхивают и дают отстояться.
В ультрафиолетовом свете появляется синяя
флюоресценция верхнего слоя (см. тиамина хлорид).
К раствору фосфотиамина добавляют раствор
аммония молибдата и азотную кислоту и нагревают –
образуется жёлтый кристаллический осадок,
растворимый в растворе аммиака (фосфаты)
H3PO4 + 12 (NH4)2MoO4 +21 HNO3 →
→ (NH4)3 PO4 . 12MoO3↓ +21 HNO3+12 H2 O
Уф-спектр поглощения фосфотиамина должен иметь
полосу поглощения с максимумом при 246 нм.
ИК-спектр фосфотиамина должен совпадать с ИКспектром стандартного образца.
24.
Количественное определение фосфотиаминапроводят спектрофотометрическим методом.
Измерение оптической плотности проводят в
фосфатном буфере при длине волны 268 нм. В
качестве стандартного образца используют
раствор тиамина хлорида и используют
коэффициент пересчёта тиамина хлорида на
фосфотиамин.
Применяют фосфотиамин при невритах,
невралгиях, при астении и других заболеваниях,
которые связяны с недостатком тиамина.
Выпускается фосфотиамин в таблетках по 0,01 и
0,03 г.
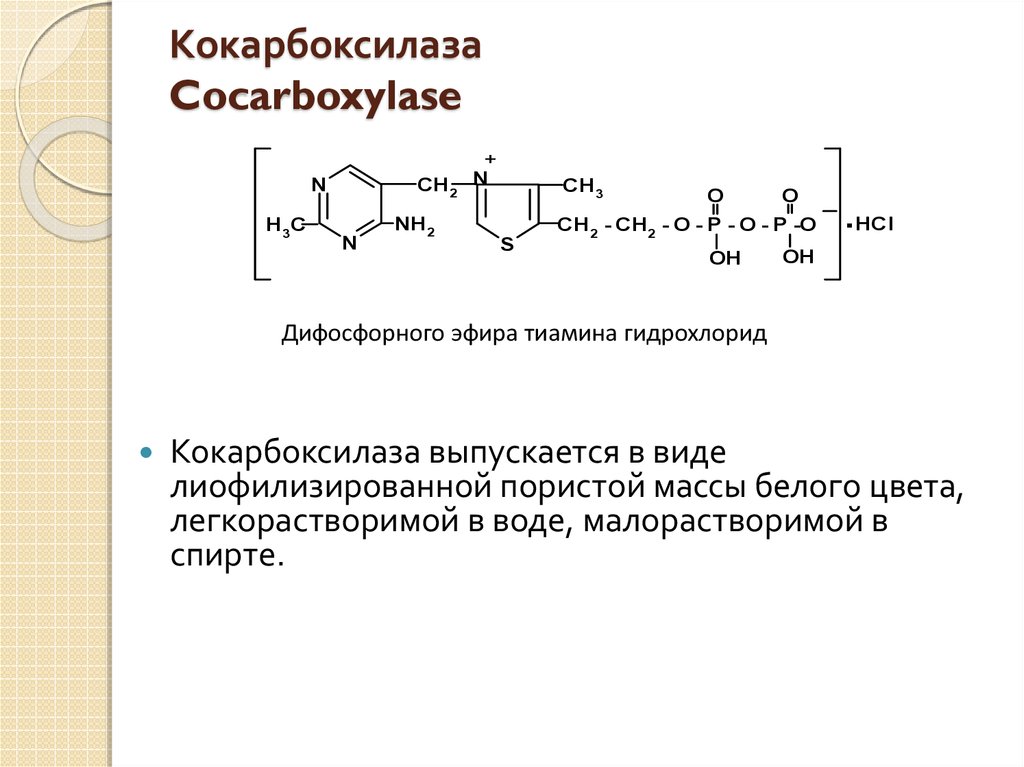
25. Кокарбоксилаза Cocarboxylase
CH 2N
H 3C
N
NH 2
+
N
CH 3
S
O
O
CH 2 - CH 2 - O - P - O - P -O
OH
. HCl
OH
Дифосфорного эфира тиамина гидрохлорид
Кокарбоксилаза выпускается в виде
лиофилизированной пористой массы белого цвета,
легкорастворимой в воде, малорастворимой в
спирте.
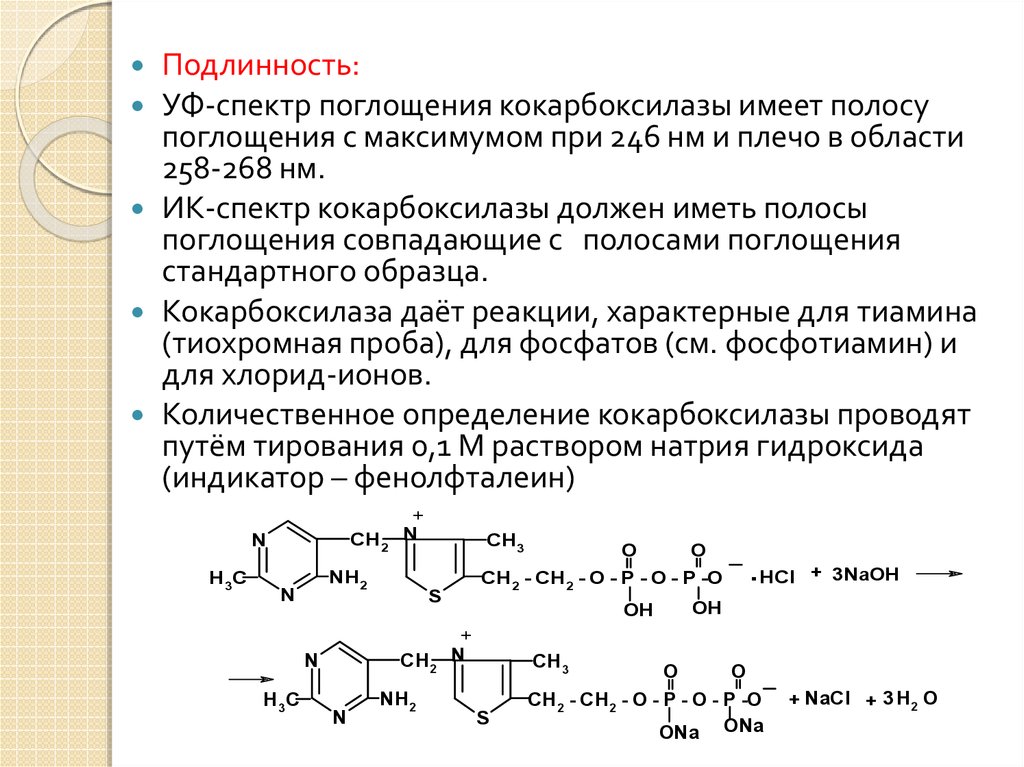
26.
Подлинность:УФ-спектр поглощения кокарбоксилазы имеет полосу
поглощения с максимумом при 246 нм и плечо в области
258-268 нм.
ИК-спектр кокарбоксилазы должен иметь полосы
поглощения совпадающие с полосами поглощения
стандартного образца.
Кокарбоксилаза даёт реакции, характерные для тиамина
(тиохромная проба), для фосфатов (см. фосфотиамин) и
для хлорид-ионов.
Количественное определение кокарбоксилазы проводят
путём тирования 0,1 М раствором натрия гидроксида
(индикатор – фенолфталеин)
CH 2
N
H 3C
NH 2
N
CH 3
N
NH 2
O
O
. HCl
CH 2 - CH 2 - O - P - O - P -O
S
CH 2
N
H 3C
+
N
OH
OH
+
N
CH 3
S
+ 3NaOH
O
O
CH 2 - CH 2 - O - P - O - P -O
ONa ONa
+ NaCl + 3 H 2 O
27.
В отличие от тиамина кокарбоксилаза проявляетв меньшей степени витаминные свойства.
Однако она является эффективным средством
при нарушениях коронарного кровообращения,
нарушениях сердечного ритма, при
диабетической и печёночной коме, при
патологиях, вызванных нарушениями
углеводного обмена.
Вводят кокарбоксилазу внутривенно,
внутримышечно или подкожно по 0,05-0,1 г. К
ампулам прилагают растворитель в ампулах.
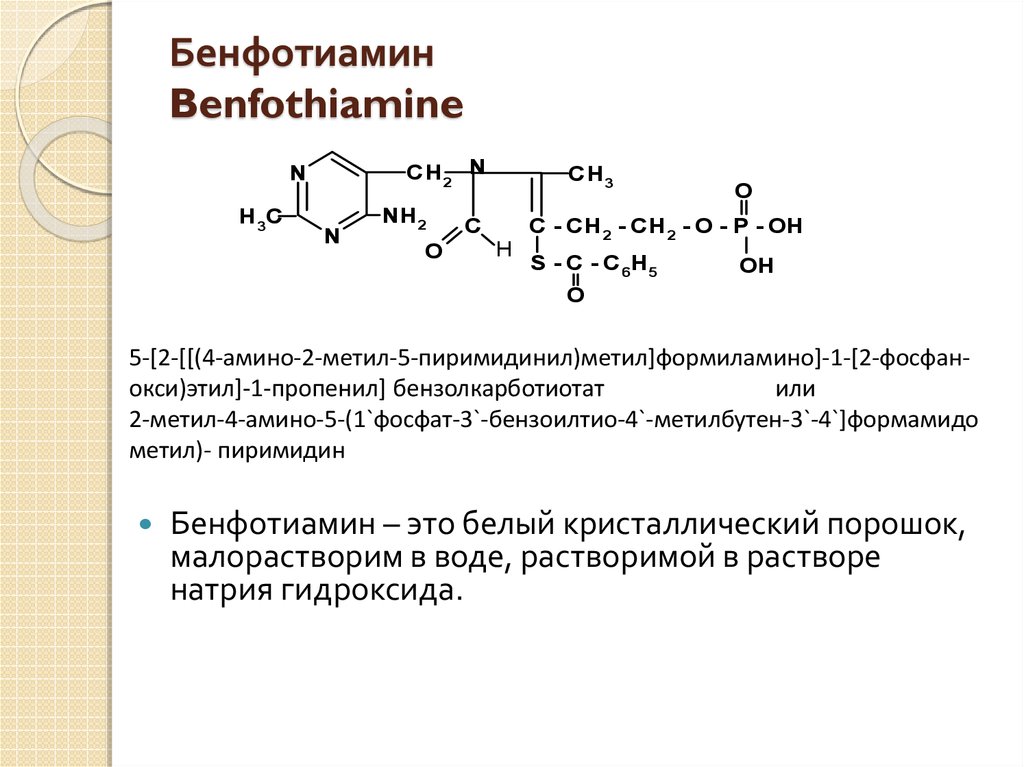
28. Бенфотиамин Benfothiamine
CH 2 NN
H 3C
N
NH 2
O
CH 3
C
H
O
C - CH 2 - CH 2 - O - P - OH
S - C - C 6H 5
OH
O
5-[2-[[(4-амино-2-метил-5-пиримидинил)метил]формиламино]-1-[2-фосфанокси)этил]-1-пропенил] бензолкарботиотат
или
2-метил-4-амино-5-(1`фосфат-3`-бензоилтио-4`-метилбутен-3`-4`]формамидо
метил)- пиримидин
Бенфотиамин – это белый кристаллический порошок,
малорастворим в воде, растворимой в растворе
натрия гидроксида.
29.
Подлинность бенфотиамина устанавливают по УФспектру и с помощью химических реакций.УФ-спектр поглощения в фосфатном буфере должен
иметь полосу поглощения с максимумом при 244 нм
и плечо в области 262-273 нм.
Бенфотиамин в отличие от тиамина даёт реакцию
образования флуоресцирующего продукта только в
присутствии цистеина. Смесь 0,01 г препарата и 0,04
г цистеина растворяют в воде при нагревании,
охлаждают, прибавляют раствор калия
гексацианоферрата(III) и раствор натрия гидроксида,
бутиловый (изоамиловый) спирт и встряхивают.
После отстаивания слой органического
растворителя даёт синюю флюоресценцию в
ультрафиолетовом свете.
Бенфотиамин даёт реакцию на фосфаты (см.
фосфотиамин).
30.
Количественное определение бенфотиаминапроводят спектрофотометричес-ким методом.
Измерение оптической плотности проводят при
длине волны 244 нм. Расчёт содержания
бенфотиамина проводят по молярному
коэффициенту поглощения.
По фармакологическому действию бенфотиамин
близок к тиамину и кокарбоксилазе. Его применяют
при хроническом гепатите, полинейропатии,
дерматозах и других заболеваниях, при которых
показано применение тиамина.
Назначают бенфотиамин по 0,025-0,05 г 3-4 раза в
день.
Выпускается бенфотиамин в таблетках по 0,005 и
0,0025 г или драже по 0,15г.
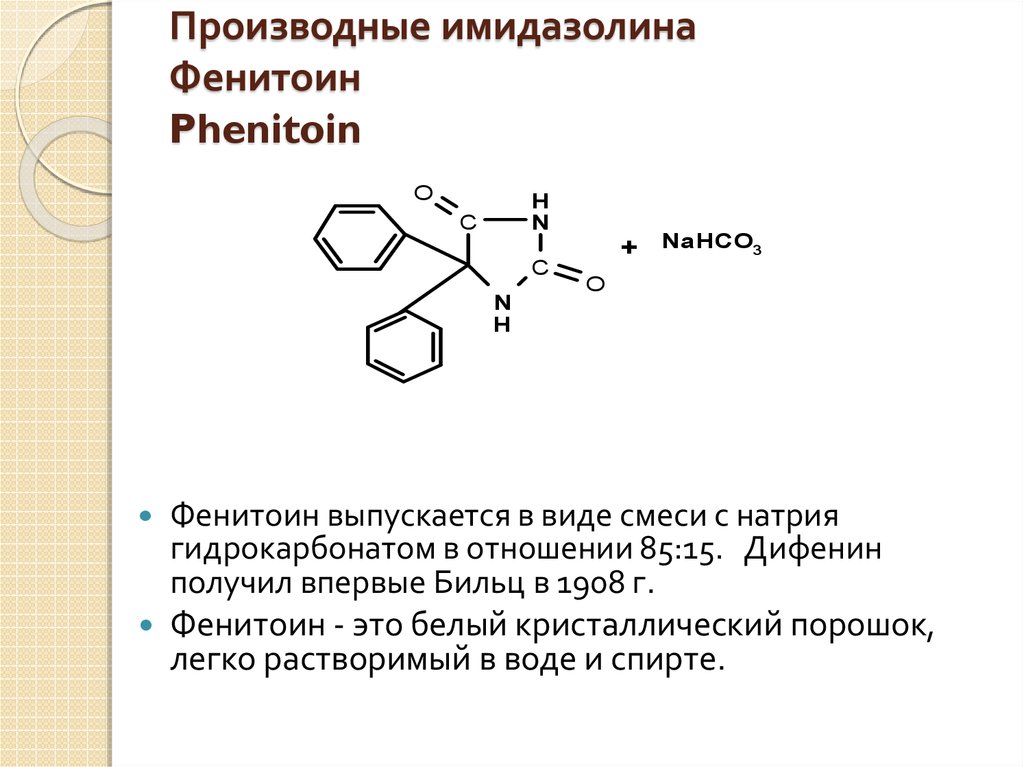
31. Производные имидазолина Фенитоин Phenitoin
OH
N
C
C
N
H
+ NaHCO3
O
Фенитоин выпускается в виде смеси с натрия
гидрокарбонатом в отношении 85:15. Дифенин
получил впервые Бильц в 1908 г.
Фенитоин - это белый кристаллический порошок,
легко растворимый в воде и спирте.
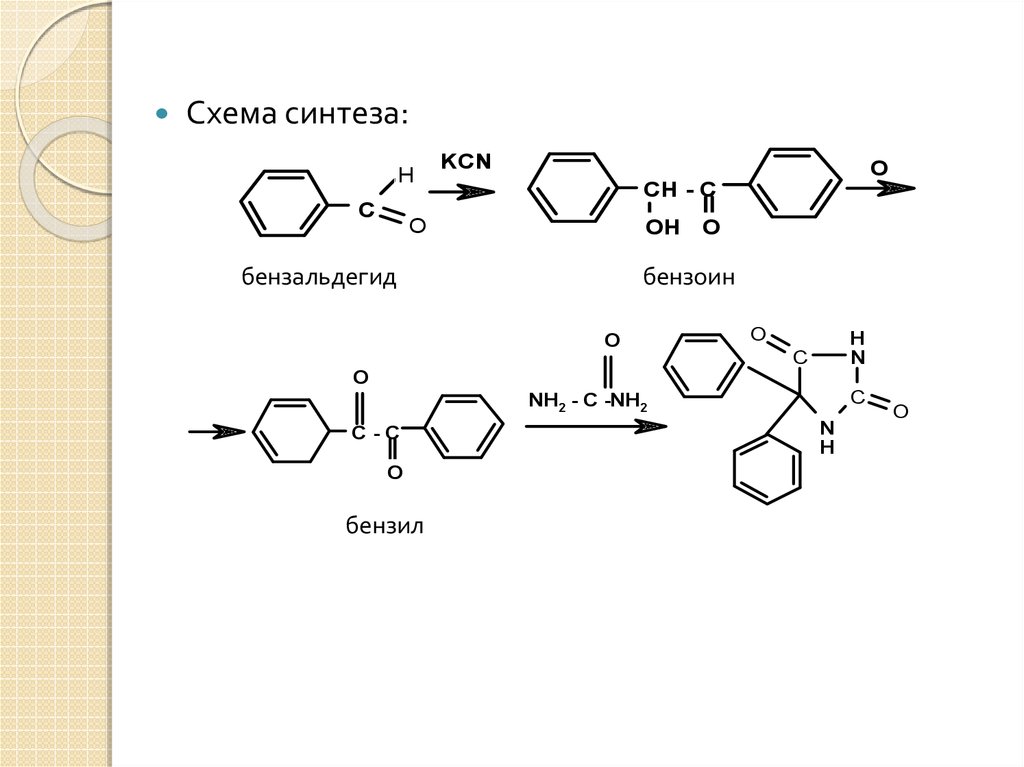
32.
Схема синтеза:H
C
KCN
O
CH - C
O
OH
бензальдегид
O
бензоин
O
O
H
N
C
O
C
NH2 - C -NH2
C-C
O
бензил
N
H
O
33.
Для идентификации фенитоина к его водномураствору добавляют раствор кислоты
хлористоводородной разведенной – выделяются
пузырькиуглерода диоксида и выпадает белый
осадок. Осадок экстрагируют эфиром. Экстракт
выпаривают досуха и определяют температуру
плавления основания фенитоина (2950С).
В метанольном растворе фенитоин даёт фиолетовое
окрашивание с раствором кобальта нитрата в
присутствии пиперидина.
С раствором меди сульфата фенитоин в метанольном
растворе также образует комплексную соль голубого
цвета.
ИК-спектр фенитоина должен соответствовать ИКспектрому стандартного образца.
УФ-спектр фенитоина в 0,1 М растворе натрия
гидроксида должен иметь полосу поглощения с
максимумом при длине волны 217 нм.
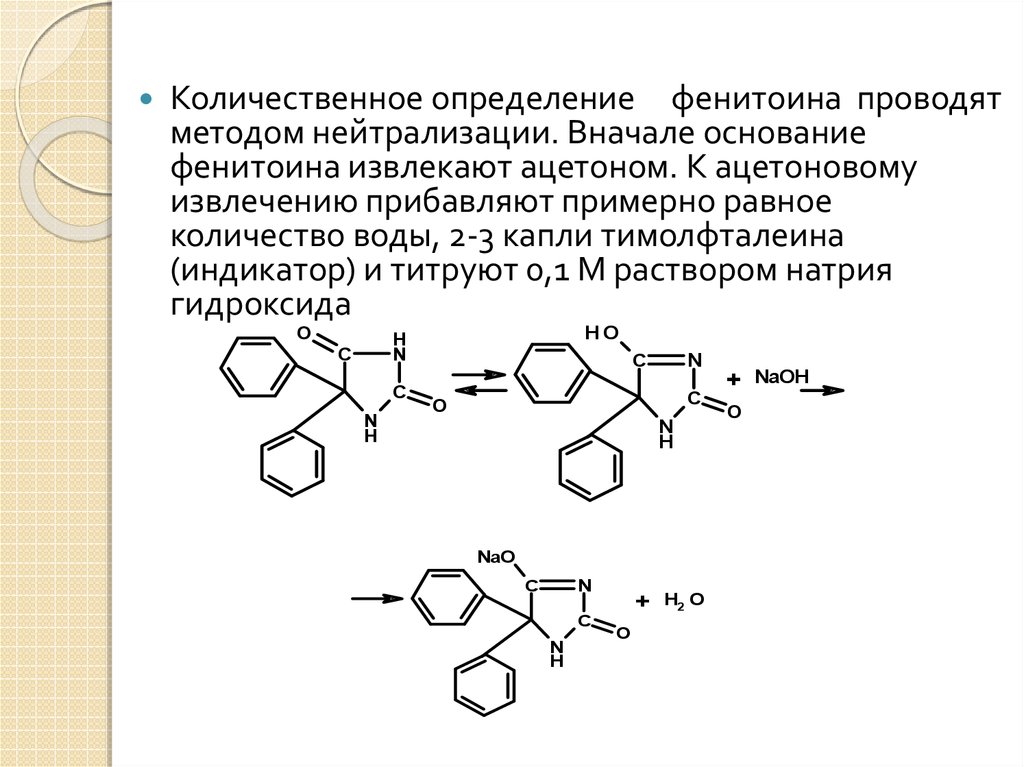
34.
Количественное определение фенитоина проводятметодом нейтрализации. Вначале основание
фенитоина извлекают ацетоном. К ацетоновому
извлечению прибавляют примерно равное
количество воды, 2-3 капли тимолфталеина
(индикатор) и титруют 0,1 М раствором натрия
гидроксида
O
HO
H
N
C
C
N
H
N
C
C
O
N
H
NaO
N
C
C
N
H
+ H2 O
O
+
O
NaOH
35.
Остаток на фильтре после извлечения фенитоинапредставляющий собой натрия гидрокарбонат
переносят в колбу для титрования, растворяют в
воде и титруют 0,1 М раствором кислоты
хлористоводородной
NaHCO3 + HCl → NaCl + H2O + CO2↑
Фенитоин проявляет противосудорожное действие
без выраженного седативного и снотворного
действия. Он проявляет также антиаритмическое
действие.
Применяют фенитоин как противоэпилептическое
средство в дозах от 0,1 до 0,2 г.
Выпускается фенитоин в таблетках по 0,117 г или в виде
1% раствора для инъекций в ампулах.











 Химия
Химия








