Похожие презентации:
Научные принципы химического производства. Производство аммиака
1. Основные научные принципы химического производства
Производствоаммиака
Ленкова Н.Г.
Красносельский р-н
ГОУ СОШ № 414
2. Современные производства
3. Аварии на производстве и даже в космосе
4. Перевозка аммиака и ТБ
5. Применение аммиака
6. 105 метровая башня для производства гранул
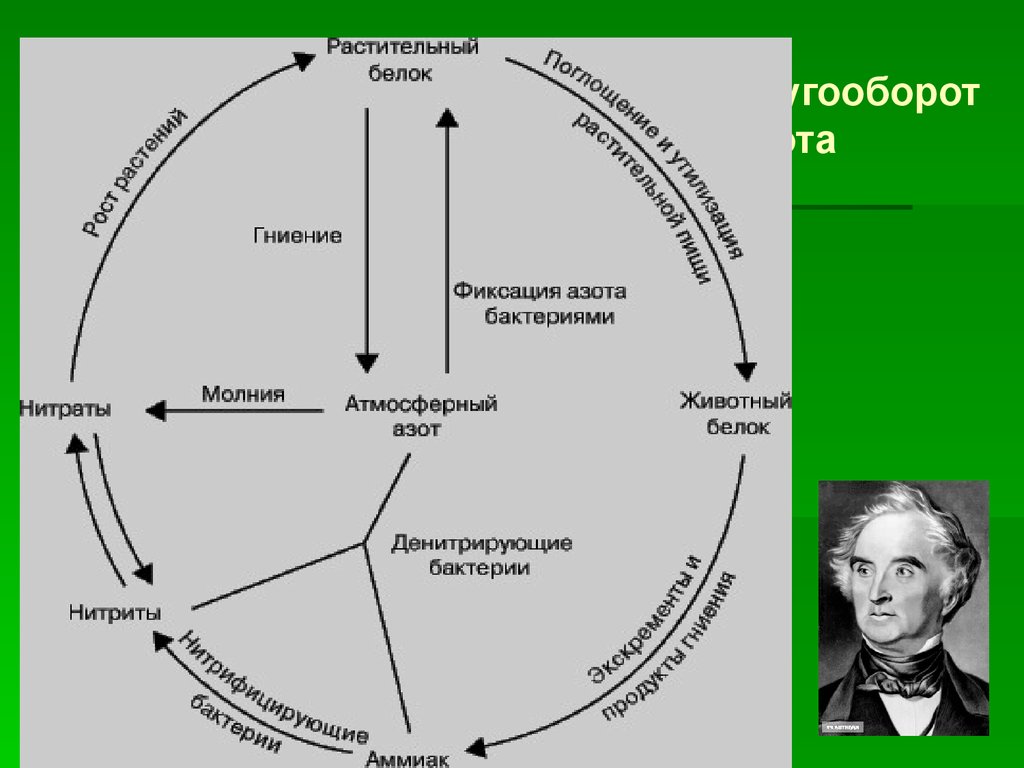
7. Кругооборот азота
8. В 1840 выходит книга « Органическая химия в применении к сельскому хозяйству и физиологии» Ю.Либиха.
« Рим выбрасывает в сточные трубы плодородие Сицилии».Юстус
Либих
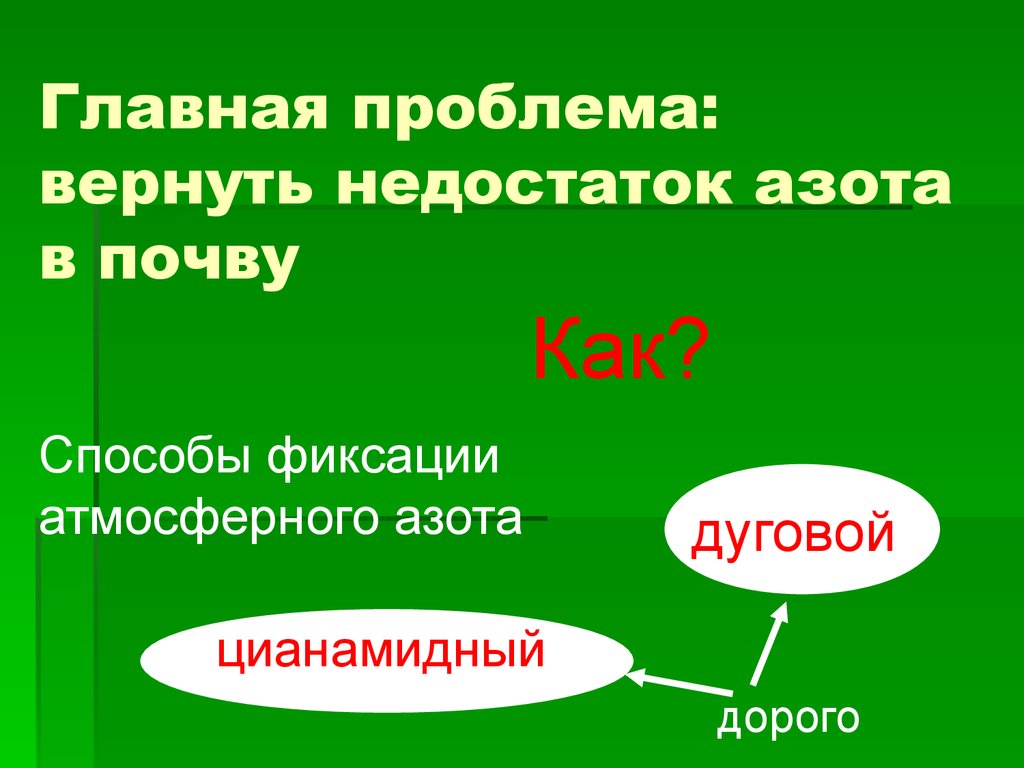
9. Главная проблема: вернуть недостаток азота в почву
Как?Способы фиксации
атмосферного азота
дуговой
цианамидный
дорого
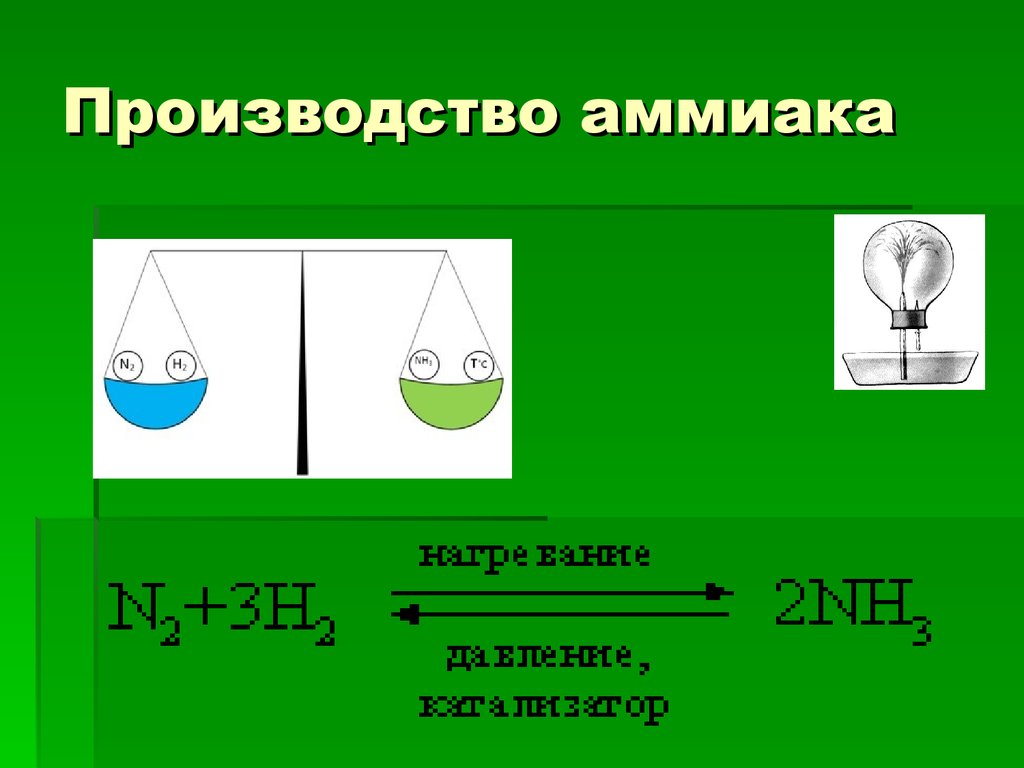
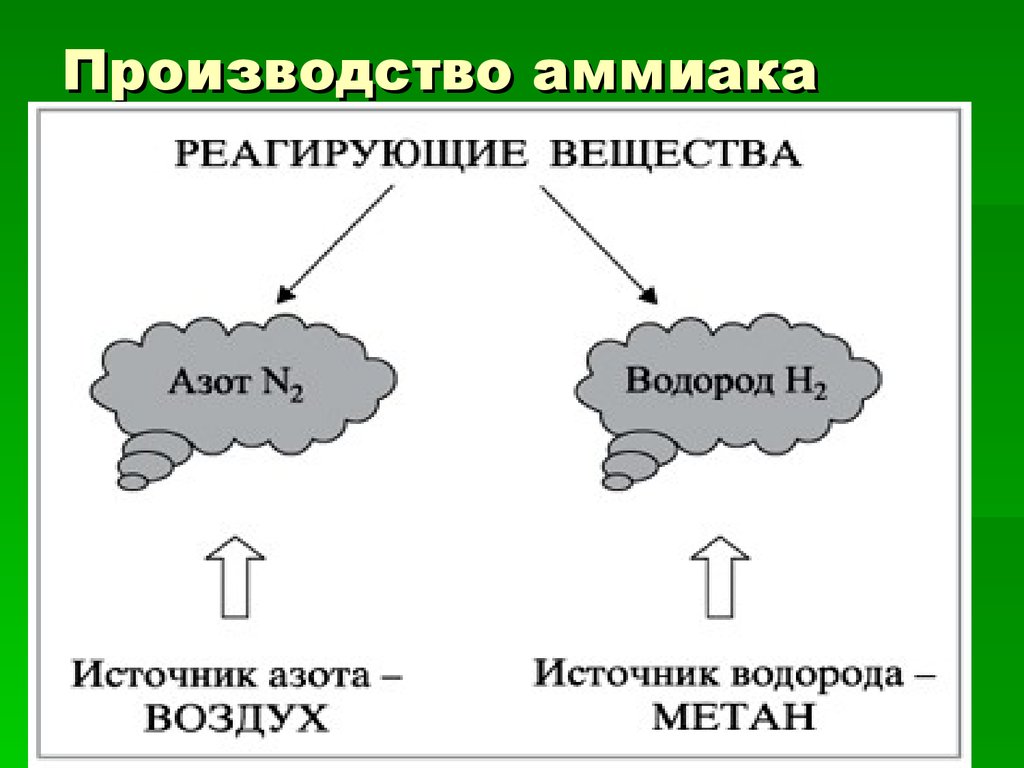
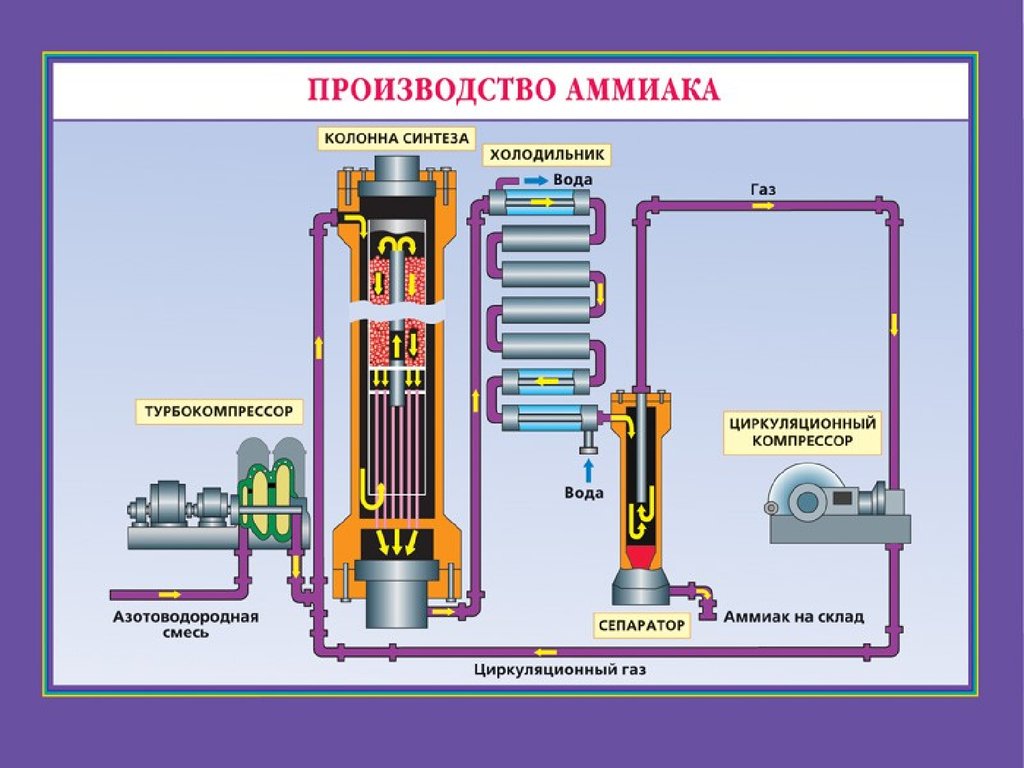
10. Производство аммиака
11. Историческая справка
Ле ШательеФриц Габер 1918
год Нобелевская
премия
Карл Бош
история
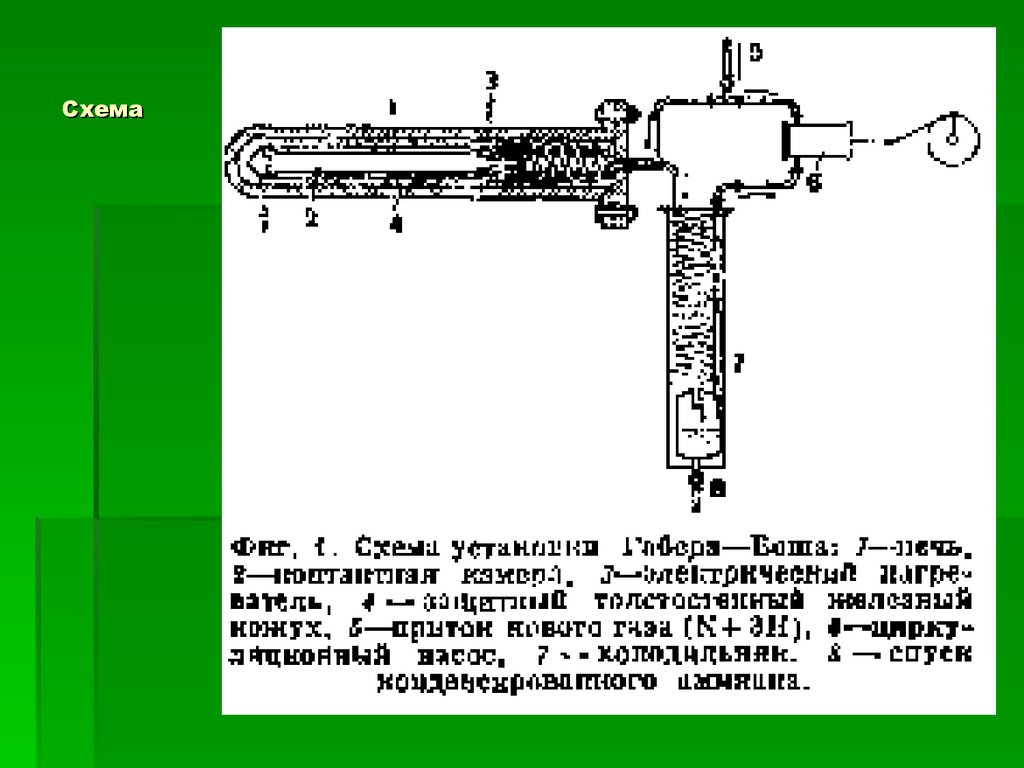
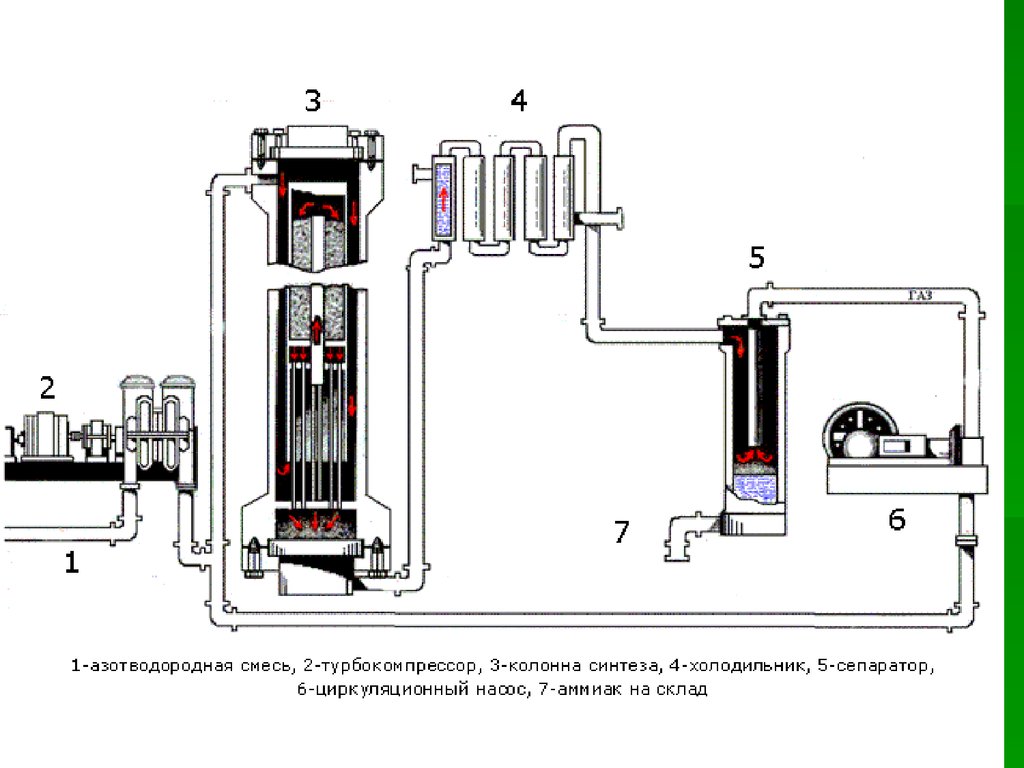
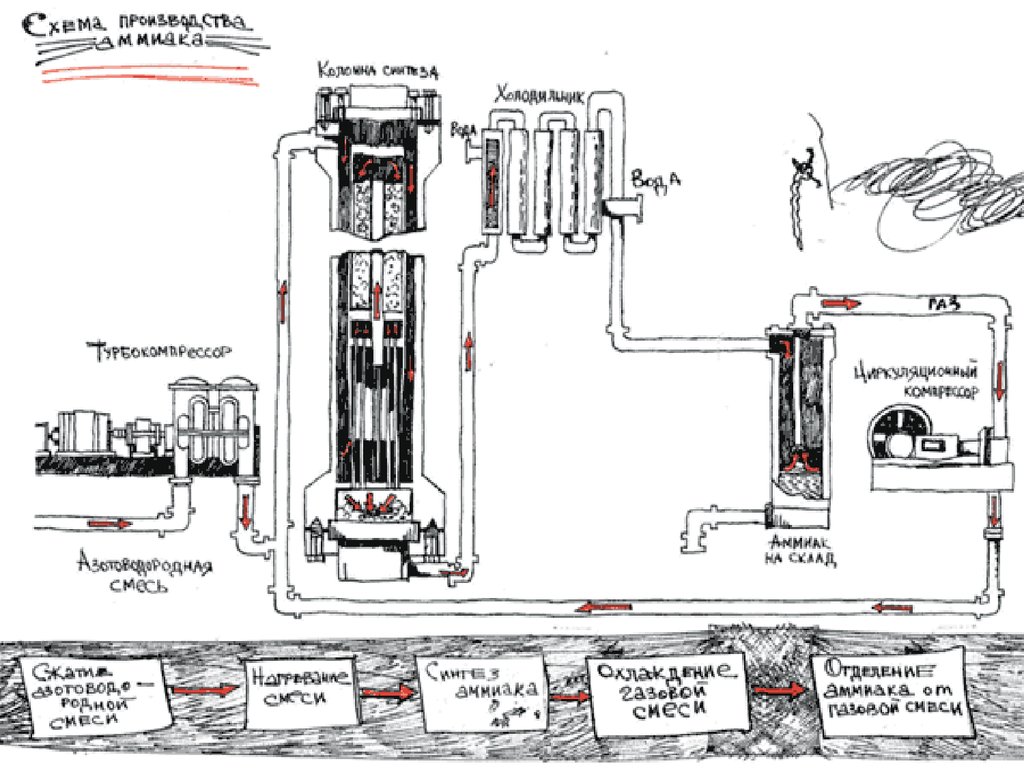
12. Схема
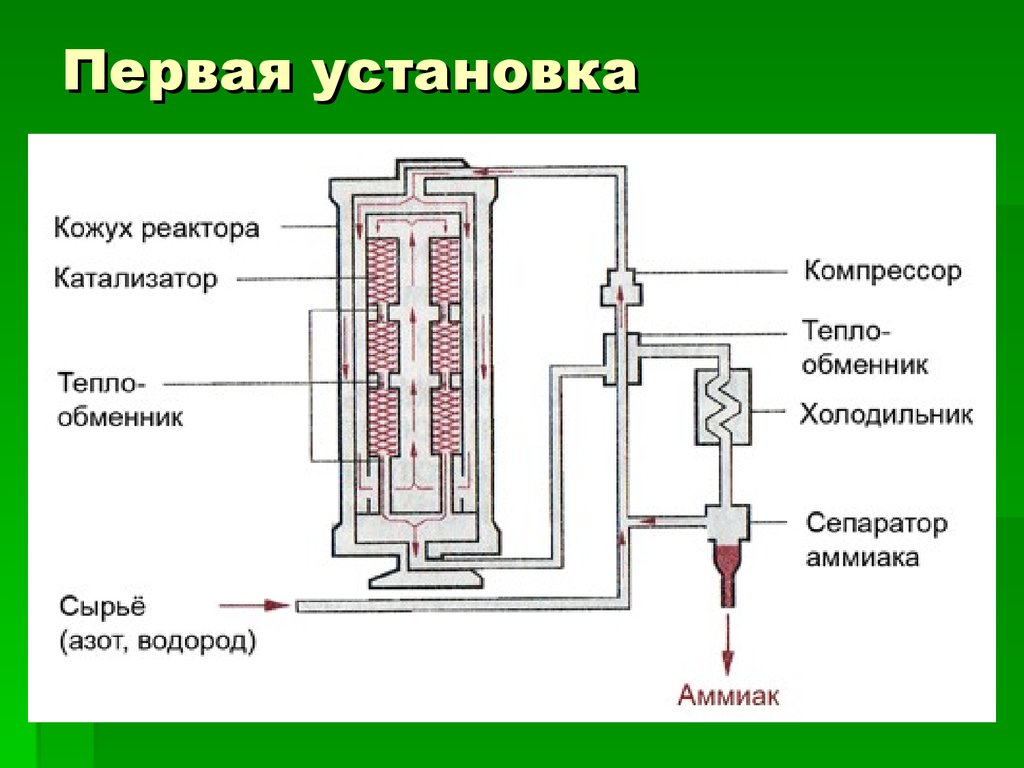
13. Первая установка
14. Химический процесс
Реакция Ф. Габера – К.БошаN2 + 3H2
2 NH3 + O
H = - 92 кДж
15. 10 элементов химической технологии
1 физико-химия процесса ипоиски оптимальных условий
16. 10 элементов
2Сырьё, основные и
побочные продукты,
отходы производства
17. 10 элементов
3Энергетика процесса
4
Аппаратура
18. 10 элементов
5Материалы аппаратуры и
средства их защиты от
коррозии
19. 10 элементов
6Аналитический контроль и
управление процессом.
Включая автоматизацию
и новые технологии
20. 10 элементов
7 Организация и охрана труда8 Защита окружающей среды и
создание экотехнологии
21. 10 элементов
9Экономика производства,
включая
капиталовложения.
Производительность
труда и себестоимость
продукции.
22. 10 элементов
10Развитие принципиально
новых химико –
технологических процессов,
в том числе экстремальных
воздействий(космическая
технология, радиационные,
плазмохимические, криохимические
процессы)
23. Основные технологические принципы
Непрерывность процессаПротивоток
Утилизация теплоты реакции
Теплообмен
Комплексное использование сырья и
отходов производства
Циркуляционный процесс
Принцип кипящего слоя
24. Основные технологические принципы
Теплообменники25.
26. План
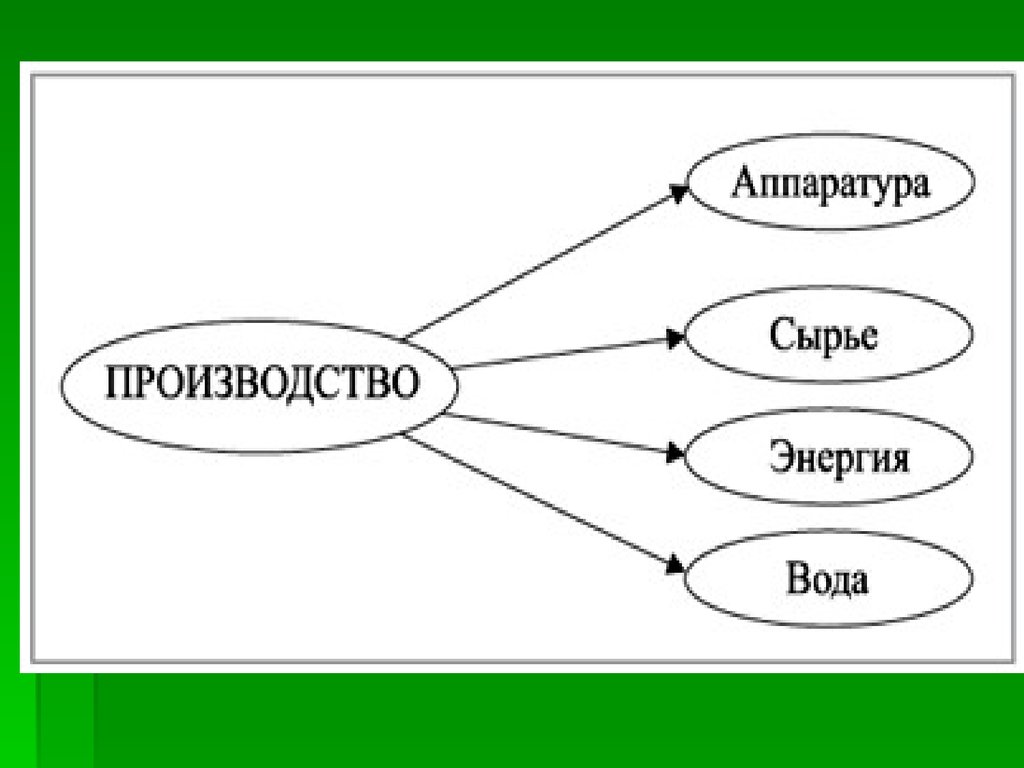
СырьёАппаратура
Технологические принципы
Химические процессы и
условия их протекания
Продукт
27. Производство аммиака
28.
29.
30. Условия протекания реакции
Условия протеканияN2 + 3H2 = 2 NH3 + Q
реакции
Температура 450-550 С
оптимальная
Давление 250-350 атм
или 25-35 Мпа
Катализатор FeO+Fe2O3
Концентрация веществ
31. Выход продукта
15% - 20 %32. Какие факторы влияют на химическое равновесие системы:
33. Вопросы
Почему процесс циркуляционный?Какое сырьё используют для
производства аммиака?
Какой технологический принцип
используется в колонне синтеза?
Какие факторы смещают
химическое равновесие в сторону
образования продукта реакции?
Какую роль играет катализатор?
34. Из предложенных принципов выберите, характерные для данного производства.
35. Производство аммиака в России 2009 год
36.
37.
38. Производство синтетического аммиака
1905-1910 немецкий учёный Ф. Габерназад
предложил и теоретически обосновал
прямой синтез аммиака из простых веществ
1913 при участии К.Боша осуществил
процесс на пилотной установке
1916 реализовал синтез в промышленных
условиях
история






























 Химия
Химия Промышленность
Промышленность








