Похожие презентации:
Газовые законы
1. Газовые законы
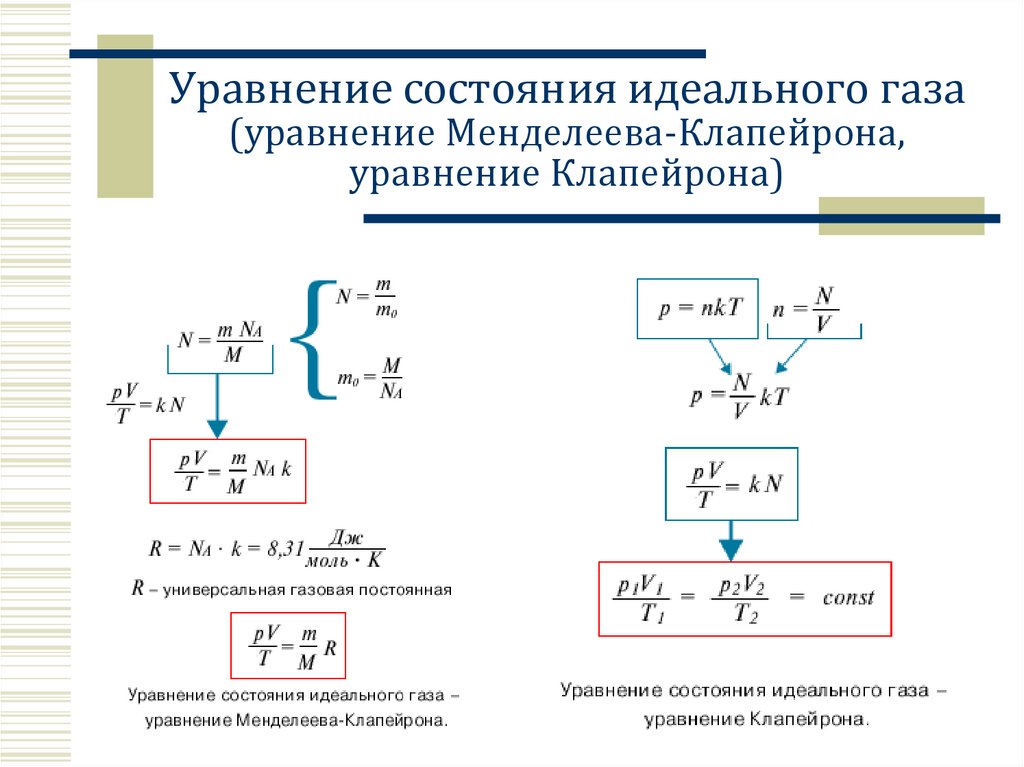
2. Уравнение состояния идеального газа (уравнение Менделеева-Клапейрона, уравнение Клапейрона)
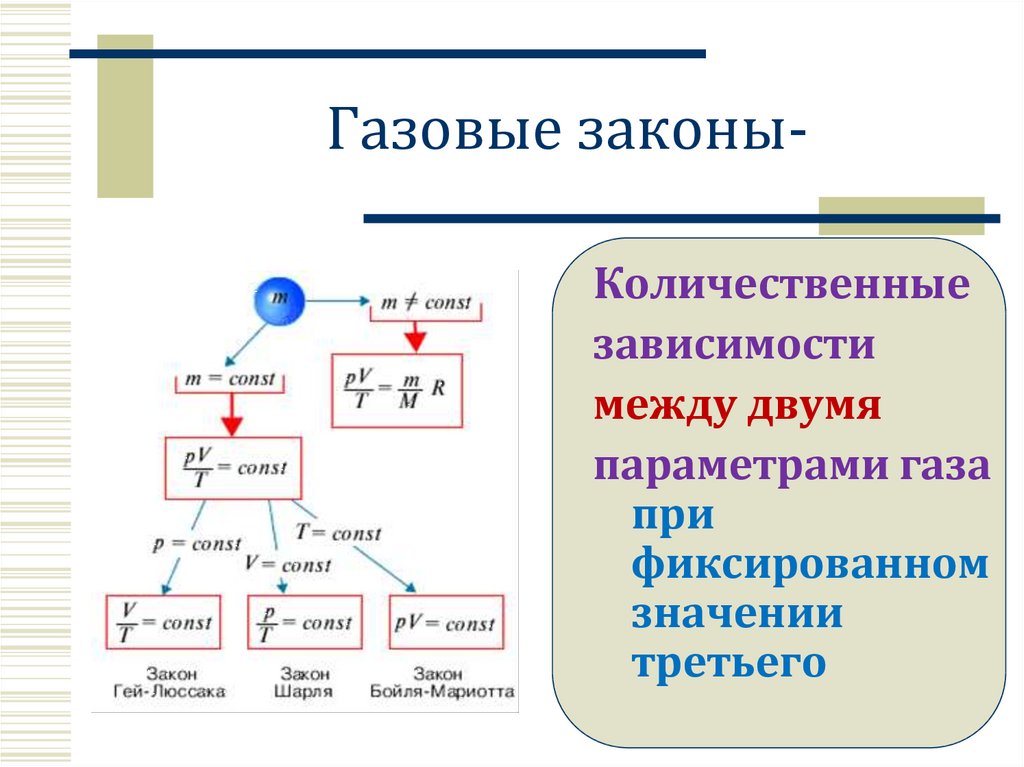
3. Газовые законы-
Газовые законыКоличественныезависимости
между двумя
параметрами газа
при
фиксированном
значении
третьего
4. Изотермический процесс T=const
В термостатеЗакон Бойля – Мариотта.
Для газа данной массы произведение
давления газа на его объем постоянно,
если температура газа не меняется.
pV = const
p↑ , V↓
обратная
пропорциональность
5. Изотермы
Изотермическое расширение T = constp
1
2
V
T
V↑, p↓
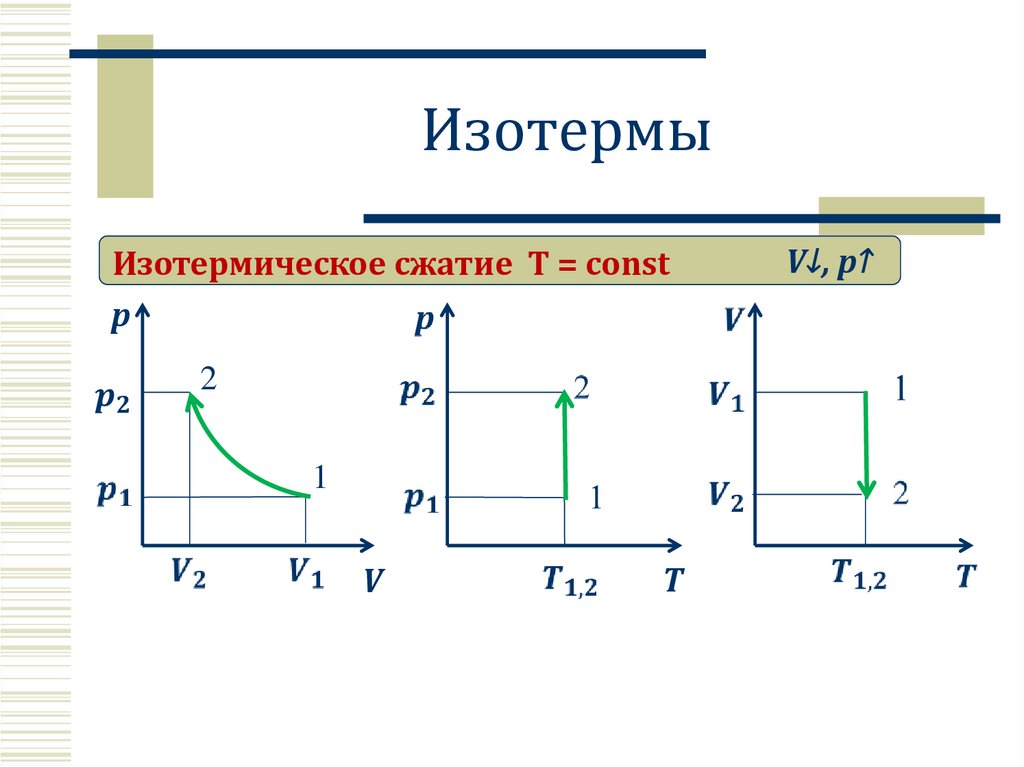
6. Изотермы
Изотермическое сжатие T = constp
2
1
V
T
V↓, p↑
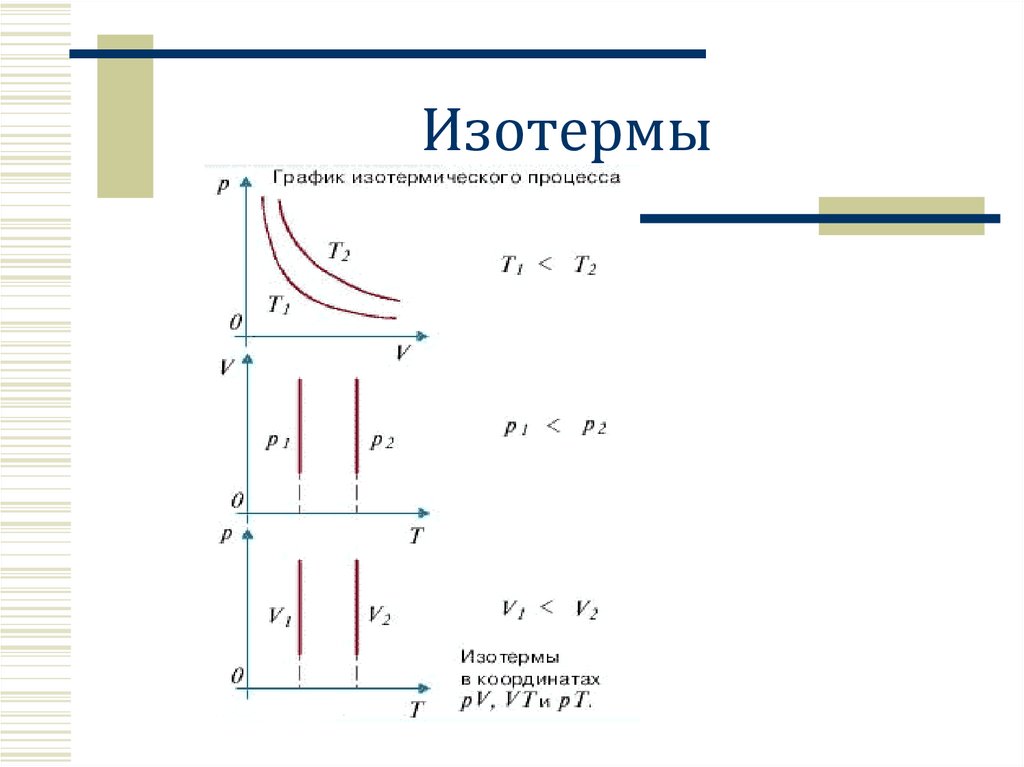
7. Изотермы
8. Изобарный процесс p=const
В цилиндре сподвижным поршнем
Закон Гей – Люссака.
Для газа данной массы отношение
объема газа к температуре постоянно,
если давление газа не меняется.
V↑ , T↑
прямая
пропорциональность
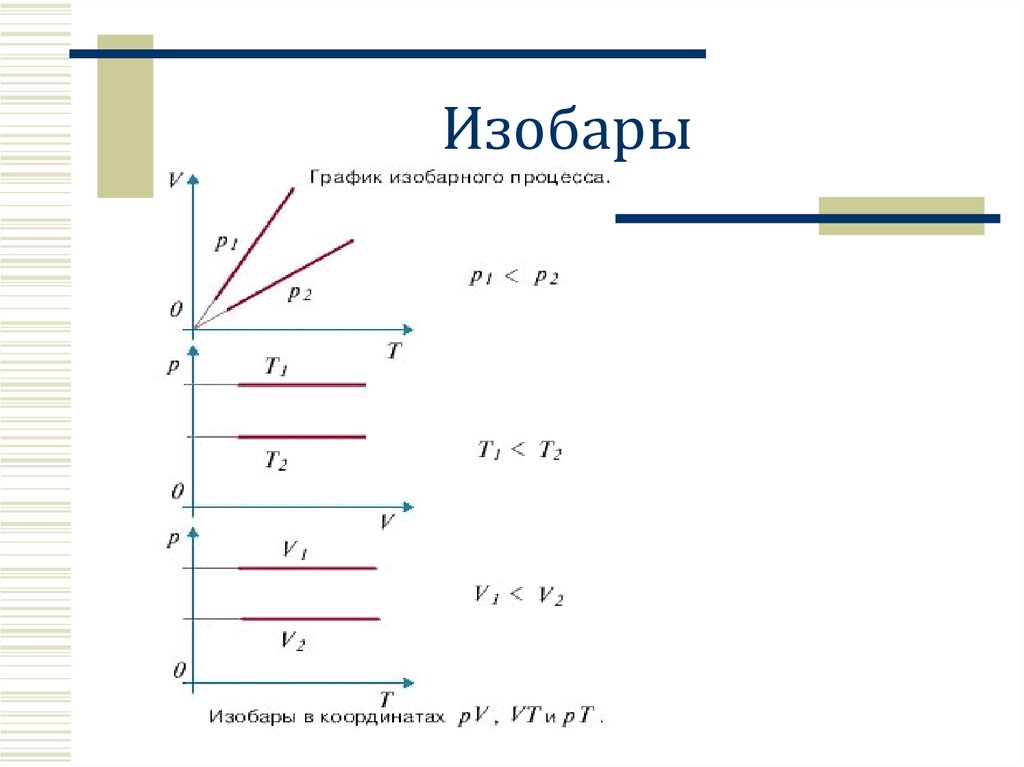
9. Изобары
Изобарное расширение (нагревание) p = const V↑, T↑p
1
2
V
T
10. Изобары
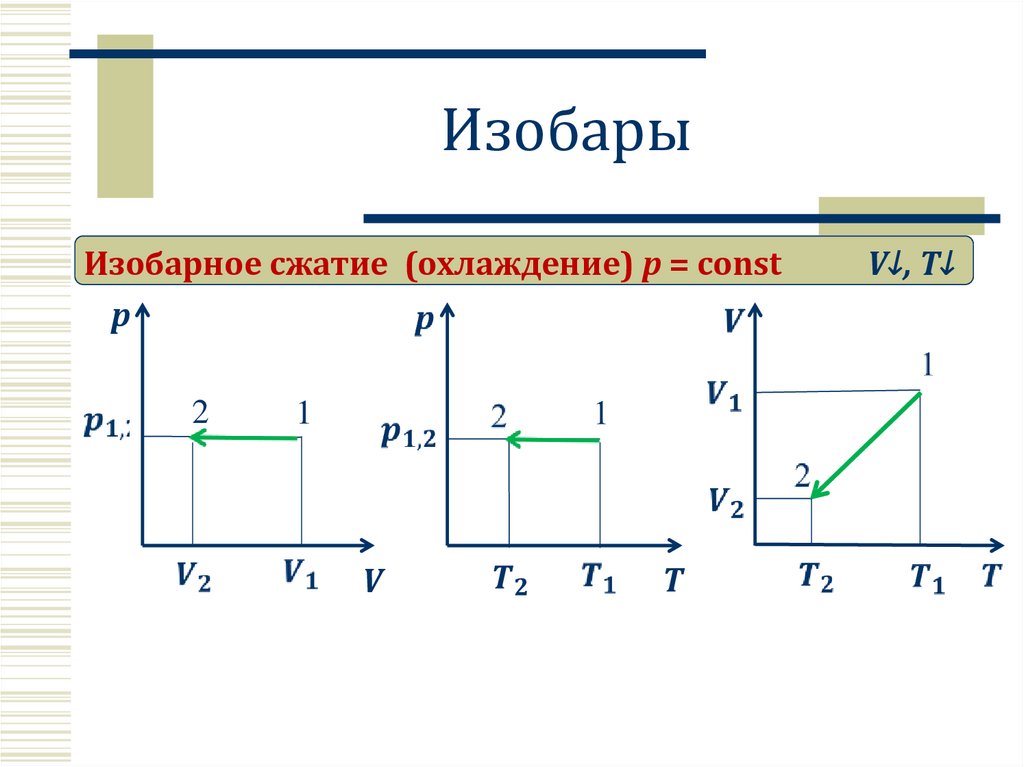
Изобарное сжатие (охлаждение) p = constp
2
1
V
T
V↓, T↓
11. Изобары
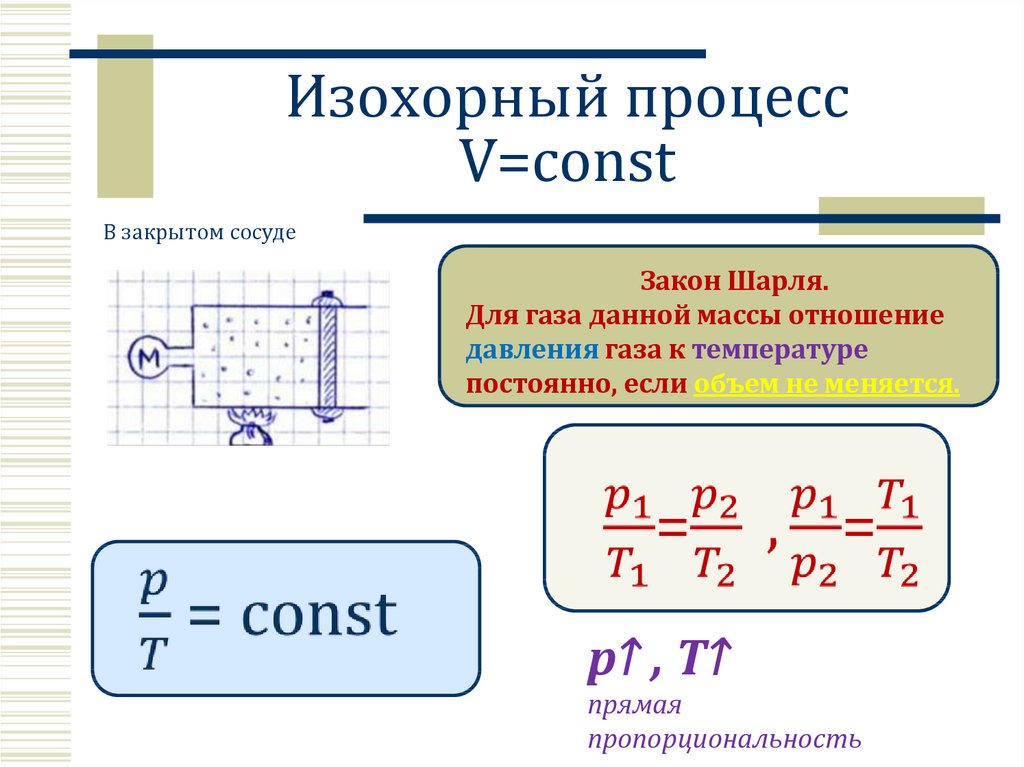
12. Изохорный процесс V=const
В закрытом сосудеЗакон Шарля.
Для газа данной массы отношение
давления газа к температуре
постоянно, если объем не меняется.
p↑ , T↑
прямая
пропорциональность
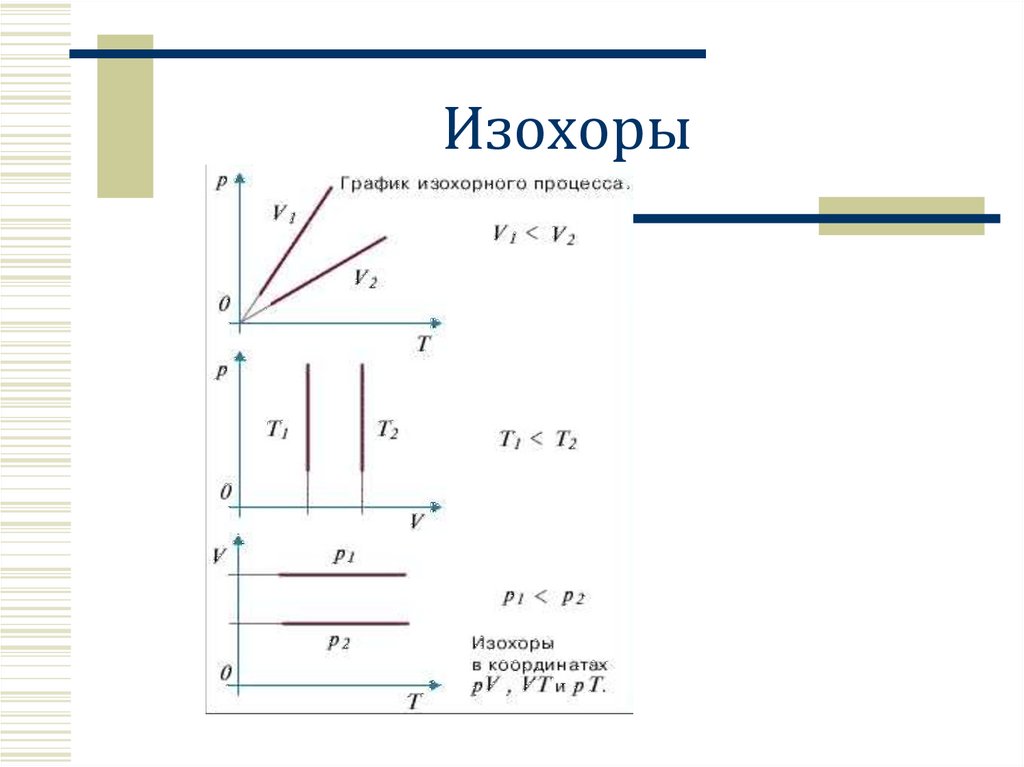
13. Изохоры
p↑, T↑Изохорное нагревание V = const
p
2
1
V
T
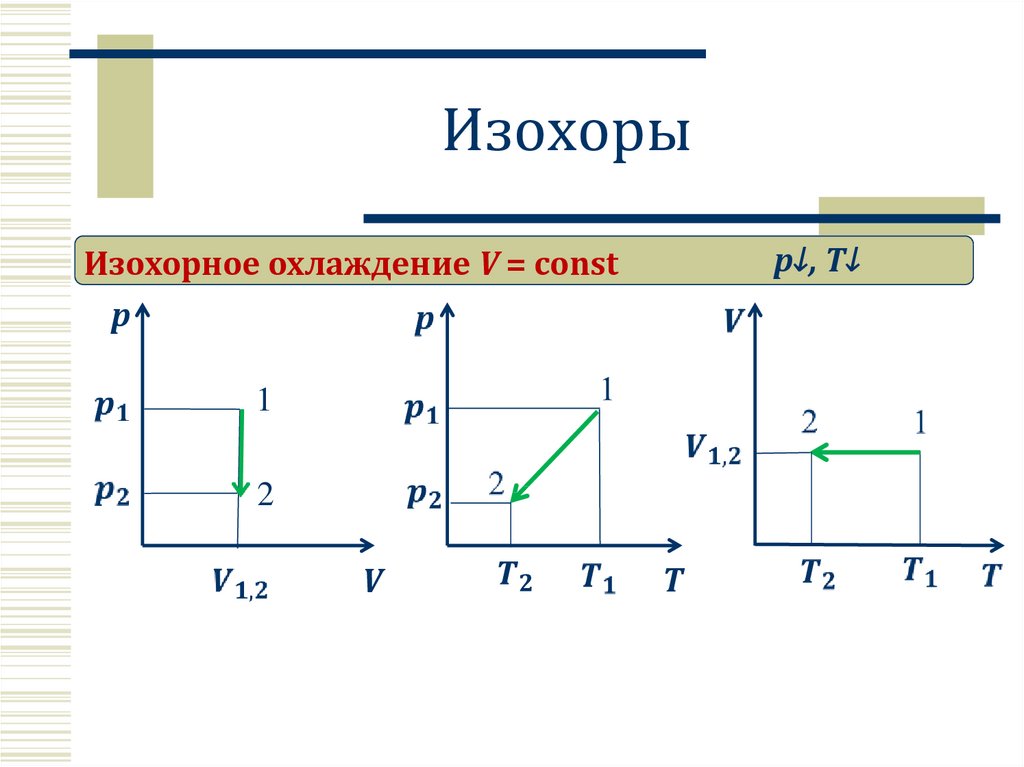
14. Изохоры
p↓, T↓Изохорное охлаждение V = const
p
1
2
V
T
15. Изохоры
16. Закон Дальтона
Если идеальный газ являетсясмесью нескольких газов, то
согласно закону Дальтона,
давление смеси идеальных газов
равно сумме парциальных
давлений входящих в нее газов.
ПАРЦИАЛЬНОЕ ДАВЛЕНИЕ –
это такое давление, которое
производил бы газ, если бы один
занимал весь объем, равный
объему смеси.







 Физика
Физика








