Похожие презентации:
Практикум по органической и биоорганической химии
1. Практикум по органической и биоорганической химии
Эшмаков Р.С.2. Качественные реакции в биохимии
Реакции на углеводы3. Качественная реакция на углеводы (и все прочие гликоли)
• Образование хелатных комплексов смедью-II в щелочной среде (растворение
осадка гидроксида и синее окрашивание)
• Специфическая качественная реакция на
крахмал – образование
внутрикомплексного соединения с йодом
4. Выявление восстанавливающих сахаров
• Альдозы при смешении с щелочнымраствором гидроксида меди-II дают желтый, а
затем оранжевый осадок (даже при стоянии
раствора гликолята):
R-CHO + Cu(OH)2 + OH- = RCOOH + Cu(OH) + H2O
2 CuOH = Cu2O + H2O
• Кетозы дают эту же реакцию при кипячении, а
поли- и олигосахариды эту реакцию не дают.
5. Гидролиз олиго- и полисахараидов
• Сахароза и крахмал в кислой средерасщепляются при нагревании до мономеров.
(C6H10O5)n + H2O H+ n C6H12O6
C12H22O11 + H2O = 2 C6H12O6
• Доказательством наличия
восстанавливающего сахара (глюкозы) в
составе крахмала и сахарозы служит
окислительно-восстановительная реакция с
гидроксидом меди-II.
6. Качественные реакции в биохимии
Реакции на белки7. Биуретовая реакция (на амидные группы)
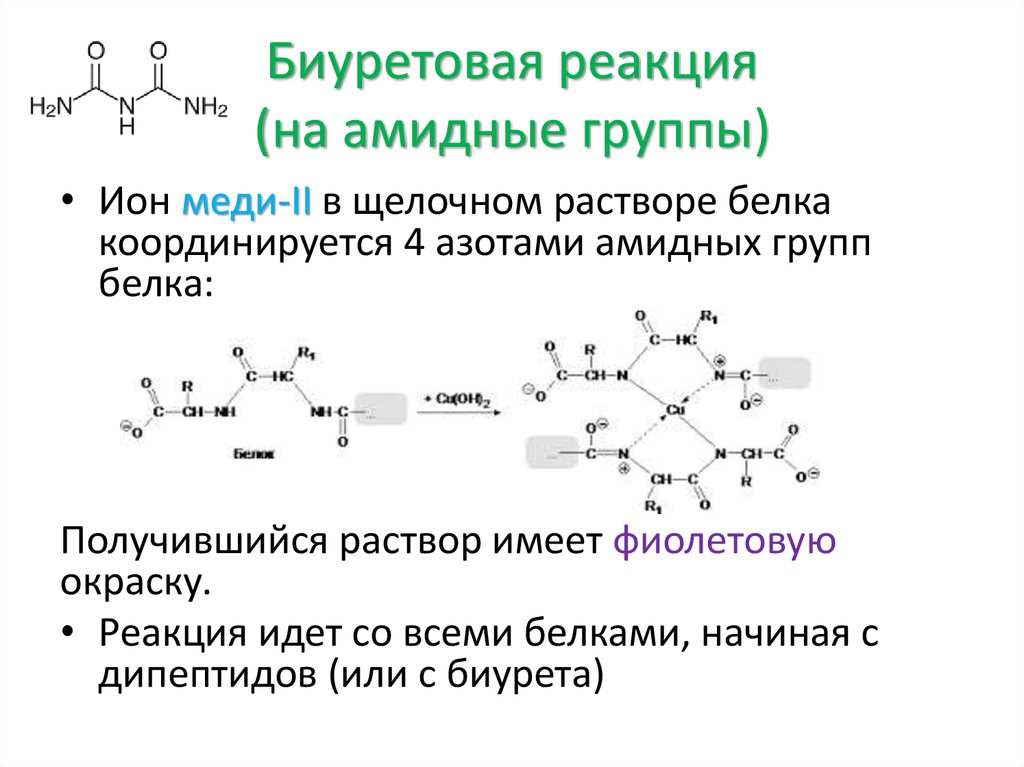
• Ион меди-II в щелочном растворе белкакоординируется 4 азотами амидных групп
белка:
Получившийся раствор имеет фиолетовую
окраску.
• Реакция идет со всеми белками, начиная с
дипептидов (или с биурета)
8. Ксантопротеиновая реакция (на ароматические белки)
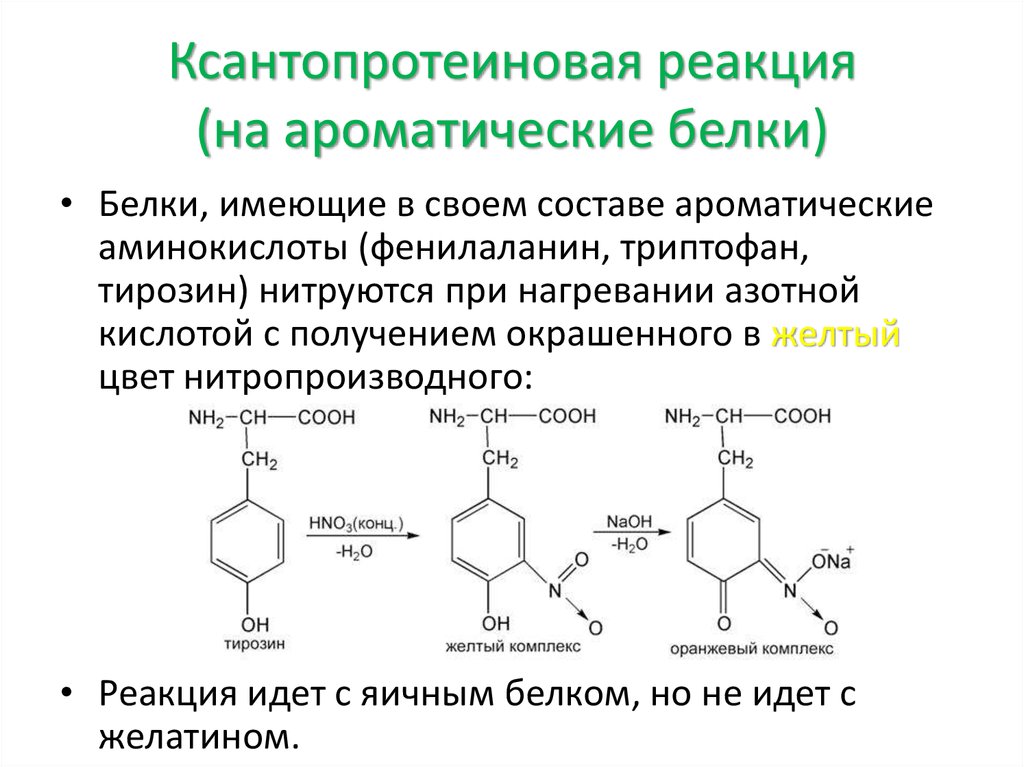
• Белки, имеющие в своем составе ароматическиеаминокислоты (фенилаланин, триптофан,
тирозин) нитруются при нагревании азотной
кислотой с получением окрашенного в желтый
цвет нитропроизводного:
• Реакция идет с яичным белком, но не идет с
желатином.
9. Выявление серосодержащих белков
• Белки, в состав которых входятсеросодержащие аминокислоты (цистеин,
метионин), при взаимодействии с щелочным
раствором гидроксида свинца образуют
сульфид свинца бурого цвета при нагревании:
(CH3COO)2Pb + 4 NaOH = CH3COONa + Na2[Pb(OH)4]
Na2S + Na2[Pb(OH)4] = 4 NaOH + PbS
10. Осаждение белка
Белки осаждаются без денатурации в разныхусловиях:
• При нагревании белка вблизи
изоэлектрической точки;
• При добавлении сильных кислот;
• При добавлении сильного электролита
(соли) до насыщения (альбумины) или
полунасыщения (глобулины).
11. Качественные реакции в органической химии
Различение органических кислот12. Различение органических кислот, дающих нерастворимые осадки
• Некоторые анионы органических кислоты способныдавать нерастворимые осадки с ионами металлов
группы кальция (или с медью-II):
2NaOH + H2C2O4 = Na2C2O4 + 2H2O
BaCl2 + Na2C2O4 = BaC2O4 + 2NaCl
**Чистая щавелевая кислота - твердая
***Оксалат кальция ответственен за образование
камней в почках и т.д.
13. Окисление органических кислот гидроксидом меди-II
• Муравьиная кислота является не толькокислотой, но и альдегидом. Потому ей тоже
свойственна реакция «медного зеркала»:
HCOOH + NaOH = HCOONa + H2O
2 HCOONa + 4 Cu(OH)2 = Na2CO3 + 4 CuOH + CO2 + 3 H2O
2 CuOH = Cu2O + H2O
**Муравьиная кислота так сильно пахнет, что ее часто проще
отличить по запаху
***Однако все же большинство кислот каких-то специфических
реакций не имеют
14. Качественные реакции в органической химии
Проба на фенолы15. Бромирование фенолов
• Растворы фенолов реагируют с бромной водой собразованием малорастворимых производных. В
случае с фенолом это белый трибромфенол, в случае же
с гидрохиноном это тетрабромгидрохинон – игольчатые
кристаллы цвета потемневшей латуни.
**Самый обычный фенол проще определить по запаху –
он пахнет гуашью (точнее, наоборот – гуашь пахнет
фенолом)
***Обычно для реакции требуются весьма
концентрированные растворы, иной раз раствор стоит
подогреть
16. Образование фенолятов железа
• Практически все фенолы способны даватьсильно окрашенные соединения с ионами
железа-III:
Fe3+ + 6 C6H5OH = [Fe(C6H5OH)6]3+
Простейшие фенолы дают темно-фиолетовую
окраску, а сложные (танины, например) – почти
черную.
***На этом основан один из опытов с
получением «невидимых чернил»














 Химия
Химия








