Похожие презентации:
Физико-химические свойства лекарственных препаратов железа
1. ГБОУ ВПО Уральский Государственный Медицинский Университет Министерства здравоохранения Российской Федерации Кафедра общей химии
Учебная научно-исследовательская работа студентов на тему:«ИССЛЕДОВАНИЕ ФИЗИКО – ХИМИЧЕСКИХ СВОЙСТВ
ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ ЖЕЛЕЗА.
СОРБИФЕР ДУРУЛЕС»
Состав группы: Боровикова И. А., Аввакумова А. М.,
Беззубенко С.В.
ОЛД-212
Научный руководитель: доцент, доктор технических наук,
кандидат химических наук Белоконова Н. А.
Екатеринбург
2016
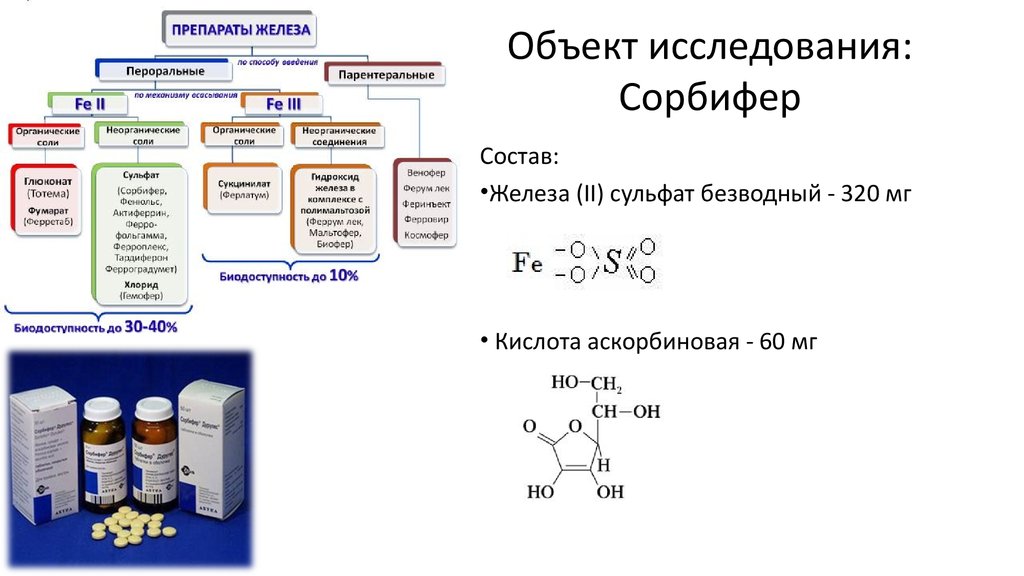
2. Объект исследования: Сорбифер
Состав:•Железа (II) сульфат безводный - 320 мг
• Кислота аскорбиновая - 60 мг
3.
Методы исследования:-Трилонометрический
-Кондуктометрия (кондуктометр АНИОН-7020)
-Потенциометрия (рН-150МИ)
-Спектрофотометрия (КФК-3 )
-Перманганатометрия
4. Приготовление водных растворов железа (III) и определение концентрации трилонолометрическим методом.
Погрешность измерения:Р1 = 10,6%
Р2 = 3,6%
РП = 16%
Большая погрешность в измерении концентрации железа в
растворе лекарственного препарата обусловлена
присутствием аскорбиновой кислоты, которая не позволила
до конца окислить железо персульфатом.
Окисление железа (II):
H2S2O8 + 2 FeSO4 = Fe2(SO4)3 + H2SO4
С6Н4(ОН) СООН + FeCl3 =>сине-фиолетовый комплекс
Комплекс Fe с
салициловой
кислотой
Трилон Б
№ пп
Наименова Va, мл V
Концентрация
ние пробы
трилон железа, мг/л
а, мл
Теорет. Экспер
им.
1
2
3
4
5
6
Р1
Р1
Р2
Р2
РП1
РП2
20
20
20
20
20
20
Комплекс трилона Б с Fe(III)
3,9
4
1,9
1,8
60
1,5
50
50
25
25
1000
25
54,6
56
26,6
25,2
840
21
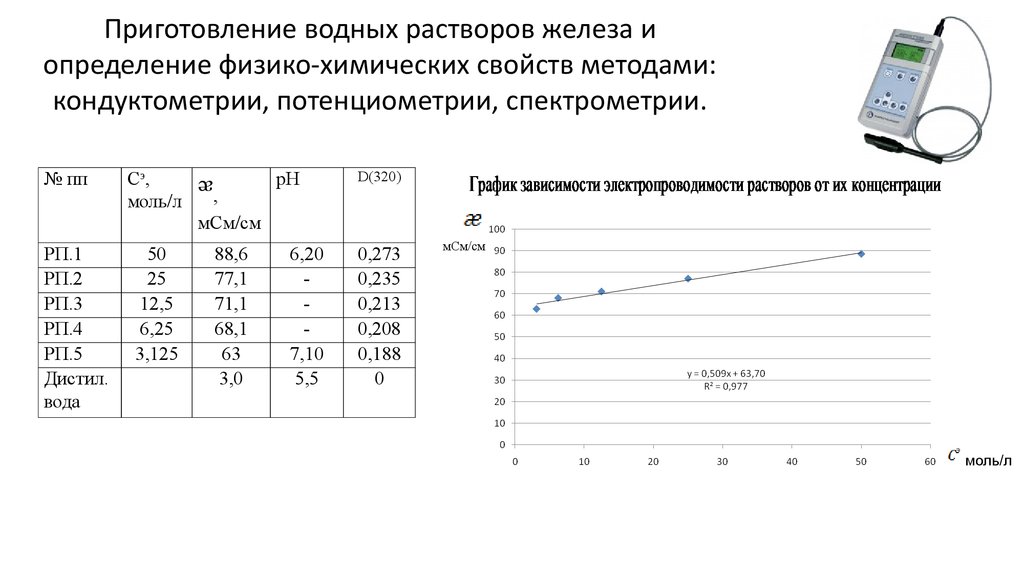
5. Приготовление водных растворов железа и определение физико-химических свойств методами: кондуктометрии, потенциометрии, спектрометрии.
№ ппCэ,
моль/л
ᵆ,
рН
D(320)
мСм/см
РП.1
РП.2
РП.3
РП.4
РП.5
Дистил.
вода
50
25
12,5
6,25
3,125
88,6
77,1
71,1
68,1
63
3,0
6,20
7,10
5,5
0,273
0,235
0,213
0,208
0,188
0
мСм/см
моль/л
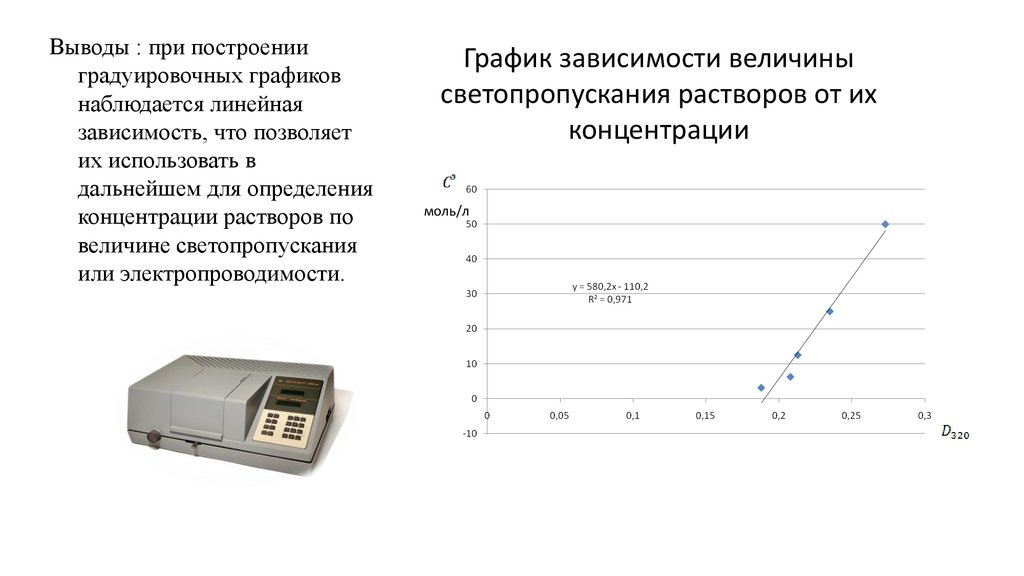
6. График зависимости величины светопропускания растворов от их концентрации
Выводы : при построенииградуировочных графиков
наблюдается линейная
зависимость, что позволяет
их использовать в
дальнейшем для определения
концентрации растворов по
величине светопропускания
или электропроводимости.
График зависимости величины
светопропускания растворов от их
концентрации
моль/л
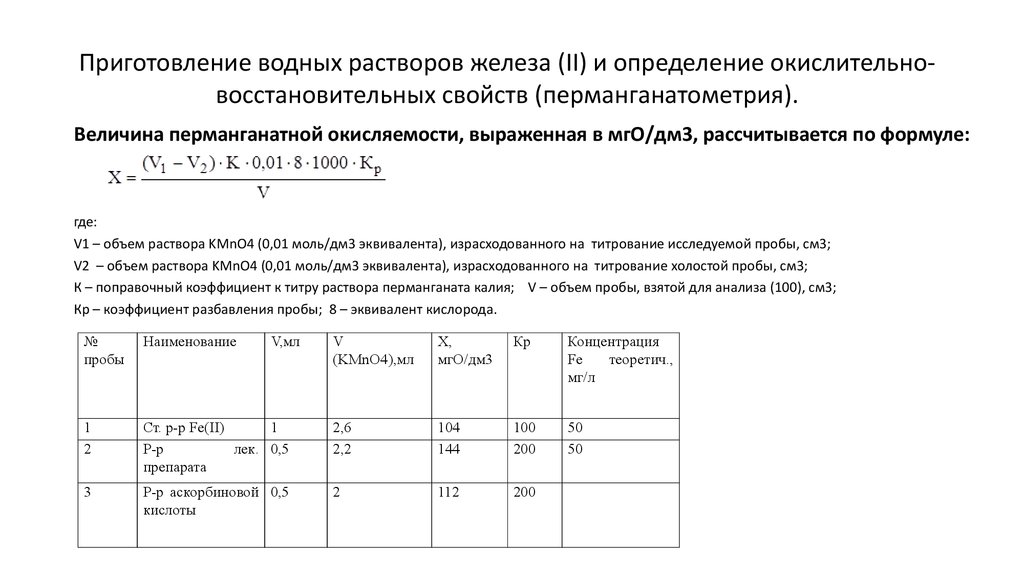
7. Приготовление водных растворов железа (II) и определение окислительно- восстановительных свойств (перманганатометрия).
Приготовление водных растворов железа (II) и определение окислительновосстановительных свойств (перманганатометрия).Величина перманганатной окисляемости, выраженная в мгО/дм3, рассчитывается по формуле:
где:
V1 – объем раствора KMnO4 (0,01 моль/дм3 эквивалента), израсходованного на титрование исследуемой пробы, см3;
V2 – объем раствора KMnO4 (0,01 моль/дм3 эквивалента), израсходованного на титрование холостой пробы, см3;
К – поправочный коэффициент к титру раствора перманганата калия; V – объем пробы, взятой для анализа (100), см3;
Кр – коэффициент разбавления пробы; 8 – эквивалент кислорода.
№
пробы
Наименование
1
2
3
V,мл
V
(KMnO4),мл
Х,
мгО/дм3
Кр
Концентрация
Fe
теоретич.,
мг/л
Ст. р-р Fe(II)
1
Р-р
лек. 0,5
препарата
2,6
2,2
104
144
100
200
50
50
Р-р аскорбиновой 0,5
кислоты
2
112
200
8. Выводы
Взаимодействие соли Мора с перманганатом калия:
10 FeSO4*(NH4)2SO4*6H2O + 2 KMnO4 + 8 H2SO4 = 5Fe2(SO4)3 + 2 MnSO4 + 10 (NH4)2SO4 + K2SO4 + 68 H2O
Удаление избытка перманганата калия щавелевой кислотой:
2MnO4- + 5C2O42- + 16H+ → 2Mn2+ + 10CO2 + 8H2O
При данной методике железо окисляется полностью, и более высокое значение окисляемости у раствора
лекарственного препарата (при той же концентрации – 50 мг/л) говорит о том, что вместе с железом
окислялась аскорбиновая кислота, которая при попадании препарата в ЖКТ предохраняет железо от
окисления и тем самым сохраняет его биодоступность.
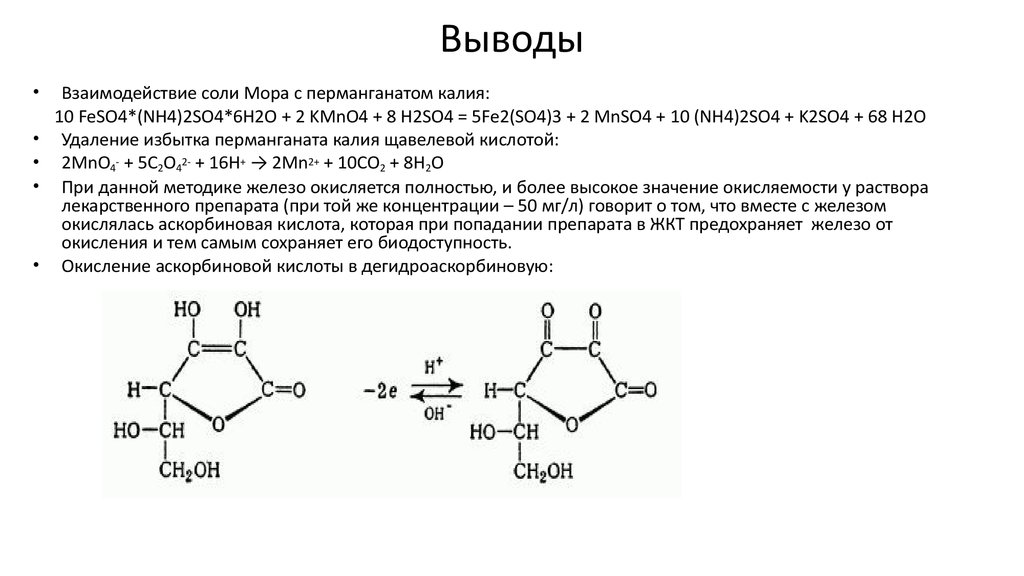
Окисление аскорбиновой кислоты в дегидроаскорбиновую:




 Медицина
Медицина Химия
Химия








