Похожие презентации:
Атом. Изотопы
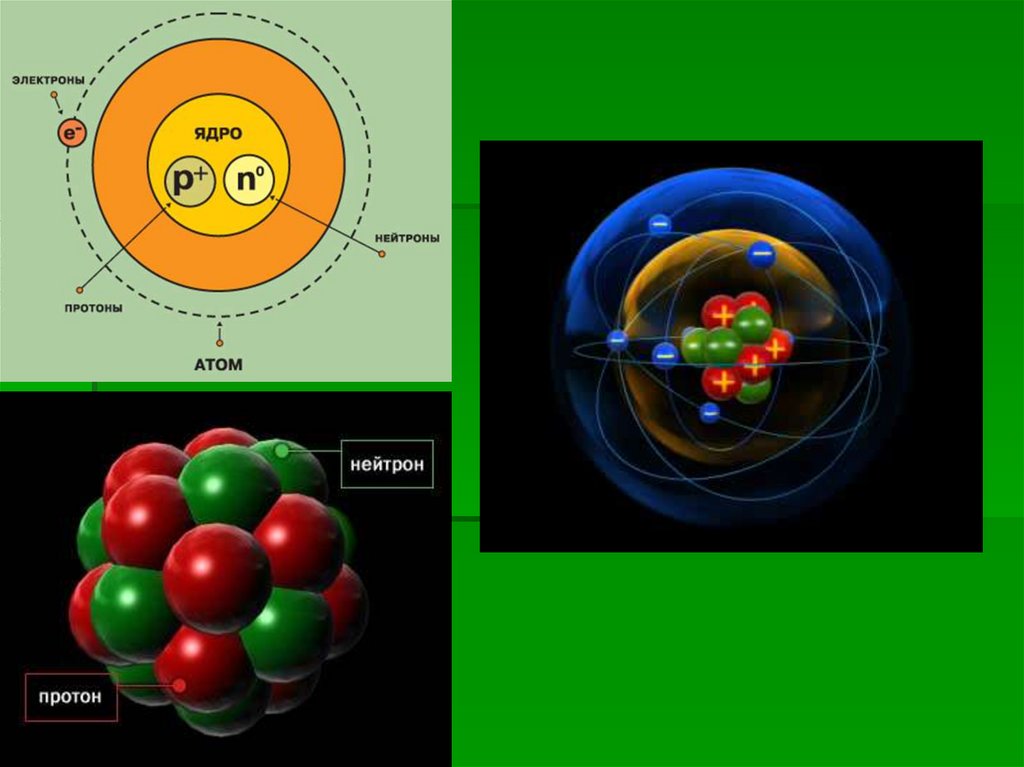
1. АТОМ.
ИЗОТОПЫ.2. Формулировка Периодического закона
Свойстваэлементов, а также
формы и свойства
их соединений
находятся в
периодической
зависимости от
величины их
атомных весов
3. Нарушение закономерности
Co – NiAr – K
Te - I
4. Важная закономерность ( на основании работ Генри Мозли – Англия,1914г.)
Порядковый номер элемента равензаряду ядра атома
№ - порядковый номер элемента
Z – заряд ядра атома
5.
6.
7.
8. В природе существуют атомы одного и того же элемента с различной массой(А) - изотопы
В природе существуют атомы одного и тогоже элемента с различной массой(А) изотопы
9. Вычисление атомной массы элемента
Ar (Cl) = 35 ∙ 0,75 + 37∙ 0,25=35,510.
11.
12. Запомнить!
Атомы одного элемента, имеющиеодинаковое число протонов, но
различное число нейтронов, называются
изотопами.
Изотопы имеют одинаковые химические
свойства, но немного различаются по
физическим свойствам, в частности по
весу.
Большинство элементов встречаются в
природе в виде нескольких изотопов.
13. Современная формулировка Периодического закона: «Свойства элементов, а также формы и свойства их соединений находятся в
периодическойзависимости от зарядов
ядер их атомов»












 Химия
Химия








