Похожие презентации:
Обезвреживание аммиака. Остаточный азот крови. Биохимия полости рта. Лекция 7
1. СЗГМУ им. И.И.МЕЧНИКОВА КАФЕДРА БИОЛОГИЧЕСКОЙ И ОБЩЕЙ ХИМИИ 2018 / 2019 уч. год БИОЛОГИЧЕСКАЯ ХИМИЯ - БИОХИМИЯ ПОЛОСТИ РТА
Раздел 4ЛК-7
ЛЕКЦИЯ
ОБЕЗВРЕЖИВАНИЕ АММИАКА.
ОСТАТОЧНЫЙ АЗОТ КРОВИ.
Доцент АНТОНОВА Ж.В.
2. ПЛАН ЛЕКЦИИ
I. Источники аммиака в клетках.II. Причины токсичности аммиака.
III. Первичное обезвреживание аммиака в тканях (образование амидов АК, восстановительное
аминирование, глюкозо-аланиновый цикл, биологическая роль) .
IV. Окончательное обезвреживание аммиака в почках (образование солей аммония, б/роль)
V. Окончательное обезвреживание аммиака в печени (орнитиновый цикл, б/ роль).
VI. Нарушения работы орнитинового цикла.
VII. Приложение. Взаимосвязь работы орнитинового цикла с ЦТК.
VIII. Понятие остаточного азота крови. Азотемия
ЛК-7
IX. Изменения содержания мочевины в крови /моче и аммонийных солей в моче (таблица).
X. Изменения содержания компонентов остаточного азота в крови (таблица).
XI. Список литературы.
3. I. Источники аммиака в клетках
клетках1) дезаминирование АК
в различных органах и тканях
2) дезаминирование
биогенных аминов под действием МАО
3) дезаминирование пуриновых и пиримидиновых
оснований
4) гниение АК в кишечнике под действием ферментов м.
о.
Рис.1
В крови и цитозоле клеток при физиологических
+
значениях рН:
Н+
NH3
1%)
NН4
(99%),
NH3 (~
4. II. Причины токсичности аммиака:
аммиака:1. Высокое содержание NH3 в тканях
количество
α-кетоглутарата (α-КГ), т. к. он связывает избыток
NH3, превращаясь в ГЛУ, при участии
глутаматдегидрогеназы.
Это нарушает обмен АК (трансаминирование)
и
ЛК-7
ход ЦТК (гипоэнергетическое
состояние).
2. Избыток NH3
синтез глутамина из Глу в
нервной ткани при участии
5. II. Причины токсичности аммиака
аммиака3.
[ ГЛУ ] снижает синтез ГАМК, нарушается
проведение нервного импульса, повышается нервномышечная возбудимость, возникают судороги.
4. NH4+ нарушает трансмембранный перенос Nа+ и
К+, он конкурирует с ними за ионные каналы, что влияет
на проведение нервных импульсов.
5.
NH4+ сдвигает рН крови в щелочную сторону
( NH4OH),
ЛК-7
вызывает алколоз. Это
кислороду, он
сродство Hb к
плохо отдает его тканям, что приводит к гипоксии
и гипоэнергетическому состоянию, отчего страдает
6. III. ПЕРВИЧНОЕ ОБЕЗВРЕЖИВАНИЕ АММИАКА В ТКАНЯХ:
1) ОБРАЗОВАНИЕ АМИДОВ АК:а) образование ГЛУТАМИНА (митохондрии) - основной путь
первичного
обезвреживания NH3 во всех тканях (особ в
нервной). ГЛН с током крови идет в печень и почки.
COOH
Рис.
2
ÑÍ
2
ÑÍ
2
ÑÍ
NH3
CO NH2
ÀÒÔ
ãëóò àì èí ñèí ò åò àçà
NH2
Mg
2+
ÀÄÔ + Ði
ÑÍ
2
ÑÍ
2
ÑÍ
NH2
COOH
COOH
ãëóòàì àò
ãëóòàì èí
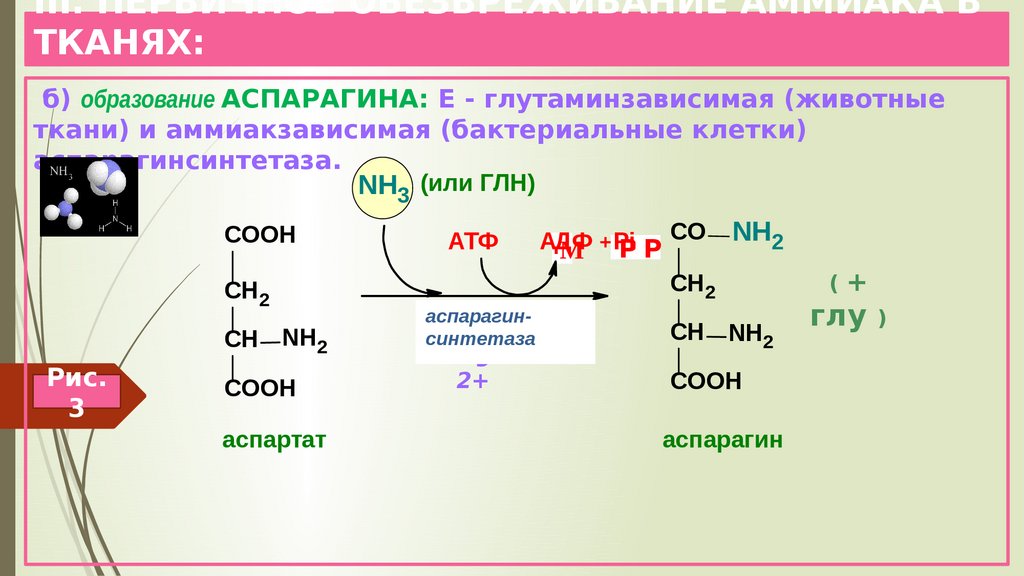
7. III. ПЕРВИЧНОЕ ОБЕЗВРЕЖИВАНИЕ АММИАКА В ТКАНЯХ:
б) образование АСПАРАГИНА: Е - глутаминзависимая (животныеткани) и аммиакзависимая (бактериальные клетки)
аспарагинсинтетаза.
NH3 (или ГЛН)
COOH
СН2
СН NH2
Рис.
3
COOH
аспартат
АТФ
глутаминаспарагинсинтетаза
синтетаза
Mg
2+
CO
+
АДФ
Рi
М РР
NH2
СН2
СН NH2
COOH
аспарагин
(
+
глу
)
8. III. ПЕРВИЧНОЕ ОБЕЗВРЕЖИВАНИЕ АММИАКА В ТКАНЯХ:
2) ВОССТАНОВИТЕЛЬНОЕ АМИНИРОВАНИЕ (мозг и др.ткани):
α-КГ + NH3 + НАДФН
ГЛУ
Гл ДГ
глутаминсинтетезы
ГЛН
ГЛУ + НАДФ+
(Рис.2)
Роль реакций :
СВЯЗЫВАНИЕ ТОКСИЧНОГО NH3 в тканях
ОБРАЗОВАНИЕ ЗАМЕНИМЫХ АК (ГЛУ, ГЛН и АСН)
ЛК ОБРАЗОВАНИЕ ТРАНСПОРТНЫХ ФОРМ NH3 в крови (ГЛН и
7
АСН)
(растворимых и нетоксичных)
ГЛН и АСН – источники азота в анаболических реакциях
3) ВЫВЕДЕНИЕ NH3 ИЗ МЫШЦ в виде АЛА:
9. III. 3). Глюкозоаланиновый цикл
МЫШЦα-КК
αКГ
ГЛИКОЛ
ИЗ
АМИНОКИСЛОТ
Ы
2
NH3
КРОВЬ
ГЛЮКОЗ
А
3,35,5
ММОЛЬ/
Л
3
ГЛУТАМ
АТ
αКГ
4
АЛАНИ
Н
ГЛЮКОЗ
А
АЛАНИН
МОЧЕВИ
НА
NH
3
6
ПИРУВ
АТ
ПИРУВ
АТ
АЛТ
(ПФ)
ПЕЧЕ
НЬ
ГЛЮКОНЕОГЕ
НЕЗ
Интенсивная
Аработа
БЕЛОК
ГЛЮКОЗ
МЫШЦ
А
1
ЦИКЛ
МОЧЕВИН
Ы
Рис.
4
АЛТ
(ПФ)
АЛАНИ
Н
5
ГЛУТАМ
АТ
αКГ
10. III. 3). Глюкозоаланиновый цикл
1. Распад белков мышц/интенсивная мышечная работа2. Дезаминирование АК/энергия
3. Восстановительное аминирование (ГлДГ, НАДФН+Н+)/первичное
обезвреживание.
4. Трансаминирование
αПВК и ГЛУ (АЛТ,ПФ)
КГ
5. Трансаминирование Ала и
(АЛТ,ПФ)
6. Дезаминирование Глу (ГлДГ, НАД+)
ЛК-7
Гликолиз- анаэробное дихотомическое окисление Глюкозы (2 АТФ)
Глюконеогенез-синтез глюкозы из неуглеводных
веществ/печень, почки
БИОЛОГИЧЕСКАЯ РОЛЬ:
1. Из мышц выводится аммиак и пируват в виде аланина, к-й
поступает в печень;
2. В печени из аланина образуется глюкоза, которая поддерживает
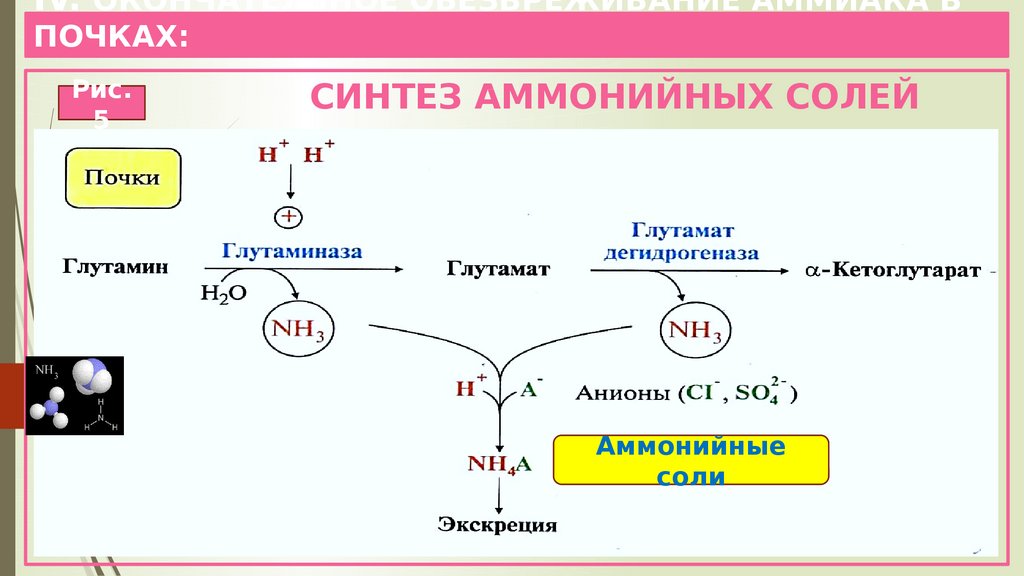
11. IV. ОКОНЧАТЕЛЬНОЕ ОБЕЗВРЕЖИВАНИЕ АММИАКА В ПОЧКАХ:
Рис.5
СИНТЕЗ АММОНИЙНЫХ СОЛЕЙ
Аммонийные
соли
12. IV. ОКОНЧАТЕЛЬНОЕ ОБЕЗВРЕЖИВАНИЕ АММИАКА В ПОЧКАХ:
РОЛЬ ОБРАЗОВАНИЯ СОЛЕЙ АММОНИЯ:в виде СОЛЕЙ АММОНИЯ с мочой удаляется токсичный аммиак;
это один из механизмов поддержания кислотно-основного
равновесия в организме;
выводится избыток анионов кислот без потери катионов Na+,
K+ и др.;
ЛК-7
В ПЕЧЕНИ ГЛН И АСН гидролитически
дезаминируются:
Глн + Н2О
глутаминаза
Глу + NH3
Асн + Н2О аспарагиназа
Асп + NH3
NH3 идет в орнитиновый цикл
13. V. ОКОНЧАТЕЛЬНОЕ ОБЕЗВРЕЖИВАНИЕ АММИАКА В ПЕЧЕНИ:
ОРНИТИНОВЫЙ ЦИКЛ МОЧЕВИНООБРАЗОВАНИЯ (ОЦ)КРЕБСА-ГЕНЗЕЛАЙТА
1) В матриксе митохондрий: NH3 (из дезаминирования) и НСО3- (из
ЦТК) и 2АТФ (из ЦТК) образуют карбамоилфосфат:
2 ÀÒÔ
NH3 + ÑÎ
Рис.
6
2+
Í 2Î
2 ÀÄÔ + Pi
êàðáàì î èëô î ñô àò ñèí ò åò àçà I
2+
Ì g
NH2
Ñ O
O ~ PO3H2
êàðáàì î èëô î ñô àò
14. ОРНИТИНОВЫЙ ЦИКЛ МОЧЕВИНООБРАЗОВАНИЯ
2) Карбамоильный остаток переносится на орнитин собразованием
цитруллина (α-АК), к-й затем переходит в
цитоплазму.
Í 3ÐÎ
NH2
NH2
Рис.
7
4
(ÑÍ 2)3
Ñ O
ÑÍ
O ~ PO3H2
COOH
êàðáàì î èëô î ñô àò
NH2
NH2
î ðí èòèí
î ðí èò èí êàðáàì î èë
ò ðàí ñô åðàçà
Ñ O
NH
(ÑÍ 2)3
ÑÍ
NH2
COOH
öèòðóëëèí
15. ОРНИТИНОВЫЙ ЦИКЛ МОЧЕВИНООБРАЗОВАНИЯ
3) В цитоплазме: 2-я аминогруппа для мочевины идет отаспартата,
к-й реагирует
с цитруллином, образуя
COOH
NH2
NH
COOH
2
аргининосукцинат
ÀÒÔ
ÀÌ Ô + ÐP
Ñ O
+
NH
(ÑÍ 2)3
Рис.
8
ÑÍ
i
H2N ÑÍ
ÑÍ
2
COOH
NН ÑÍ
HN
ÑÍ
(ÑÍ 2)3
ÑÍ
NH2
2
COOH
NH2
COOH
COOH
öèòðóëëèí
àðãèí èí î ñóêöèí àò ñèí ò åò àçà
Mg 2+
Ñ
àñï àðòàò
àðãèí èí î ñóêöèí àò
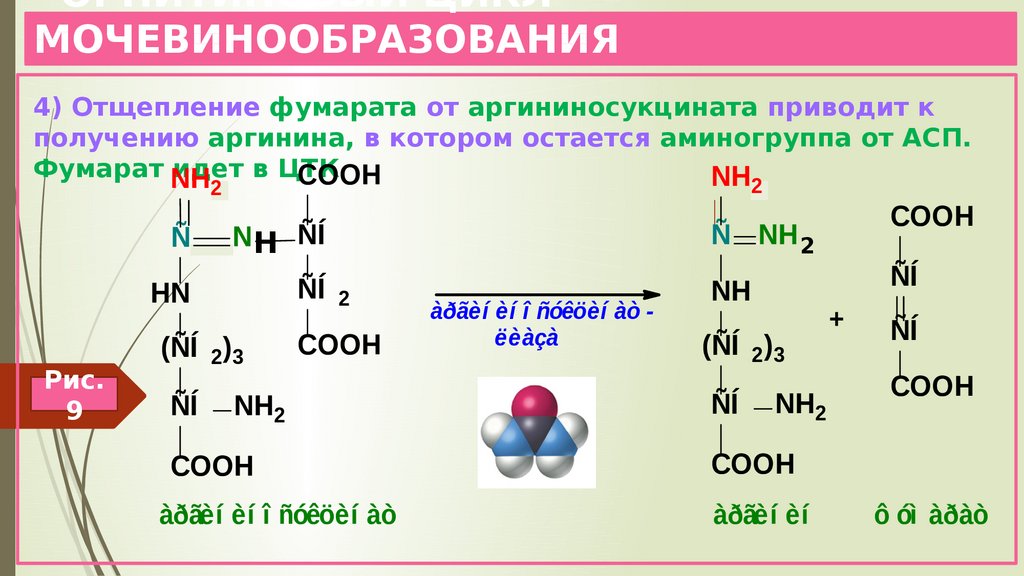
16. ОРНИТИНОВЫЙ ЦИКЛ МОЧЕВИНООБРАЗОВАНИЯ
4) Отщепление фумарата от аргининосукцината приводит кполучению аргинина, в котором остается аминогруппа от АСП.
Фумарат NH
идет в ЦТК
COOH
NH
2
2
Рис.
9
Ñ
NН ÑÍ
HN
ÑÍ
(ÑÍ 2)3
ÑÍ
COOH
Ñ NH 2
2
COOH
NH2
COOH
àðãèí èí î ñóêöèí àò
àðãèí èí î ñóêöèí àò ëèàçà
ÑÍ
NH
(ÑÍ 2)3
ÑÍ
NH2
+
ÑÍ
COOH
COOH
àðãèí èí
ô óì àðàò
17. ОРНИТИНОВЫЙ ЦИКЛ МОЧЕВИНООБРАЗОВАНИЯ
5) Гидролиз аргинина дает орнитин, к-й возвращается вмитохондрию и вновь включается в цикл, и мочевину, к-я
поступает NH
в кровь.
2
Ñ NH2
NH
(ÑÍ 2)3
Рис.1
0
ÑÍ
NH2
COOH
àðãèí èí
Í 2Î
àðãèí àçà
Сa 2+ или Mn
2+
NH2
(ÑÍ 2)3
ÑÍ
NH2
COOH
î ðí èòèí
NH2
+
Ñ O
NH2
ì î ÷åâèí à
18. VI. Б/РОЛЬ и нарушения работы ОЦ
1) РОЛЬ ОЦ:Синтез мочевины - окончательное обезвреживание аммиака
Синтез аргинина и пополнение его фонда в организме (роль АРГ
самост.)
2) РЕГУЛЯЦИЯ ОЦ (самост.); 3) ВЗАИМОСВЯЗЬ ОЦ и ЦТК (VII.Прилож.
Рис.11)
Гипераммониемия
(повышение содержания аммиака в крови)
ЛК-7
ПРИЧИНЫ:
заболевания печени (гепатит, цирроз);
наследственные дефекты ферментов ОЦ приводят к
Гипераммониемии I и II типа, Цитруллинемии,
Аргиносукцинатурии, Гипераргининемии.
19. VII. Приложение. Взаимосвязь орнитинового цикла (ОЦ) и ЦТК
Компенсация энергозатрат в ОЦ и регенерация АСП дляфумара
фумара
ОЦ
ЦТК
т
т
:
малат
орнитиновый цикл
нАд+
3АТФ
ЦПЭ
ЦТК
Рис.1
1
ПВК
нАДН+Н+
ТРАНСАМИНИРОВАН
ИЕ
оксалоацетат
АСП
Глу
α-КГ
Ала 3АТФ, затраченных на синтез 1 мол.
1. При включении ФУМАРАТА в ЦТК компенсируется
мочевины в ОЦ; 2. Из ФУМАРАТА орнитинового цикла за счет 2-х реакций ЦТК образуется
оксалоацет, к-й превращаясь в АСП (трансаминирование), идет в ОЦ. Это цикл
регенерации аспартата из фумарата.
20. VIII. Остаточный АЗОТ крови / АЗОТемия
1. Из крови мочевина поступает в почки и выводится смочой
2. «Остаточный (небелковый) азот» крови –это суммарное
содержание низкомолекулярных азотистых веществ,
которые
остаются в фильтрате после осаждения белков.
3. Компоненты остаточного азота (ОА): мочевина
(~50%),
мочевая кислота, креатин, креатинин,
ЛК-7
аминокислоты,
индикан, гиппуровая кислота, билирубин и др.
(происхождение, причины
и
в крови – см. п. X).
4. Повышение уровня остаточного азота в крови –
азотемия
21. VIII. АЗОТЕМИЯ
АЗОТЕМИЯПРОДУКЦИОННАЯ
увеличение образования
компонентов ОА
РЕТЕНЦИОННАЯ
снижение выведения
компонентов ОА с мочой
ЛК-7
ПОЧЕЧНАЯ
связана с нарушением
экскреторной функции при
патологии почек (ОПН, ХПН)
ВНЕПОЧЕЧНАЯ
связана со снижением
почечного кровотока, АД,
наруш. кровообращ. и др.
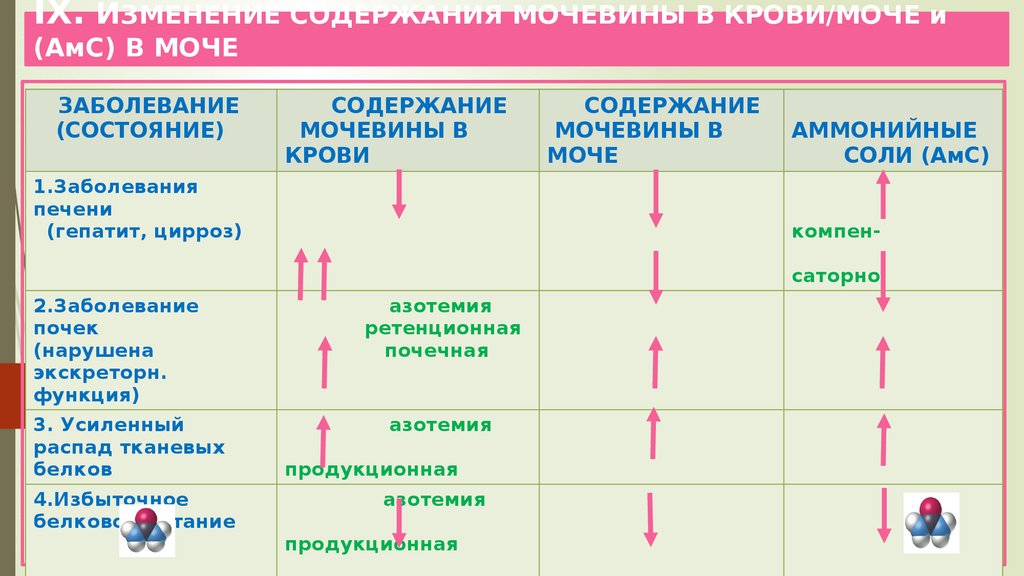
22. IX. ИЗМЕНЕНИЕ СОДЕРЖАНИЯ МОЧЕВИНЫ В КРОВИ/МОЧЕ и (АмС) В МОЧЕ
ЗАБОЛЕВАНИЕ(СОСТОЯНИЕ)
СОДЕРЖАНИЕ
МОЧЕВИНЫ В
КРОВИ
1.Заболевания
печени
(гепатит, цирроз)
СОДЕРЖАНИЕ
МОЧЕВИНЫ В
МОЧЕ
АММОНИЙНЫЕ
СОЛИ (АмС)
компенсаторно
2.Заболевание
почек
(нарушена
экскреторн.
функция)
3. Усиленный
распад тканевых
белков
4.Избыточное
белковое питание
азотемия
ретенционная
почечная
азотемия
продукционная
азотемия
продукционная
23. X. ИЗМЕНЕНИЕ СОДЕРЖАНИЯ КОМПОНЕНТОВ ОА В КРОВИ
КомпонентПроисхождение
МОЧЕВИНА
• Образуется в печени
в орнитиновом цикле
МОЧЕВАЯ
КИСЛОТА
• Распад пуринов в
печени и слизистой
оболочке кишечника
АМИНОКИСЛО
ТЫ
• Из белков тканей
• Из белков пищи
• Биосинтез
заменимых АК
КРЕАТИН
• Синтезируется в
Причины
крови
в
• Распад белков
тканей
• Заболевание почек
• Избыточное
белковое питание
• Заболевание почек
• Падагра
• Избыточное
белковое питание
• Распад белков
тканей
• Заболевание печени
• Наследственные
заболевания обмена
отдельных АК
(фенилкетонурия и
др.)
• Заболевания мышц
Причины
крови
• Заболевание
печени
• Белковое
голодание
• Белковое
голодание
• Белковое
голодание
• Заболевания
почек
(нарушение
реабсорбции)
• Нарушение
в
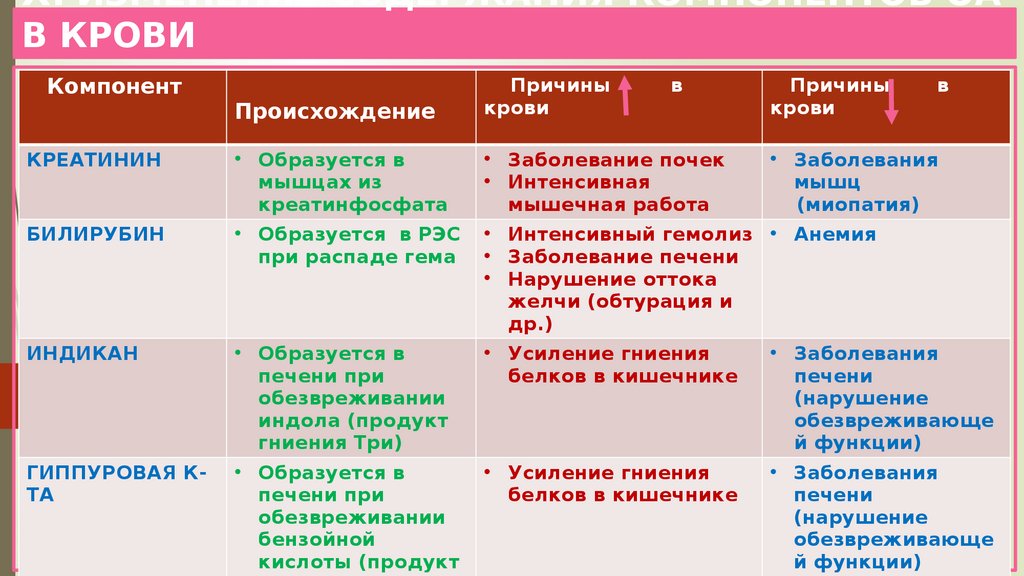
24. X. ИЗМЕНЕНИЕ СОДЕРЖАНИЯ КОМПОНЕНТОВ ОА В КРОВИ
КомпонентПроисхождение
КРЕАТИНИН
БИЛИРУБИН
ИНДИКАН
ГИППУРОВАЯ КТА
• Образуется в
мышцах из
креатинфосфата
• Образуется в РЭС
при распаде гема
• Образуется в
печени при
обезвреживании
индола (продукт
гниения Три)
• Образуется в
печени при
обезвреживании
бензойной
кислоты (продукт
Причины
крови
в
Причины
крови
в
• Заболевание почек
• Заболевания
• Интенсивная
мышц
мышечная работа
(миопатия)
• Интенсивный гемолиз • Анемия
• Заболевание печени
• Нарушение оттока
желчи (обтурация и
др.)
• Усиление гниения
• Заболевания
белков в кишечнике
печени
(нарушение
обезвреживающе
й функции)
• Усиление гниения
• Заболевания
белков в кишечнике
печени
(нарушение
обезвреживающе
й функции)
25. БЛАГОДАРЮ ЗА ВНИМАНИЕ !
ЛК-726. XI. СПИСОК ЛИТЕРАТУРЫ
Основная литература1. Биохимия: учебник/ под ред. Е.С. Северина.- М.: ГЭОТАР- Медиа, 2011. - 759 с.: ил. (2006 779 с.: ил.,) (Раздел.9,п.V)
2. Биохимия [Электронный ресурс] : учебник / под ред. Е. С. Северина. - 5-е изд., испр. и доп. М. : ГЭОТАРМедиа, 2015. - http://www.studmedlib.ru / book / ISBN9785970433126.html
(Раздел.9,п.V)
3. Биологическая химия. Биохимия полости рта: учебник / Т.П. Вавилова, А.Е. Медведев. - М.:
ГЭОТАР-Медиа, 2014. - 560 с.: ил. (стр.350-355)
4. Биологическая химия. Биохимия полости рта [Электронный ресурс] : учебник / Т.П. Вавилова,
А.Е.Медведев - М. : ГЭОТАР-Медиа, 2014. - http://www.studmedlib.ru / book /
ISBN9785970430392.html (Часть 5, Гл.16, п. Обезвреживание аммиака).
ЛК-7
Дополнительная литература
1. Биологическая химия: учебник. Т.Т. Березов, Б.Ф. Коровкин. – 3-е изд.,
перераб. и доп.– М.: Медицина, 1998. – 704 с.: ил. (стр.446-451)





















 Медицина
Медицина Биология
Биология








