Похожие презентации:
Атомный и ионный радиусы. Принципы шаровых упаковок
1. Атомный и ионный радиусы. Принципы шаровых упаковок.
2. Атомный и ионный радиусы
• Половину кратчайшего расстояния между атомами металлапринимают за соответствующий атомный радиус.
• Ионный радиус - половина расстояния между двумя
соответствующими анионами.
[3]
3. Атомный и ионный радиусы
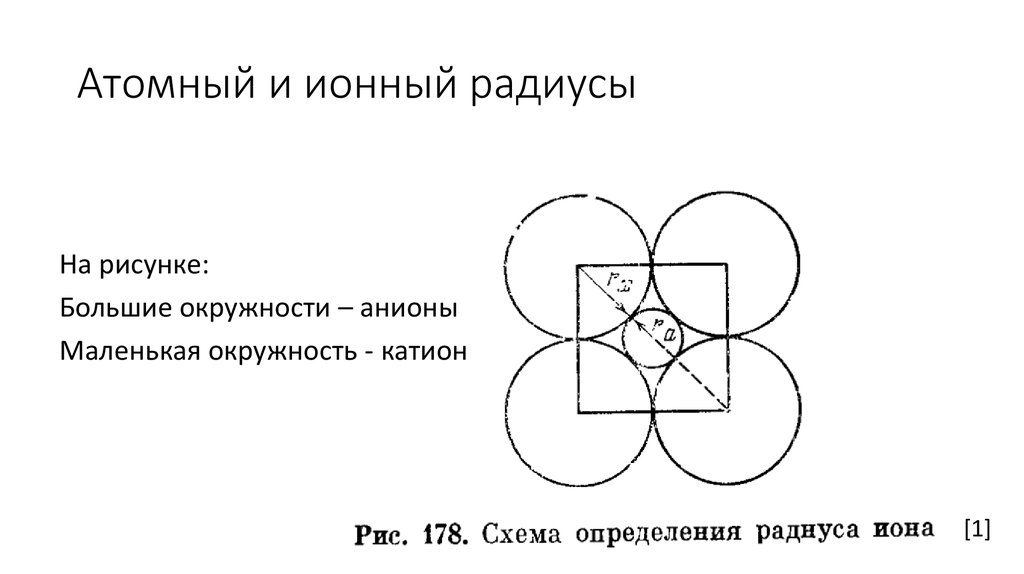
На рисунке:Большие окружности – анионы
Маленькая окружность - катион
[1]
4.
[1]5.
[1]6. Плотнейшие шаровые упаковки
Основные принципы:• 1. Пусть форма всех атомов и
ионов сферическая
• 2. Пусть весь объем кристалла
или отдельных его
структурных блоков заполнен
плотно соприкасающимися
атомами и ионами.
[1]
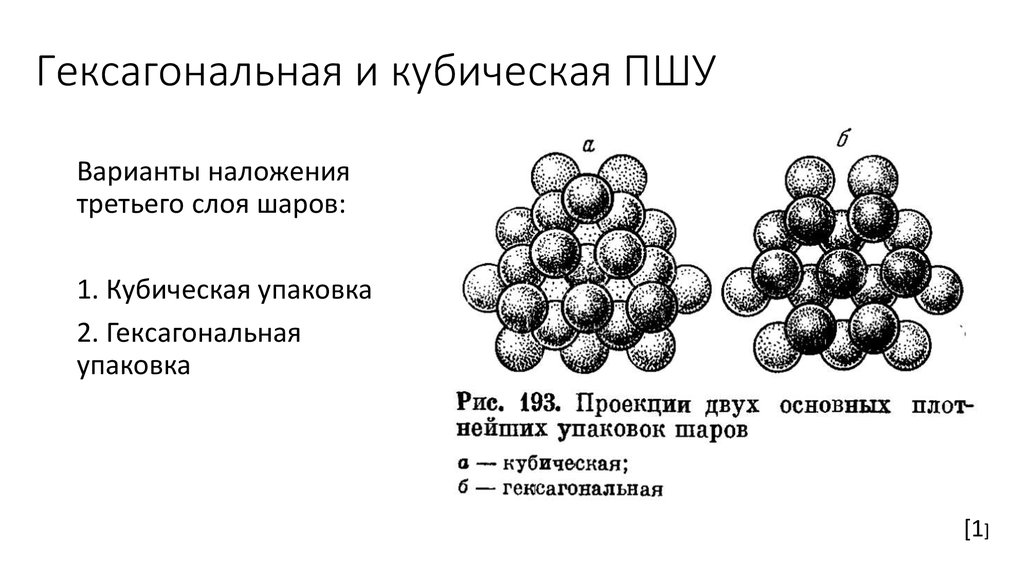
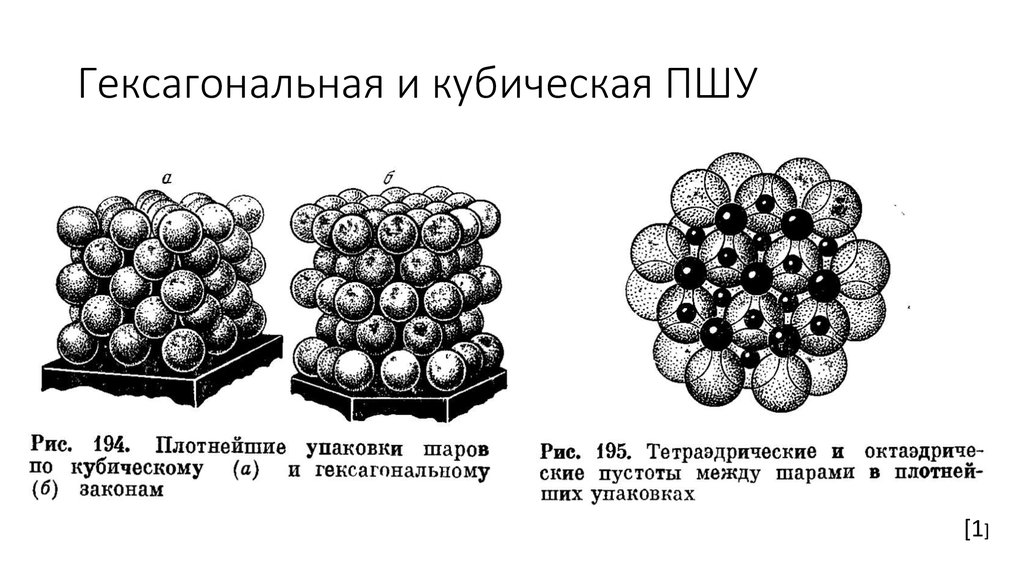
7. Гексагональная и кубическая ПШУ
Варианты наложениятретьего слоя шаров:
1. Кубическая упаковка
2. Гексагональная
упаковка
[1]
8. Гексагональная и кубическая ПШУ
[1]9. Способы обозначения ПШУ
Обозначим разные слои разнымибуквами, повторяющиеся –
одинаковыми:
• Гексагональная упаковка – … АВ
АВ АВ … - двуслойная
• Кубическая упаковка - … АВС АВС
АВС … - трехслойная
[1]
10. Список литературы:
1. Бокий Г.Б. – Кристаллохимия, 1971.2. Урусов В.С. – Теоретическая кристаллохимия
3. Кребс Г. – Основы кристаллохимии неорганических соединений





 Химия
Химия








