Похожие презентации:
Непредельные углеводороды. Алкены
1.
Государственное бюджетное профессиональноеобразовательное учреждение города Москвы
«Колледж сферы услуг № 32»
Преподаватель химии:
Семенова Елена Борисовна
1
2.
1. Понятие о непредельных углеводородах.2. Гомологический ряд алкенов.
3. Изомерия и номенклатура алкенов.
4. Получение алкенов.
5. Физические свойства.
6. Химические свойства алкенов.
7. Применение алкенов
3.
Непредельные углеводороды – этоуглеводороды, в молекулах которых между
атомами углерода наряду с одинарными
связями имеются кратные связи.
В молекулах непредельных у/в число атомов
водорода меньше, чем в молекулах
соответсвующих алканов, поэтому их называют
ненасыщенными.
Пример: Алкены, алкадиены,
алкины и др.
4.
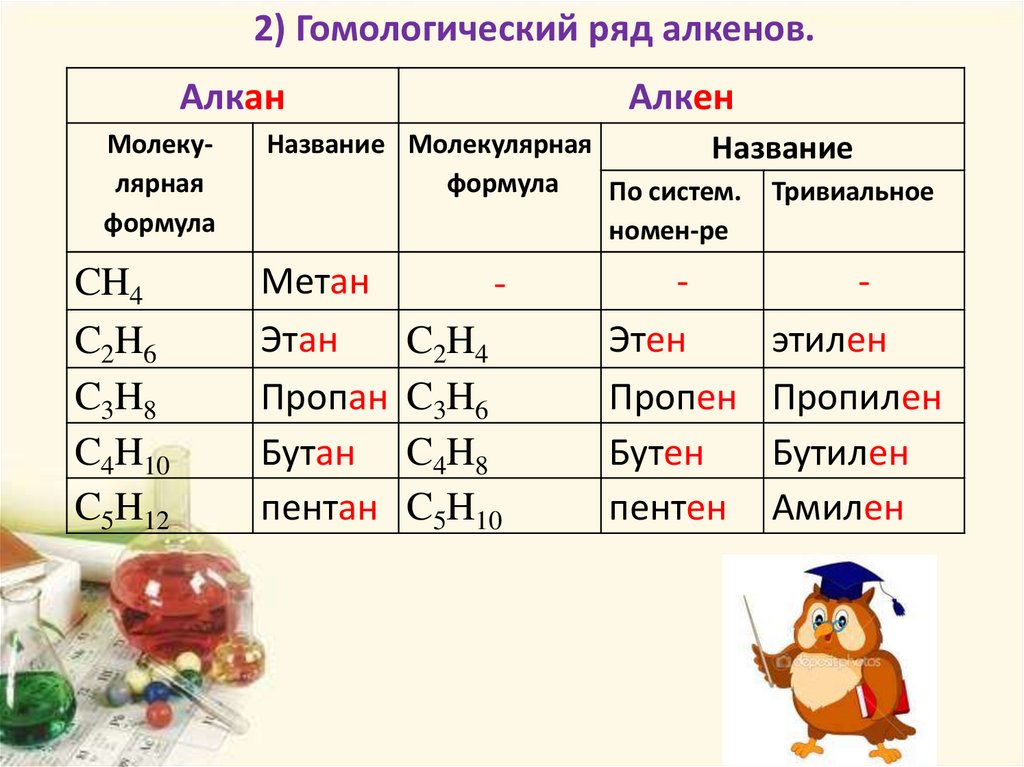
2) Гомологический ряд алкенов.Алкан
Молекулярная
формула
CH4
C2H6
C3H8
C4H10
C5H12
Алкен
Название Молекулярная
Название
формула
По систем. Тривиальное
номен-ре
Метан
Этан
Пропан
Бутан
пентан
-
C2H4
C3H6
C4H8
C5H10
Этен
Пропен
Бутен
пентен
этилен
Пропилен
Бутилен
Амилен
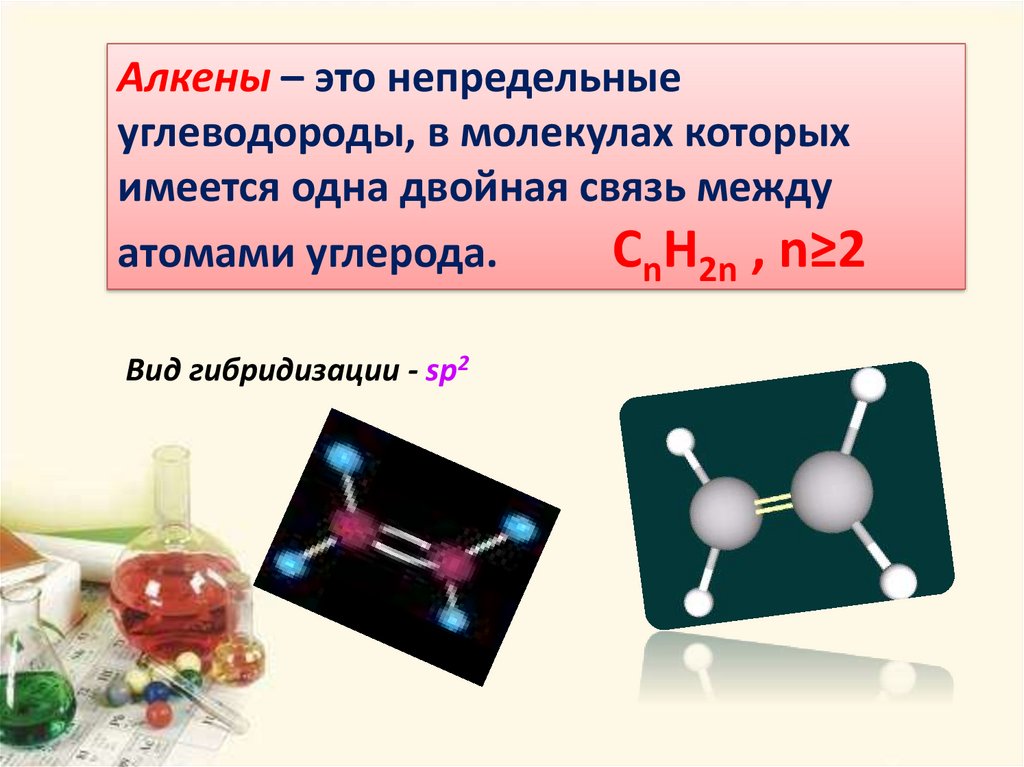
5.
Алкены – это непредельныеуглеводороды, в молекулах которых
имеется одна двойная связь между
атомами углерода.
CnH2n , n≥2
Вид гибридизации - sp2
6.
3. Изомерия и номенклатура алкенов.Алгоритм составления названия алкена:
1) В качестве главной выбрать самую длинную у/в цепь, которая
содержит двойную связь и с которой связано наибольшее число
заместителей (радикалов).
2) Пронумеровать атомы углерода в цепи, начиная с того конца, к
которому ближе находится двойная связь. Если она в центре цепи,
то нумерацию начинают с того конца, к которому ближе радикал
(заместитель).
3) Цифрами указать номера атомов углерода, с которыми связаны
радикалы, затем назвать радикалы в алфавитном порядке.
4) Назвать главную цепь.
5) Цифрой после названия алкена указать меньший
номер атома углерода, образующего двойную связь.
7.
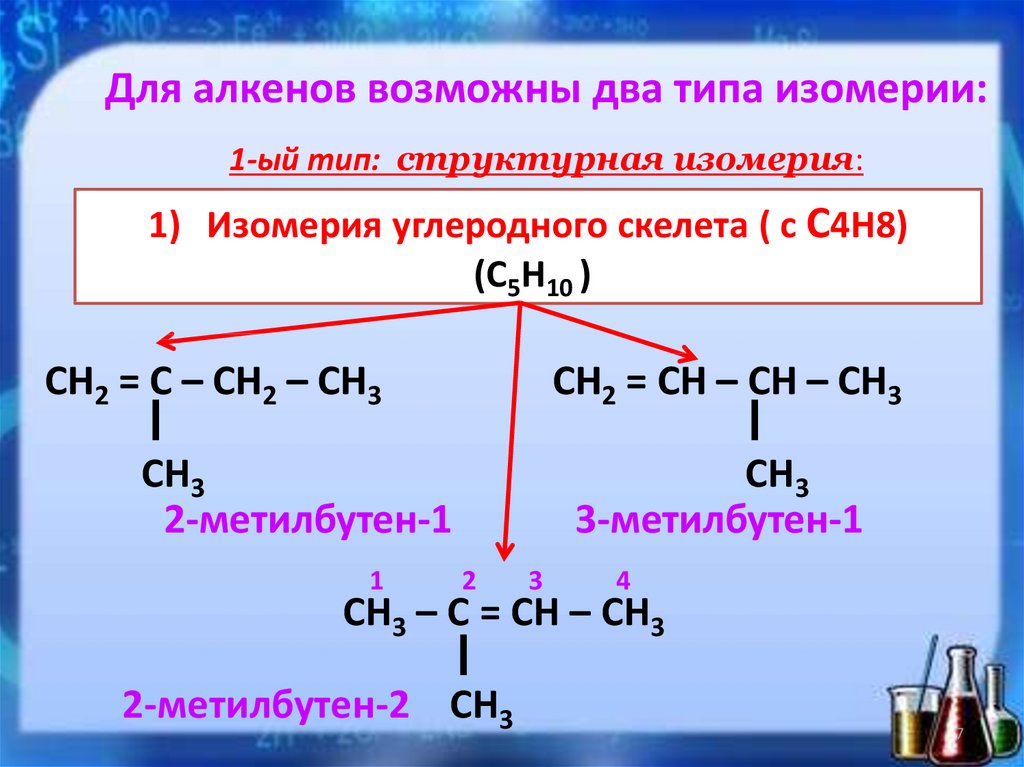
Для алкенов возможны два типа изомерии:1-ый тип: структурная изомерия:
1) Изомерия углеродного скелета ( с С4Н8)
(С5Н10 )
СН2 = С – СН2 – СН3
СН2 = СН – СН – СН3
СН3
2-метилбутен-1
1
СН3
3-метилбутен-1
2
3
4
СН3 – С = СН – СН3
2-метилбутен-2 СН3
7
8.
2) изомеров положения двойной связи ( с С4Н8)( С5Н10)
1
2
3
4
5
СН2 = СН – СН2 – СН2 – СН3
пентен-1
1
2
3
4
5
СН3 – СН = СН – СН2 – СН3
пентен-2
8
9.
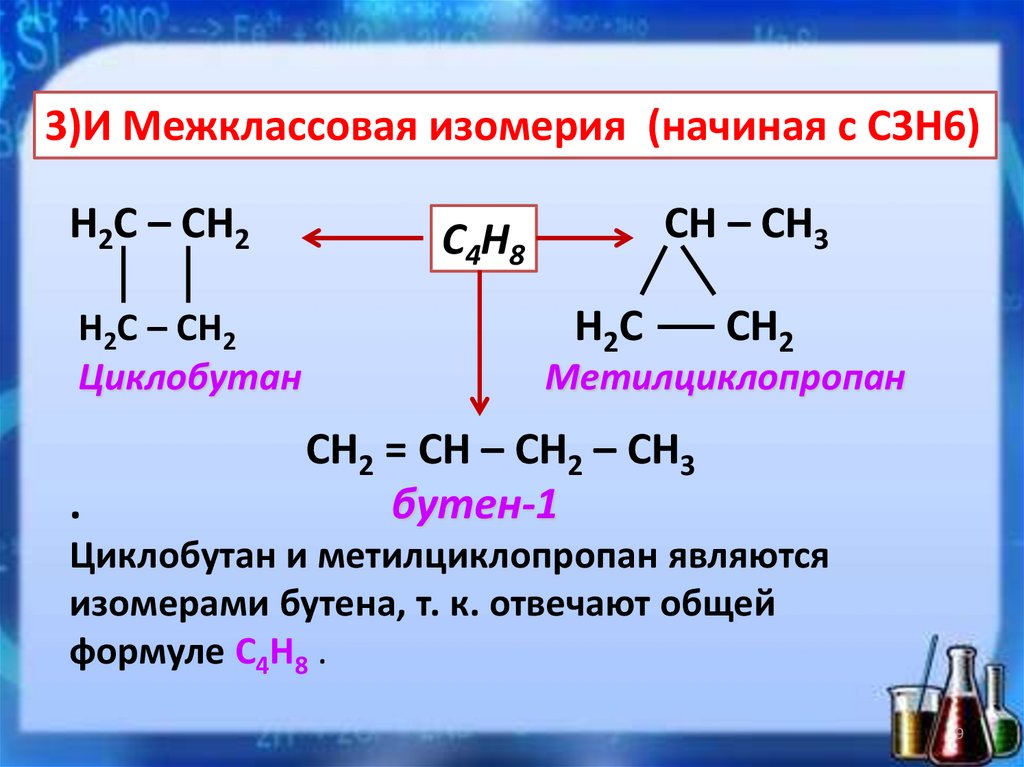
3)И Межклассовая изомерия (начиная с С3Н6)Н2С – СН2
Н2С – СН2
Циклобутан
.
СН – СН3
С4Н8
Н2С
СН2
Метилциклопропан
СН2 = СН – СН2 – СН3
бутен-1
Циклобутан и метилциклопропан являются
изомерами бутена, т. к. отвечают общей
формуле С4Н8 .
9
10.
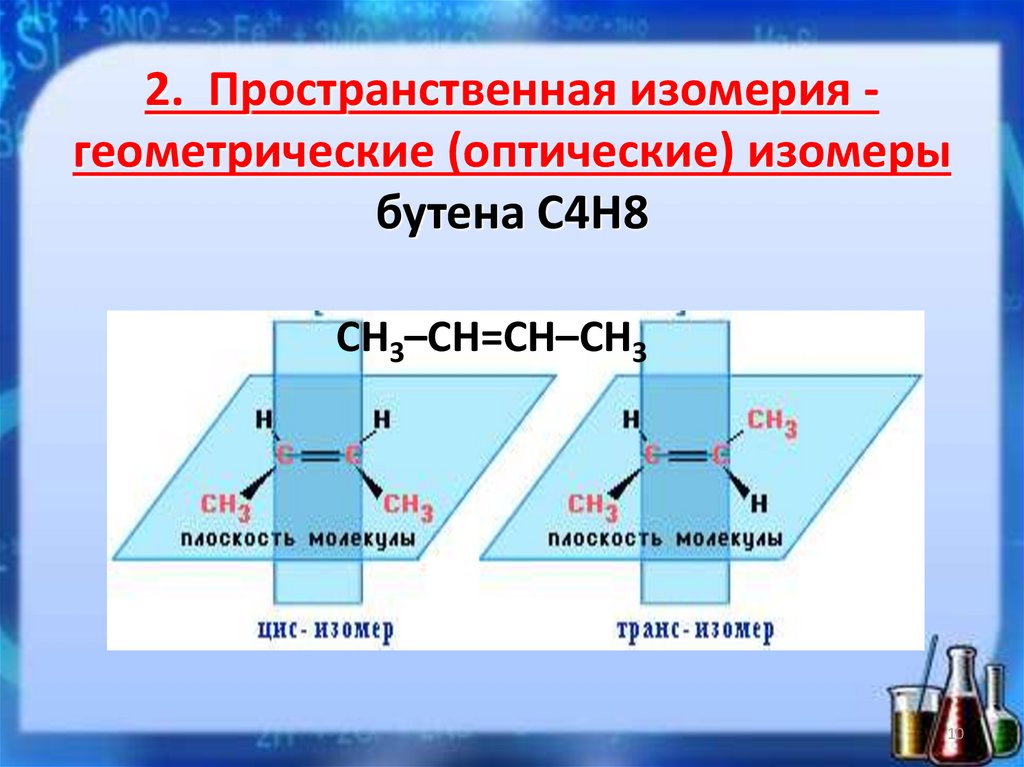
2. Пространственная изомерия геометрические (оптические) изомерыбутена С4Н8
СН3–СН=СН–СН3
10
11.
4. Способы получение алкенов.Промышленные
1)Термический крекинг алканов
С10Н22 → C5H12 + C5H10
декан пентан
пентен
Лабораторные
1) Дегидратация спиртов
СПИРТ→АЛКЕН+ВОДА
2) Дегидрогалогенирование
3) Дегалогенирование
2) Дегидрирование алканов
Ni, t=500C
Н3С - СН3 → Н2С = СН2 + Н2
этан
этен
(этилен)
11
12.
5. Физические свойства.Алкены плохо растворимы в воде, но
хорошо растворяются в органических
растворителях.
С увеличением молекулярной массы
алкенов, в гомологическом ряду,
повышаются температуры кипения и
плавления, увеличивается плотность
веществ
С2– С4 - газы
С5– С16 - жидкости
С17… - твёрдые вещества
12
13. 7. Применение алкенов
1314.
1415.
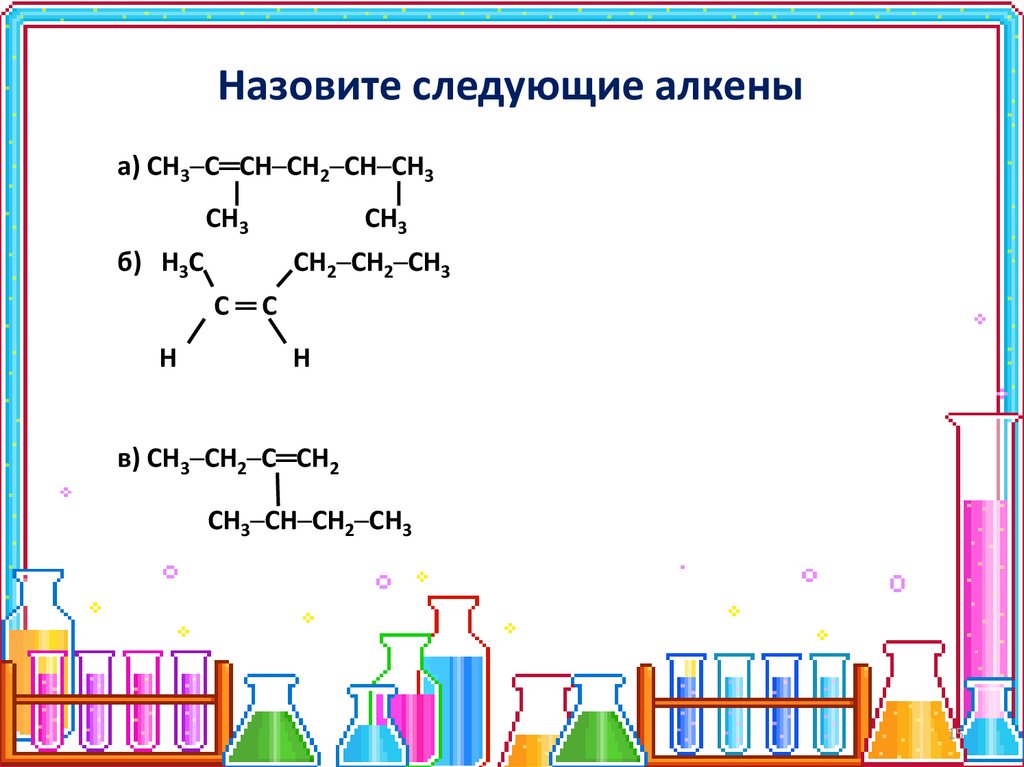
Назовите следующие алкеныа) СН3─С═СН─СН2─СН─СН3
СН3
б) Н3С
СН3
СН2─СН2─СН3
С═С
Н
Н
в) СН3─СН2─С═СН2
СН3─СН─СН2─СН3
15









 Химия
Химия








