Похожие презентации:
Основания. Химические свойства. Способы получения
1.
Химические свойстваСпособы получения
2. Химические свойства
Гидроксид– ионы (ОН-),
образующиеся при
диссоциации оснований,
обуславливают их
химические свойства
1. Действие на индикаторы
3. Химические свойства оснований (щелочей и нерастворимых оснований)
Химические свойст ва оснований(щелочей и нераст воримых оснований)
2. Взаимодействие с кислотами
Cu(OH)2 + H2SO4=CuSO4 + 2H 2O
нерастворимое
основание
+
кислота
=
соль
+
вода
Cu(OH)2 + 2H+ + SO42- = Cu2+ + SO4 2- + 2H2O
Cu(OH)2 + 2H += Cu2+ + 2H2O
2NaOH
+ H2SO4 →
основание + кислота
=
Na2SO4 +
соль
2H2O
+ вода
2Na++2OH-+2H++SO42-→2Na++SO42- + 2H2O
2H+ + 2OH- →2H2O
Реакция нейтрализации – реакция
между кислотой и основанием
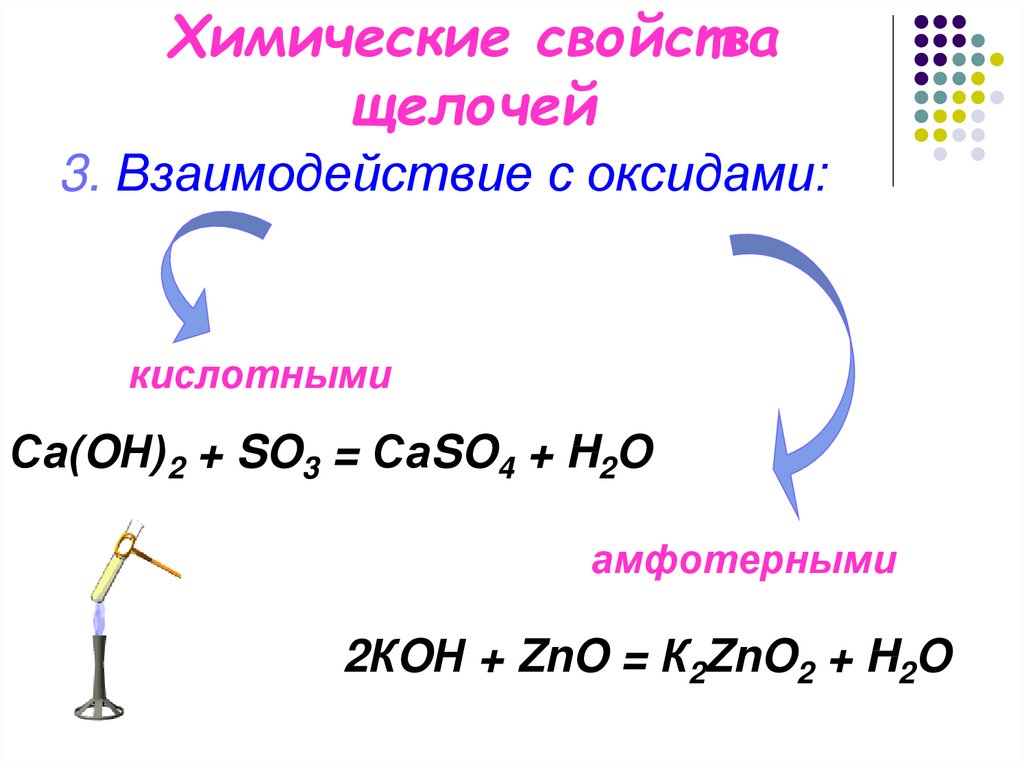
4. Химические свойства щелочей
3. Взаимодействие с оксидами:кислотными
Са(OН)2 + SO3 = СаSO4 + H2O
амфотерными
2КOН + ZnO = К2ZnO2 + H2O
5. Химические свойства щелочей
4. Взаимодействие с растворами солей:2NaОН + CuSO4 → Cu(OH)2 + Na2SO4
6. Химические свойства нерастворимых оснований
Разложение при нагреванииt0
Сu(OН)2 ---> СuO + H2O
7. Способы получения растворимых оснований (щелочей)
1. Взаимодействие щелочных ищелочно-земельных металлов с водой
2Na + 2H2O = 2NaOH + H2
2. Взаимодействие оксидов щелочных и
щелочно-земельных металлов с водой
СаO + H2O = Са(OН)2
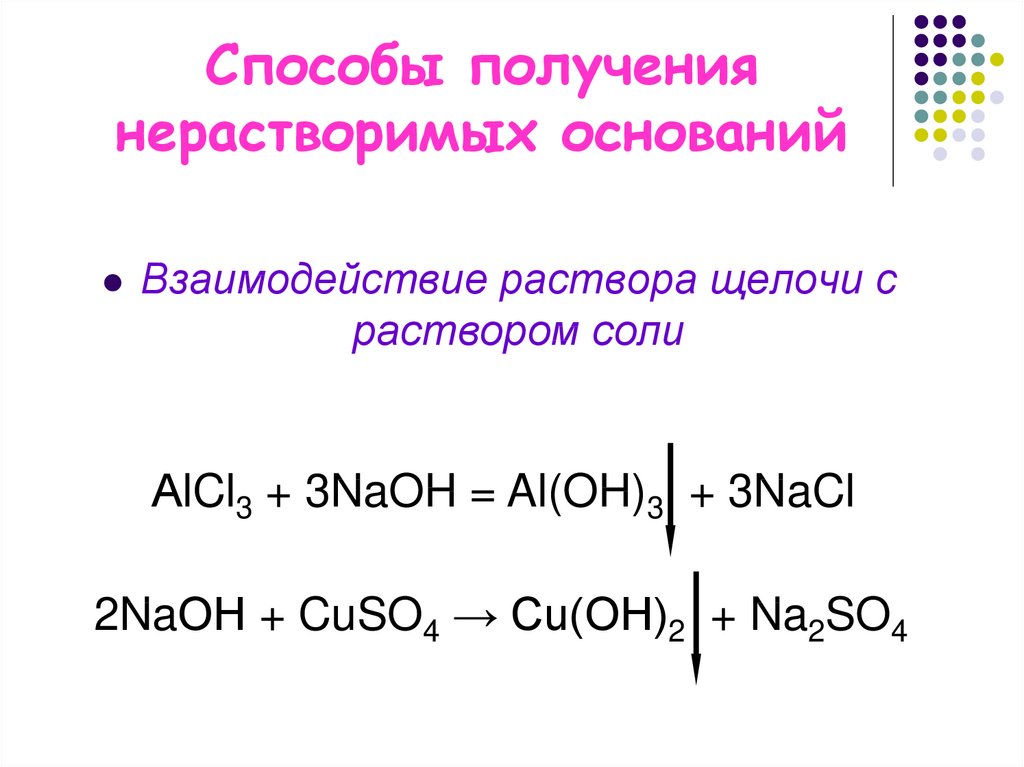
8. Способы получения нерастворимых оснований
Взаимодействие раствора щелочи сраствором соли
АlCl3 + 3NaOH = Al(OH)3 + 3NaCl
2NaОН + CuSO4 → Cu(OH)2 + Na2SO4






 Химия
Химия








