Похожие презентации:
Кальций - Са. 9 класс
1. § 43 Кальций - Са
2. Са
Щëлочно - земельный металл
Элемент IIA (II группа главная подгруппа) ПС
4 период
Z (порядковый номер) = 20
Ar (относительная атомная масса) = 40
Электронная формула 1S22S22P63S23P64S2
Cильный восстановитель
Степень окисления +2
3. Са в природе
• 3% в земной коре (3 место после Al и Fe)• Важнейшие соединения Са:
1) СаСО3 – минерал кальцит, образующий
мел, мрамор, известняк
2) CaSO4•2H2O – гипс
3) Ca3(PO4)2 - фосфорит
• Са – макроэлемент в организме
растений, животных и человека(2%)
4. Физические свойства
Кальций — металл серебристо-серогоцвета, относительно легкий и довольно
твердый, t°плавления = 854 °С,
окисляется на воздухе.
5. Химические свойства
При обычной температуре Ca легковзаимодействует с кислородом и
влагой воздуха, поэтому его хранят в
герметически закрытых сосудах или
под минеральным маслом.
6. Химические свойства
1. С простыми веществами - НЕМЕТАЛЛАМИ:• 2Са + О2 → 2СаО оксид кальция
• Ca+O2 → CaO2 пероксид кальция
• Са + Н2 → СаН2 гидрид кальция
• Ca + 2C → CaC2 карбид кальция
• Са + F2 → CaF2 фторид кальция
• Са + Br2 → CaBr2 бромид кальция
• Са + Cl2 → CaCl2 хлорид кальция
• ЗСа + N2 → Са3N2 нитрид магния
• ЗСа + 2Р → Са3Р2 фосфид кальция
• Са + S → СаS сульфид кальция
7. Химические свойства
2. Со сложными веществами:1) с водой
Ca + 2H2O → Ca(OH)2 + H2 ↑
2) с кислотами
Ca + H2SO4 → CaSO4 + H2↑
3)восстанавливает менее активные
металлы из их оксидов
2Са + ТiO2 = 2СаО + Тi
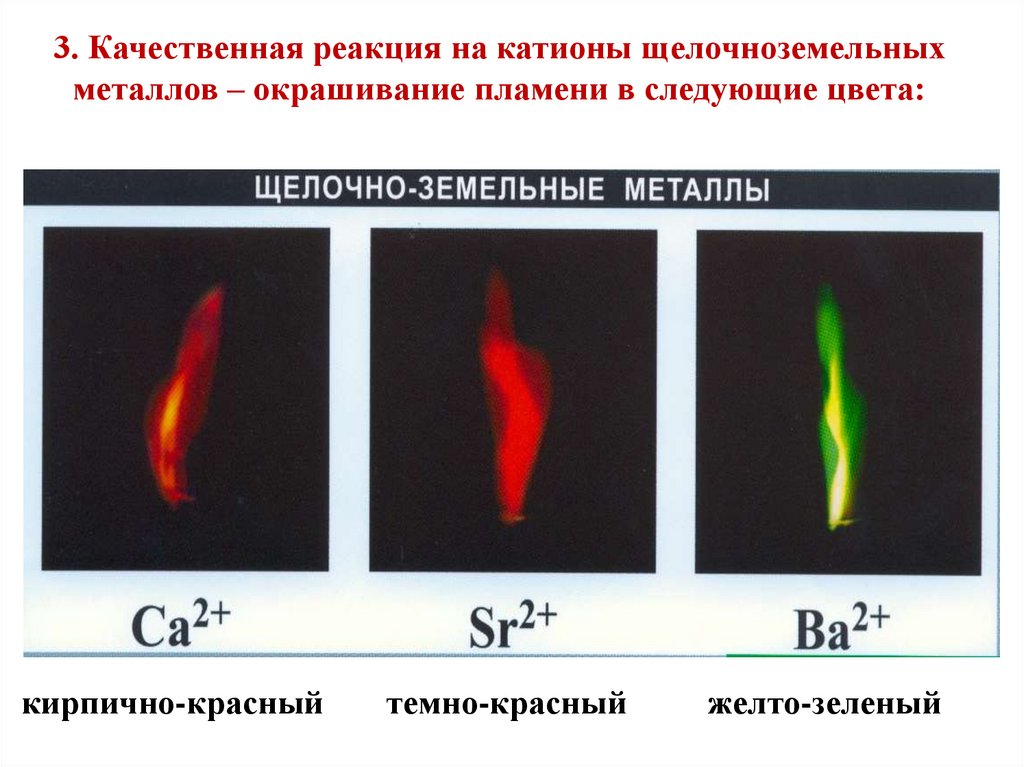
8. 3. Качественная реакция на катионы щелочноземельных металлов – окрашивание пламени в следующие цвета:
кирпично-красныйтемно-красный
желто-зеленый
9. Получение в промышленности
1. Электролиз расплавов солейкальция
CaCl2 → Ca + Cl2
2. Алюмотермия с оксидом кальция
3CaО + 2Al → 3Ca + Al2O3
10. 1. СаО - оксид кальция
• СаО – жженая или негашенаяизвесть
• Гашение извести – экзотермическая
реакция
СаО + Н2О → Са(ОН)2
11. 2. Са(ОН)2 - гидроксид кальция
• Са(ОН)2 – щелочь• Известковая вода – ненасыщенный
раствор Са(ОН)2
• Известковое молоко – пересыщенный
раствор Са(ОН)2
• Известковый раствор – раствор Са(ОН)2 с
песком SiO2
12. Применение
• В медицине• В строительстве
• В пищевой промышленности
• В металлургии











 Химия
Химия








