Похожие презентации:
Соли. Формулы солей
1. Соли
Сложные вещества, состоящие изатомов металла и атомов
кислотного остатка.
2.
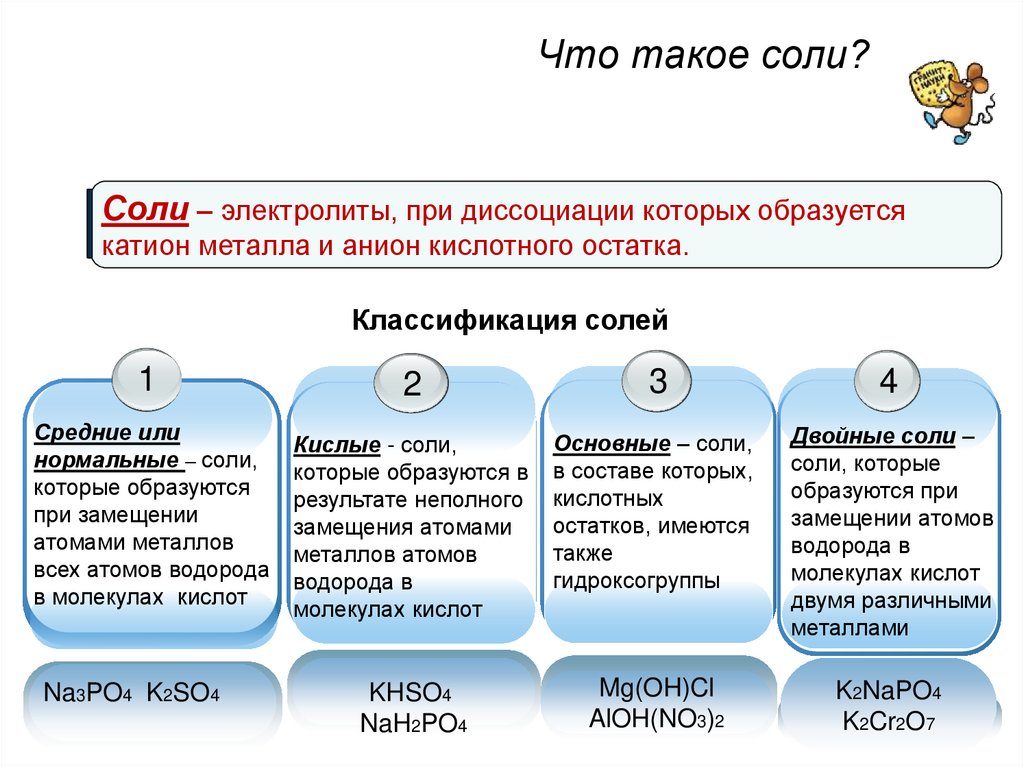
Что такое соли?Соли – электролиты, при диссоциации которых образуется
катион металла и анион кислотного остатка.
Классификация солей
1
Средние или
нормальные – соли,
которые образуются
при замещении
атомами металлов
всех атомов водорода
в молекулах кислот
Na3PO4 K2SO4
2
3
4
Кислые - соли,
которые образуются в
результате неполного
замещения атомами
металлов атомов
водорода в
молекулах кислот
Основные – соли,
в составе которых,
кислотных
остатков, имеются
также
гидроксогруппы
Двойные соли –
соли, которые
образуются при
замещении атомов
водорода в
молекулах кислот
двумя различными
металлами
KHSO4
NaH2PO4
Mg(OH)Cl
AlOH(NO3)2
K2NaPO4
K2Cr2O7
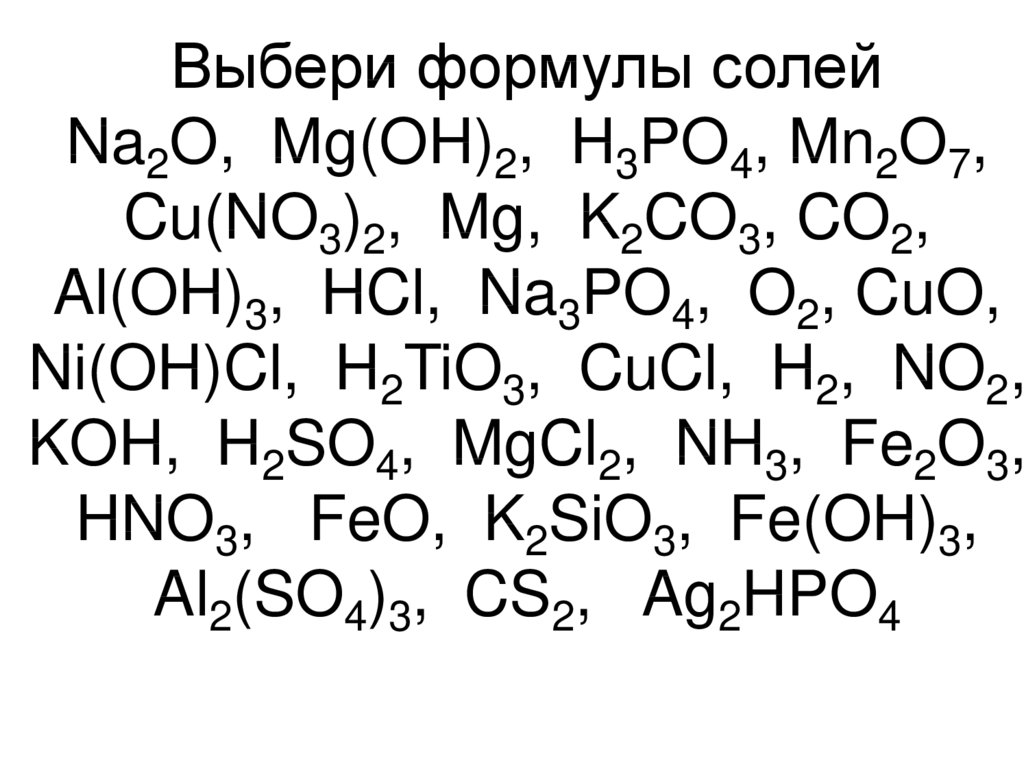
3. Выбери формулы солей Na2O, Mg(OH)2, H3PO4, Mn2O7, Cu(NO3)2, Mg, K2CO3, CO2, Al(OH)3, HCl, Na3PO4, O2, CuO, Ni(OH)Cl, H2TiO3,
CuCl, H2, NO2,KOH, H2SO4, MgCl2, NH3, Fe2O3,
HNO3, FeO, K2SiO3, Fe(OH)3,
Al2(SO4)3, CS2, Ag2HPO4
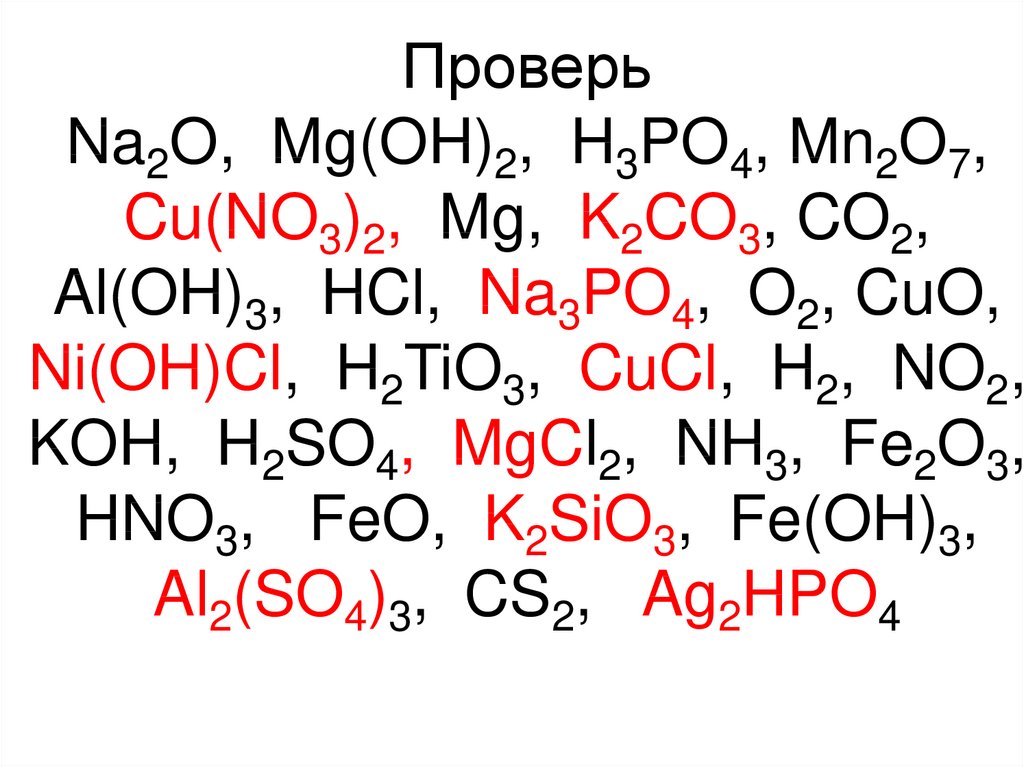
4. Проверь Na2O, Mg(OH)2, H3PO4, Mn2O7, Cu(NO3)2, Mg, K2CO3, CO2, Al(OH)3, HCl, Na3PO4, O2, CuO, Ni(OH)Cl, H2TiO3, CuCl, H2, NO2,
KOH, H2SO4, MgCl2, NH3, Fe2O3,HNO3, FeO, K2SiO3, Fe(OH)3,
Al2(SO4)3, CS2, Ag2HPO4
5. Составить формулы солей.
Нитрат кальция
Фосфат натрия
Силикат калия
Хлорид цинка
Сульфат алюминия
Карбонат меди
Ca(NO3)2
Na3 PO4
K2SiO3
ZnCl2
Al2(SO4)3
CuCO3
6. Соли с точки зрения теории электролитической диссоциации.
• Соль1 + кислота1 = соль2 (н\р)+ кислота2( н\р или ↑)Na2S + HNO3 = H2S↑ + NaNO3
• Соль1(р) + основание(р) = соль(н/р) + основание(н/р)
LiOH + AgNO3 = AgOH↓ + LiNO3
• Соль1(р) + соль2(р) = соль 3 + соль 4 (н\р)
Na2CO3 + BaCl2 = BaCO3↓ + 2NaCl
• Соль1(р)+ металл1 = соль2 + металл2
CuSO4 + Zn = ZnSO4 + Cu
7. Дописать уравнения возможных реакций в молекулярном и ионном виде
H2SO4 + PbCl2=
K2CO3 + AlCl3 =
H2SO4 + ZnCl2=
Ba(OH)2 + Na3PO4 =
Na2SO3 + H2SO4 =
MgSiO3 + HNO3 =
Ba + K3PO4 =





 Химия
Химия








