Похожие презентации:
Реакции ионного обмена
1.
Тема: Реакции ионного обменаТерлецкая Алла
Доктор химических наук
Учитель химии, высшая дидактическая степень
Теоретический Лицей имени Антона Чехова
2.
К концу урока ты будешь способен:1. Различать необратимые и обратимые реакции;
2. Составлять уравнения электролитической
диссоциации кислот, оснований и солей;
3. Определять молекулярные и ионные уравнения
реакций;
4. Составлять и записывать полные ионные и
сокращенные ионные уравнения реакций.
3. Дайте определение с точки зрения ТЭД:
Что такое кислоты?Кислоты – это электролиты, которые диссоциируют с
образованием катиона (H+) и анионов кислотных остатков
Нm(Кисл.ост.)
m H+
Anm-(Кисл.ост.)
4. Дайте определение с точки зрения ТЭД:
Что такое основания?Щёлочи (ратворимые в воде основания) – это электролиты,
которые диссоциируют с образованием анионов ОH- и
катионов металлов.
Me (OH)n
Men+
nОН-
5. Дайте определение с точки зрения ТЭД:
Что такое соли?Соли – это электролиты, которые диссоциируют с на
катионы металла и анионы кислотного остатка.
Меm (Кисл.ост.)n
m Men+
nAnm-(Кисл.ост.)
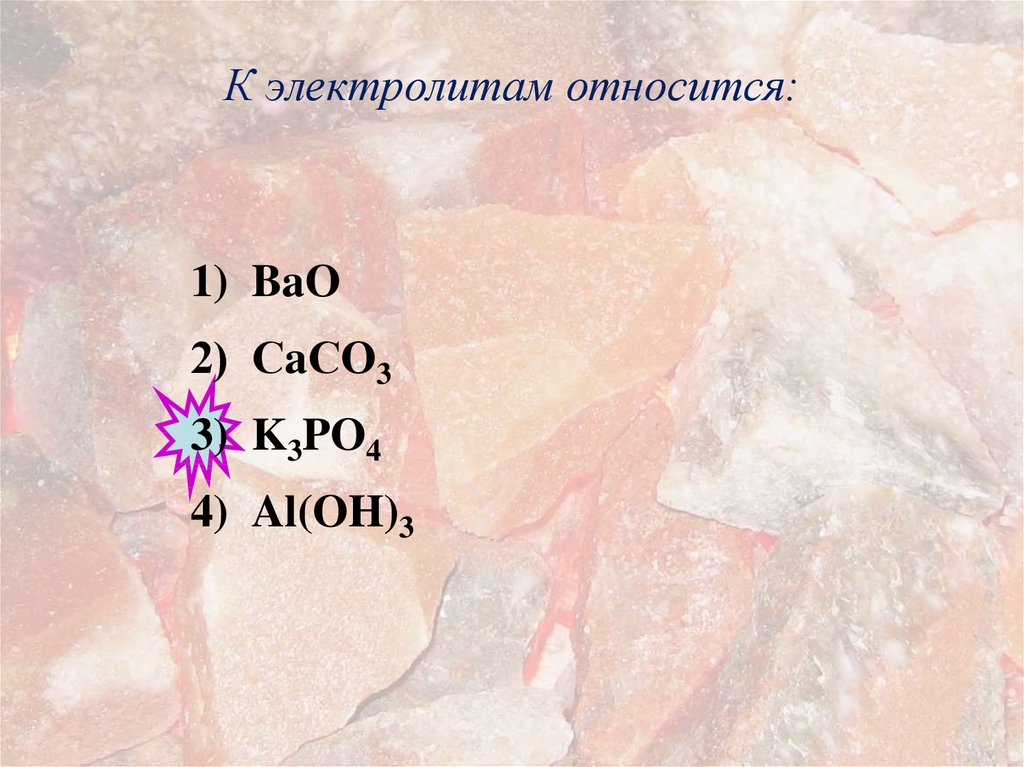
6. К электролитам относится:
1) BaO2) СaСO3
3) K3PO4
4) Al(OH)3
7. К электролитам не относится:
1) BaCl22) ZnSO4
3) H2SO4
4) CO2
8. Сильный электролит – это:
1) H2SO32) H2SiO3
3) H2SO4
4) H2S
9. Вещество, при диссоциации которого образуются силикат-ионы, – это:
1) K2SiO32) SiO2
3) H2SiO3
4) CaSiO3
10. Вещество, при диссоциации которого образуются катионы цинка, – это:
1) ZnSO32) ZnO
3) Zn(OH)2
4) Zn(NO3)2
11.
https://images.app.goo.gl/xqiSUVbZNnyCgpGx612. При протекании реакции обмена в растворе, взаимодействие происходит между ионами, а не молекулами, т.к. электролиты способны
диссоциировать инаходятся в растворе в виде ионов!
Al(NO3)3 = Al3+ + 3NO3NaOH = Na+ + OH-
13. Соль и щёлочь могут взаимодействовать (см. учебник 8 класса на стр.85,87)
Составим уравнение этой реакцииAl(NO3)3 + 3NaOH = Al(OH)3+ 3NaNO3
Проверим растворимость каждого вещества
по таблице растворимости
14.
Учебник Химии 8 класс, стр. 15615.
Al(NO3)3 + 3NaOH = Al(OH)3+ 3NaNO3Р
Р
Н
Р
Каждое растворимое вещество представим в диссоциированной форме, собрав все
ионы в одном уравнении, нерастворимые вещества оставим без изменений.
ПИУ:
Al3+ + 3NO3- + 3Na+ + 3OH- = Al(OH)3 + 3Na+ + 3NO3Такое уравнение называется Полным Ионным Уравнением или сокращенно: ПИУ
16.
Можно заметить, что в левой и правой частях уравнения естьодинаковое число одинаковых ионов.
Это ионы 3NO3- и 3Na+ , которые можно сократить и записать
то, что осталось:
СИУ:
Al3+ + 3OH- = Al(OH)3
Такое уравнение, показывающее, какие ионы связывались
(вступали в реакцию), называется Сокращенным Ионным
Уравнением: СИУ
17.
При составлении ионных уравнений следуетпроверить две вещи:
1. Растворимо или нет каждое вещество?
2. Сильный или слабый электролит данное вещество?
МУ:
CuSO4 + 2KOH = Cu(OH)2↓ + K2SO4
ПИУ:
Cu2+ + SO42- + 2K+ + 2OH- = Cu(OH)2↓ + 2K+ + SO42-
СИУ:
Cu2+ + 2OH- = Cu(OH)2↓
Учебник 8 кл., стр. 134
18.
Cоставь полные ионные и сокращенные ионныеуравнения следующих реакций:
BaCl2 + K2СO3 = BaСO3 + 2KCl
NaCl + AgNO3 = NaNO3 + AgCl
19.
Проверь себя:МУ:
BaCl2 + K2СO3 = BaСO3 + 2 KCl
ПИУ:
Ba2+ + 2Cl - + 2K+ + СO32 -= BaСO3+ 2K+ + 2Cl -
СИУ:
Ba2+ + СO32- = BaСO3
20.
Проверь себя:МУ:
NaCl + AgNO3 = NaNO3 + AgCl
ПИУ:
Na+ + Сl- + Ag+ + NO3- = Na+ + NO3- + AgCl
СИУ:
Сl- + Ag+ = AgCl
21. Если тебя заинтересовала данная тема:
1. Изучи §5.11.3, учебник 8 класс2. Выполни упр. 11, стр. 137.
Спасибо за урок !
22. Использованные ресурсы:
1.CHIMIA Curriculum pentru învăţămîntul gimnazial clasele a VII-a - a IX-a, Chişinău,2010
https://mecc.gov.md/sites/default/files/curric_chimia_tipar.pdf
2. Химия, Гид по внедрению модернизированного куррикулума для гимназического
образования (7-9 классы), Кишинэу – 2011
3.Галина Драгалина, Надежда Велишко, Светлана Кудрицкая, Борис Пасечник
Химия, учебник для 8 класса, Издательство ARC, Кишинэу 2019 ISBN 978-9975-61739-0
4.https://pptcloud.ru/medicina/solyanaya-sauna-solyanaya-komnata-solyanoy-grot-solyanayapeschera-speleokamera-galokamera-solyanaya-kartina-solyanoe-panno
5.http://www.myshared.ru/slide/558988/

















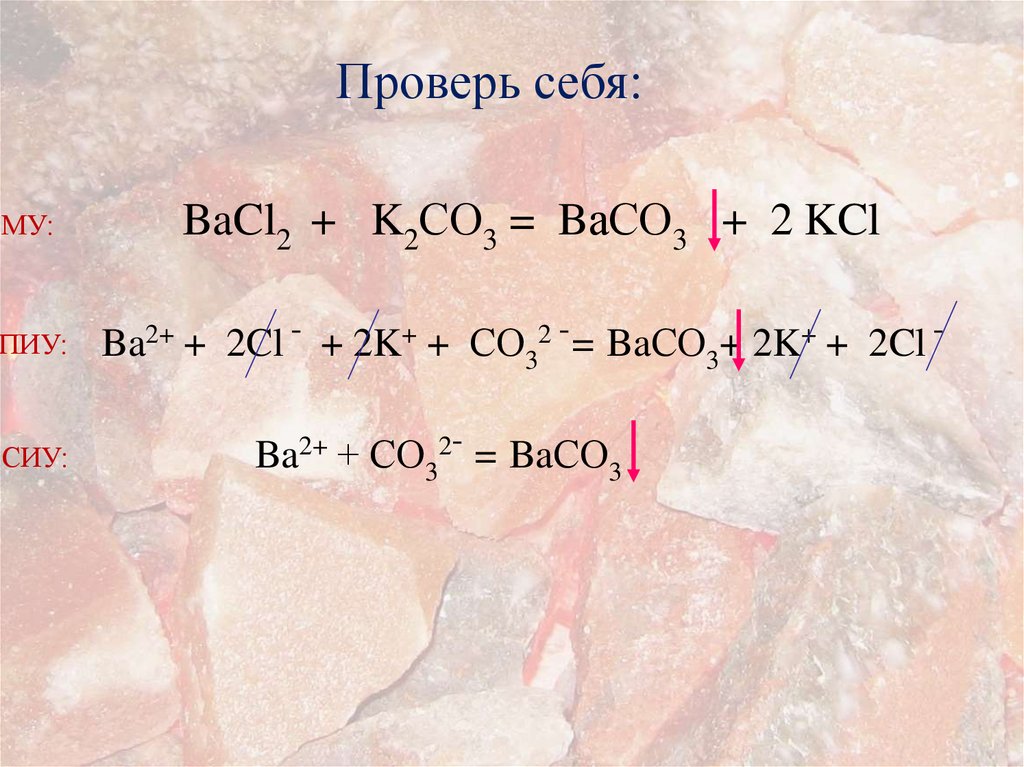



 Химия
Химия








