Похожие презентации:
Белки. Биологическая роль белков. Функции белков
1.
O H║ |
—C—N—
Emw
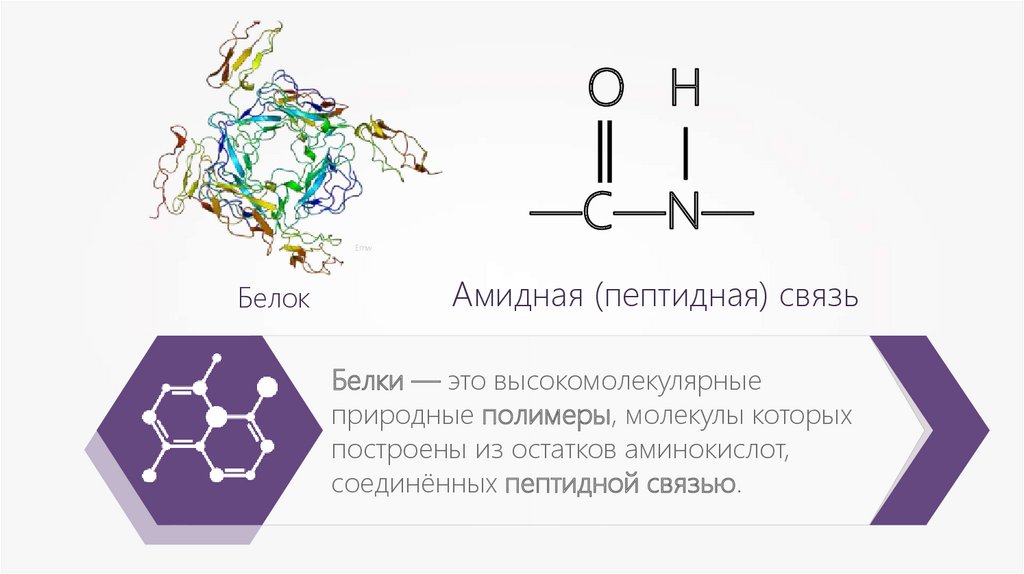
Белок
Амидная (пептидная) связь
Белки — это высокомолекулярные
природные полимеры, молекулы которых
построены из остатков аминокислот,
соединённых пептидной связью.
2.
EmwБелки
Образуют
20 различных
α-аминокислот
3.
Остаткиα-аминокислот
Остатки
α-аминокислот
O H
║ |
—C—N—
Белок
Амидная (пептидная) связь
Остатки
α-аминокислот
Остатки
α-аминокислот
4.
Биологическая роль белковФункции белков
1. Каталитическая
(ферментативная).
Фермент
Каталаза
5.
Биологическая роль белковКлеточная мембрана
Функции белков
2. Строительная.
Emw
Белки
Клетка
6.
Биологическая роль белковФункции белков
Thomas Splettstoesser
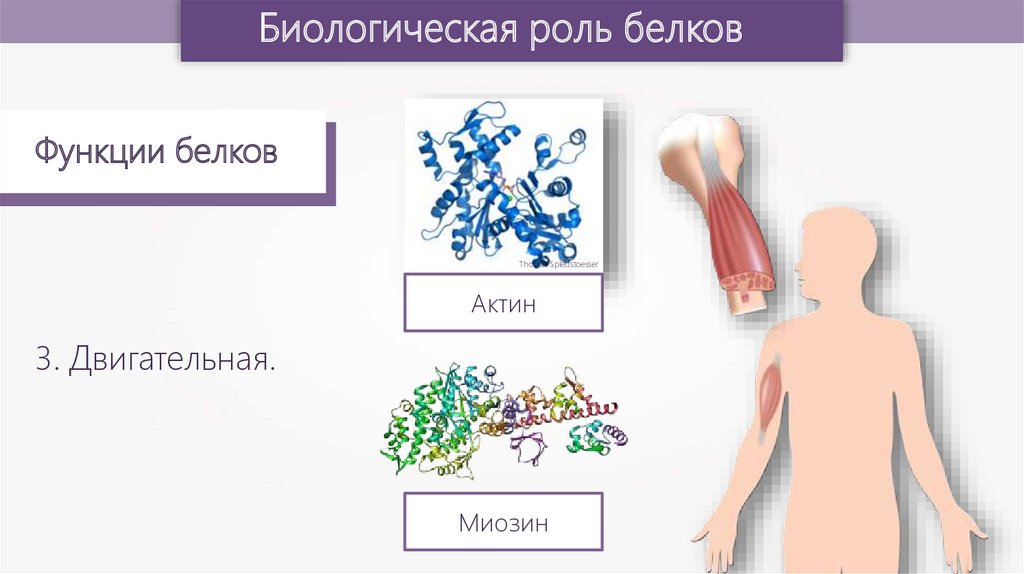
Актин
3. Двигательная.
Миозин
7.
Биологическая роль белковФункции белков
Nevit Dilmen
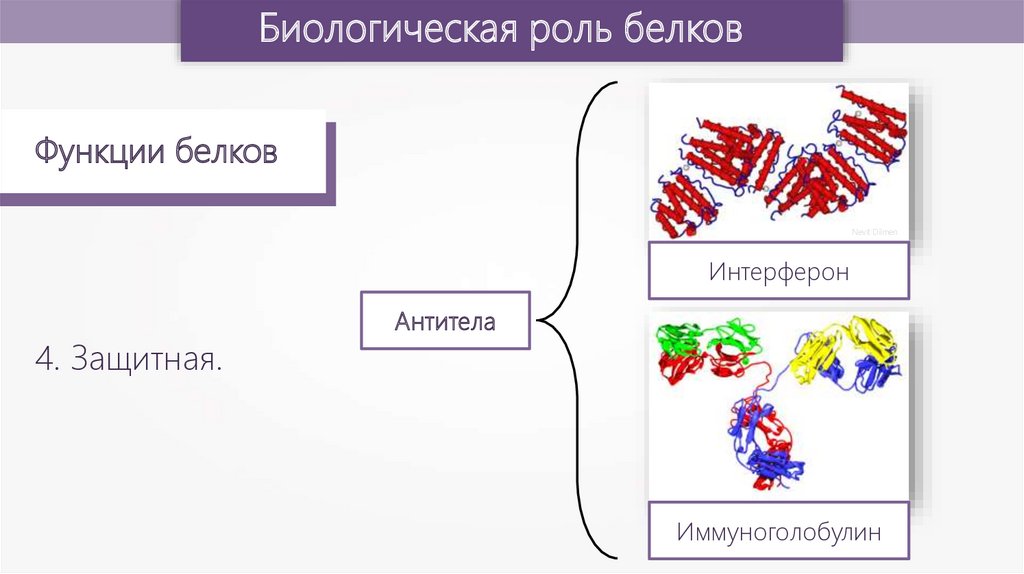
Интерферон
4. Защитная.
Антитела
Иммуноголобулин
8.
Биологическая роль белковФункции белков
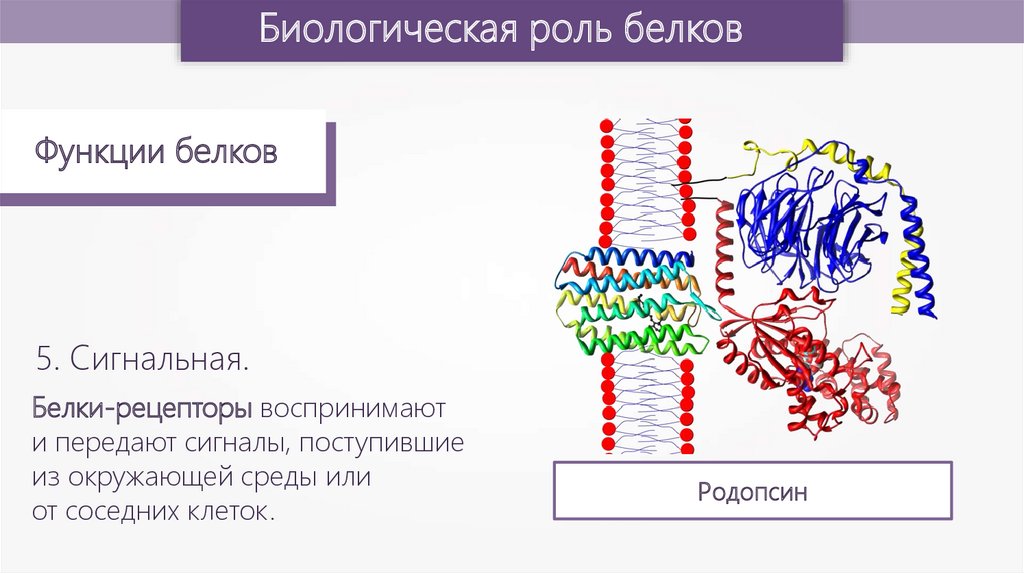
5. Сигнальная.
Белки-рецепторы воспринимают
и передают сигналы, поступившие
из окружающей среды или
от соседних клеток.
Родопсин
9.
Биологическая роль белковФункции белков
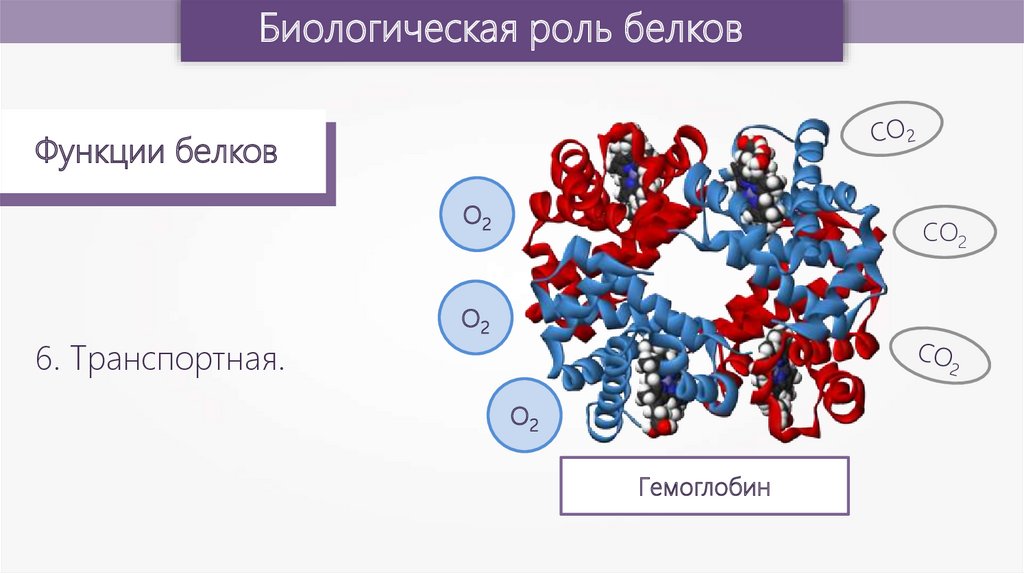
О2
6. Транспортная.
СО2
О2
О2
Гемоглобин
10.
Биологическая роль белковФункции белков
17,6 кДж
7. Энергетическая.
11.
Биологическая роль белковФункции белков
8. Регуляторная.
Инсулин
12.
Биологическая роль белковФункции белков
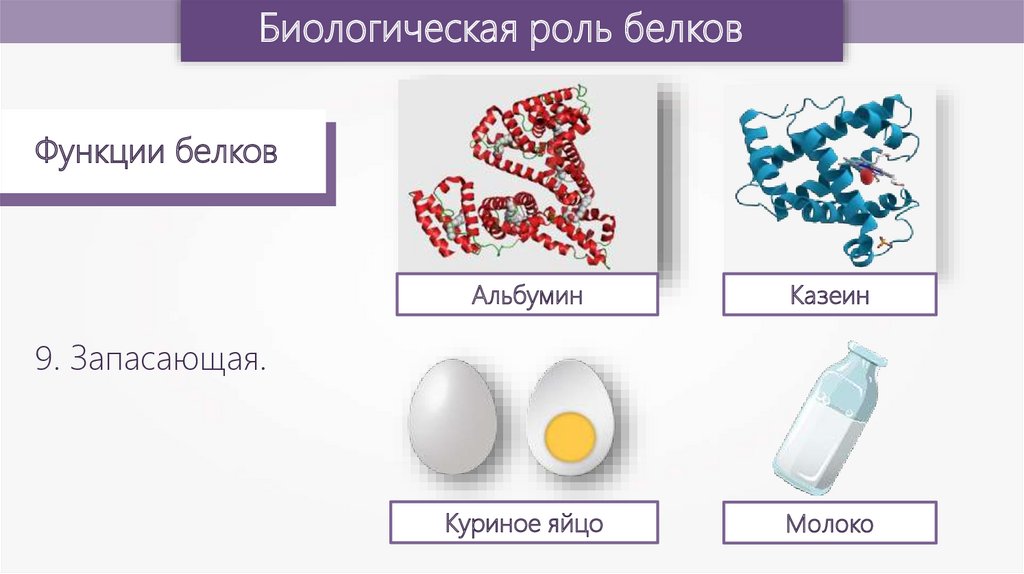
Альбумин
Казеин
Куриное яйцо
Молоко
9. Запасающая.
13.
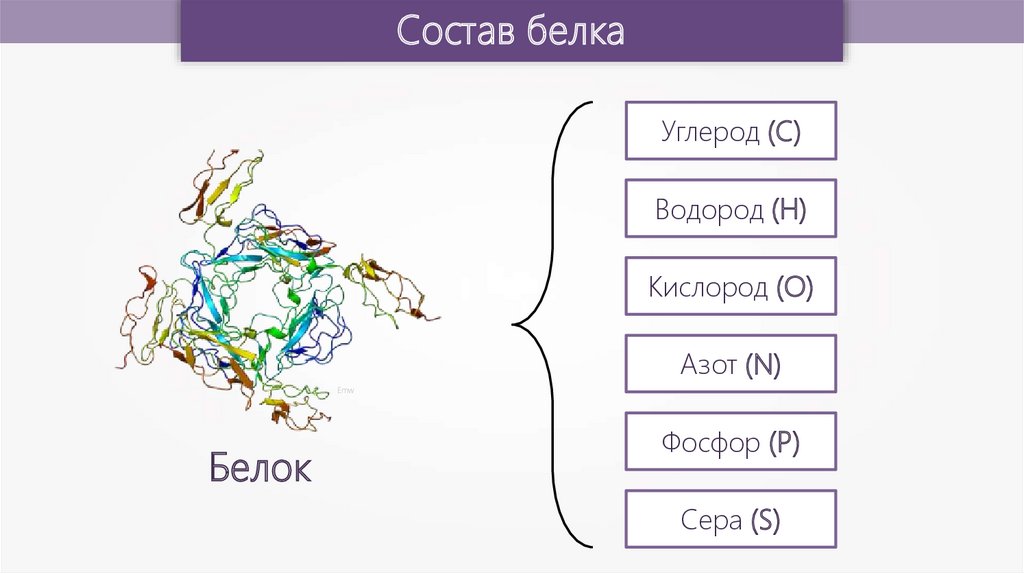
Состав белкаУглерод (C)
Водород (H)
Кислород (O)
Азот (N)
Emw
Белок
Фосфор (P)
Сера (S)
14.
Эмиль ГерманФишер
1852–1919 гг.
Эмиль Герман Фишер
в 1901 г. предположил и
затем экспериментально
обосновал положение
о том, что белковые
молекулы построены
из аминокислот, остатки
которых соединены
пептидными связями.
15.
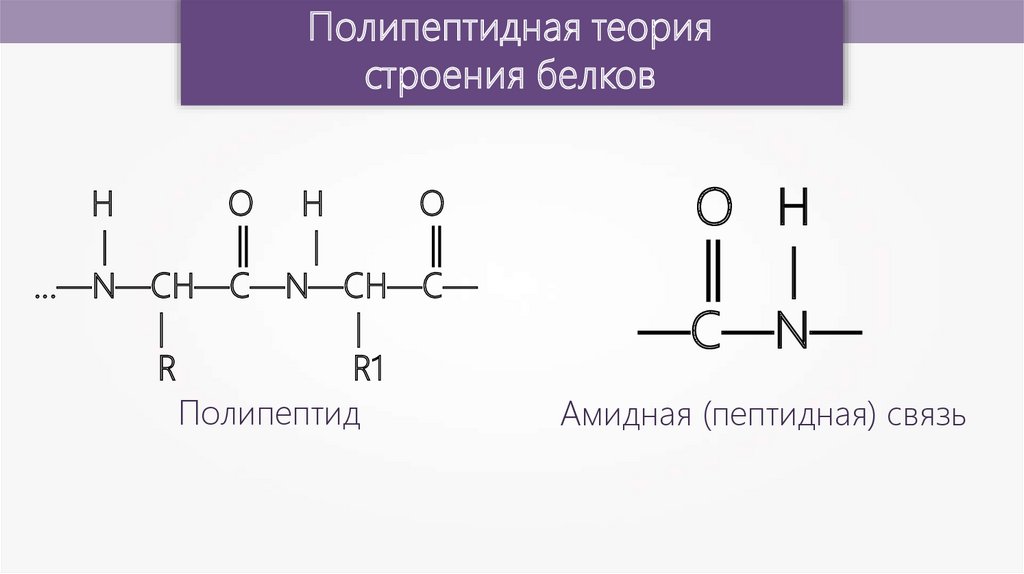
Полипептидная теориястроения белков
H
O H
O
|
║
|
║
…—N—CH—C—N—CH—C—
|
|
R
R1
Полипептид
O H
║ |
—C—N—
Амидная (пептидная) связь
16.
Первичная структурабелка — линейная.
Это определённая
последовательность
соединения остатков
аминокислот
в полипептидной цепи.
Первичная структура белка
17.
Вторичная структурабелка — представляет
собой закрученную
полипептидную
линейную цепь в спираль.
Вторичная структура белка
18.
Третичная структурабелка образуется
при закручивании
в пространстве вторичной
структуры, при этом
образуется клубок.
Третичная структура белка
19.
Четвертичная структура белкаЧетвертичная структура —
ещё более усложнённая
в пространстве третичная,
когда отдельные
субъединицы белка образуют
сложные ансамбли, которые
поддерживаются как
водородными связями,
так и электростатическим
взаимодействием.
20.
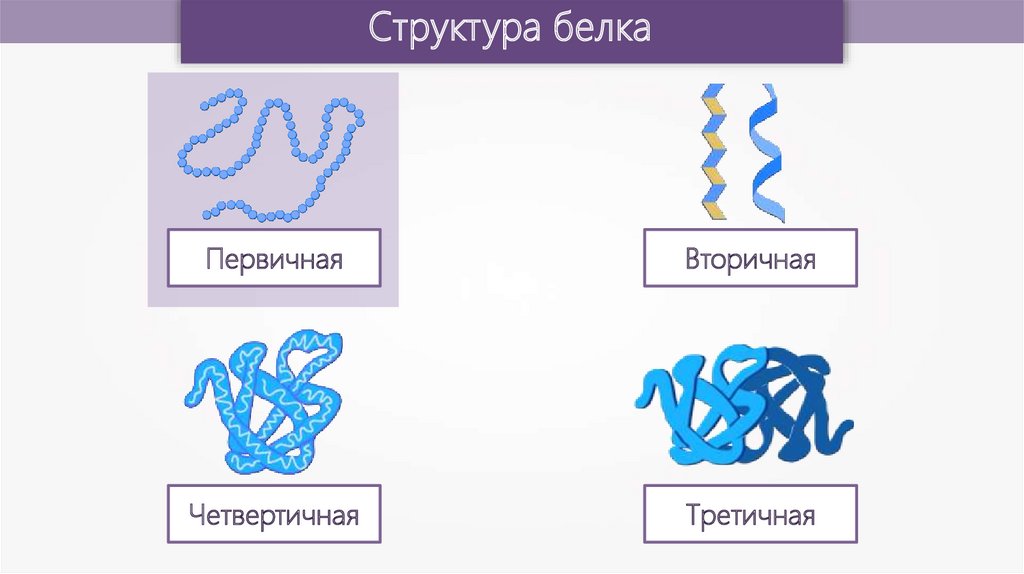
Структура белкаПервичная
Вторичная
Четвертичная
Третичная
21.
Химические свойстваСтруктура
Вторичная
Третичная
Четвертичная
Денатурация белка —
разрушение вторичной,
третичной, четвертичной
структур белка под
действием внешних
факторов.
Первичная структура и
химический состав белка
не меняются.
22.
Химические свойстваИзменение физических
свойств
Снижение
растворимости
Снижение
способности
к гидратации
Потеря биологической
активности
Денатурация белка —
разрушение вторичной,
третичной, четвертичной
структур белка под
действием внешних
факторов.
Первичная структура и
химический состав белка
не меняются.
23.
Химические свойстваМеняется форма
белковой макромолекулы,
происходит
агрегирование.
Opabinia regalis
Молекула белка
24.
Химические свойстваТретичная структура белка
Разрушение третичной
структуры белка —
обратимый процесс.
При этом возможна
ренатурация —
восстановление
структуры.
25.
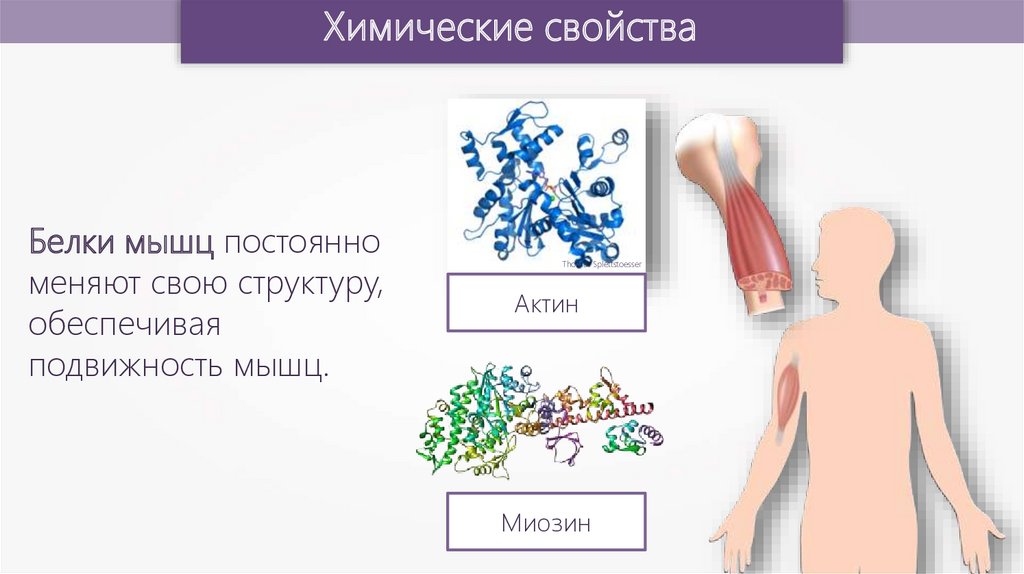
Химические свойстваБелки мышц постоянно
меняют свою структуру,
обеспечивая
подвижность мышц.
Thomas Splettstoesser
Актин
Миозин
26.
Белок + H2OСмесь аминокислот
Гидролиз белка — расщепление белка до аминокислот.
27.
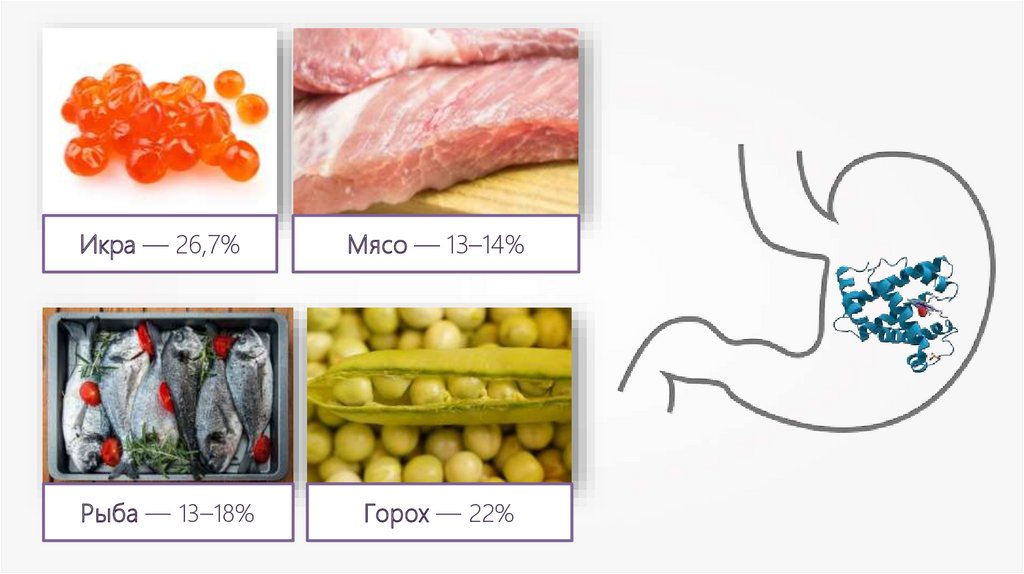
Икра — 26,7%Рыба — 13–18%
Мясо — 13–14%
Горох — 22%
Белки — основной
продукт питания.
Средняя потребность
человека в белке
за сутки составляет
80–100 г.
28.
Икра — 26,7%Рыба — 13–18%
Мясо — 13–14%
Горох — 22%
29.
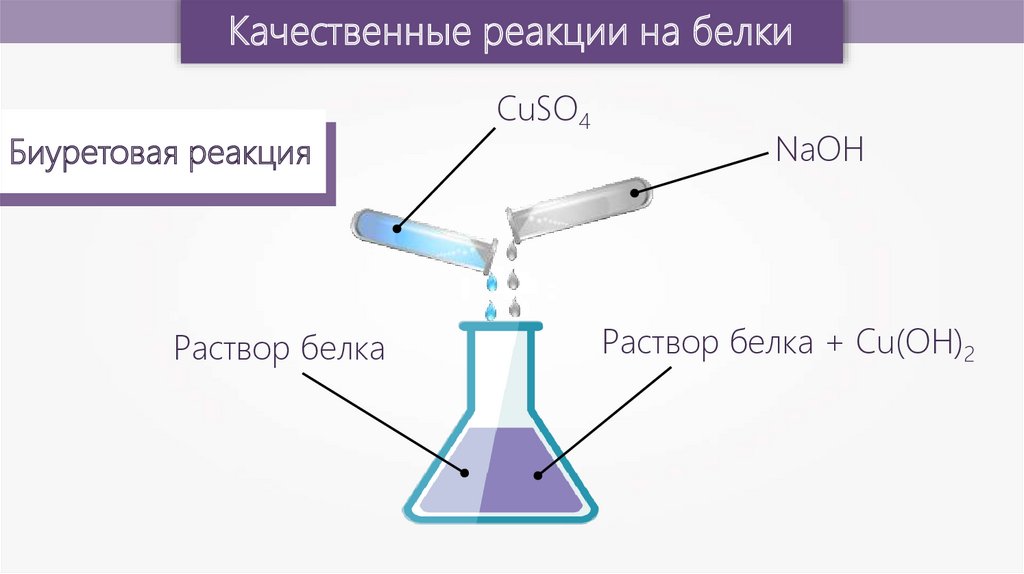
Качественные реакции на белкиБиуретовая реакция
Раствор белка
CuSO4
NaOH
Раствор белка + Cu(OH)2
30.
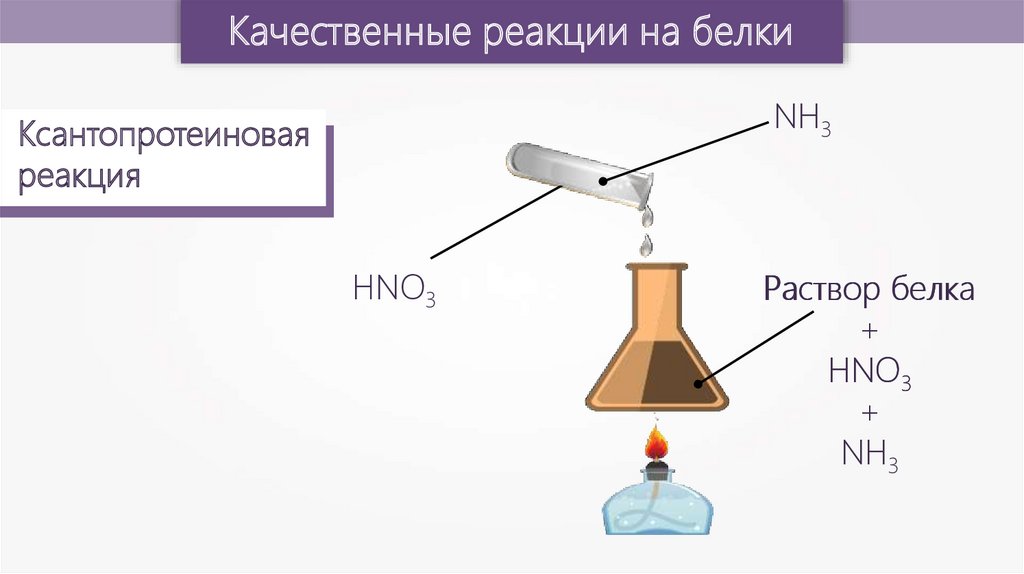
Качественные реакции на белкиNH3
Ксантопротеиновая
реакция
HNO3
Раствор белка
+
HNO3
+
NH3
31.
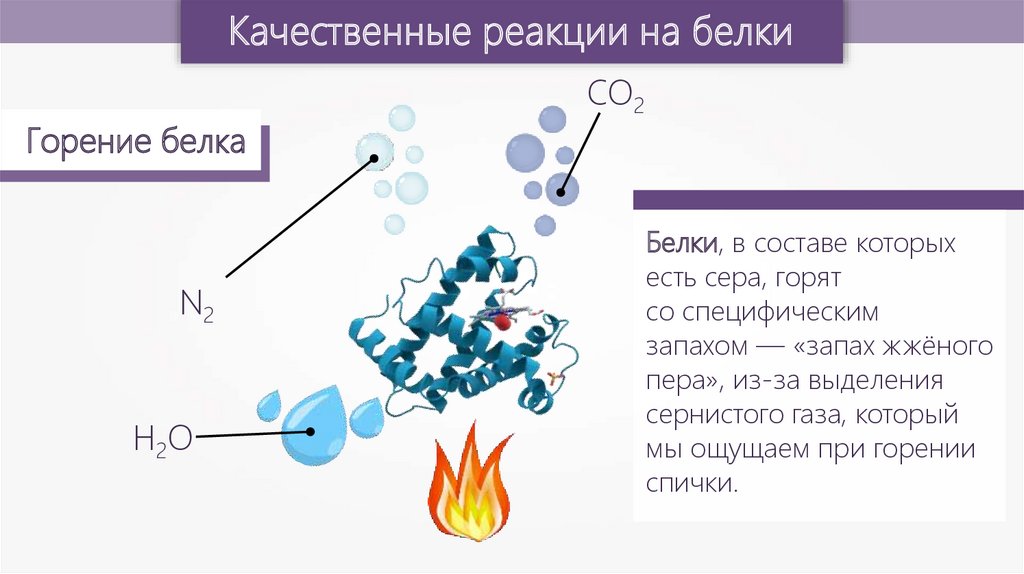
Качественные реакции на белкиГорение белка
N2
H2O
CO2
Белки, в составе которых
есть сера, горят
со специфическим
запахом — «запах жжёного
пера», из-за выделения
сернистого газа, который
мы ощущаем при горении
спички.
32.
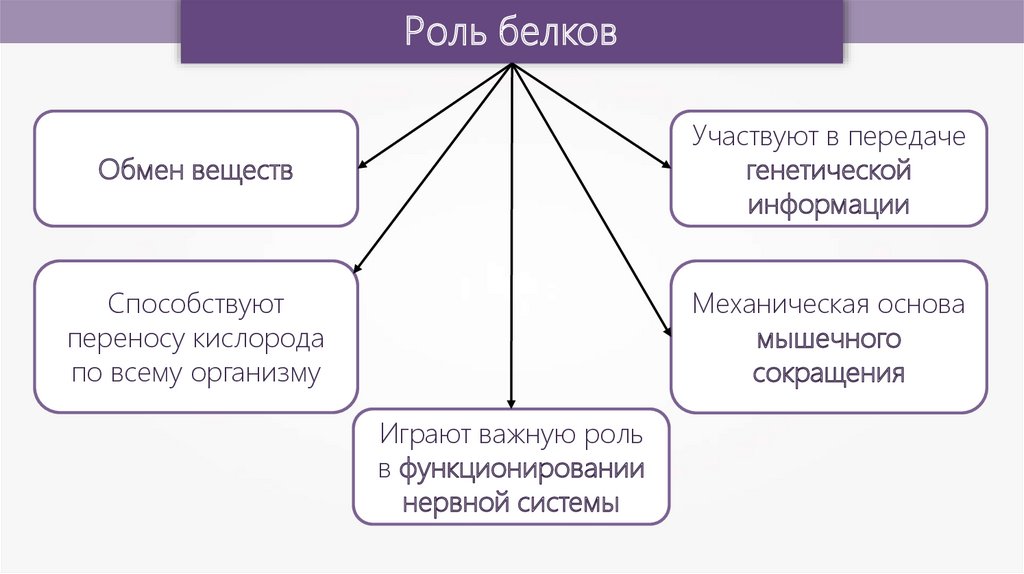
Роль белковОбмен веществ
Участвуют в передаче
генетической
информации
Способствуют
переносу кислорода
по всему организму
Механическая основа
мышечного
сокращения
Играют важную роль
в функционировании
нервной системы












 Биология
Биология Химия
Химия








