Похожие презентации:
Щелочноземельные металлы
1.
Щелочноземельныеметаллы
2.
Общая характеристика элементов главной подгруппы IIгруппы
Элемент
Ar
Количество
электронов
на
последнем
уровне
Be
9
2s2
+2
))
24
3s2
+2
)))
40
4s2
+2
))))
88
5s2
+2
)))))
137
6s2
+2
))))))
[226] 7s2
+2
)))))))
Mg
Ca
Sr
Ba
Ra
СО
Атомный
радиус
Металличе
ские
свойства
Восстанов
ительные
свойства
3.
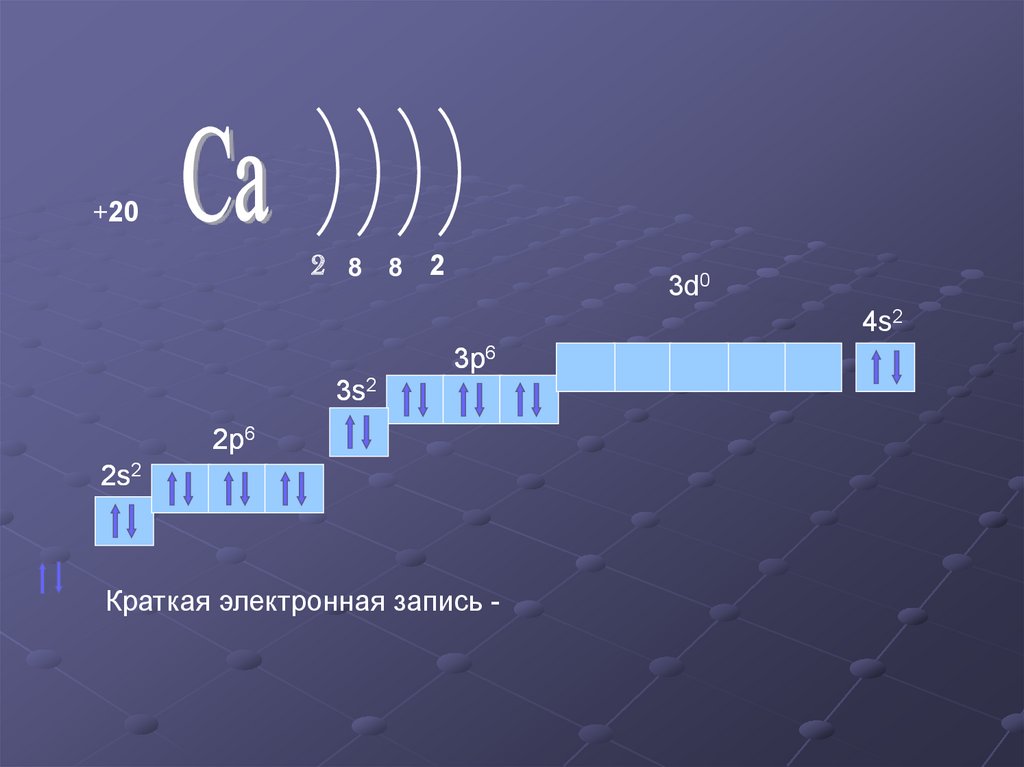
+202 8 8 2
3d0
4s2
3p6
3s2
2p6
2s2
Краткая электронная запись -
4.
Ве - амфотерный металл,Mg – металл,
Сa, Sr,Ba - щёлочноземельные металлы
Ra –радиоактивный элемент
5.
Общая характеристика элементовглавной подгруппы II группы
Одинаковое строение внешнего электронного слоя
Элементы проявляют С.О. +2
Атомы элементов являются сильными
восстановителями, т.к содержат 2 электрона на
внешнем энергетическом уровне, которые отдают при
взаимодействиями с другими элементами.
С увеличением № элементов увеличивается атомный
радиус, увеличивается число электронных слоев,
следовательно возрастает легкость отдачи электронов.
Восстановительные свойства увеличиваются в группе
сверху вниз.
6.
Ca – твердый, пластичныйMg – относительно мягкий, пластичный,
ковкий
Be – светло-серый, твердый,
хрупкий
Sr – ковкий
7.
Химические свойства элементов II группыглавной подгруппы
2Me0 +O2 → 2Me+2O-2
Me0 +H2 → Me+2H2
Me0 +Cl02 → Me+2Cl2
Me0 +S0 → Me+2S-2
Me0 +2HCl → Me+2Cl2 + H2
Me0 +2HOH → Me+2(OH)2 +Н2
8.
Проверка знанийСравните атомы элементов, поставив знаки <, > или =
вместо *:
а) заряд ядра: Mg * Ca, Na *Mg, Ca * К;
б) число электронных слоев: Mg * Ca, Na * Mg,
Ca * К;
в) число электронов на внешнем уровне: Mg * Ca, Na *Mg,
Ca * К;
г) радиус атома: Mg * Ca, Na * Mg, Ca * K;
д) восстановительные свойства: Mg * Ca, Na * Mg,
Ca * K.
9.
Домашнее задание:П. 31 (до соединений), упр. 1, 2








 Химия
Химия








