Похожие презентации:
Уравнение состояния идеального газа
1.
Уравнение состоянияидеального газа.
2.
Клапейрон Бенуа Поль Эмиль(1799–1864)
французский физик и инженер.
Родился 26 января 1799 в Париже.
Окончил Политехническую школу
(1818). Работал в Институте инженеров
путей сообщения в Петербурге (1820–
1830). По возвращении во Францию
стал профессором Школы мостов и
дорог в Париже.
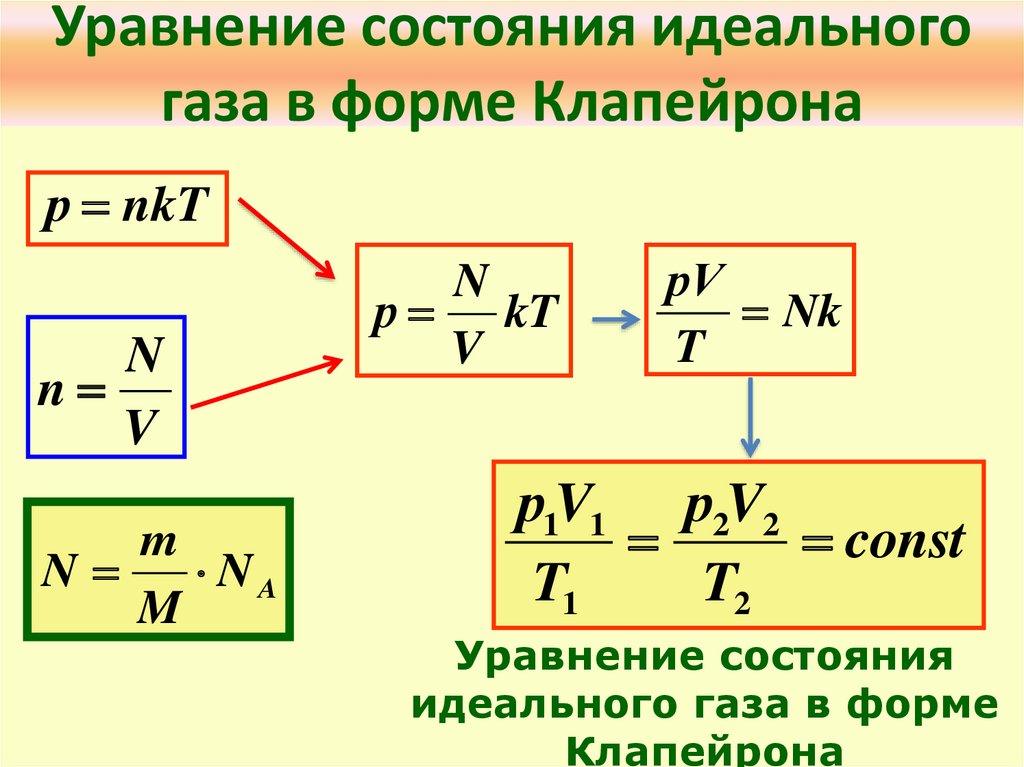
3. Уравнение состояния идеального газа в форме Клапейрона
р nkTN
n
V
m
N
NA
M
N
р kT
V
рV
Nk
T
р1V1 р2V2
const
T1
T2
Уравнение состояния
идеального газа в форме
Клапейрона
4.
Менделеев Дмитрий Иванович(8.II.1834–2.II.1907)
• Обобщив уравнение
Клапейрона,
в 1874 вывел общее
уравнение состояния
идеального газа
5.
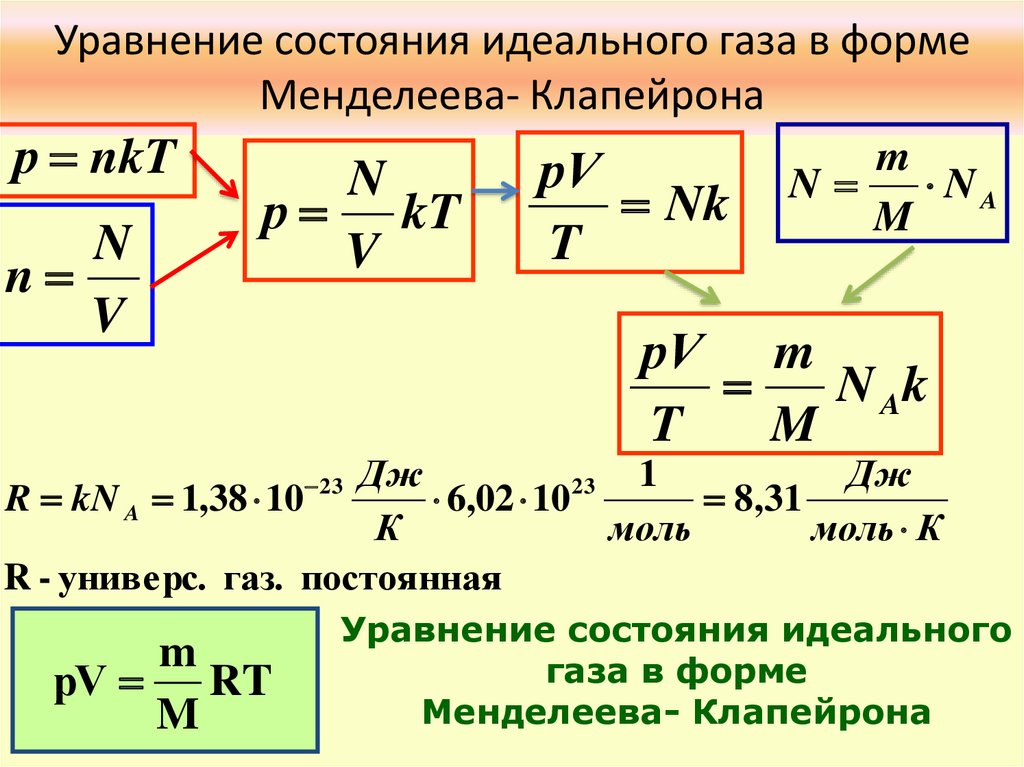
Уравнение состояния идеального газа в формеМенделеева- Клапейрона
р nkT
N
n
V
N
р kT
V
рV
Nk
T
m
N
NA
M
рV m
N Ak
T
M
Дж
1
Дж
23
R kN A 1,38 10
6,02 10
8,31
К
моль
моль К
R - универс. газ. постоянная
23
m
рV RT
M
Уравнение состояния идеального
газа в форме
Менделеева- Клапейрона
6. Практическое применение уравнения состояния:
1. В термометрах…• Уравнение позволяет
определить одну из
величин, характеризующих
состояние, если известны
две другие величины
• Это используют в
термометрах
7. 2. В газовых законах…
• Зная уравнениесостояния, можно
сказать, как протекают
в системе процессы
при определённых
внешних условиях
8. 3. В молекулярной физике…
• Зная уравнениесостояния, можно
определить, как
меняется состояние
системы, если она
совершает работу или
получает теплоту от
окружающих тел
9. Определите температуру кислорода массой 1,6 кг, находящегося в сосуде объёмом 0,0831 м3 при давлении 2 • 106 Па.
Пример решения задач.Определите температуру кислорода массой 1,6 кг,
находящегося в сосуде объёмом 0,0831 м3 при давлении 2
106 Па.
1. Дано:
V = 0,0831 м3,
m = 1,6 кг,
M(O2) = 32 • 10–3 кг/моль,
p = 2 • 106 Па.
_______________
T–?
Решение:
10.
Д/з.1. Конспект.
2. Задачи для самостоятельного решения:
1. Определите температуру кислорода массой 64 г,
находящегося в сосуде объёмом 1 л при
давлении 5•106 Па.
2. Определите плотность азота при температуре 300
К и давлении 2 атм. (Молярная масса азота М =
0,028 кг/моль).








 Физика
Физика








