Похожие презентации:
ЕГЭ - 2017. Химия. Задания части II
1.
ЕГЭ - 2017ХИМИЯ
Задания части II
№30 «ОВР»
Дистанционные консультации и задания для самоподготовки
обучающихся 9 и 211 классов
Учитель- Овчарова Ольга Эдуардовна
Санкт-Петербург
2016
2.
ИСПОЛЬЗУЯ МЕТОД ЭЛЕКТРОННОГО БАЛАНСА,СОСТАВТЕ УРАВНЕНИЯ РЕАКЦИЙ.
ОПРЕДЕЛИТЕ ОКИСЛИТЕЛЬ И ВОССТАНОВИТЕЛЬ.
1. H2SO4 + Zn = H2S + ZnSO4 + H2O
2. Ca3(PO4)2 + AI = Ca3Р2 + AI2O3
3. H2SO4 + C = SO2 + CO2 + H2O
4. H2S +K2Cr2O7+ H2SO4 =S +K2SO4 + Cr2(SO4)3 + H2O
5. SO2 + I2 + H2O = H2SO4 + HI
6. H2S + HNO3 = H2SO4 +NO2 + H2O
7. NO +K2Cr2O7 +H2SO4= HNO3 +Cr2(SO4)3+K2SO4+H2O
8. FeSO4 + H2O2 + H2SO4 = Fe2(SO4)3 + H2O
9. MnSO4+NaCIO +NaOH=MnO2+ NaCI+ Na2SO4+H2O
10. KMnO4 + HCI = KCI + MnCI2 + CI2 + H2O
11. KCIO3 + P = KCI + P2O5
12. KCIO3 = KCI + O2
13. KCIO3 = KCI + KCIO4
3.
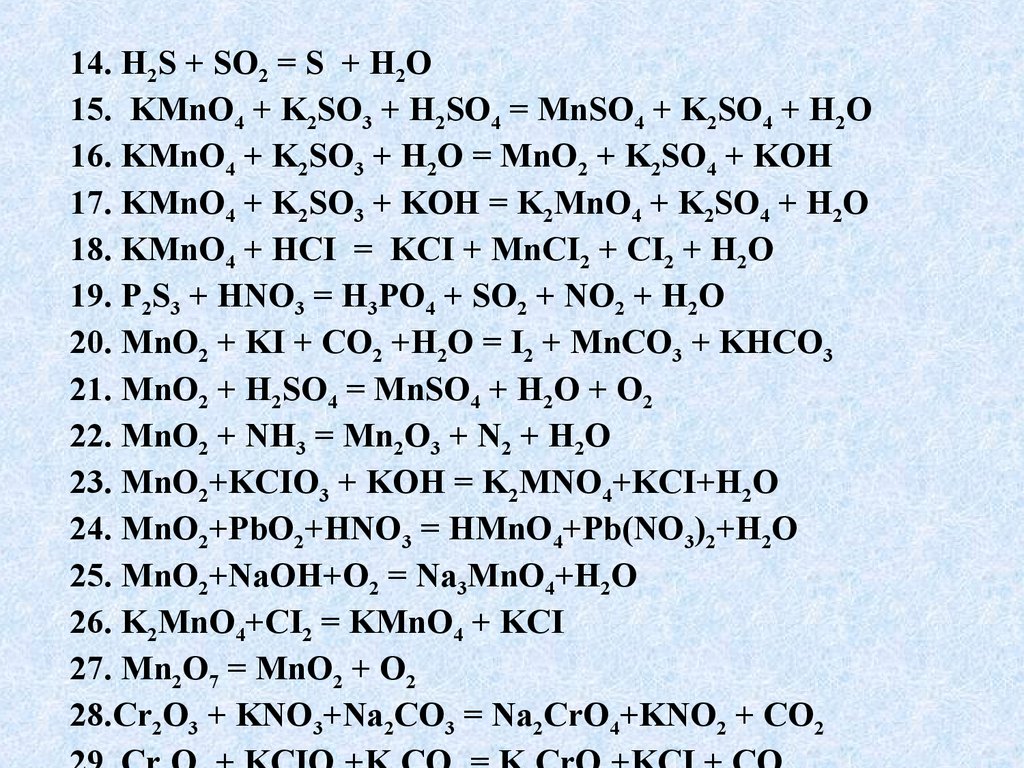
14. H2S + SO2 = S + H2O15. KMnO4 + K2SO3 + H2SO4 = MnSO4 + K2SO4 + H2O
16. KMnO4 + K2SO3 + H2O = MnO2 + K2SO4 + KOH
17. KMnO4 + K2SO3 + KOH = K2MnO4 + K2SO4 + H2O
18. KMnO4 + HCI = KCI + MnCI2 + CI2 + H2O
19. P2S3 + HNO3 = H3PO4 + SO2 + NO2 + H2O
20. MnO2 + KI + CO2 +H2O = I2 + MnCO3 + KHCO3
21. MnO2 + H2SO4 = MnSO4 + H2O + O2
22. MnO2 + NH3 = Mn2O3 + N2 + H2O
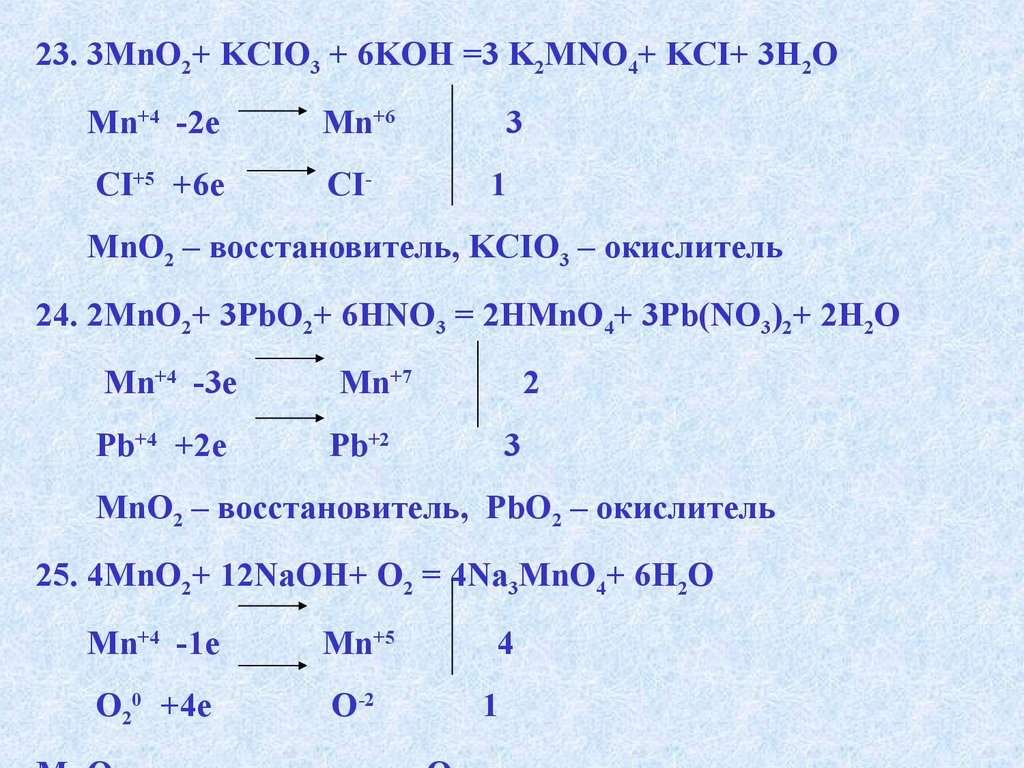
23. MnO2+KCIO3 + KOH = K2MNO4+KCI+H2O
24. MnO2+PbO2+HNO3 = HMnO4+Pb(NO3)2+H2O
25. MnO2+NaOH+O2 = Na3MnO4+H2O
26. K2MnO4+CI2 = KMnO4 + KCI
27. Mn2O7 = MnO2 + O2
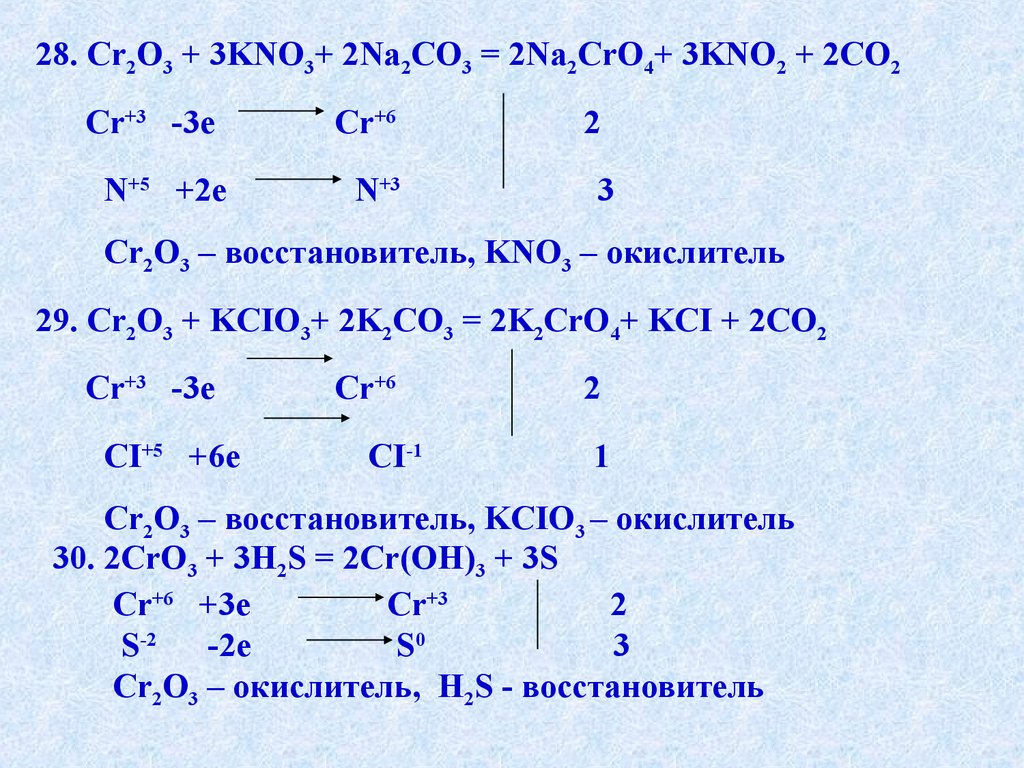
28.Cr2O3 + KNO3+Na2CO3 = Na2CrO4+KNO2 + CO2
4.
ЕГЭ - 2017ХИМИЯ
БЛОК ЗАДАНИЙ №30
(ПРАВИЛЬНЫЕ РЕШЕНИЯ)
5.
ИСПОЛЬЗУЯ МЕТОД ЭЛЕКТРОННОГО БАЛАНСА,СОСТАВТЕ УРАВНЕНИЯ РЕАКЦИЙ.
ОПРЕДЕЛИТЕ ОКИСЛИТЕЛЬ И ВОССТАНОВИТЕЛЬ.
1. 5H2SO4 + 4 Zn = H2S + 4ZnSO4 + 4H2O
Zn0– 2e
Zn+2
4
S+6 + 8e
S-2
1
Zn – восстановитель, H2SO4 - окислитель
2. 3Ca3(PO4)2 + 16AI = 3Ca3Р2 + 8 AI2O3
P+5 + 8e
P-3
3
AI0 - 3e
AI+3
8
AI – восстановитель, Ca3(PO4)2 - окислитель
6.
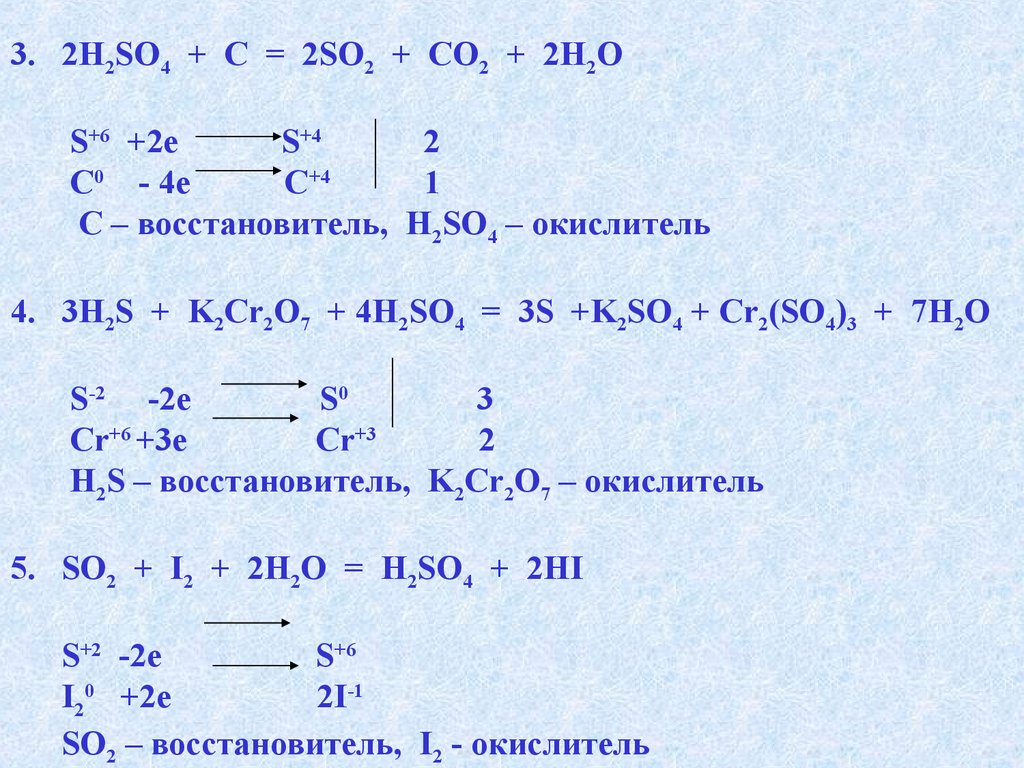
3. 2H2SO4 + C = 2SO2 + CO2 + 2H2OS+6 +2e
S+4
2
C0 - 4e
C+4
1
C – восстановитель, H2SO4 – окислитель
4. 3H2S + K2Cr2O7 + 4H2SO4 = 3S +K2SO4 + Cr2(SO4)3 + 7H2O
S-2 -2e
S0
3
Cr+6 +3e
Cr+3
2
H2S – восстановитель, K2Cr2O7 – окислитель
5. SO2 + I2 + 2H2O = H2SO4 + 2HI
S+2 -2e
S+6
I20 +2e
2I-1
SO2 – восстановитель, I2 - окислитель
7.
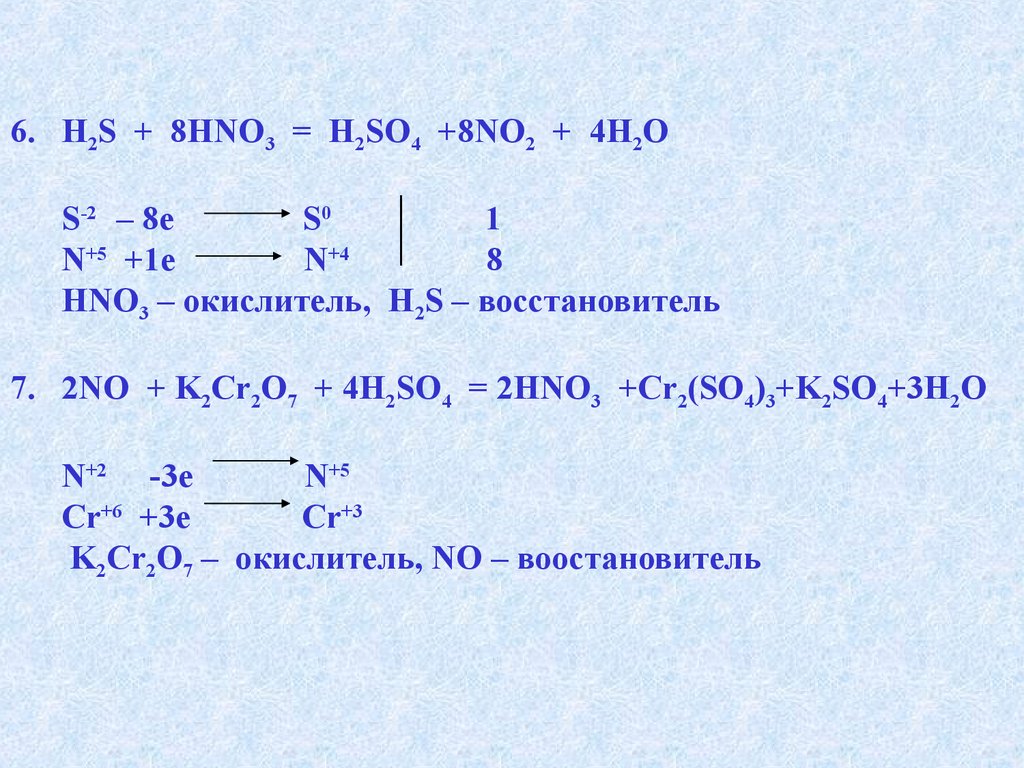
6. H2S + 8HNO3 = H2SO4 +8NO2 + 4H2OS-2 – 8e
S0
1
N+5 +1e
N+4
8
HNO3 – окислитель, H2S – восстановитель
7. 2NO + K2Cr2O7 + 4H2SO4 = 2HNO3 +Cr2(SO4)3+K2SO4+3H2O
N+2 -3e
N+5
Cr+6 +3e
Cr+3
K2Cr2O7 – окислитель, NO – воостановитель
8.
8. 2FeSO4 + H2O2 + H2SO4 = Fe2(SO4)3 + 2H2OFe+2 -1e
Fe+3
O-1 +1e
O-2
H2O2 – окислитель, FeSO4 – восстановитель
9. MnSO4 + NaCIO + 2NaOH = MnO2+ NaCI + Na2SO4 +H2O
Mn+2 -2e
Mn+4
CI+1 +2e
CI-1
MnSO4 – восстановитель, NaCIO - окислитель
9.
10. 2KMnO4 + 16HCI = 2KCI + 2MnCI2 +5CI2 + 8H2OMn+7 +5e
Mn+2
2CI-1
CI2
-2e
2
5
KMnO4 – окислитель, HCI- восстановитель
11. 2KMnO4 + 6P = 5KCI + 3P2O5
CI+5 +6e
P0
-5e
CI-1
5
P+5
6
KMnO4 – окислитель, P - восстановитель
12. 2KCIO3 = 2KCI + 3O2
CI+5 +6e
CI-1
2O-2 -4e
O 20
2
3
10.
13. 4KCIO3 = KCI + 3KCIO4CI+5 +6e
CI-1
1
CI+5 -2e
CI+7
3
KCIO3 – и окислитель, и восстановитель
14. 2H2S + SO2 =3 S + 2H2O
S-2 - 2e
S0
2
S+4 +4e
S0
1
H2S – восстановитель, SO2 - окислитель
15. 2KMnO4 + 5K2SO3 + 3H2SO4 = 2MnSO4 + 6K2SO4 + 3H2O
Mn+7 +5e
Mn+2
2
S+4
S+6
5
-2e
11.
16. 2KMnO4 + 3K2SO3 + H2O =2 MnO2 + 3K2SO4 + 2KOHMn+7 +3e
S+4
-2e
Mn+4
2
S+6
3
KMnO4 – окислитель, K2SO3 – восстановитель
17. 2KMnO4 + K2SO3 + 2KOH = 2K2MnO4 + K2SO4 + H2O
Mn+7 +1e
S+4
-2e
Mn+6
2
S+6
1
KMnO4 – окислитель, K2SO3 – восстановитель
12.
18. 2KMnO4 + 16HCI = 2KCI +2MnCI2 + 5CI2 + 8H2OMn+7 +5e
Mn+2
2
2CI-1 -2e
CI20
5
KMnO4 – окислитель, HC – восстановитель
19*. P2S3 +22HNO3 = 2H3PO4 + 3SO2 + 22NO2 + H2O
2Р+3 -4е
2P+5
4
3S-2 -18e
3S+4
18
N+5 +1e
N+4
1
P2S3 - восстановитель, HNO3 - окислитель
13.
20. MnO2 + 2KI + 3CO2 +H2O = I2 + MnCO3 + KHCO3Mn+4 +2e
Mn+2
2I-1
-2e
I 20
MnO2 – окислитель, KI - восстановитель
21. 2MnO2 + 2H2SO4 = 2MnSO4 + 2H2O + O2
Mn+4 +2e
Mn+2
2
2O-2
-4e
O20
1
MnO2 – окислитель, H2SO4 – восстановитель
22. 6MnO2 +2 NH3 = 3Mn2O3 + N2 + 3H2O
Mn+4 +1e
Mn+3
6
2N-3 -6e
N20
1
MnO2 – окислитель, NH3 - восстановитель
14.
23. 3MnO2+ KCIO3 + 6KOH =3 K2MNO4+ KCI+ 3H2OMn+4 -2e
Mn+6
CI+5 +6e
CI-
3
1
MnO2 – восстановитель, KCIO3 – окислитель
24. 2MnO2+ 3PbO2+ 6HNO3 = 2HMnO4+ 3Pb(NO3)2+ 2H2O
Mn+4 -3e
Pb+4 +2e
Mn+7
2
Pb+2
3
MnO2 – восстановитель, PbO2 – окислитель
25. 4MnO2+ 12NaOH+ O2 = 4Na3MnO4+ 6H2O
Mn+4 -1e
Mn+5
O20 +4e
O-2
4
1
15.
26. 2K2MnO4 + CI2 = 2KMnO4 + 2KCIMn+6 -1e
Mn+7
2
CI20 +2e
2CI-
1
K2MnO4 – восстановитель, CI2 – окислитель
27. 2Mn2O7 = 4MnO2 + 3O2
Mn+7 +3e
Mn+4
4
2О-2 -4e
О 20
3
Mn+7 – окислитель, О-2 - восстановтель
16.
28. Cr2O3 + 3KNO3+ 2Na2CO3 = 2Na2CrO4+ 3KNO2 + 2CO2Cr+3 -3e
N+5 +2e
Cr+6
N+3
2
3
Cr2O3 – восстановитель, KNO3 – окислитель
29. Cr2O3 + KCIO3+ 2K2CO3 = 2K2CrO4+ KCI + 2CO2
Cr+3 -3e
СI+5 +6e
Cr+6
CI-1
2
1
Cr2O3 – восстановитель, KCIO3 – окислитель
30. 2CrO3 + 3H2S = 2Cr(OH)3 + 3S
Cr+6 +3e
Cr+3
2
S-2 -2e
S0
3
Cr2O3 – окислитель, H2S - восстановитель









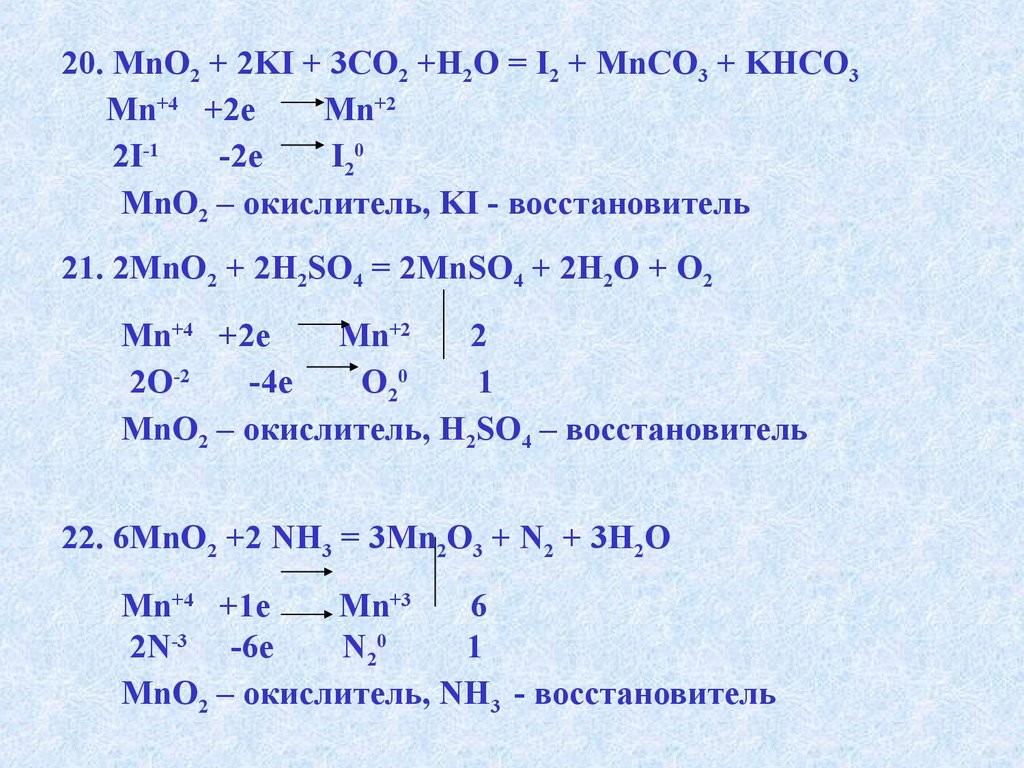

 Образование
Образование








