Похожие презентации:
Электролиз расплавов и растворов
1.
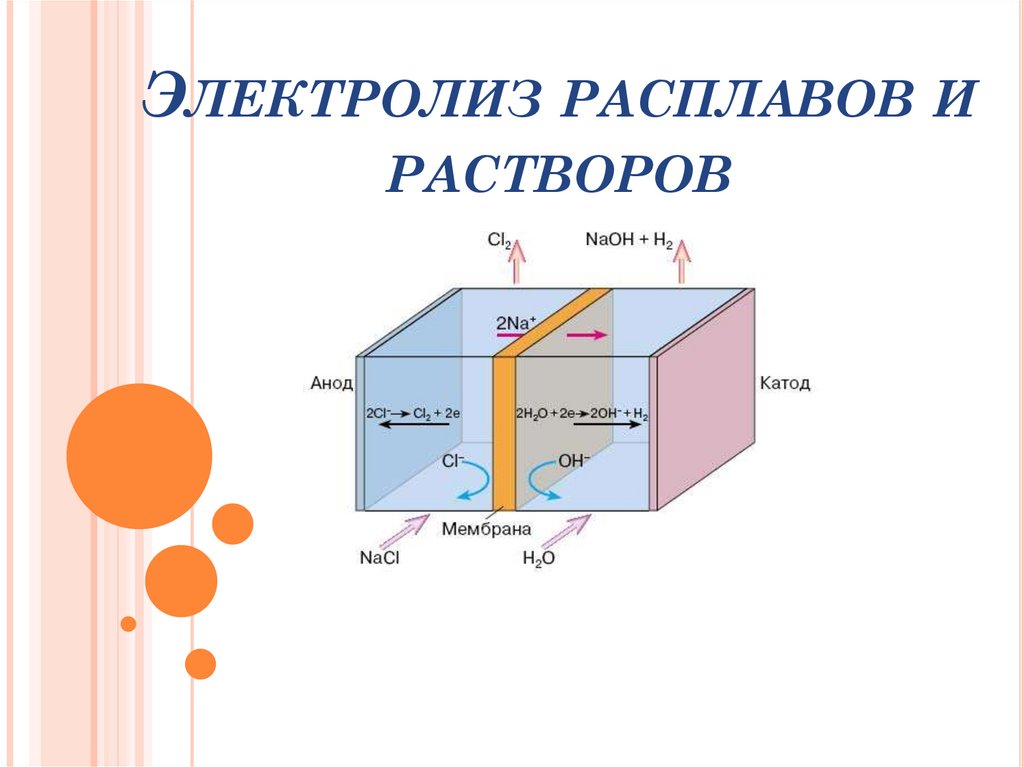
ЭЛЕКТРОЛИЗ РАСПЛАВОВРАСТВОРОВ
И
2.
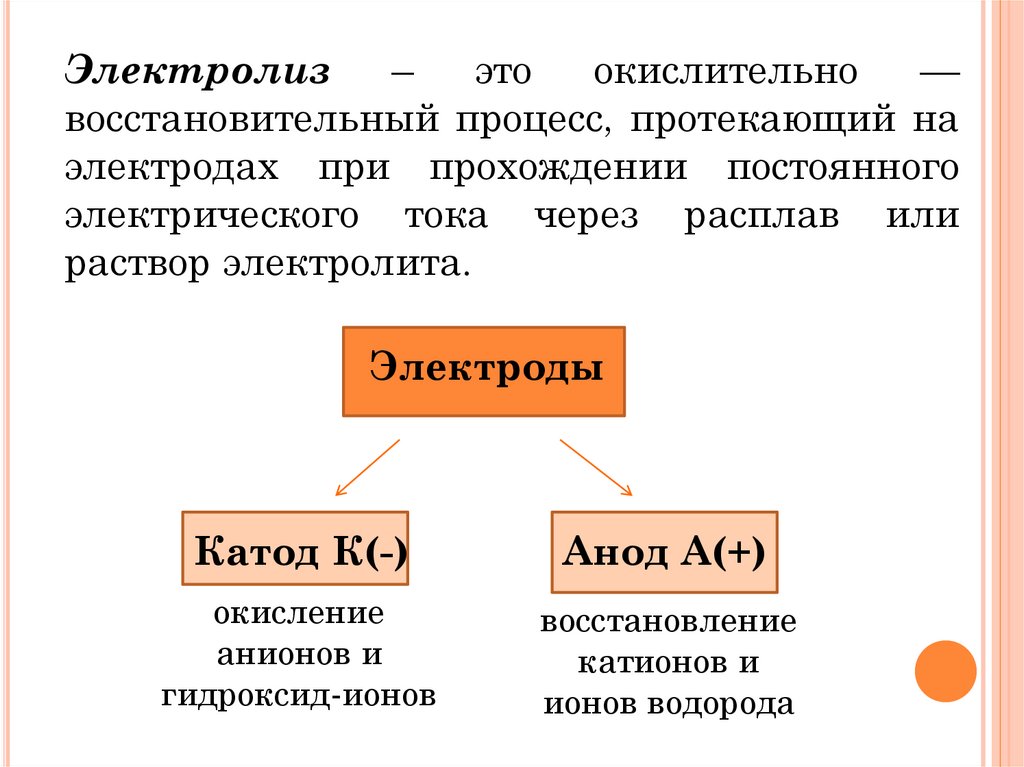
Электролиз–
это
окислительно
—
восстановительный процесс, протекающий на
электродах при прохождении постоянного
электрического тока через расплав или
раствор электролита.
Электроды
Катод К(-)
Анод А(+)
окисление
анионов и
гидроксид-ионов
восстановление
катионов и
ионов водорода
3.
Анод – это положительнозаряженный электродКатод -это отрицательно заряженный электрод
4.
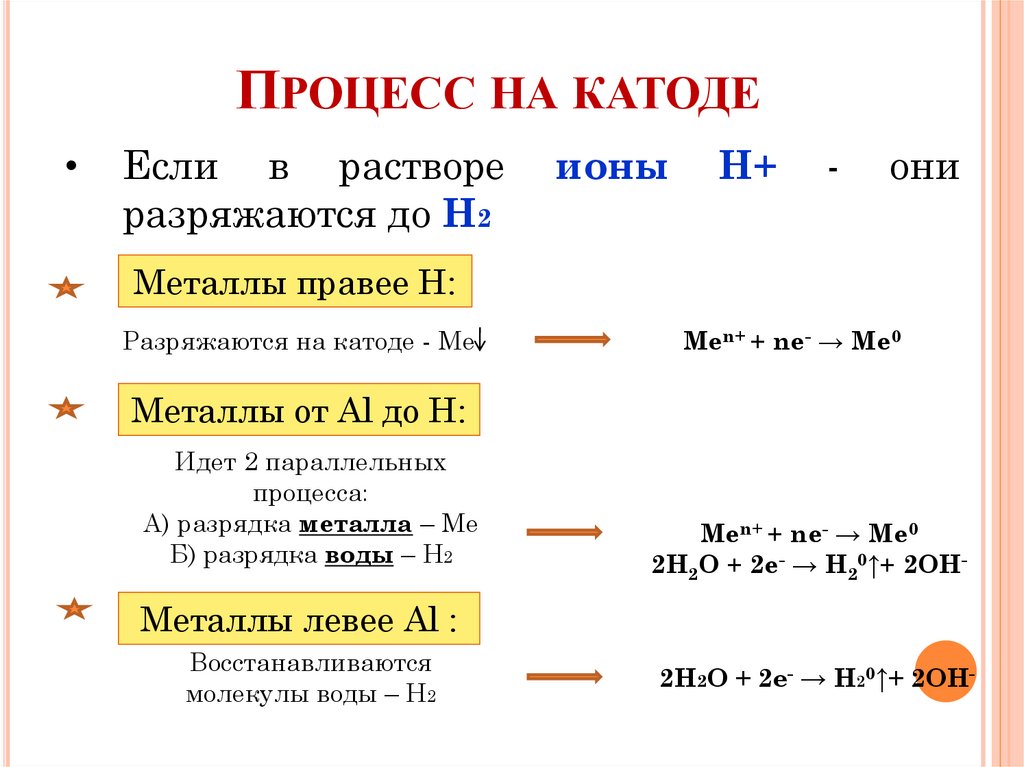
ПРОЦЕСС НА КАТОДЕЕсли в растворе
разряжаются до Н2
ионы
Н+
-
они
Металлы правее Н:
Разряжаются на катоде - Ме
Men+ + ne- → Me0
Металлы от Al до Н:
Идет 2 параллельных
процесса:
А) разрядка металла – Мe
Б) разрядка воды – Н2
Men+ + ne- → Me0
2H2O + 2e- → H20↑+ 2OH-
Металлы левее Al :
Восстанавливаются
молекулы воды – Н2
2H2O + 2e- → H20↑+ 2OH-
5.
ПРОЦЕСС НА АНОДЕесли анод растворяется (железо, цинк,
медь, серебро и все металлы, которые
окисляются в процессе электролиза), то
окисляется металл анода, несмотря на
природу аниона;
6.
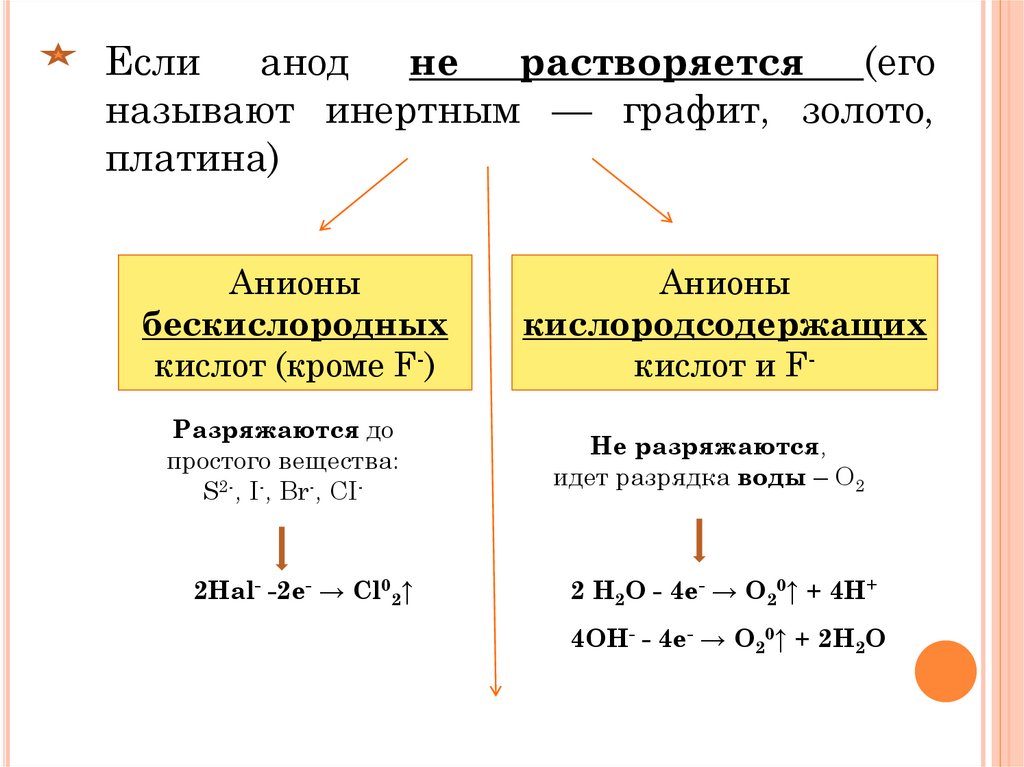
Если анод не растворяется (егоназывают инертным — графит, золото,
платина)
Анионы
бескислородных
кислот (кроме F-)
Разряжаются до
простого вещества:
S2-, I-, Br-, СI-
2Hal- -2e- → Cl02↑
Анионы
кислородсодержащих
кислот и FНе разряжаются,
идет разрядка воды – О2
2 H2O - 4e- → О20↑ + 4H+
4ОН- - 4e- → О20↑ + 2Н2О
7.
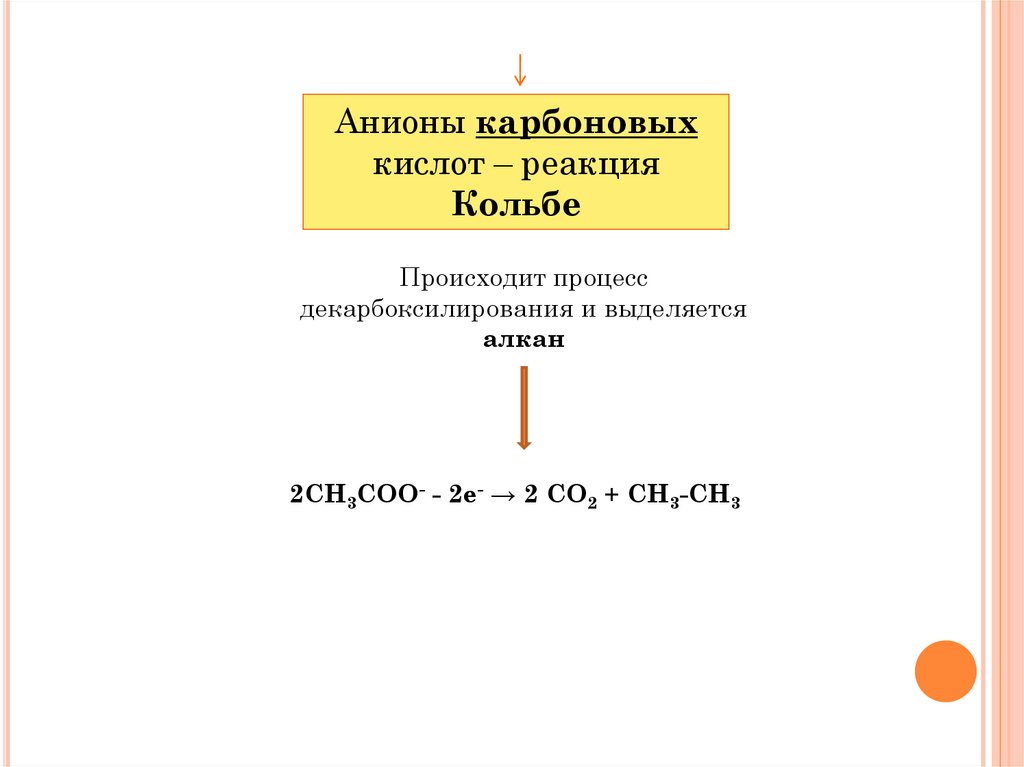
Анионы карбоновыхкислот – реакция
Кольбе
Происходит процесс
декарбоксилирования и выделяется
алкан
2СН3СОО- - 2е- → 2 СО2 + СН3-СН3
8.
1. Анод нерастворимый(например, графитовый)
Пример №1.
Суммарное уравнение:
Учитывая присутствие ионов Na в растворе:
9.
Пример №2.Суммарное ионное уравнение:
Суммарное молекулярное уравнение:
10.
2. Анод растворимый(например, медный)
Если анод растворимый, то металл анода будет окисляться:
Катионы Cu2+ в ряду напряжений стоят после (Н+),
поэтому они и будут восстанавливаться на катоде.
11.
Проверь себя…Задания на
электролиз
12.
Задание 1Установите соответствие между формулой соли и продуктом,
образующимся на катоде при электролизе её водного раствора:
к каждой
позиции,
обозначенной буквой,водного
подберите
При
электролизе
соответствующую позицию, обозначенную цифрой.
раствора хлорида лития (LiCL)
на аноде в результате
ПРОДУКТ НА
ФОРМУЛА СОЛИ
электролиза образуется:
КАТОДЕ
А) CuCl2
Б) AgNO3
В) K2S
Г) NaBr
1) водород
1) хлор 2) кислород
3) металл
2) литий 4) галоген
5) сера
3)
6) азот
кислород
4) водород
13.
Задание 2Установите соответствие между формулой соли и продуктом,
который образуется на инертном аноде в результате электролиза
её водного раствора: к каждой позиции, обозначенной буквой,
подберите соответствующую позицию, обозначенную цифрой.
При электролизе водного
раствора
хлорида ПРОДУКТ
литияНА(LiCL)
ФОРМУЛА СОЛИ
АНОДЕ
на аноде в результате
A) Na2SO4
1) SO2
электролиза
образуется:
3 )2
Б) Ca(NO
2) O2
B) ZnBr2
Г) CuCl2
3) NO2
1) хлор 4) Br2
5) Cl2
2) литий6) H2
3)
кислород
4) водород
14.
Задание 3Установите соответствие между формулой соли и продуктом,
образующимся на катоде при электролизе её водного раствора:
к каждой позиции, обозначенной буквой, подберите
соответствующую позицию, обозначенную цифрой.
ФОРМУЛА СОЛИ
А) RbCl
Б) K2CO3
В) BaBr2
Г) Cu(NO3)2
ПРОДУКТ НА
КАТОДЕ
1) хлороводород
2) оксид азота(IV)
3) кислород
4) хлор
5) бром
6) углекислый газ
15.
Задание 4Установите соответствие между формулой соли и продуктом,
образующимся на катоде при электролизе её водного раствора:
к каждой позиции, обозначенной буквой, подберите
соответствующую позицию, обозначенную цифрой.
ФОРМУЛА СОЛИ
А) Ca(NO3)2
Б) CuSO4
В) Al2(SO4)3
Г) AgNO3
ПРОДУКТ НА КАТОДЕ
1) серебро
2) алюминий
3) медь
4) кальций
5) водород
6) кислород
16.
Задание 5Установите соответствие между веществом и продуктами
его электролиза в растворе или расплаве: к каждой позиции,
обозначенной буквой, подберите соответствующую позицию,
обозначенную цифрой.
ВЕЩЕСТВО
А) KCl (водный раствор)
Б) NaCl (расплав)
В) KNO3(водный
раствор)
Г) Cu(NO3)2 (водный
раствор)
ПРОДУКТЫ ЭЛЕКТРОЛИЗА
1) Na, Cl2
2) K , NO2, O2
3) H2, Cl2, KOH
4) Cu, O2, HNO3
5) H2, O2
6) Cu, NO2, H2
17.
Задание 6Вычислите объём в литрах газа, выделяющегося
на
аноде
при
электролизе
водного
раствора
гидроксида кальция с инертными электродами, если
на катоде выделился газ объемом 67,2 л (при н.у.).
18.
Задание 7Какая масса (в граммах) гидроксида лития образуется
в растворе при электролизе водного раствора хлорида
лития с инертными электродами с инертными
электродами, если на аноде выделяется 10,08 л газа
(н.у.)?
19.
Задание 8Какая масса газа выделится на аноде (в граммах) при
полном электролизе 320 г 10 %-го водного раствора
сульфата меди?














 Химия
Химия








