Похожие презентации:
Физические и химические свойства алкинов
1.
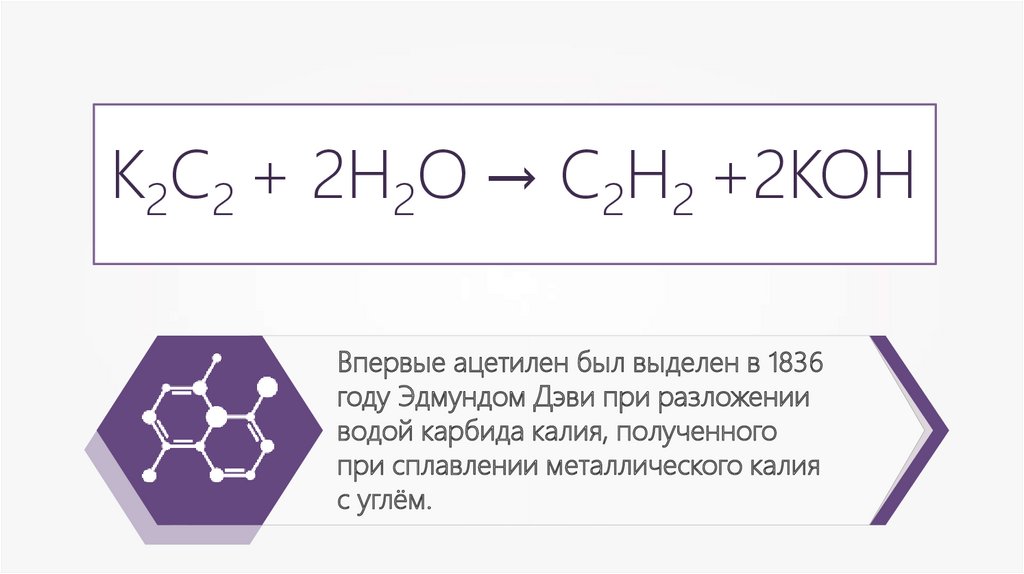
К2С2 + 2Н2О → С2Н2 +2КОНВпервые ацетилен был выделен в 1836
году Эдмундом Дэви при разложении
водой карбида калия, полученного
при сплавлении металлического калия
с углём.
2.
В 1860 г. Марселен Бертловпервые получил ацетилен
в разряде дуги между
угольными электродами
в атмосфере водорода.
М. Бертло
1827–1907 гг.
3.
Свойстваацетилена
Способность
реагировать
с хлором
Растворимость
в воде
Плотность
Горение на воздухе
коптящим пламенем
4.
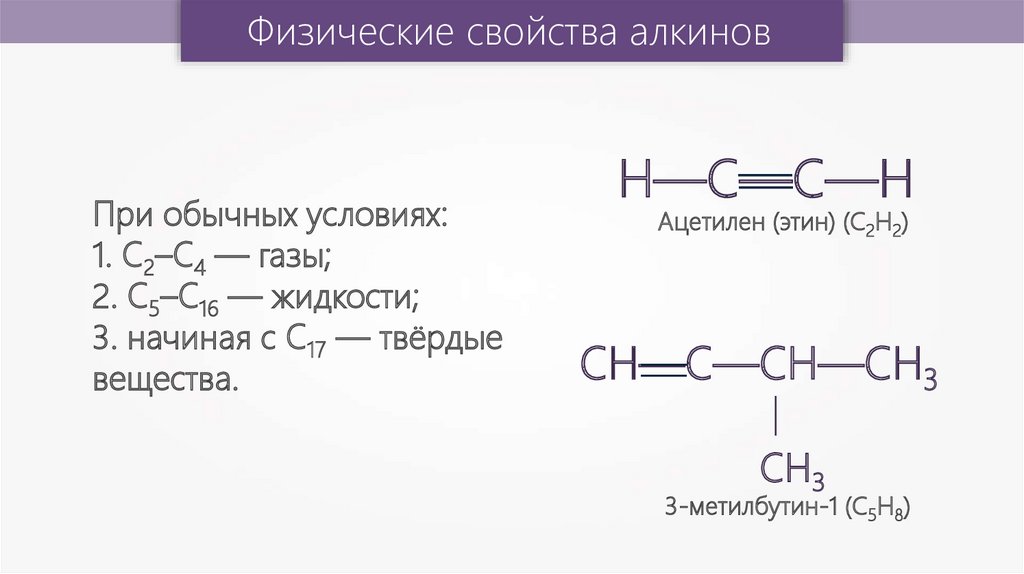
Физические свойства алкиновАцетилен (этин) (С2Н2)
—
СН—С—СН—СН
—
3
—
При обычных условиях:
1. С2–С4 — газы;
2. C5–C16 — жидкости;
3. начиная с C17 — твёрдые
вещества.
—
Н—С—С—Н
—
СН3
3-метилбутин-1 (С5Н8)
5.
Физические свойства алкиновНазвание
Формула
t пл °С
t кип °С
Ацетилен (этин)
HC≡CH
-81,8
-84,0
НС≡С—СН3
-101,5
-23,2
НС≡С—С2Н5
-125,7
+8,1
Метилацетилен
(пропин)
Этилацетилен
(бутин-1)
6.
Физические свойства алкиновРастворимость низших алкинов
в воде несколько выше,
чем алкенов и алканов, однако
она всё же очень мала. Алкины
хорошо растворимы
в неполярных органических
растворителях.
—
СН—С—СН
—
2—СН3
Этилацетилен (бутин-1)
—
СН3—С—С—СН
—
3
Диметилацетилен (бутин-2)
7.
Химические свойства алкиновАлкины способны вступать
в реакции присоединения,
замещения, полимеризации
и окисления.
—
СН—С—СН
—
2—СН3
Этилацетилен (бутин-1)
—
НС—С—СН
—
3
Пропин
8.
Реакция гидрирования+Н2
+Н2
—
—
→ CH3—CH2—СН3
НC—С—СН
—
t, Ni CH2—CH—СН3 t, Ni
3→
9.
Реакция галогенирования+Br
+Br
—
—
НC—СН
→ Br2HC—CHBr2
— → BrHC—СНBr
2
2
1,2-дибромэтен
1,1,2,2-тетрабромэтан
10.
Химические свойства алкиновУглеродные атомы в молекулах
алкинов расположены ближе
друг к другу, чем в алкенах, и
обладают большей
электроотрицательностью.
—
СН—С—СН
—
2—СН3
Этилацетилен (бутин-1)
—
НС—С—СН
—
3
Пропин
11.
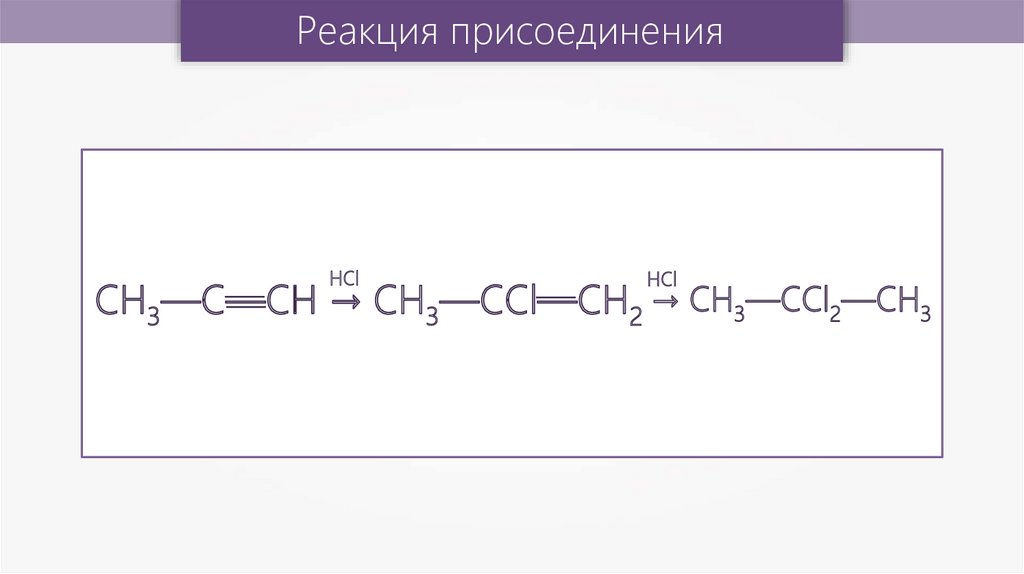
Реакция присоединенияHCl
HCl
—
— 2 → CH3—CСl2—СН3
CH3—C—СН
→ CH3—CСl—СН
—
12.
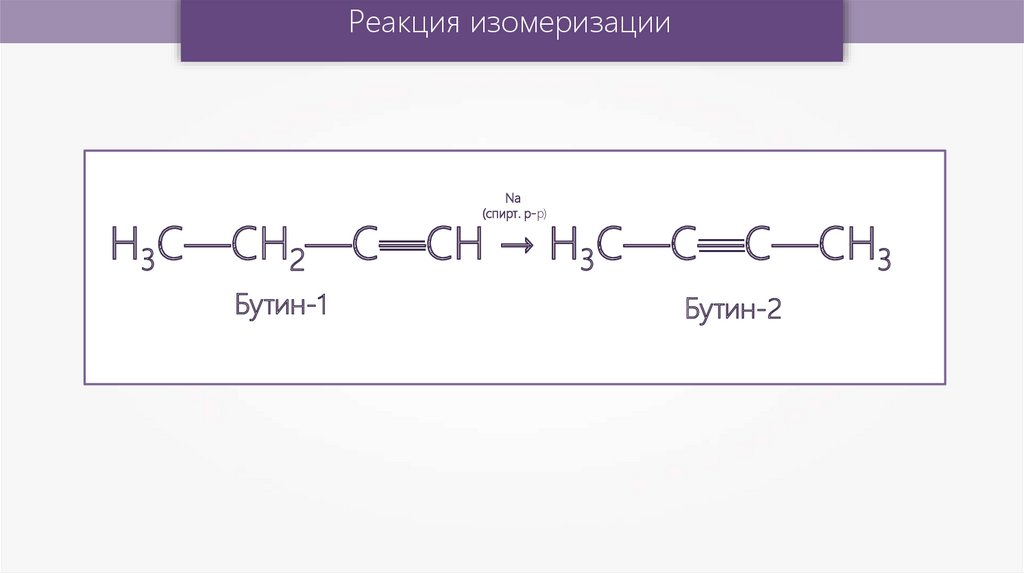
Реакция изомеризацииNa
(спирт. р-р)
—
—
Н3С—CН2—С—СН
→ H3C—С—С—CH
—
3
Бутин-1
Бутин-2
13.
Ацетилен в зависимостиот условий реакции способен
образовывать различные
продукты полимеризации —
линейные или циклические.
14.
Реакция полимеризации—
—
—
— 2
НС—CН
+ НС—СН
→ HC—СН—СН—CH
—
—
Cu2Cl2
Винилацетилен
15.
Реакция полимеризацииt °С
—
—
—
3НС—CН
→ CН2—СН—С—CH—3С
—
—
2Н 2 →С6Н6
Бензол
16.
Doudnick_ValУксусная кислота
Синтетический
каучук
Перчатки
из поливинилхлорида
Растворитель
17.
Кислородно-ацетиленовоесоединение используют
для сварки металлов.












 Химия
Химия








