Похожие презентации:
Бензол молекуласында байланыстардың түзілу сызбанұсқасы
1.
Қостанай облысыЖангелдин ауданы
Аралбай ауылы
Жангелдин орта
мектебінің
Химия-биология
пәні мұғалімі
Естайлақ Ақгүл
Абусағитқызы
2.
3. Ашылу тарихы
Бензолды алғаш алғаннеміс химигі Иоганн
Глаубер. Ол 1649 жылы
бұл қосылысты таскөмір қосылысын айдау
кезінде алды.Бірақ
қосылыстың аты да,
құрылысы да белгісіз
болды.
4. Екінші рет ашылуы
Бензолды 1825 ж.М.Фарадей жарық
газын зерттей
отырып, соның
құрамынан тапқан.
5. Жаңадан алынуы
Неміс физико-химигіЭйльгард Митчерлих 1834 ж.
бензой қышқылын құрғақ
айдау арқылы бензолды алған.
Осыдан бензол атауы шыққан.
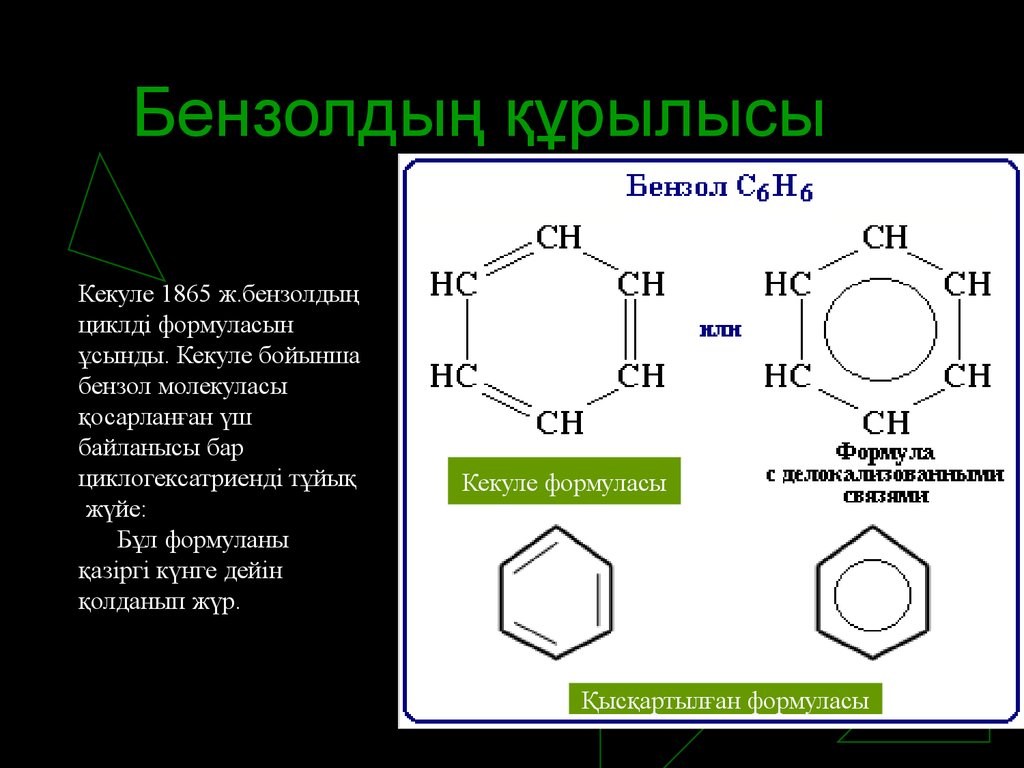
6. Бензолдың құрылысы
Кекуле 1865 ж.бензолдыңциклді формуласын
ұсынды. Кекуле бойынша
бензол молекуласы
қосарланған үш
байланысы бар
циклогексатриенді тұйық
жүйе:
Бұл формуланы
қазіргі күнге дейін
қолданып жүр.
Кекуле формуласы
Қысқартылған формуласы
7. Бензол молекуласында байланыстардың түзілу сызбанұсқасы
8. Квантомеханикалық теория және бензол молекуласы
Немісхимигі Э. Хюккель ароматтық
қосылыстарға квантомеханикалық
теорияны қолданып бензолдың алты пэлектроны кеңістікте орналасып, тұйық
электрон бұлты пайда болатынын
көрсетті
9. Физикалық қасиеттері
Бензолдың гомлогтық қатарының төменгі өкілдері, негізіненсұйықтық болады.Оның молекулалық массасы өскен сайын
қайнау температурасы да, артады, орта-изомерлер, әдетте,
пара-изомерлерге қарағанда жоғары температурада
қайнайды.
Бензолдың қайнау температурасы (80,10С) гексанның қайнау
температурасынан (68,80С) жоғары.
Симметриялы құрылысты изомерлердің балқу температурасы
жоғарырақ болып келеді. Екі орынбасарлары изомерлердің
ішінде-пара-изомер ең жоғары температурада балқиды.
Май қатары мен алициклді қатар көмірсутектерден
тығыздығы және жарық сындыру көрсеткіштері анағұрлым
жоғары.
Бензол қатарындағы ароматты көмірсутектер судан жеңіл,
суда ерімейді, ал көптеген органикалық еріткіштерде жақсы
ериді.Олардың буымен ұзақ уақыт тыныс алғанда адам
уланады.
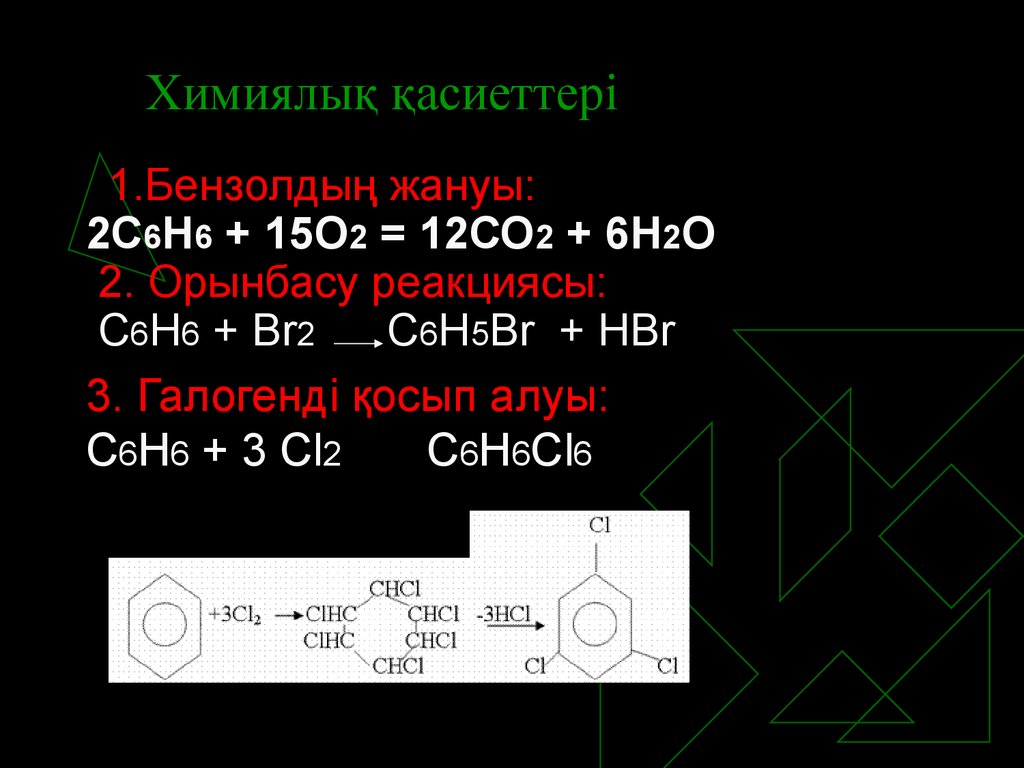
10. Химиялық қасиеттері
1.Бензолдың жануы:2С6Н6 + 15О2 = 12СО2 + 6Н2О
2. Орынбасу реакциясы:
С6Н6 + Br2
C6H5Br + HBr
3. Галогенді қосып алуы:
С6Н6 + 3 Cl2
C6H6Cl6
11.
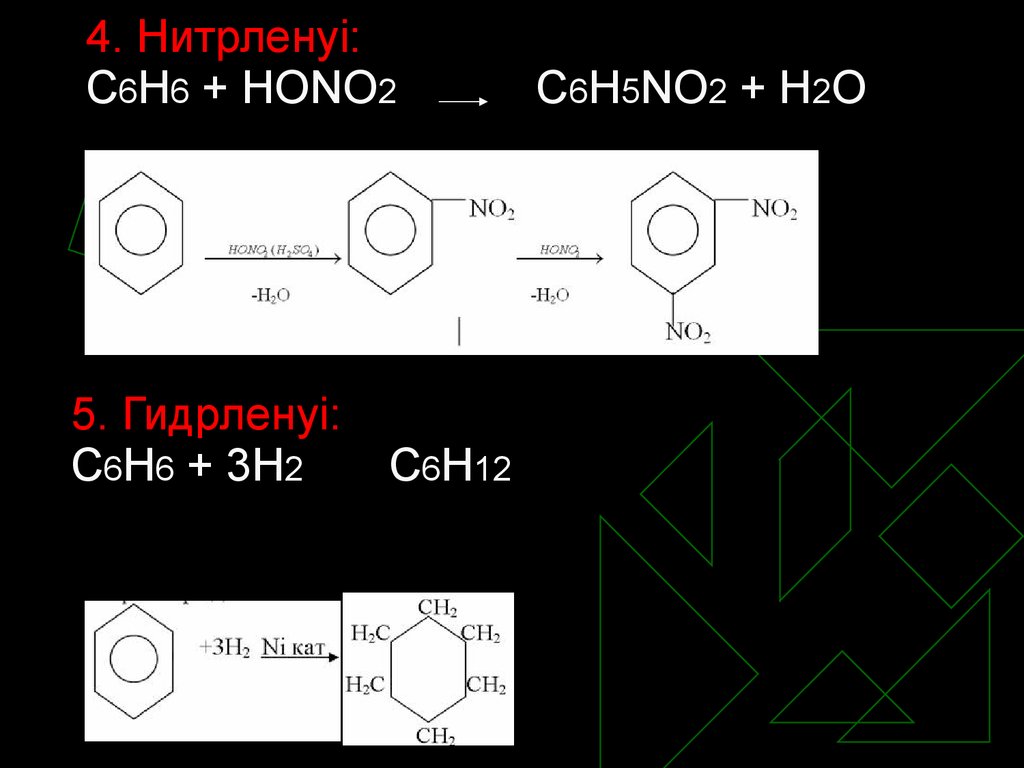
4. Нитрленуі:С6Н6 + НОNО2
5. Гидрленуі:
С6Н6 + 3Н2
С6Н12
С6Н5NО2 + Н2О
12. Алынуы
Бензолдытас көмір шайырын
айдап алады
Қазіргі уақытта бензолды
мұнайдан алады.
Бензолды жасанды жолмен алады
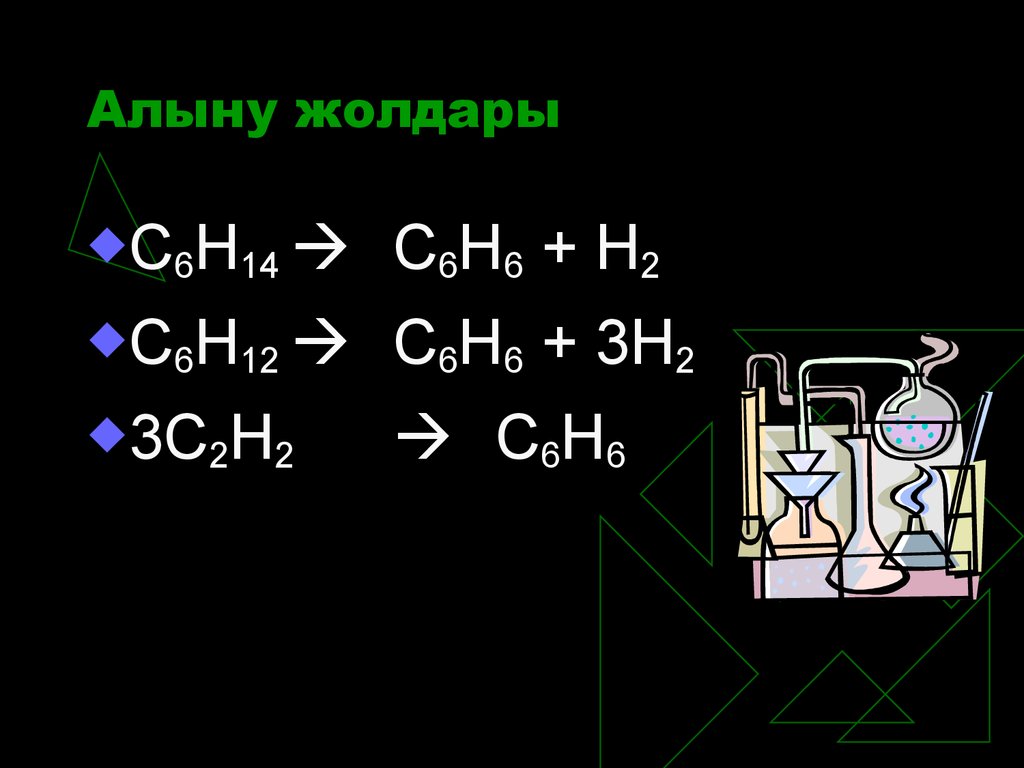
13. Алыну жолдары
С6Н14С 6 Н 6 + Н2
С6Н12
С6Н6 + 3Н2
3С2Н2
С 6Н 6
14. Табиғи шикізаттары:
Табиғижәне серік газдар
Мұнай
Тас
көмір










 Химия
Химия








