Похожие презентации:
Спирттер және фенолдар
1.
Семей қаласы. Медициналық колледж«Авиценна»
Тақырыбы: Спирттер және фенолдар
Орындаған :Талантқызы Мадина
Л-202 топ студенті.
Тексерген:Туменбаева Н.С.
2018-2019жыл.
2. Жоспар.
І. Кіріспе;ІІ. Негізгі бөлім:
Спирттердің жіктелуі, қасиеттері,қолданылуы.
Фенолдардың қасиеттері,алынуы,қолданылуы.
ІІІ. Қорытынды;
ІV. Пайдаланылған әдебиеттер.
3. Спирттер
СnH2n+1OHСпирттер - малекулаларында көмірсутек
радикалымен байланысқан (ОН) гидроксил
тобы бар заттар.
4.
Алыну жолдарыШарап спирті немесе этил спиртінің формуласы-С2Н5ОН
Этил спиртін әртүрлі жолдармен алады. Соның біріглюкозадан ашытқы қатысында мына жалпы реакция
бойынша алады: С6Н12О6
2С2Н5ОН+ 2СО2
5.
TitleAdd your text
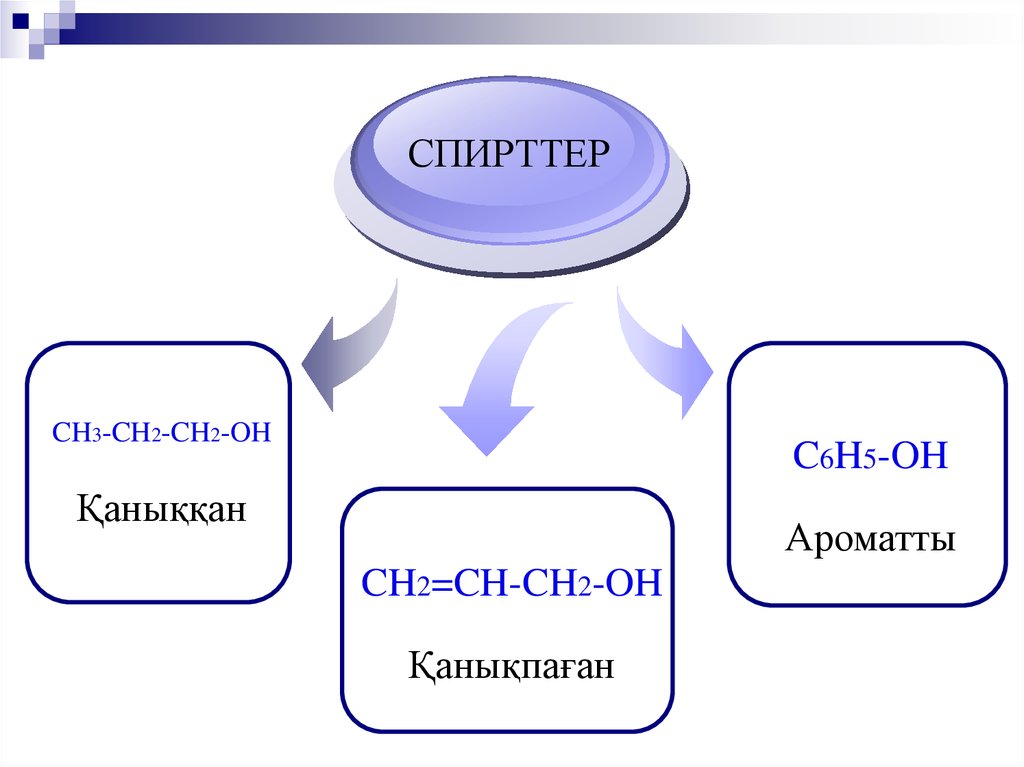
СПИРТТЕР
CH3-CH2-CH2-OH
C6H5-OH
Қаныққан
Ароматты
CH2=CH-CH2-OH
Қанықпаған
6. Спирттердің жіктелуі
Гидроксил тобымен байланысқан көмірсутекрадикалына байланысты
гидроксил тобының саңына байланысты
гидроксил тобымен байланысқан көміртек
атомының табиғатына байланысты
7.
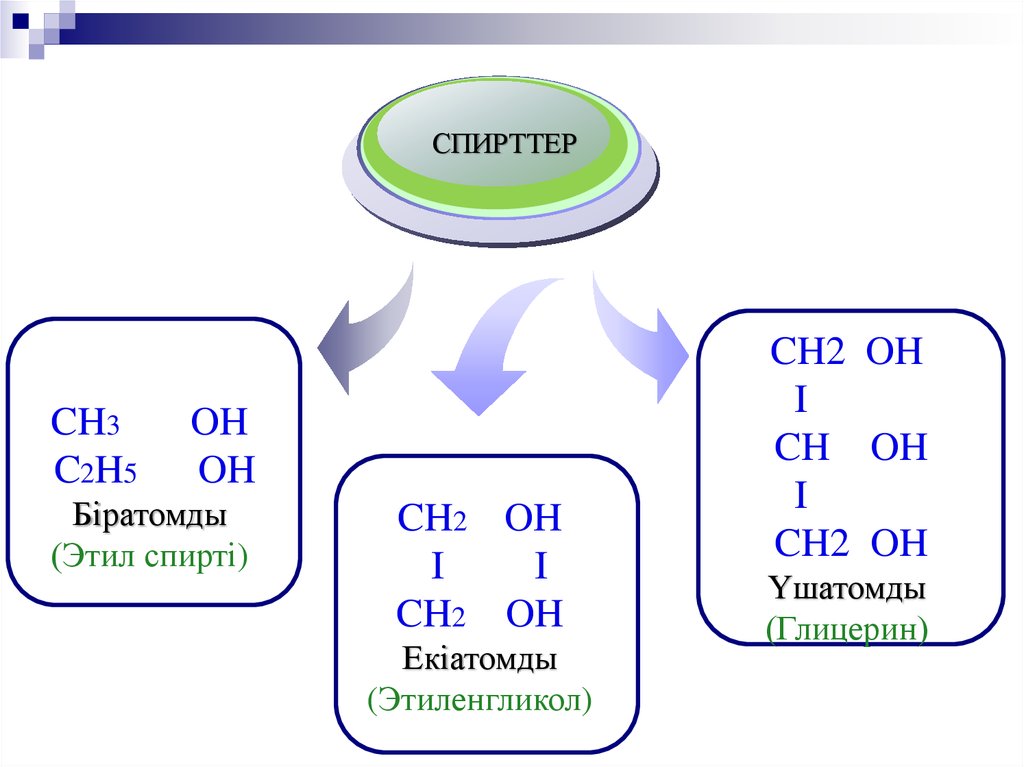
TitleСПИРТТЕР
Add your text
CH3
C2H5
OH
OH
Біратомды
(Этил спирті)
CH2 OH
I
I
CH2 OH
Екіатомды
(Этиленгликол)
CH2 OH
I
CH OH
I
CH2 OH
Үшатомды
(Глицерин)
8.
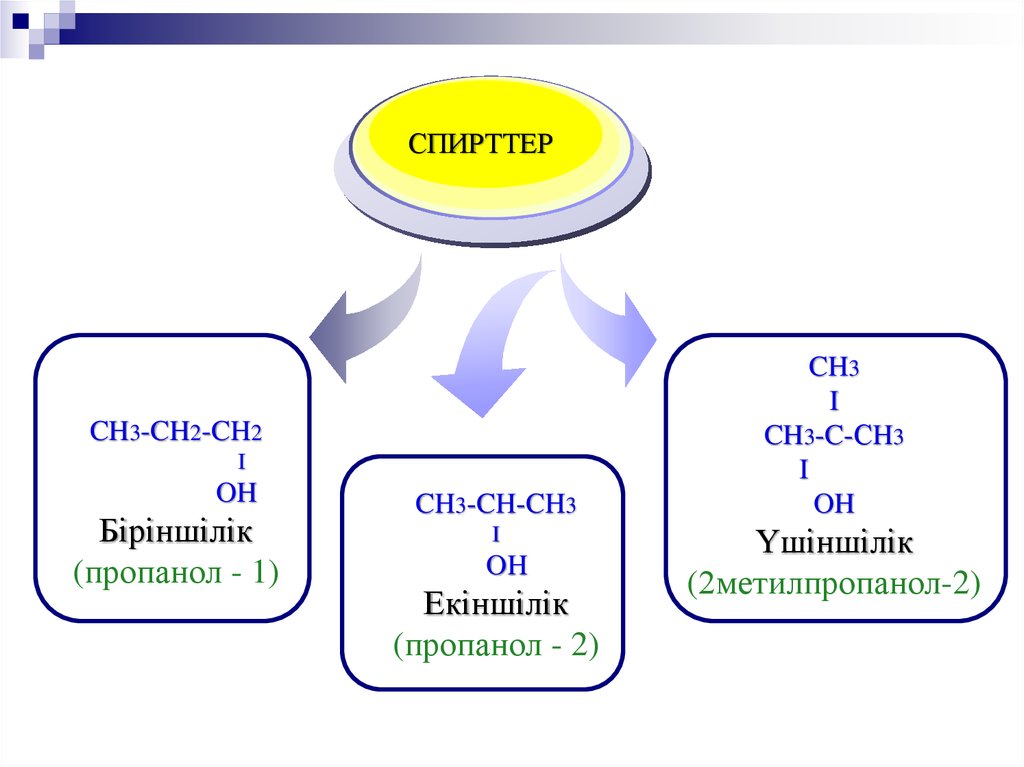
TitleСПИРТТЕР
Add your text
CH3-CH2-CH2
I
OH
Біріншілік
(пропанол - 1)
CH3-CH-CH3
I
OH
Екіншілік
(пропанол - 2)
CH3
I
CH3-C-СH3
I
OH
Үшіншілік
(2метилпропанол-2)
9. Спирттердің гомологтық қатары
Метил спиртіCH3-OH - метанол
Этил спирті
C2H5-OH - этанол
Пропил спирті
СН3-СН2-СН2-ОН - пропанол
Бутил спирті
СН3-СН2-СН2-СН2-ОН - бутанол
Спирттердің жалпы формуласы CnH2n+1OH
Жүйелік номенклатура бойынша спирттерге «ол» деген
жүрнақ қосылады
10. Спирттердің физикалық қасиеттері
Қалыпты температурада С10- ға дейінгіспирттер сұйық заттар, С11-ден бастап қатты
заттар. Алғашқы үшеуі сұйық спирттер
өздеріне тән иісі болады, ал бутанол мен
пентанолдың иістері жағымсыз.
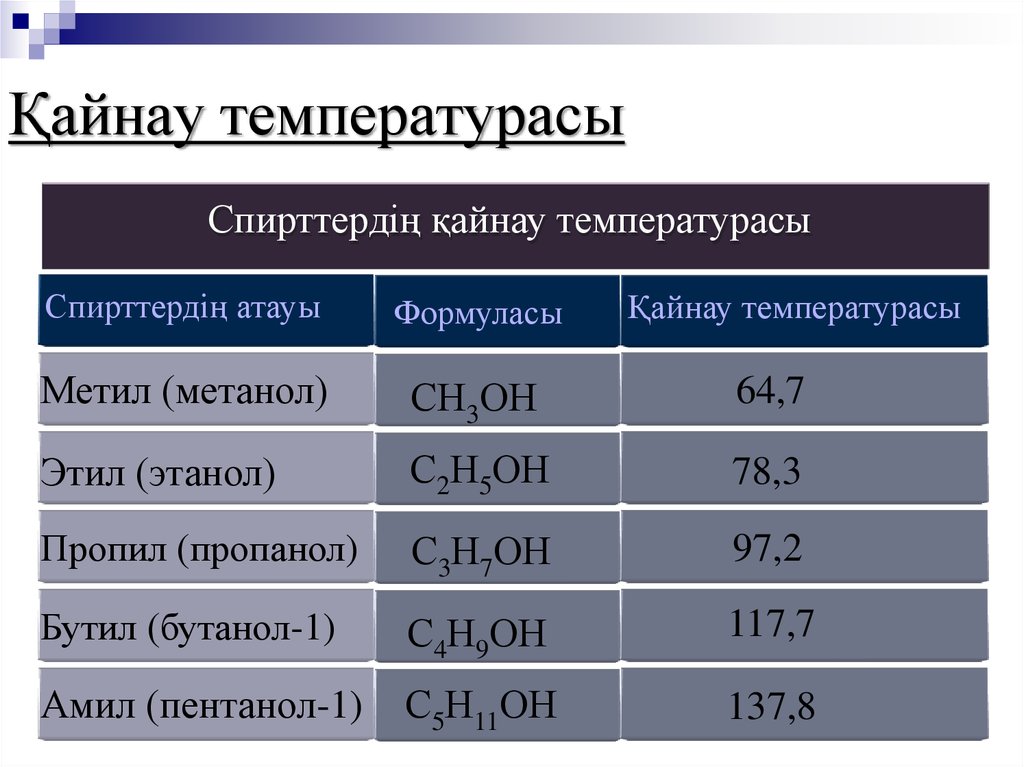
11. Қайнау температурасы
Спирттердің қайнау температурасыСпирттердің атауы
Формуласы
Метил (метанол)
СН3ОН
64,7
Этил (этанол)
С2Н5ОН
78,3
Пропил (пропанол)
С3Н7ОН
97,2
Бутил (бутанол-1)
С4Н9ОН
117,7
Амил (пентанол-1)
С5Н11ОН
137,8
Қайнау температурасы
12. Спирттердің химиялық қасиеттері
Спирттердін химиялыққасиеттерін анықтайтың
гидроксил тобы және ол
байланысқан
радикалдардың
құрылысы.
Спирттерге қышқылды–
негіздік қасиет тәң
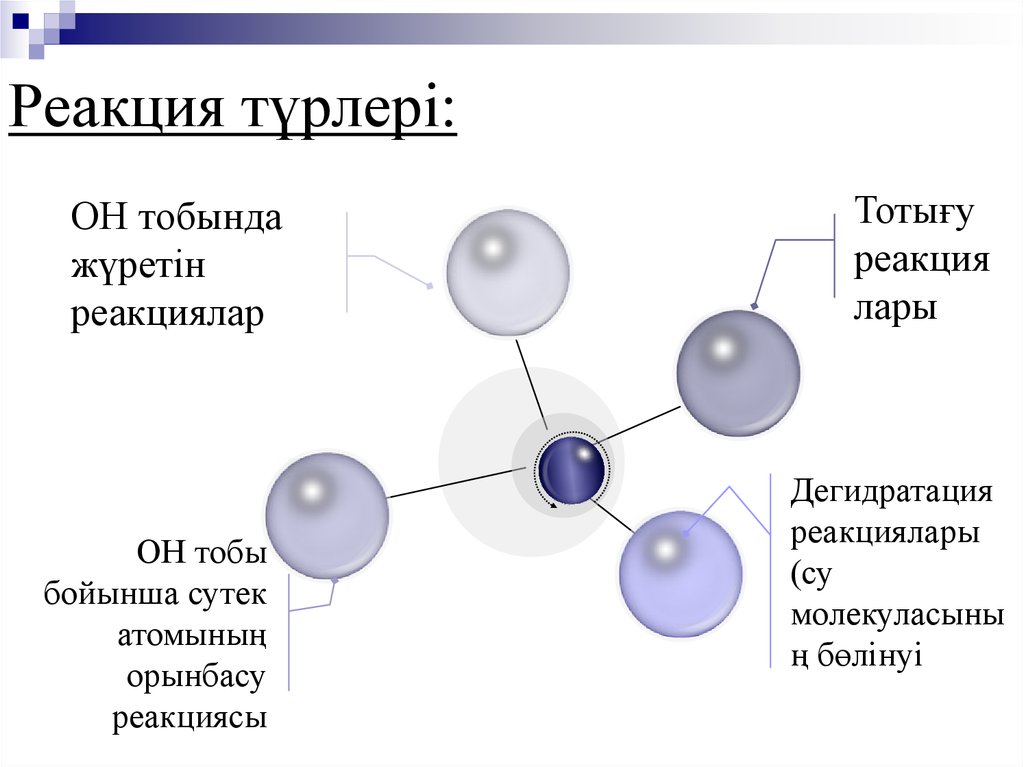
13. Реакция түрлері:
ОН тобындажүретін
реакциялар
ОН тобы
бойынша сутек
атомының
орынбасу
реакциясы
Тотығу
реакция
лары
Дегидратация
реакциялары
(су
молекуласыны
ң бөлінуі
14. ОН тобы бойынша сутек атомының орынбасу реакциясы
С2Н5ОН + Na → C2H5ONa + H2C2H5ONa + H2O → C2H5OH + NaOH
Спирттер
әлсіз
қышқылдар
тәрізді
сілтілік
металдармен әрекеттеседі. Спирттің мұндай металл
туындыларын алкоголяттар деп атайды.
15. ОН тобында жүретін реакциялар
Спирттер галогенсутектермен әрекеттеседі, реакциягидроксил тобының орнын галоген басу арқылы өтетін
қайтымды реакция.
16. Дегидратация реакциялары
Cпирттерге дегидратацияның екі түрі тәң:- молекула ішілік
- молекула аралық
Молекула ішілік - дегидратацияда алкендер.
Молекула аралықта- жай эфирлер түзіледі.
17. Тотығу реакциялары
Спирттердің тотығуы күштітотықтырғыштар
әсерінен
тотығады. Түзілу өнімдері
спирттердін
орынбасу
дәрежесіне
сай,
және
пайдаланатын
тотықтырғыштың табиғатына
байланысты.
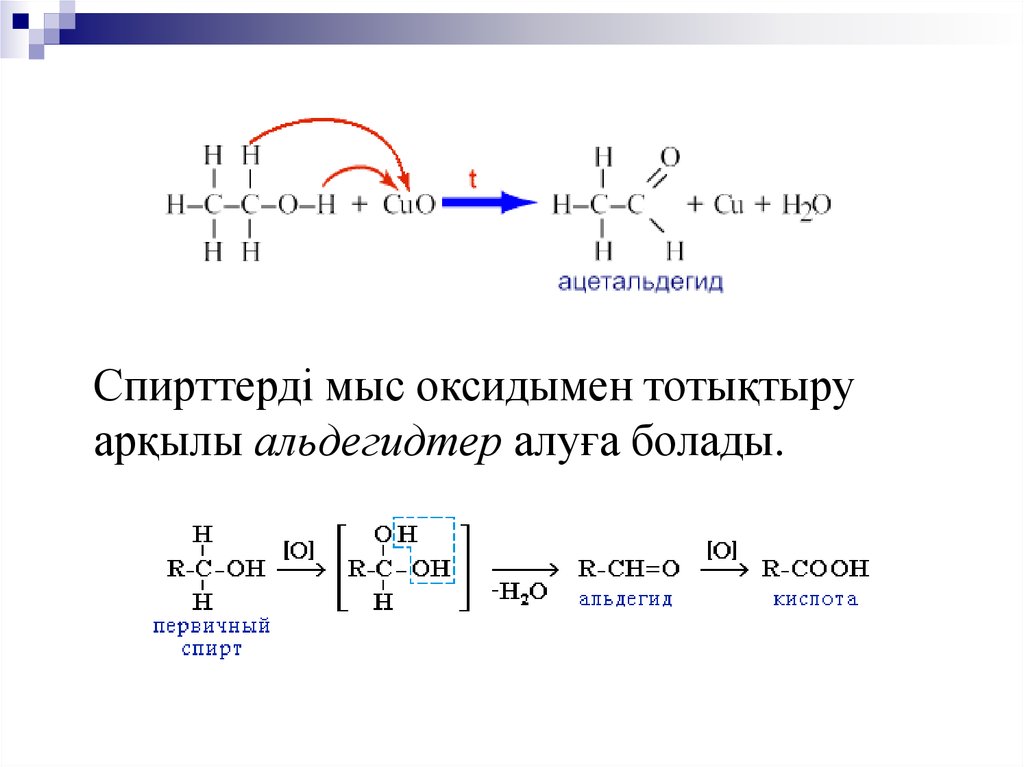
18.
Спирттерді мыс оксидымен тотықтыруарқылы альдегидтер алуға болады.
19.
Қолданылуы:Медициналық практикада этил спирті негізінен
сүртінуге, компресстерге арналған сыртқы
антисептикалық және тітіркендіргіш зат ретінде
қолданылады.
- хирургтың қолын, операция жасалатын аумақты,
медициналық құралдарды тазалап-өңдеуде
Қолдану тәсілі және дозалары
Сыртқа – мақта тампондар, сүрткілердің көмегімен
теріге жағады. Компресс жасайды.
20.
Фенолдар — бензол сақинасындағы бір немесебірнеше сутек атомдарының орнын гидроксотоп
басқан ароматты көмірсутектердің туындылары.
Ең қарапайым өкілі — фенол С6Н5ОН немесе
гидроксибензол.
21.
Алынуы.Фенолды көбіне тас көмір шайырын өңдеу арқылы
алады. Сондай-ақ ароматты көмірсутектерінің
галогентуындыларын сілтімен әрекеттестіріп те
алады. Өндірісте бастапқы шикізаттар ретінде бензол
мен пропиленді пайдаланып, кумолді әдіспен фенол
алу іске асырылған.
22.
Қасиеттері:Физикалық қасиеттері.
Фенол — түссіз кристалдық зат. 43°С-та
балқиды. Ауада ашық қалғанда
тотығатындықтан, қызғылт түсті болады.
Бөлме температурасында аздап қана
ериді, ал 60°С-тан жоғары қыздырғанда,
суда шексіз ериді. Фенол — улы зат,
теріні күйдіреді. Ерітіндісі антисептик
ретінде қолданылады.
Химиялық қасиеттері.
Фенол молекуласындағы атомдар бірбіріне өзара әсер ететіндіктен, полярлы
қосылыс болады.
23.
Қолданылуы.Фенолдың 3—5%-тік ерітіндісін зиянды
микробтарды жою үшін антисептик ретінде
қолданады. Фенолдан түрлі дәрі-дәрмектік
препараттарды, бояуларды, синтездік шайырлар мен
пластмассаларды, қопарғыш заттарды синтездеп
алады. Фенолдарды фотографияда айқындаушы
есебінде және кейбір туындыларды, мысалы
адреналинді алу үшін қолданылады. Үш атомды
фенолдар техникада өте күшті тотықсыздандырғыш
ретінде, мысалы газдардағы оттекті анықтауда,
мединицада бояғыштар дайындау үшін
пайдаланылады.
24. Қорытынды:
Сутектік байланыс –бір сутегі молекуласыменэлектртерістігі жоғары атомдар (О,F,N,Cl)
арасында пайда болатын байланыс.
Этерификация реакциясы – спирттердің
органикалық
және
бейорганикалық
қышқылдармен әрекеттесуі нәтижесәнде
кұрделі эфирлердің түзілуі.
25.
Пайдаланылған әдебиеттер.http://statref.ru/ref_otrqasujgqas.html
https://kopilkaurokov.ru
https://ppt-online.org
multiurok.ru

















 Химия
Химия








