Похожие презентации:
Теория электролитической диссоциации
1. Теория электролитической диссоциации
Урок химии в 8 классе2.
3.
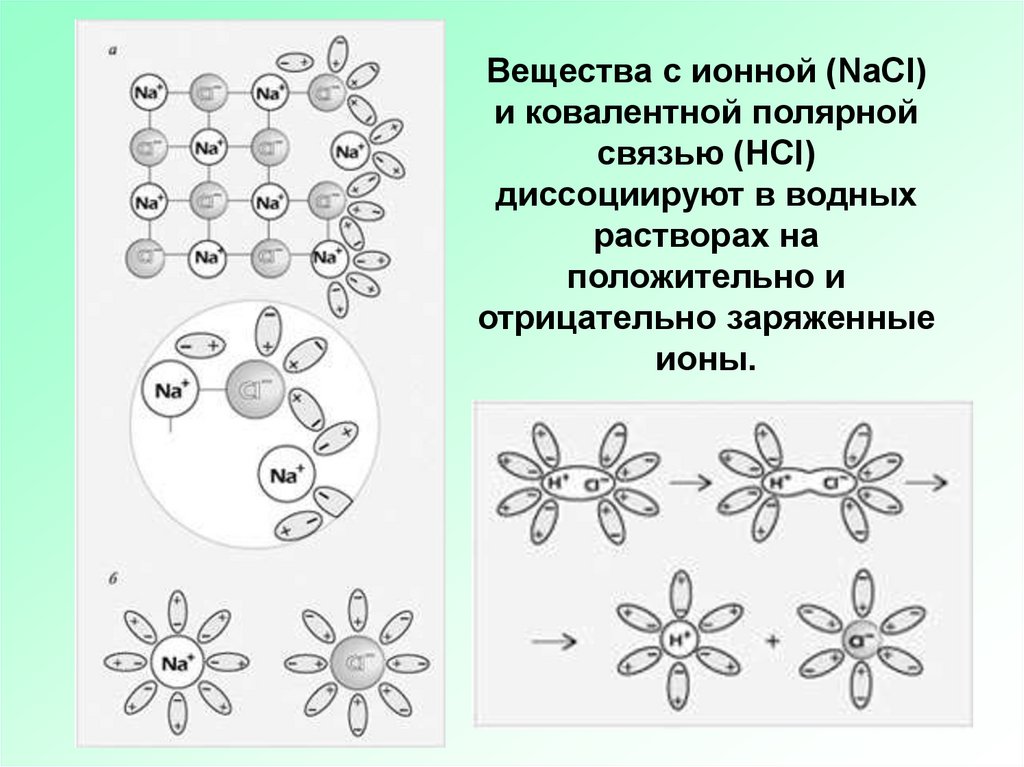
Вещества с ионной (NaCl)и ковалентной полярной
связью (HCl)
диссоциируют в водных
растворах на
положительно и
отрицательно заряженные
ионы.
4.
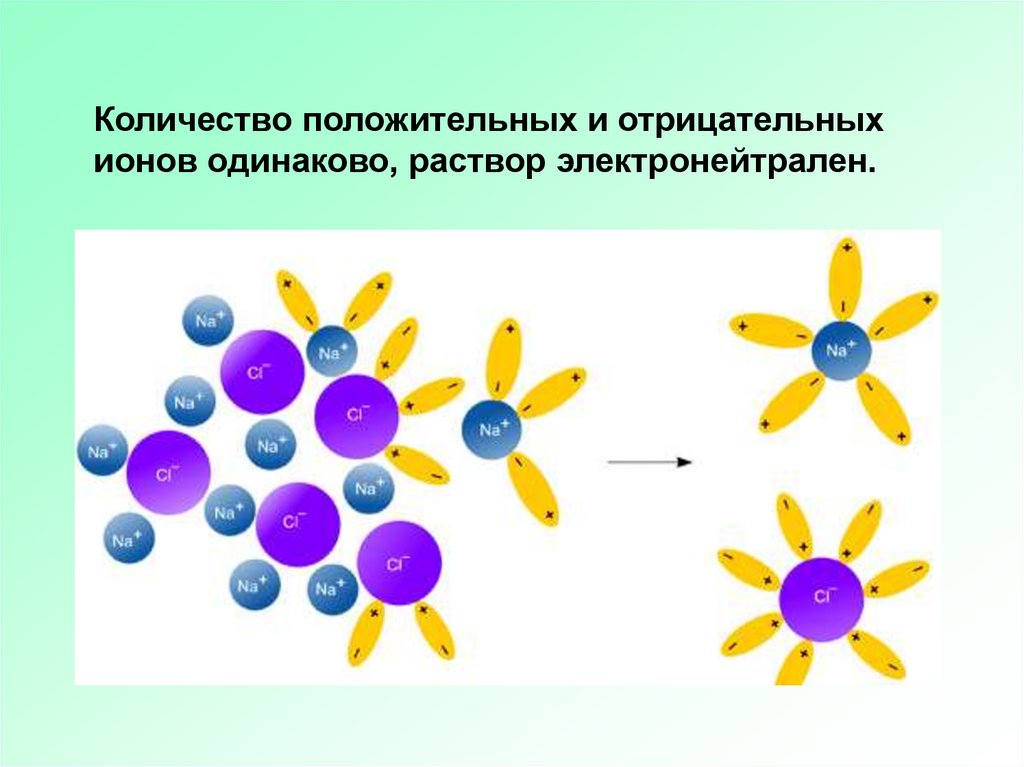
Количество положительных и отрицательныхионов одинаково, раствор электронейтрален.
5.
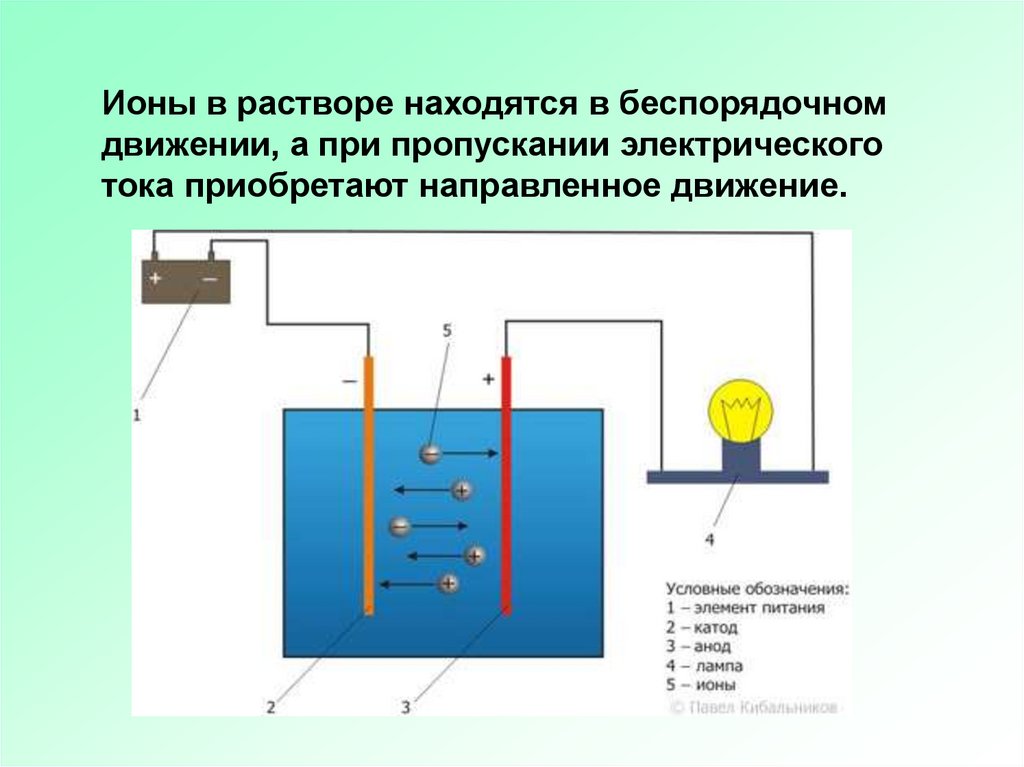
Ионы в растворе находятся в беспорядочномдвижении, а при пропускании электрического
тока приобретают направленное движение.
6.
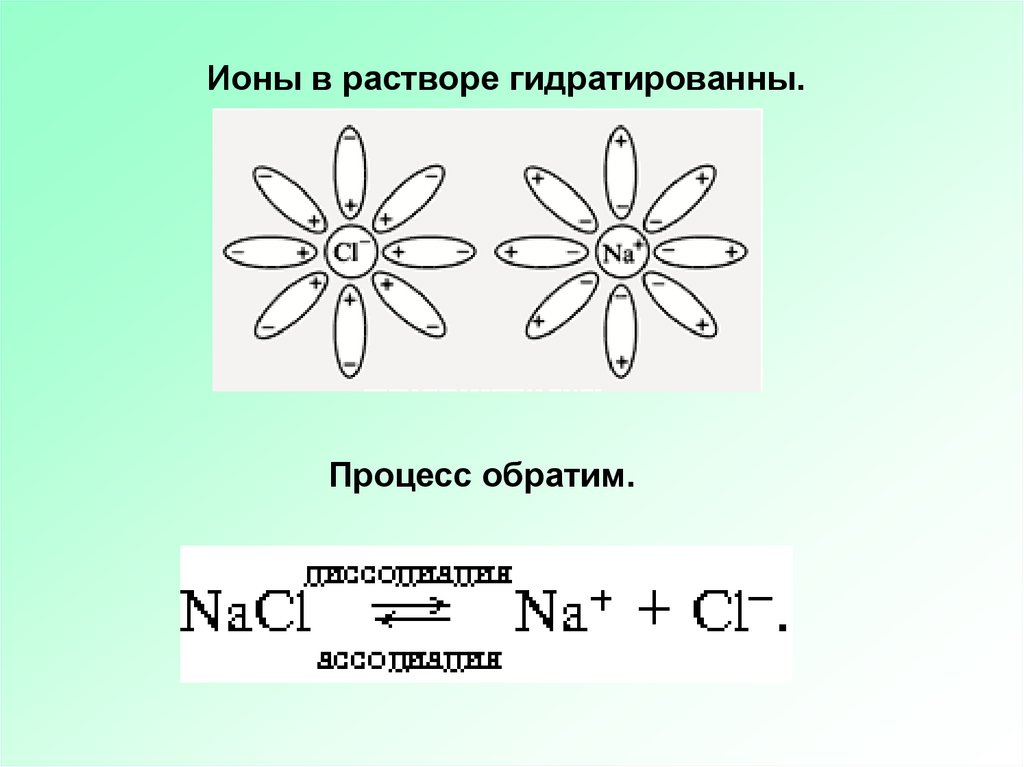
Ионы в растворе гидратированны.Процесс обратим.
7.
Сванте Аррениусустановил факт
диссоциации
8.
Каблуков Иван Алексеевичустановил роль воды в
процессе электролитической
диссоциации
Кистяковский Владимир
Александрович
объединил взгляды Аррениуса,
Каблукова и теорию растворов
Менделеева и сформулировал
основные положения ТЭД
9. Испытание веществ на электропроводность
10. Зависимость электропроводности от концентрации
11. Изменение диссоциации при температуре
12. Степень электролитической диссоциации
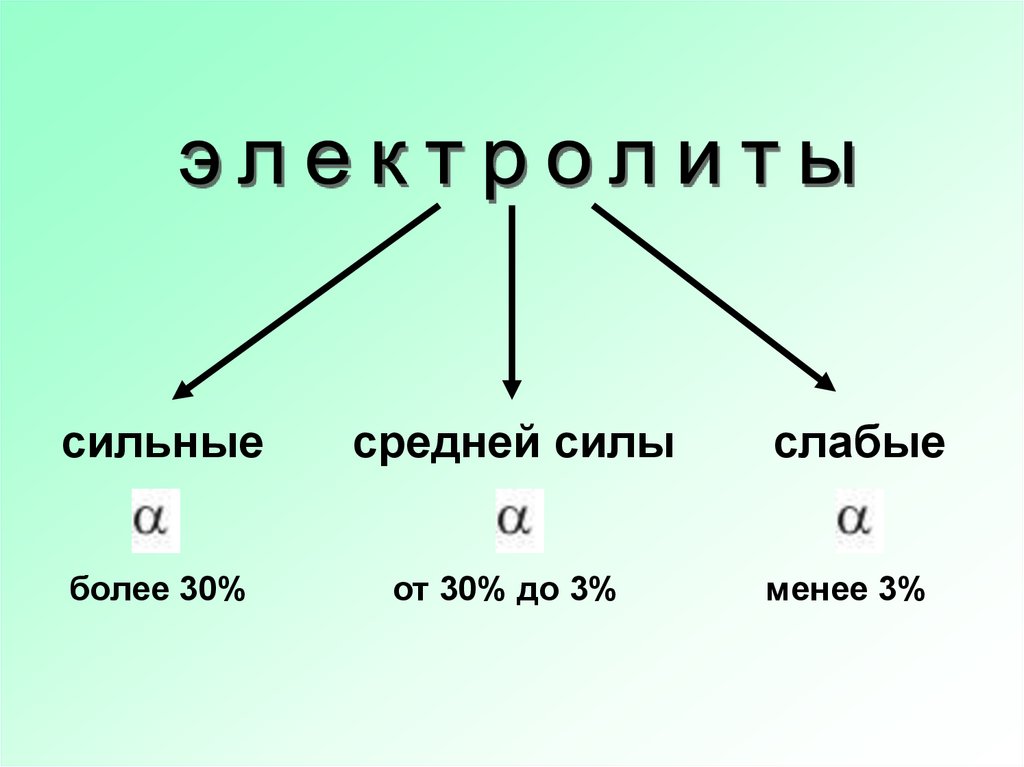
13.
сильныесредней силы
более 30%
от 30% до 3%
слабые
менее 3%
14. Глоссарий
Электролит
Неэлектролит
Диссоциация
Ассоциация
Диполь
Катионы
Анионы
Катод
Анод
Электрод
Ионы
Ионы гидратированны
Электролитическая
диссоциация
Термическая
диссоциация
Кислоты
Щелочи
Соли









 Химия
Химия








