Похожие презентации:
Особенности органических реакций
1. Особенности органических реакций
учитель химии КОГОБУ СОШ пгт ОричиВолодина Татьяна Валериевна
2. Специфические особенности органических реакций
• Реакции идут медленнее• Чаще требуют жестких условий для их
осуществления:
1.
2.
3.
4.
Повышение температуры
Катализатор
Давление
Облучение УФ светом
3. Специфические особенности органических реакций
• Реакции протекают в несколько стадий,поэтому редко дают высокий выход
продукта
• Вместо уравнений – схема, над
условия
реакций: t, p, катализатор.
• Изменяется не вся молекула, а только её
части – реакционные центры молекулы
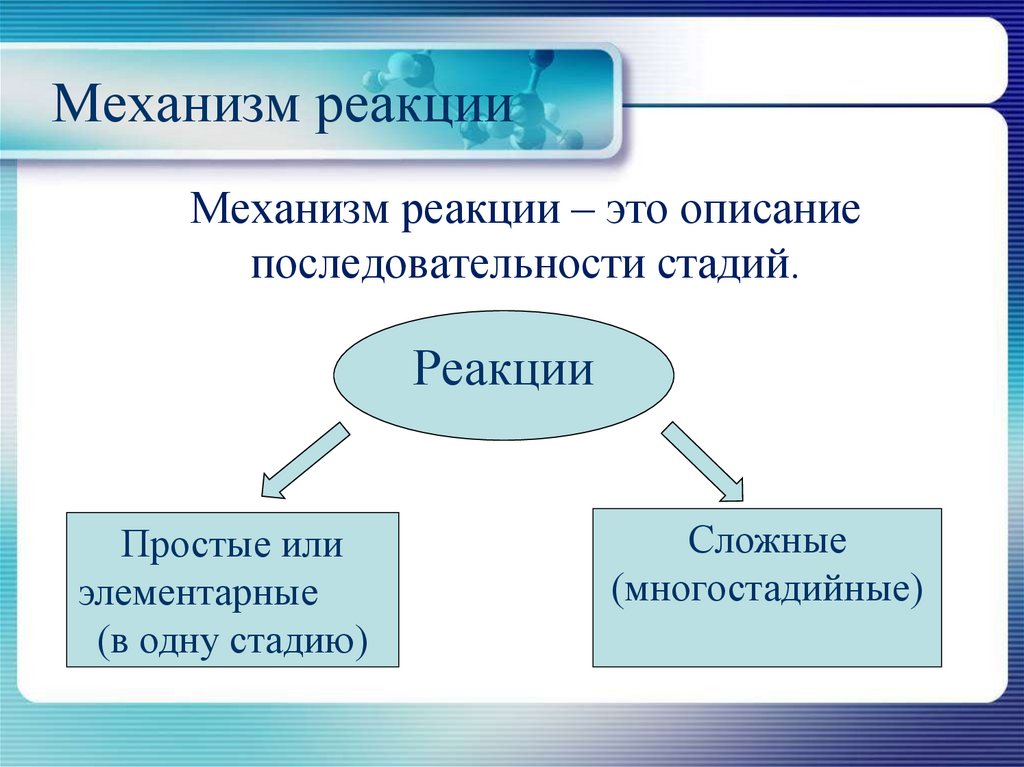
4. Механизм реакции
Механизм реакции – это описаниепоследовательности стадий.
Реакции
Простые или
элементарные
(в одну стадию)
Сложные
(многостадийные)
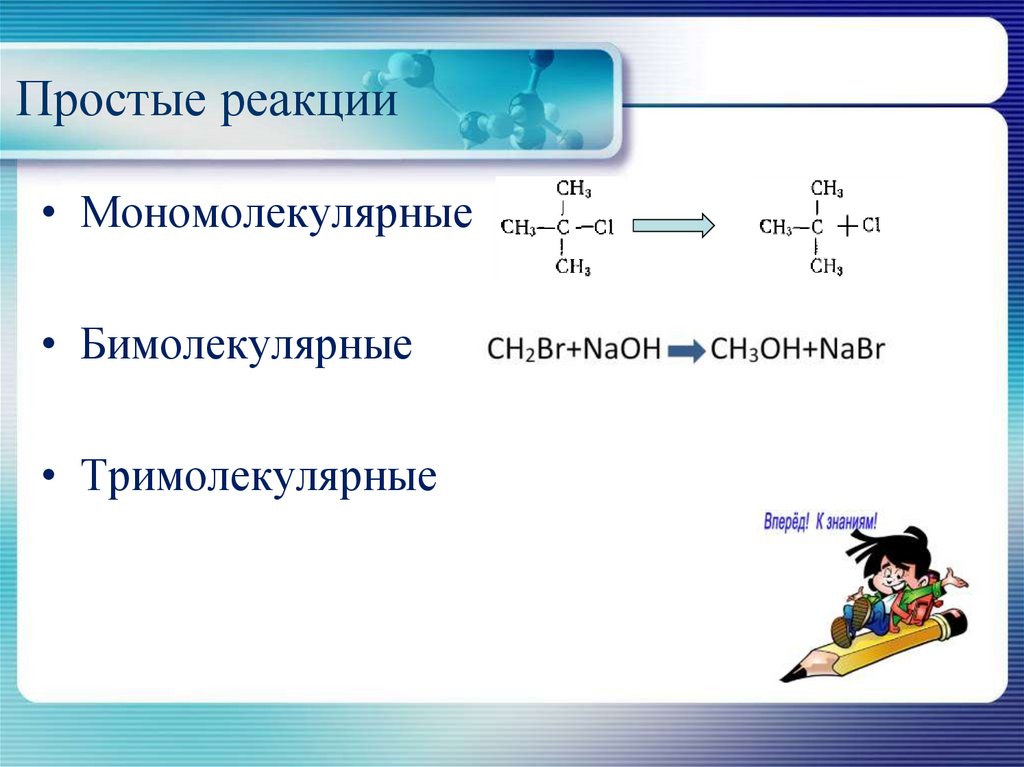
5. Простые реакции
• Мономолекулярные• Бимолекулярные
• Тримолекулярные
6. Сложные реакции
Хлорирование метана реакция замещения7. Хлорирование метана
1 стадия-зарождение цепи (инициирование)8. Хлорирование метана
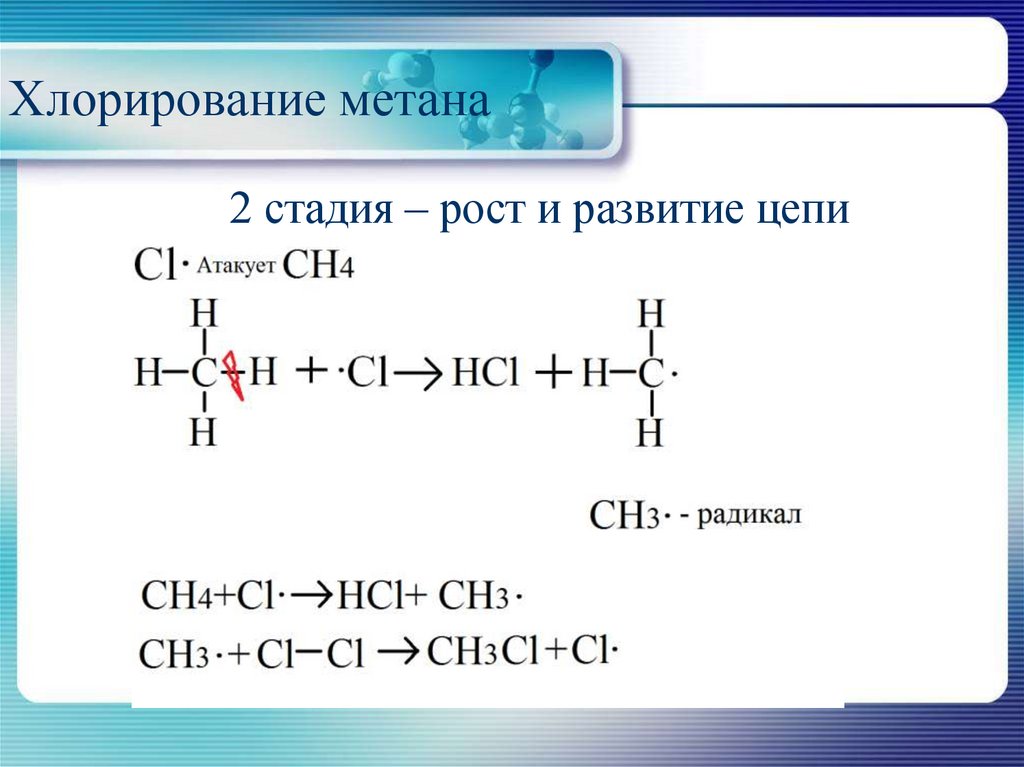
2 стадия – рост и развитие цепи9. Хлорирование метана
3 стадия – обрыв цепи10. Атакующие частицы
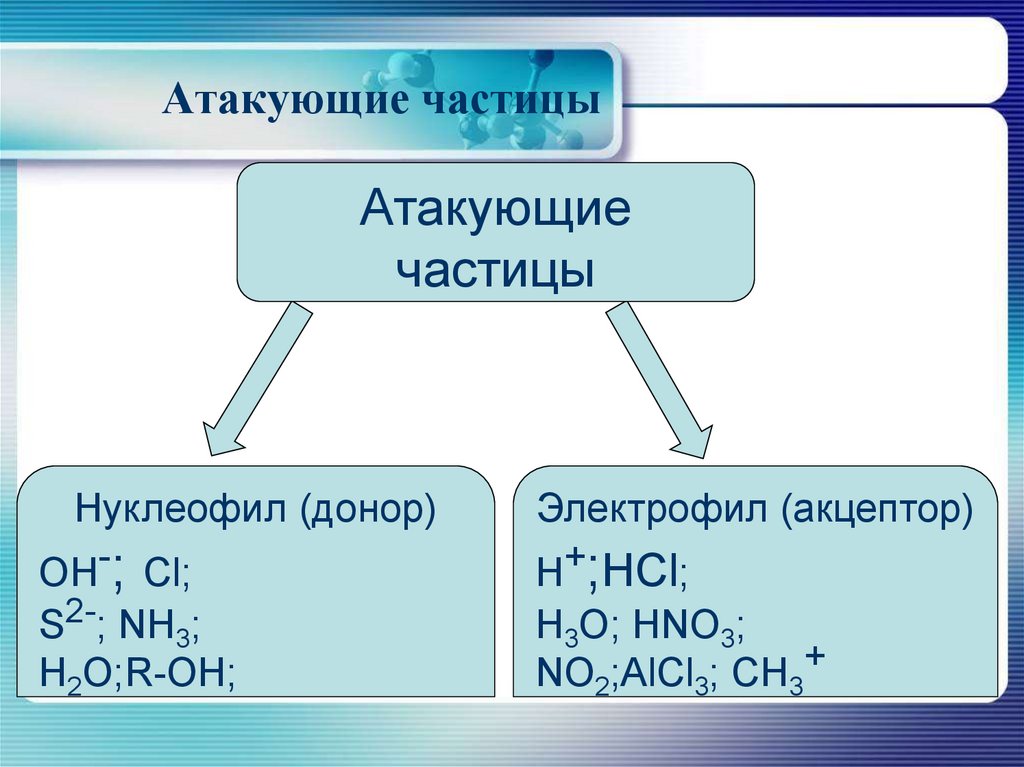
Атакующиечастицы
Нуклеофил (донор)
OH-; Cl;
Электрофил (акцептор)
H+;HCl;
S2-; NH3;
H2O;R-OH;
H3O; HNO3;
NO2;AlCl3; CH3+
11. Способы разрыва химических связей
Гомолитический (радикальный)Гетеролитический (ионный)
12. Гомолитический разрыв химической связи
Гомолитический разрыв ковалентной связи(радикальный)
Радикалы:
CH3CH2
Cl
13. Гомолитический разрыв химической связи
Гомолизу подвергаются:Неполярные связи (С-С; Сl-Cl)
Малополярные связи (С-Н)
Гомолиз осуществляется
• При высокой температуре
• На свету
• В отсутствии растворителя
14. Гетеролитический разрыв химической связи
• Гетеролитические (электрофильныенуклеофильные или ионные) реакции:15. Гетеролитический разрыв химической связи
Гетеролизу подвергаются:• ковалентные неполярные связи
Гетеролизу способствуют:
Наличие растворителя
Или наличие катализатора











 Химия
Химия