Похожие презентации:
Металлическая и водородная и химическая связь
1. Металлическая и водородная и химическая связь
http://rpg.lv/node/1368?video_id=949- видеоурок2. Тест по теме «Ионная и ковалентная химическая связь»
1.Химическая связь в соединении хлора с элементом, в атомекоторого распределение электронов по слоям 2е, 8е, 7е:
1) ионная;
3) ковалентная неполярная;
2)металлическая;
4) ковалентная полярная.
2.Ковалентной полярной связью образовано вещество, формула
которого:
1)N2;
2) NaBr; 3) Na2S; 4) HF.
3. Ионной связью образовано вещество, формула которого:
l) Na;
2) СаСI2; 3) SiO2; 4) Н2.
4.Соединениями с ковалентной неполярной и ковалентной полярной
связью являются соответственно:
1) НВг и Вг2; 2) СI2 и H2S;
3) Na2S и SO3; 4) Р8 и NaF.
5. В соединении калия с кислородом химическая связь:
1) металлическая;
3) ковалентная неполярная;
2) ковалентная полярная;
4) ионная.
6. Ковалентная неполярная связь в веществе:
1) аммиак; 2) сероводород;
3) хлор; 4) железо.
3. Определить вид химической связи у следующих соединений:
• Вариант 1К2О, I2, H2O, Cl2, CaO, HBr, CaCl2, O2,
Na2O, HCl
• Вариант 2
Br2, NO2, CO2, Na2O, O2, HCl, H2O
CuCl2, N2, Н2O2
4.
• Определите элементы, ставшие не в ту«очередь»:
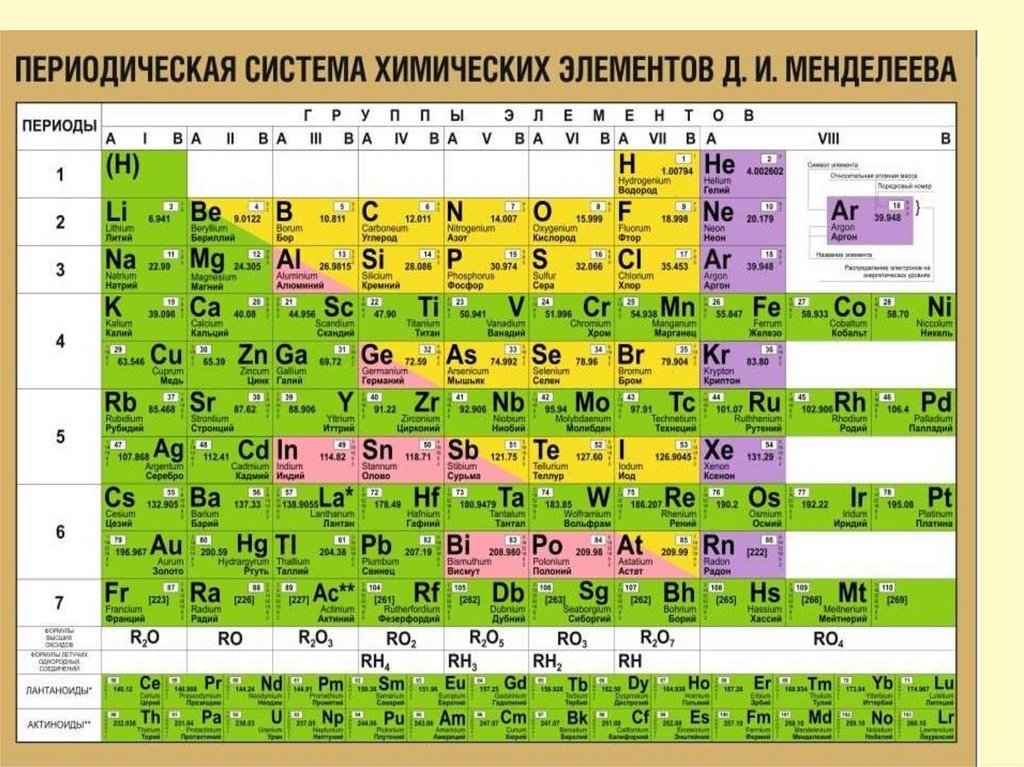
Ca Fe P K Al Mg Na
• Почему?
5.
6.
7.
Атомы металлов легкоотдают валентные
электроны и
превращаются в
положительные
заряженные ионы:
Ме0 – n ē =Men+
8.
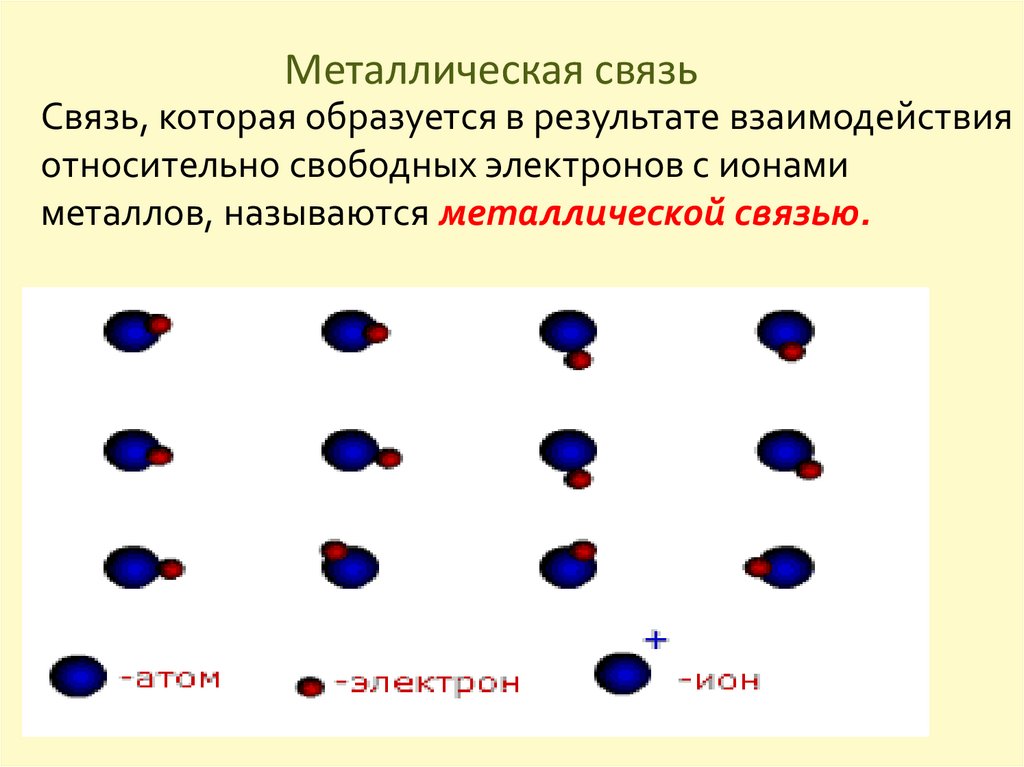
Свободные электроны, оторвавшиеся отатома, перемещаются между
положительными ионами металлов.
Между ними возникает металлическая связь,
т. е. электроны как бы цементируют
положительные ионы кристаллической
решетки металлов.
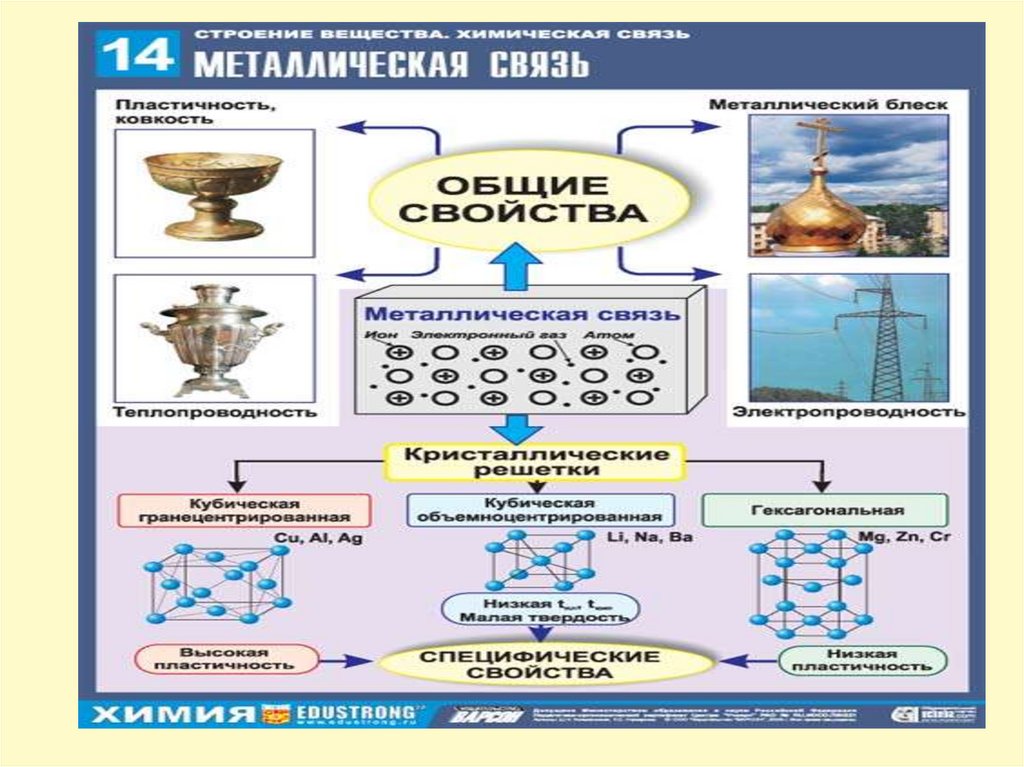
9. Металлическая связь
Связь, которая образуется в результате взаимодействияотносительно свободных электронов с ионами
металлов, называются металлической связью.
10.
11. Водородная связь
Связь, которая образуетсямежду атомом водорода
одной молекулы и
атомом сильно
электроотрицательного
элемента (O, N, F) другой
молекулы, называется
водородной связью.
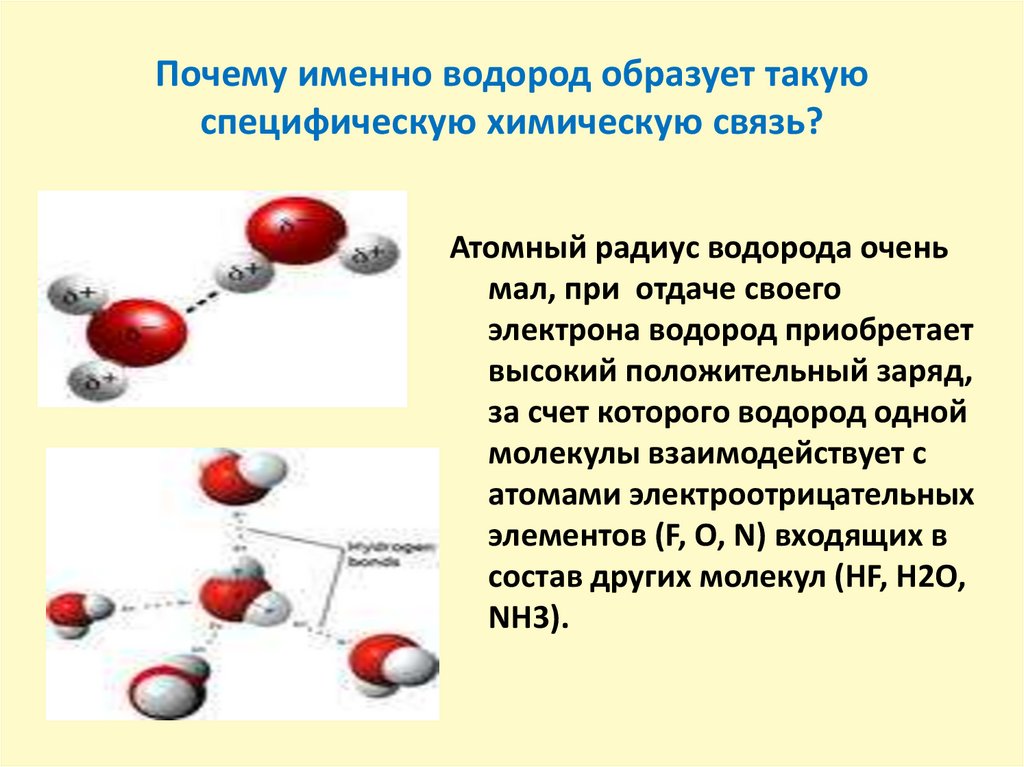
12. Почему именно водород образует такую специфическую химическую связь?
Атомный радиус водорода оченьмал, при отдаче своего
электрона водород приобретает
высокий положительный заряд,
за счет которого водород одной
молекулы взаимодействует с
атомами электроотрицательных
элементов (F, O, N) входящих в
состав других молекул (HF, H2O,
NH3).
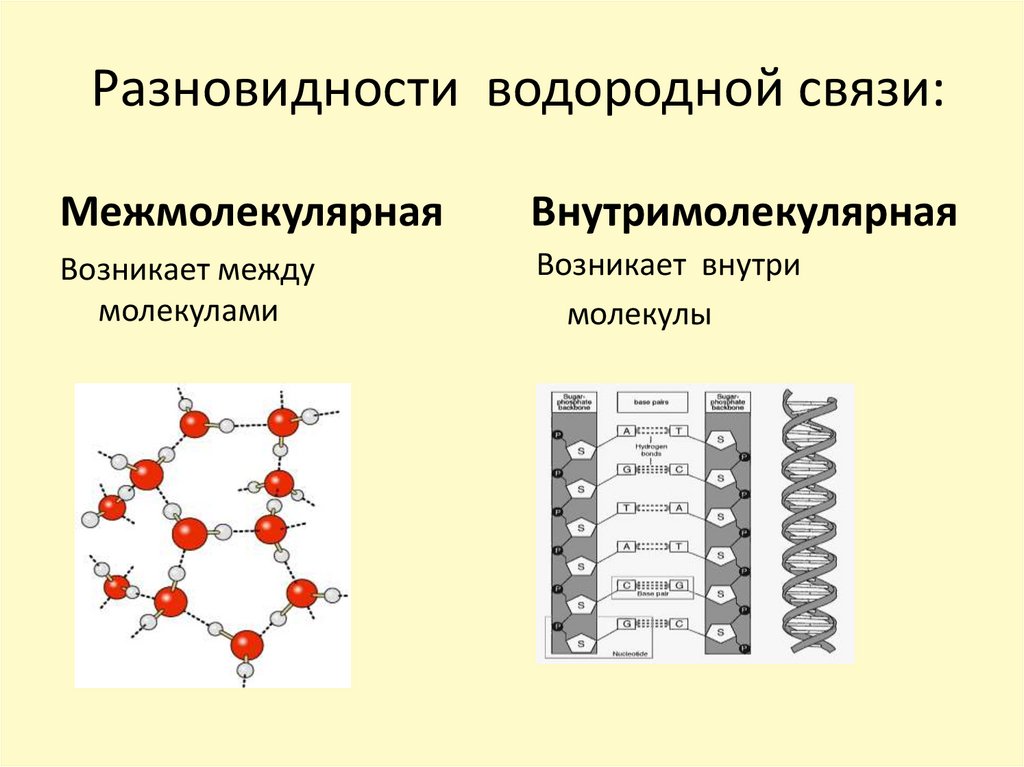
13. Разновидности водородной связи:
МежмолекулярнаяВнутримолекулярная
Возникает между
молекулами
Возникает внутри
молекулы
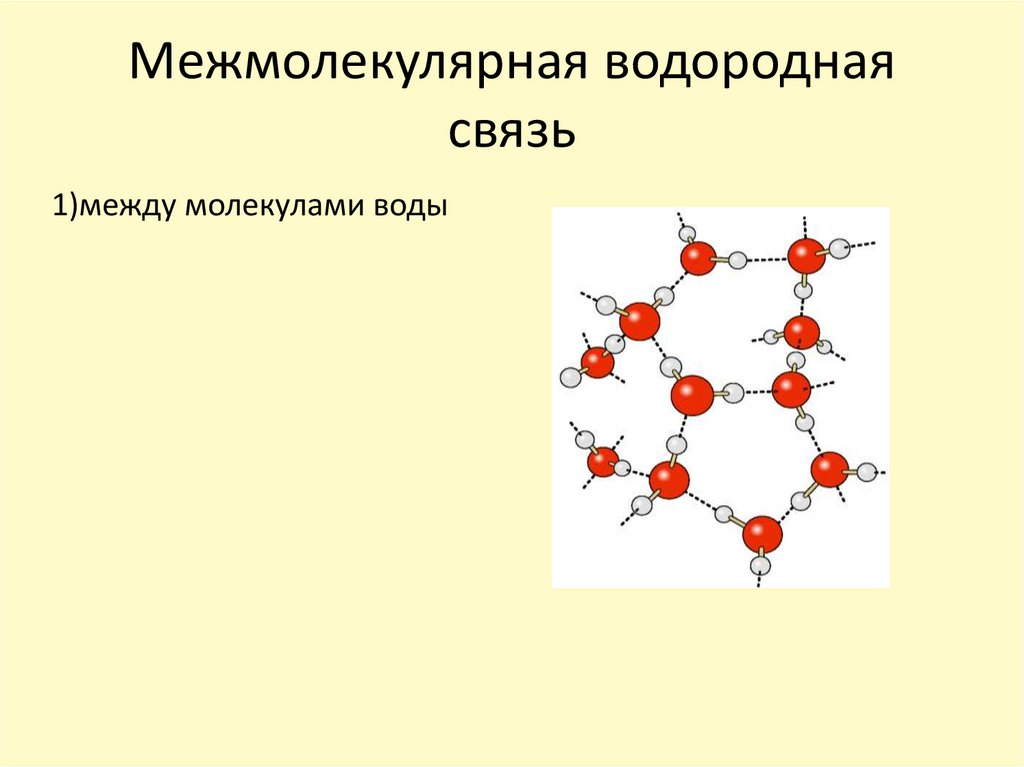
14. Межмолекулярная водородная связь
1)между молекулами воды15. Межмолекулярная водородная связь
2)между молекулами аммиака16. Межмолекулярная водородная связь
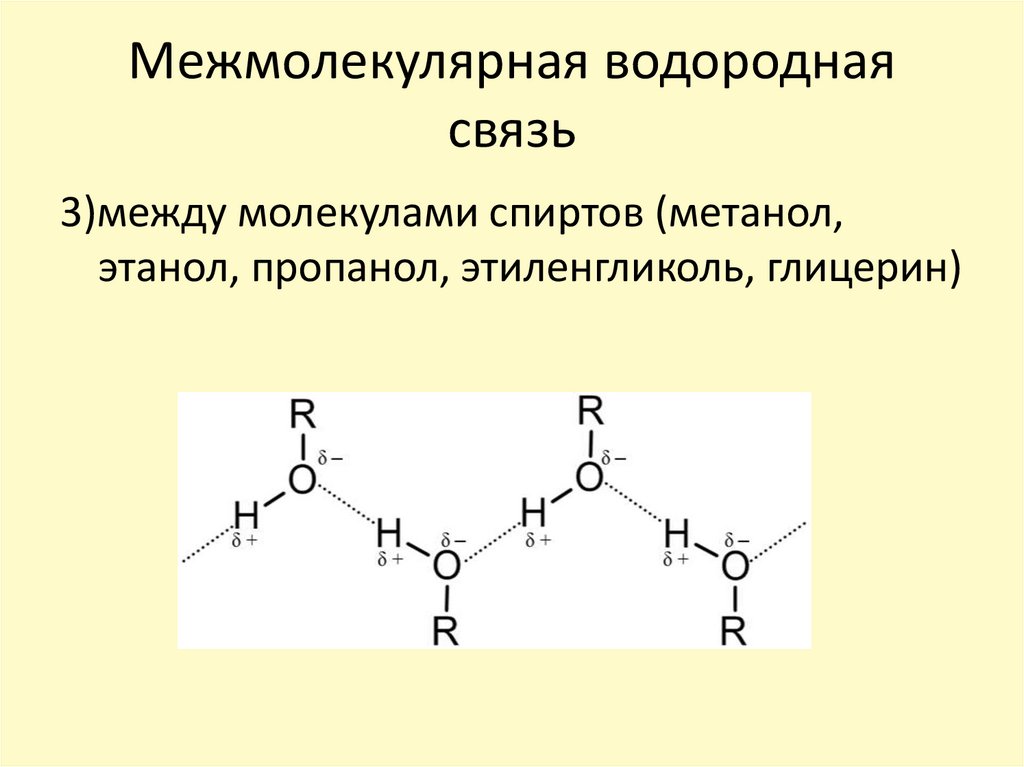
3)между молекулами спиртов (метанол,этанол, пропанол, этиленгликоль, глицерин)
17. Межмолекулярная водородная связь
4)между молекулами карбоновых кислот(муравьиная, уксусная)
18. Межмолекулярная водородная связь
5)Между молекулами фтороводородаН – Fδ- … δ+ H – F δ- … δ+Н – F δ- …
19. Особые свойства веществ, образованных межмолекулярной водородной связью
1)вещества с низкой молекулярной массой –жидкости или легко сжижаемые газы
(вода, метанол, этанол, муравьиная кислота,
уксусная кислота, фтороводород, аммиак)
20. Особые свойства веществ, образованных межмолекулярной водородной связью
2)некоторые спирты и кислотынеограниченно растворимы в воде
21. Особые свойства веществ, образованных межмолекулярной водородной связью
3)способствуют образованию кристаллов ввиде снежинок или измороси
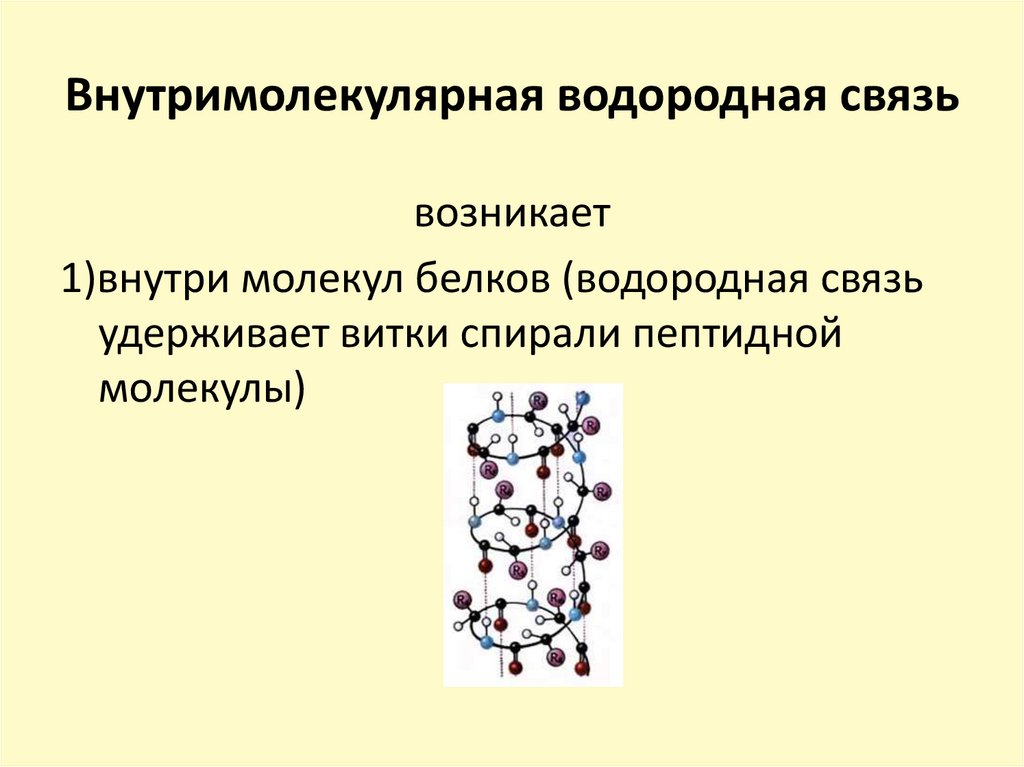
22. Внутримолекулярная водородная связь
возникает1)внутри молекул белков (водородная связь
удерживает витки спирали пептидной
молекулы)
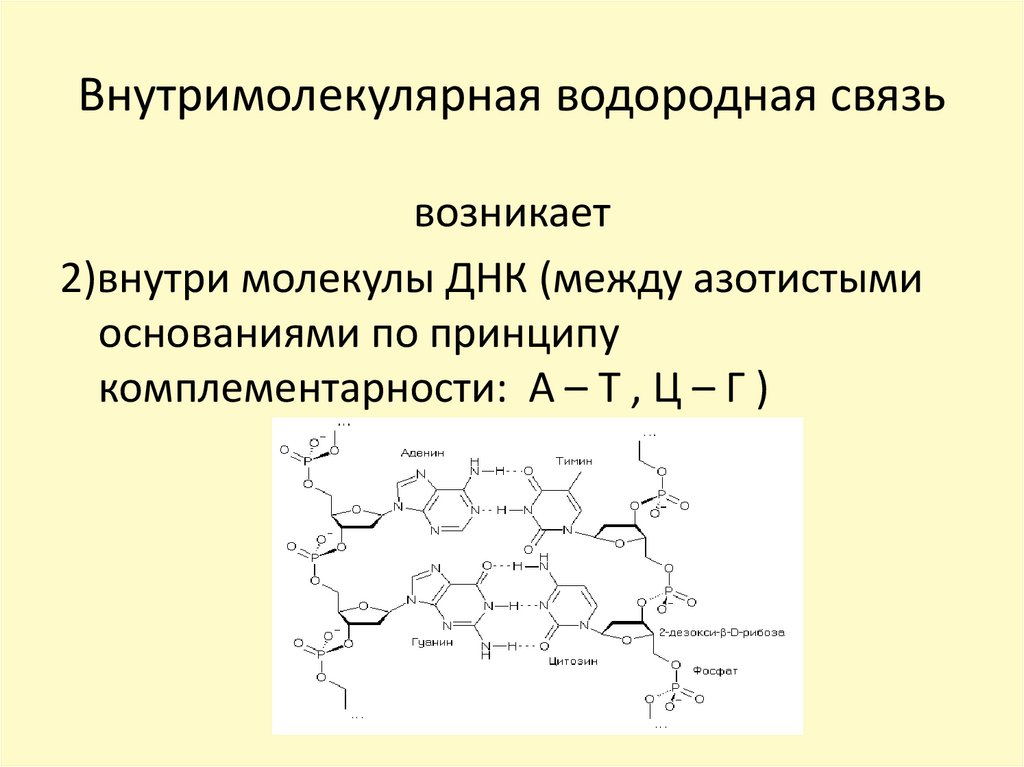
23. Внутримолекулярная водородная связь
возникает2)внутри молекулы ДНК (между азотистыми
основаниями по принципу
комплементарности: А – Т , Ц – Г )
24. Значение внутримолекулярной связи
• Способствует образованию молекул белков,ДНК и РНК и определяет их
функционирование.
25. Факторы, разрушающие водородную связь в белковой молекуле (денатурирующие факторы)
ВибрацииВысокие температуры
Химические вещества
Электромагнитное
излучение
26.
ТЕСТ1) Для какого вещества характерна водородная
связь:
б
а) C₂H₆ б) C₂H₅OH в) CH₃-O-CH₃ г) CH₃COOCH₃
в
2) Укажите вещество с металлической связью:
а) оксид магния б) сера в) медь г) нитрид лития
3) Установите соответствие между формулой вещества и
видом химической связи в нем:
А) CaCl₂
Б)SO₃
В) KOH
Г) Fe
Д) N₂
Е) H₂O
1)металлическая
2) только ионная
3) только ковал.полярная
4) ков.полярная и ионная
5) ков.полярная и неполярная 6) только ков.неполярная
7) ков.полярная и водородная
ОТВЕТ:
3: А - 1, Б - 3, В - 4, Г - 1, Д - 6, Е - 3
27.
4). Вещество, между молекулами которого существуетводородная связь:
а) этанол
б) метан
в) водород
5). Вещество с металлической связью:
а) H₂O
б) Ag
в) CO₂
г) бензол
а
г) KF
б
28. Дом. задание:
Задача № 1.В растворе массой 100 г содержится хлорид
бария массой 20 г. Какова массовая доля
хлорида бария в растворе?
Задача № 2 .
Сахар массой 5 г растворили в воде массой
20 г. Какова массовая доля (%) сахара в
растворе?
29.
• В растворе массой 100 г содержится хлоридбария массой 20 г. Какова массовая доля
хлорида бария в растворе?




















 Химия
Химия








