Похожие презентации:
железо
1. Железо
2. Положение в Периодической системе
Порядковыйномер
Период
Группа
Подгруппа
26
4
8
побочная
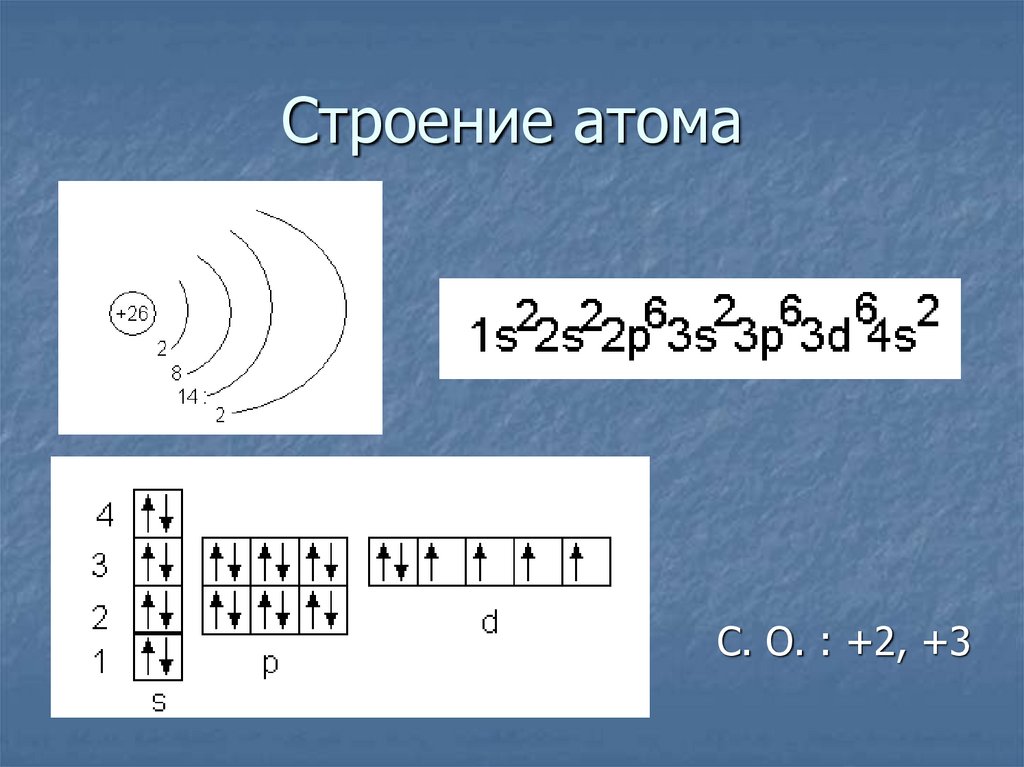
3. Строение атома
С. О. : +2, +34. Простое вещество
5. Физические свойства
ТвердоеСеро-серебристое
Блестящее
Хорошо проводит тепло и электрический ток
Достаточно ковкое и пластичное
Обладает магнитными свойствами
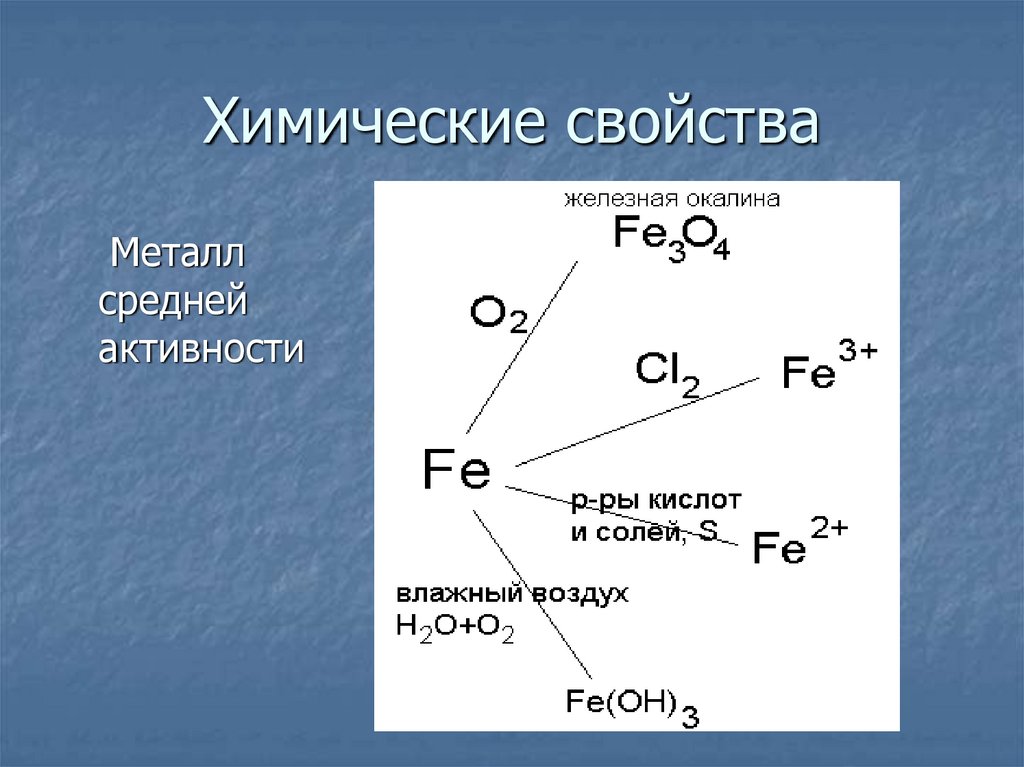
6. Химические свойства
Металлсредней
активности
7. Химические свойства
3Fe + 2O2 = Fe3O42Fe + 3Cl2 = 2FeCl3
Fe + 2HCl = FeCl2 + H2
Fe + S = FeS
Fe + CuSO4 = FeSO4 + Cu
Разобрать уравнение с окислительновосстановительной точки зрения
Fe + O2 + H2O = Fe(OH)3
8. Оксиды железа
НазваниеФормула Свойства
Характер
Оксид железа
(II)
FeO
Тверды, темно-серый,
нерастворимый в воде,
на воздухе окисляется
основный
Оксид железа
(III)
Fe2O3
Тверды, темнокоричневый,
нерастворимый в воде
основный
Железная
окалина
Смесь
FeO
и Fe2O3
Обладает магнитными
свойствами «магнитный
железняк»
9. Гидроксиды железа
НазваниеФормула Свойства
Характер
Гидроксид
железа (II)
Fe(OH)2
Тверды, белый,
нерастворимый
в воде, на
воздухе
окисляется
основный
Гидроксид
железа
(III)
Fe(OH)3
Тверды, темно
коричневый,
нерастворимый
в воде
основный







 Химия
Химия








