Похожие презентации:
Устойчивость растений к внешним факторам среды
1. Устойчивость растений к внешним факторам среды
Адаптация и акклимация – процесс приспособления организма кизменившимся условиям среды.
Адаптация – эволюционно, акклимация – под действием стрессоров,
у неприспособленных...
Устойчивость – способность организма выживать и давать
потомство в изменившихся условиях. Конечный результат
адаптации и акклимации
В настоящее время принято различать акклимацию и адаптацию…
NB – сколько организм имеет времени для адаптации:
Генетические, или эволюционные адаптации (тысячелетия)
Онтогенетические адаптации (акклимации) - в течение онтогенеза
организма
Срочные акклимации (адаптации) (часы)
Уровни:
организменный ( например, переключение С – САМ)
3
тканевой и органный (например, уход в почву корня женьшеня)
клеточный (например, синтез шаперонов, осмолитов, БТШ)
2. Адаптивный ответ конститутивно-устойчивых и неустойчивых растений
3. Примеры конститутивной устойчивости растений
4. Срочные адаптации (акклимации) – стресс-реакции
СтрессреакцияСпециализированная
адаптация
Время
Стресс-реакция: минуты – часы. Назначение – обеспечить
выживание при стрессе.
Стресс – состояние, стрессор – фактор, вызывающий стресс.
Специализированная адаптация (акклимация): длительно.
Назначение – нормальное функционирование в изменившихся
условиях.
Механизмы стресс-реакции:
отключение процессов, не имеющих жизненно-важных функций
(нарпимер, нитратредуктазы – причем, на всех уровнях)
«быстрая» энергетика (например, работа альтернативной оксидазы)
синтез протекторных соединений – высокомолекулярных (БТШ,
других стрессовых белков – осмтин-подобных, низкотемпературных),
низкомолекулярных – ди- и полиаминов, пролина, бетаинов.
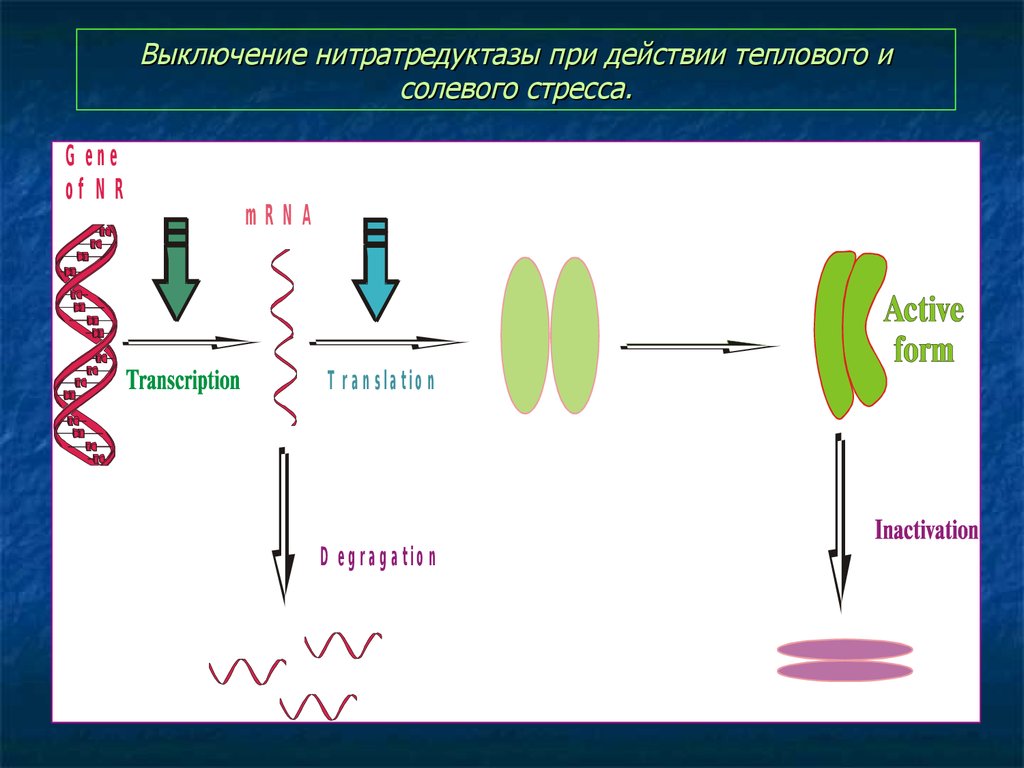
5. Выключение нитратредуктазы при действии теплового и солевого стресса.
G eneof N R
mRNA
T r a n sla tio n
D e g r a g a tio n
6. Биологические функции индивидуальных БТШ
ВЫСОКОМОЛЕКУЛЯРНЫЕ БТШБТШ 90 – защищает места связывания рецепторов, главным
образом гормонов
БТШ 70 – а) распад неправильно собранных белков
б) защита и обеспечение транспорта макромолекул
через мембраны
БТШ 60 - обеспечение правильной сборки макромолекул
НИЗКОМОЛЕКУЛЯРНЫЕ БТШ
БТШ 20 – обеспечивает работу макромолекул при стрессе. Входит
в гранулы теплового шока (например, БТШ 17 + БТШ 70
– защита нетранслируемых РНК от РНК-аз)
БТШ 8.5 – убиквитины. Консервативные белки 75 -76 а-к, служат
в качестве «метки» для белков, обреченных на смерть…
7. Индукция экспрессии генов HSP70
t!HSэлемент
HSфактор
8. Стрессовые белки – это не только HSP
Дегидрины (синоним – LEA: late embryogenesis abundant).Синтез при водном дефиците, но не только.
Регулируется JA и/или ABA. От 9 kDa (Wsi 72 у риса) до 200kDa
(Vcs у пшеницы). У некоторых – консервативные а-к домены,
богаты лизином (сегмент К) и серином. Регулируются
фосфориллированием. Локализация в цитоплазме и в ядре (в
эухроматине). Стабилизируют макромолекулы, в т.ч. ДНК.
Белки низких температур:
COP – cold-acclimated proteins
COR – cold regulated proteins
LTI – low temperature inducible
AFP – anti-freeze proteins
Осмотины и осмотин-подобные белки
9. Пролин – мультифункциональная протекторная молекула
I n a c tiva to r o fa c tiv e r a d ic a ls
C om ponent of
str e ss p r o te in s
a n d r ec e p to rs
G e n e e x p r e ssio n
c o n tr o l
P rec u rso r o f
C H 3 d e r iv a tiv e s
( o sm o ly te s )
R e se r v e n itr o g e n
so u rc e
C arbo n
so urc e
O sm o r e g u la to r
C e ll p H - s ta t
sy stem
com ponent
M a c r o m o le c u le
and m em brane
p r o tec to r
E nergy
so urc e
R e d o x p o te n tia l
r e g u la to r
R e d u c in g e q u iva le n t
gen e ra to r
10. Антиоксиданты и антиоксидативные ферменты при стрессе
D roughtP r o lin e
P o ly a m in e s
G lu ta th io n e
N aC L
H ig h t
L ow t
O
3
C O
P e r o x id a se s
o
SO D
o
G lu t a th io n e
redu c ta se
H 2O
2
1
O 2*
2
O
-
2
*O H
11. Патогенов много и они специфичны для разных органов растения
Проникновение грибаRhynchosporium secalis после
прорастания спор через
поверхность листа ячменя
12. Взаимодействие патоген – растение: все правила военного искусства…
13. Стратегия защиты растения от патогенов. Три круга обороны.
Примеры защитныхсоединений «первого
круга» обороны.
Авенацин А1 присутствует только в
корнях овса, его нет у пшеницы и ячменя.
Мощная защита от патогенного гриба
Gaeumannomyces graminis var. tritici,
который поражает пшеницу и ячмень, но
никогда – овес. У гриба Gaeumannomyces
graminis var. avenae есть фермент
авенациназа, который удаляет концевые
глюкозы и делает молекулу нетоксичной и этот гриб прекрасно «кушает» овес…
14.
.3
OCH
C
H
C
O
C
O
OH
O
O
OCH
3
C
O
H
C
O
3
C
O
C
H 3
O
O
H
O
.
.
C
H
O
Летучие вторичные метаболиты – защита,
привлечение насекомых-опылителей,
защита, а также средство «общения»…
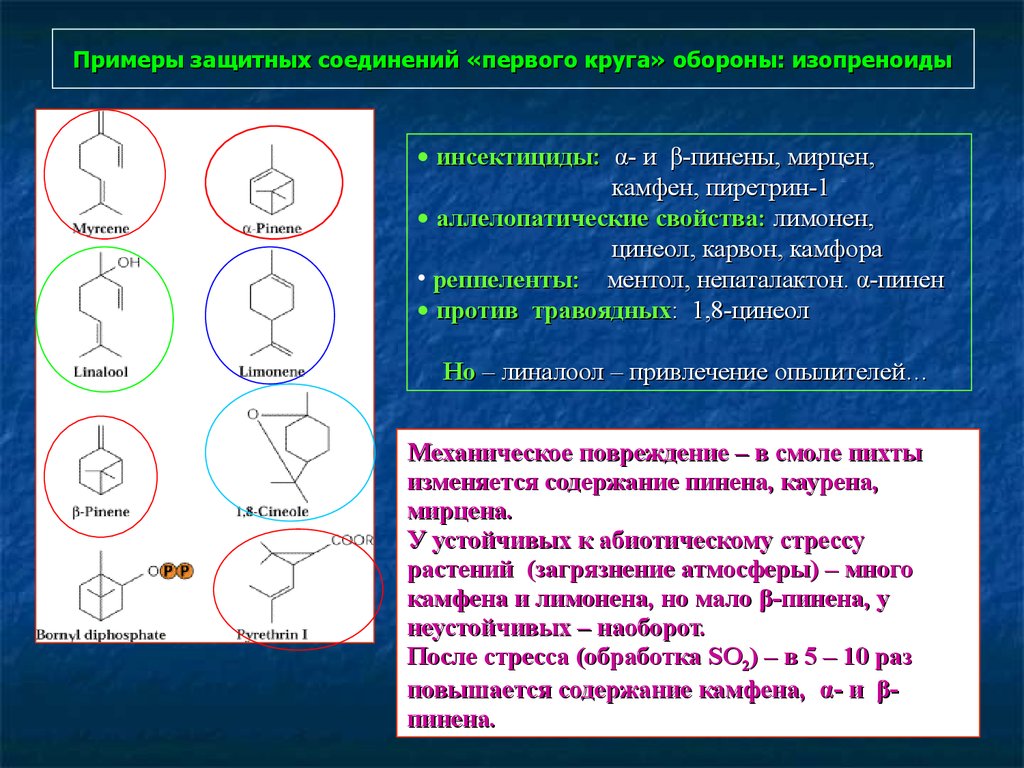
15. Примеры защитных соединений «первого круга» обороны: изопреноиды
• инсектициды: α- и β-пинены, мирцен,камфен, пиретрин-1
• аллелопатические свойства: лимонен,
цинеол, карвон, камфора
• реппеленты: ментол, непаталактон. α-пинен
• против травоядных: 1,8-цинеол
Но – линалоол – привлечение опылителей…
Механическое повреждение – в смоле пихты
изменяется содержание пинена, каурена,
мирцена.
У устойчивых к абиотическому стрессу
растений (загрязнение атмосферы) – много
камфена и лимонена, но мало β-пинена, у
неустойчивых – наоборот.
После стресса (обработка SO2) – в 5 – 10 раз
повышается содержание камфена, α- и βпинена.
16. Примеры защитных соединений «второго круга» обороны: цаногенные гликозиды, глюкозинолаты.
17. Третий круг обороны.
Проще всего доказать защитную роль вторичных метаболитов,участвующих в работе третьего круга обороны: фитоалексины
18. Общая схема ответа растения на атаку патогена
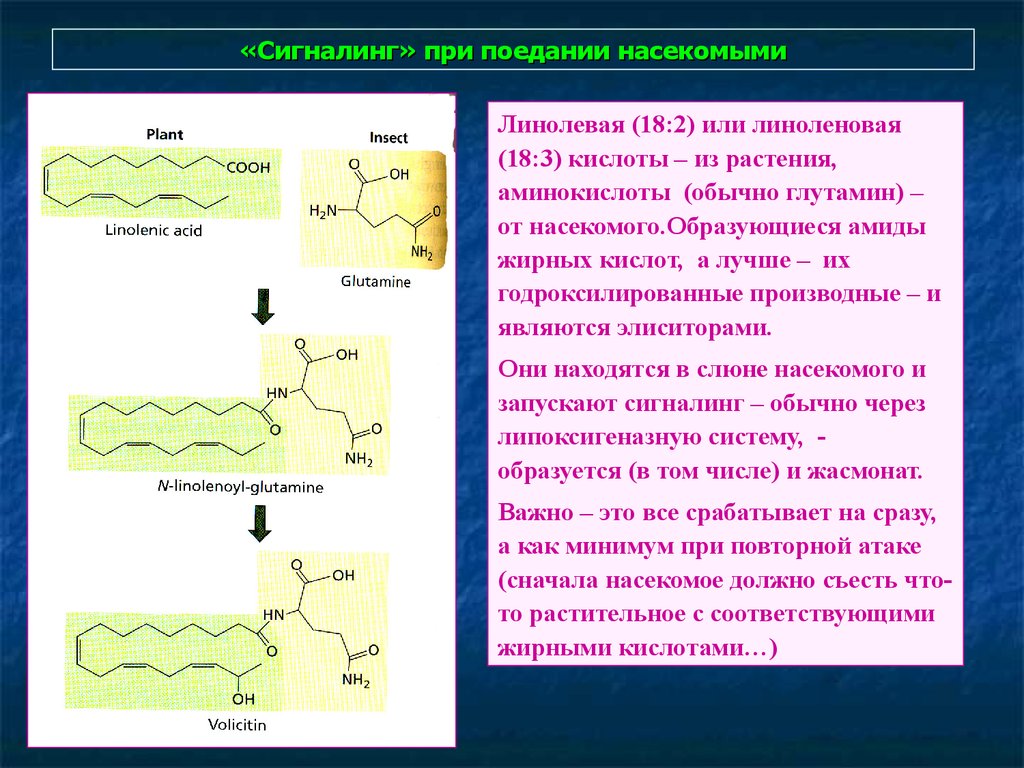
Рецептор19. «Сигналинг» при поедании насекомыми
Линолевая (18:2) или линоленовая(18:3) кислоты – из растения,
аминокислоты (обычно глутамин) –
от насекомого.Образующиеся амиды
жирных кислот, а лучше – их
годроксилированные производные – и
являются элиситорами.
Они находятся в слюне насекомого и
запускают сигналинг – обычно через
липоксигеназную систему, образуется (в том числе) и жасмонат.
Важно – это все срабатывает на сразу,
а как минимум при повторной атаке
(сначала насекомое должно съесть чтото растительное с соответствующими
жирными кислотами…)
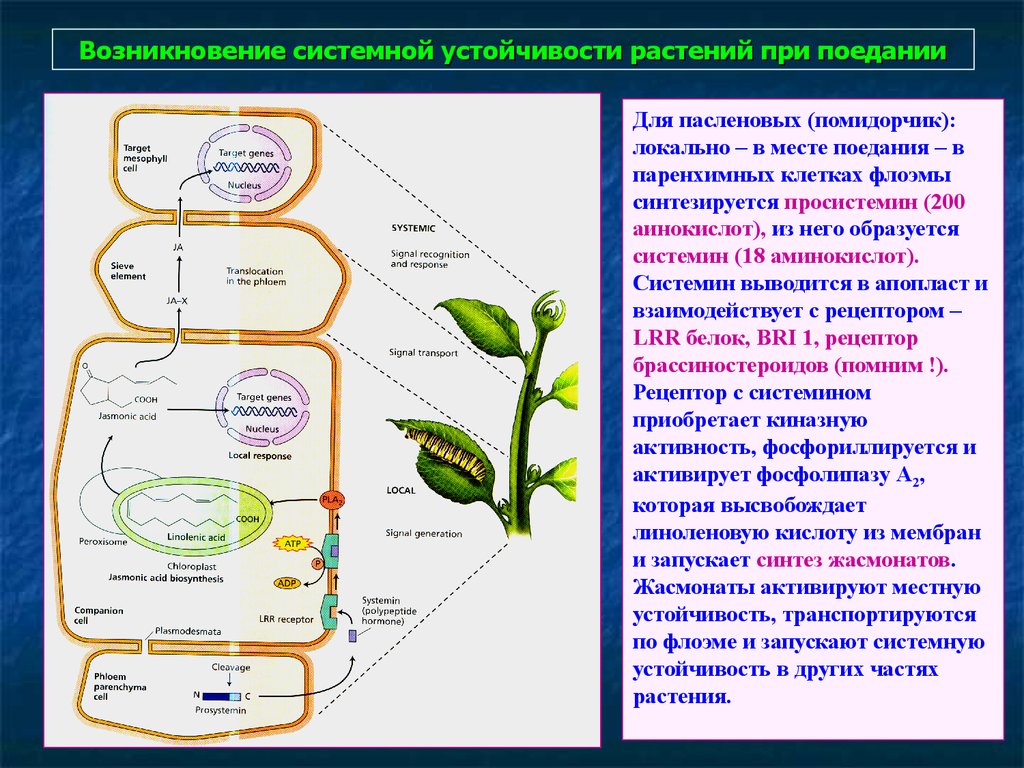
20. Возникновение системной устойчивости растений при поедании
Для пасленовых (помидорчик):локально – в месте поедания – в
паренхимных клетках флоэмы
синтезируется просистемин (200
аинокислот), из него образуется
системин (18 аминокислот).
Системин выводится в апопласт и
взаимодействует с рецептором –
LRR белок, BRI 1, рецептор
брассиностероидов (помним !).
Рецептор с системином
приобретает киназную
активность, фосфориллируется и
активирует фосфолипазу А2,
которая высвобождает
линоленовую кислоту из мембран
и запускает синтез жасмонатов.
Жасмонаты активируют местную
устойчивость, транспортируются
по флоэме и запускают системную
устойчивость в других частях
растения.
21. Жасмонат – основная сигнальная молекула для системной устойчивости.
В синтезе жасмоната участвуют двеорганеллы – хлоропласт и пероксисома.
Основные «конечные» продукты системы
защиты от поедания насекомыми:
• Ингибиторы α-амилазы (для бобовых) –
ингибируют амилазы и соответственно,
гидролиз крахмала насекомыми.
• Лектины – связываются в эпидермальных
клетках ЖКТ насекомого с углеводами и
гликолипидами и нарушают пищеварение
• Ингибиторы протеиназ. Тормозят
переваривание белков и из за отсутствия
аминокислот несекомое чувствует себя
неудовлетворительно…
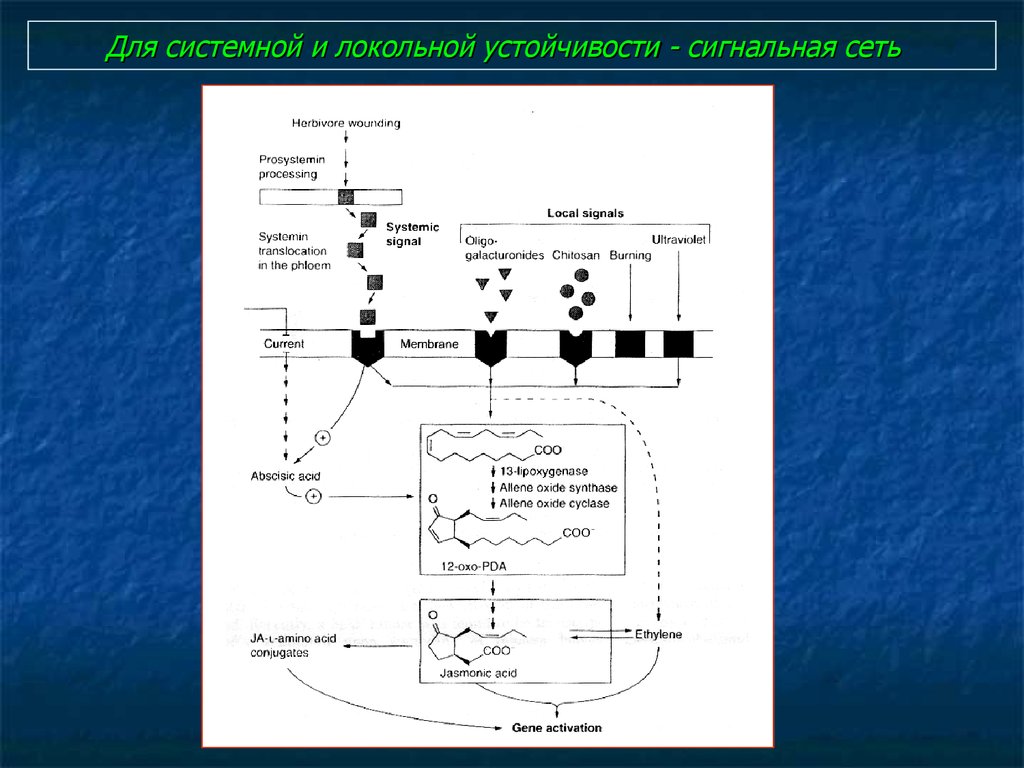
22. Для системной и локольной устойчивости - сигнальная сеть
23. «Сигналинг» при грибных и микробиальных инфекциях
Основные ферменты – NO-синтаза и НАДФ-оксидаза.Основные мессенджеры – NO и Н2О2 . Важно – что они работают вместе.
24. Общая схема ответа растения на атаку патогена
25. Этапы ответа растения на вторжение патогена
26. Протеин-киназы, участвующие в трансдукции защитного сигнала
Киназы, обнаружены в: табаке (красный), томатах (оранжевый), люцерне (синий),петрушке (желтый), рисе (коричневый), Arabidopsis (зеленый).
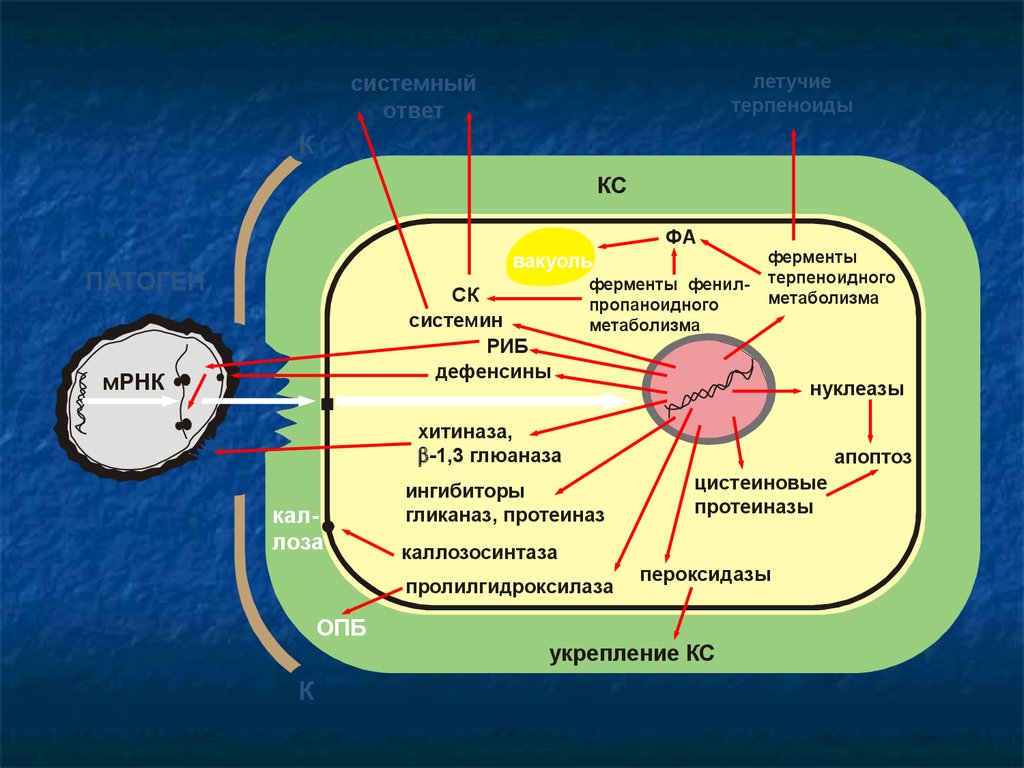
27.
летучиетерпеноиды
системный
ответ
К
КС
ФА
вакуоль
ПАТОГЕН
СК
системин
РИБ
дефенсины
мРНК
ферменты фенилпропаноидного
метаболизма
ферменты
терпеноидного
метаболизма
нуклеазы
хитиназа,
-1,3 глюаназа
каллоза
ингибиторы
гликаназ, протеиназ
каллозосинтаза
пролилгидроксилаза
апоптоз
цистеиновые
протеиназы
пероксидазы
ОПБ
укрепление КС
К
28. Возникновение системной устойчивости растений
29. Общая схема ответа растения на патогенез
30. Фитоалексины – индуцибельные вторичные метаболиты
31. Вторичный метаболизм растений: 116 лет исследований, или откуда все это началось…
Из лекции «О химическом составе клеток» немецкогобиолога Альбрехта Косселя, которую он прочел для
Берлинского общества физиологов 1891 году:
“В то время как первичные метаболиты присутствуют в каждой
растительной клетке, способной к делению, то вторичные
метаболиты присутствуют в клетках только “нечаянно” и не
необходимы для жизни растения. ... Случайное
распространение этих соединений, их нерегулярное
нахождение в близких видах растений, вероятно,
свидетельствует о том, что их синтез связан с процессами, не
являющимися неотъемлемыми для каждой клетки, а имеющими
скорее вторичный характер.... Я предлагаю называть
соединения, имеющие важность для каждой клетки
первичными, а соединения, не присутствующие в любой
растительной клетке - вторичными”
32. Растения отличают от других организмов два принципиально важных процесса: фотосинтез и вторичный метаболизм Академик А.Т.Мокроносов
Вторичные метаболиты:относительно низкомолекулярные соединения
не обязательно присутствуют в каждом растении
как правило, являются биологически активными соединениями
синтезируются из немногих первичных метаболитов.
Основные классы:
алкалоиды:
изопреноиды:
фенольные соединения
минорные группы
~ 12 000 структур
~ 35 000 структур
~ 8 000 структур
~ 10 000 ?
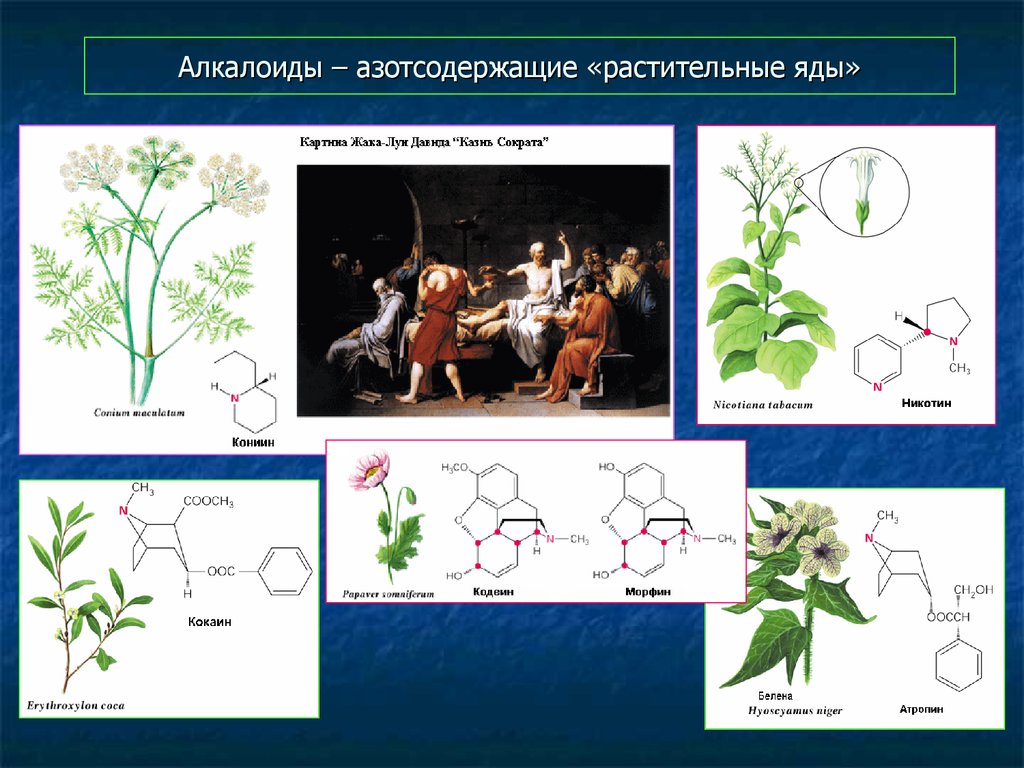
33. Алкалоиды – азотсодержащие «растительные яды»
34. … как, впрочем, и лекарства…
35. Алкалоиды разделяются на протоалкалоиды, истинные алкалоиды и псевдоалкалоиды
36.
Протоалкалоиды: азот не в гетероциклеТри группы:
1. Алифатические.
Около 50 структур; 15 семейств
Представитель - сферофизин
2. Фенилалкиламины
Около 100 структур; 37 семейств
Представители - капсаицин, эфедрин
3. Колхициновые.
Около 30 структур; лилейные, ирисовые
Представители – колхицин, колхамин
Capsicum annuum
Перец стручковый
37.
Мелантиевые(бывшие Лилейные)
Colchicum boehrnmuellerii
Б. Борнмюллера
весенние листья
Colchicum speciosum
Безвременник великолепный
Протоалкалоиды
Colchicum umbrosum,
Безвременник теневой
Крым, Кавказ
Colchicum ‘Waterlily’ –
межвидовой гибрид
38.
Nicotianaplumbaginifolia
Nicotiana langsdorfii
Nicotiana affinis
Пиридиновый
алкалоид никотин
Sedum album также
содержит алкалоид
никотин
Nicotiana sylvestris
39.
Алкалоиды тропановогоряда синтезируются из
L-орнитина.
В пасленовых одержатся:
атропин, скополамин,
гиосциамин.
Дурман индейский
Datura inoxia
Дурман обыкновенный
Datura stramonium
(алкалоид скополамин)
Скополия карниолийская
Scopolia carniolica
(алкалоид скополамин, атропин)
40.
АмариллисовыеLeucojum vernum
Leucojum aestivum
Galanthus woronowii
Leucojum aestivum
Galanthus nivalis
Galanthus nivalis f. plena
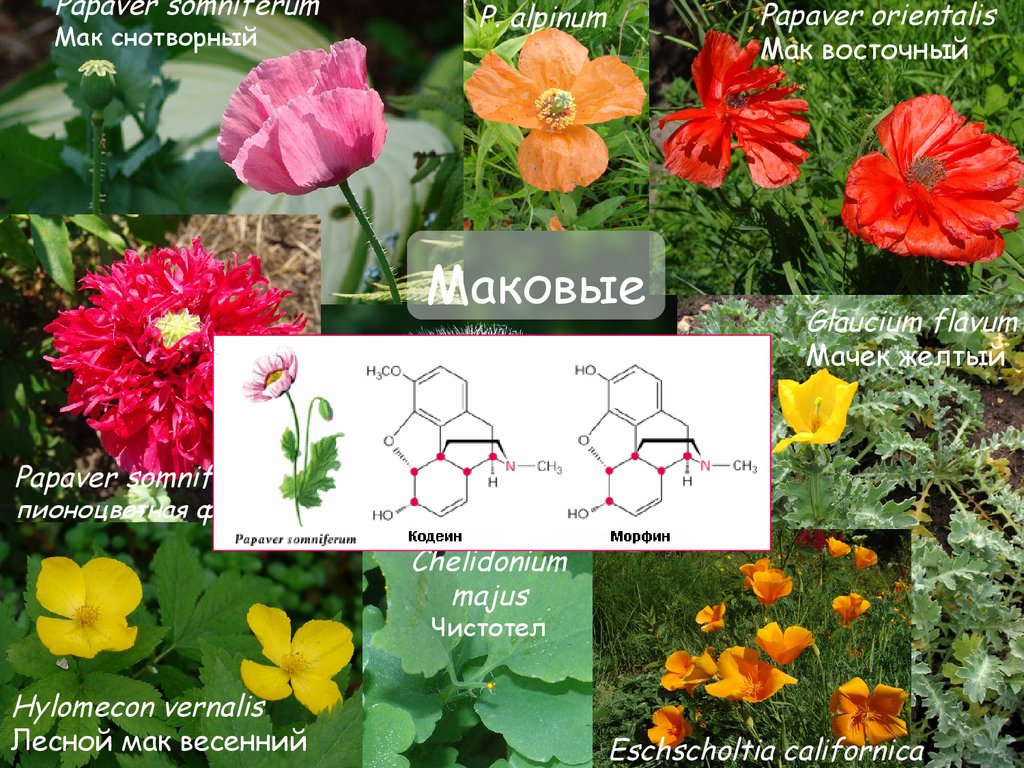
41.
Papaver somniferumМак снотворный
Papaver orientalis
Мак восточный
P. alpinum
Маковые
Glaucium flavum
Мачек желтый
Papaver somniferum
пионоцветная форма
Chelidonium
majus
Чистотел
Hylomecon vernalis
Лесной мак весенний
Eschscholtia californica
42.
ПсевдоалкалоидыЛютиковые
Дитерпеновые псевдоалкалоиды
Аконитин, атизин.
Насчитывается 37 видов аконита,
произрастающего в странах Азии,
на Сахалине, Камчатке. Аконитин
опасен не только при попадании с
пищей и водой, но и при
нанесении на неповрежденную
кожу. Слюнотечение, рвота, понос.
Далее слабость, озноб, резкое
нарушение сердечного ритма. Зуд,
двигательное возбуждениепаралич.
Наиболее ядовиты A.ferox и
A.fischeri
Aconitum lanuginosum
Аконит шерстистый
Aconitum napellus
Аконит клобучковый
43.
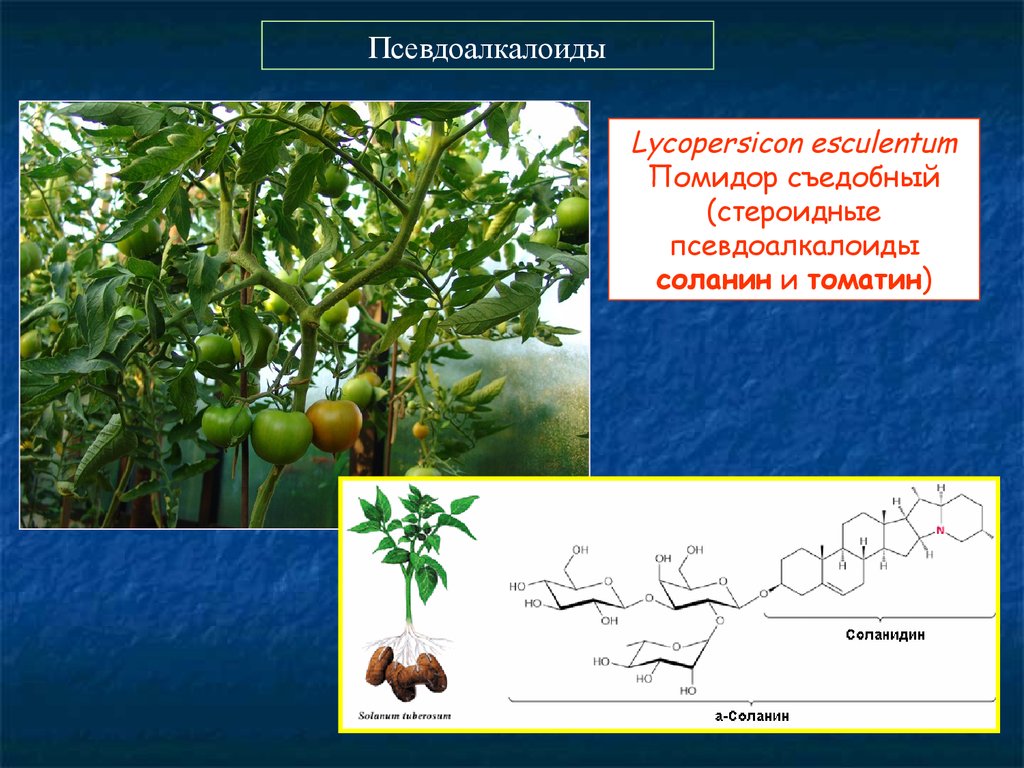
ПсевдоалкалоидыLycopersicon esculentum
Помидор съедобный
(стероидные
псевдоалкалоиды
соланин и томатин)
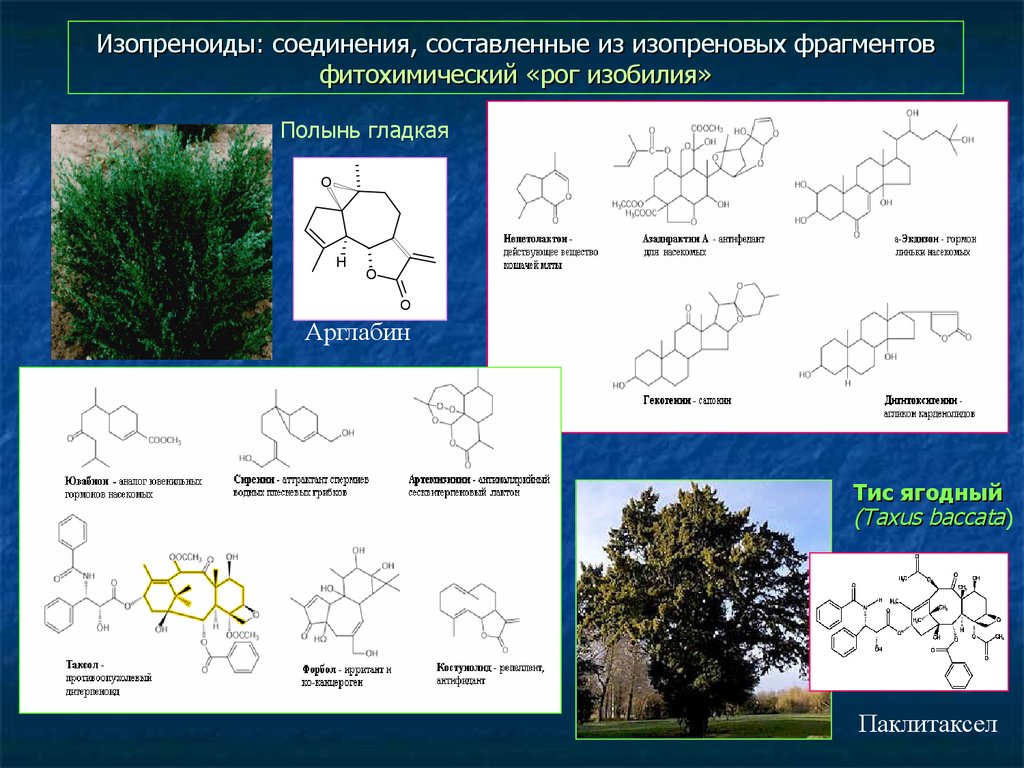
44. Изопреноиды: соединения, составленные из изопреновых фрагментов фитохимический «рог изобилия»
Полынь гладкаяO
H
O
O
Арглабин
Тис ягодный
(Taxus baccata)
Паклитаксел
45. Монотерпены, С10-соединения. Компоненты эфирных масел
46.
OHO
OCH3
OH
CH2
OH
O
methylsalicylate
H
limonene
H
linalool
benzaldehyde
phenylethanol
CH2
OH
O
OH
OH
O
H
eugenol
CH2
linalool
phenylacetaldehyde
phenylacetaldehyde
linalool
O
OH
O
OH
neral
linalool
OH
linalool
geranial
OH
CH2
nerolidol
limonene
phenylethanol
OH
CH2
OH
OH
linalool
geraniol
phenylethanol
OCH3
47. Тетрациклические дитерпеновые гликозиды стевии Stevia rebaudiana – некоторые из них в 300 раз слаще сахара…
СтевиозидR1: Glu
R2: Glu- Glu
Ребаудиозид А
R1: Glu
R2: Glu- Glu
|
Glu
Ребаудиозид С
R1: Glu
R2: Glu- Rha
|
Glu
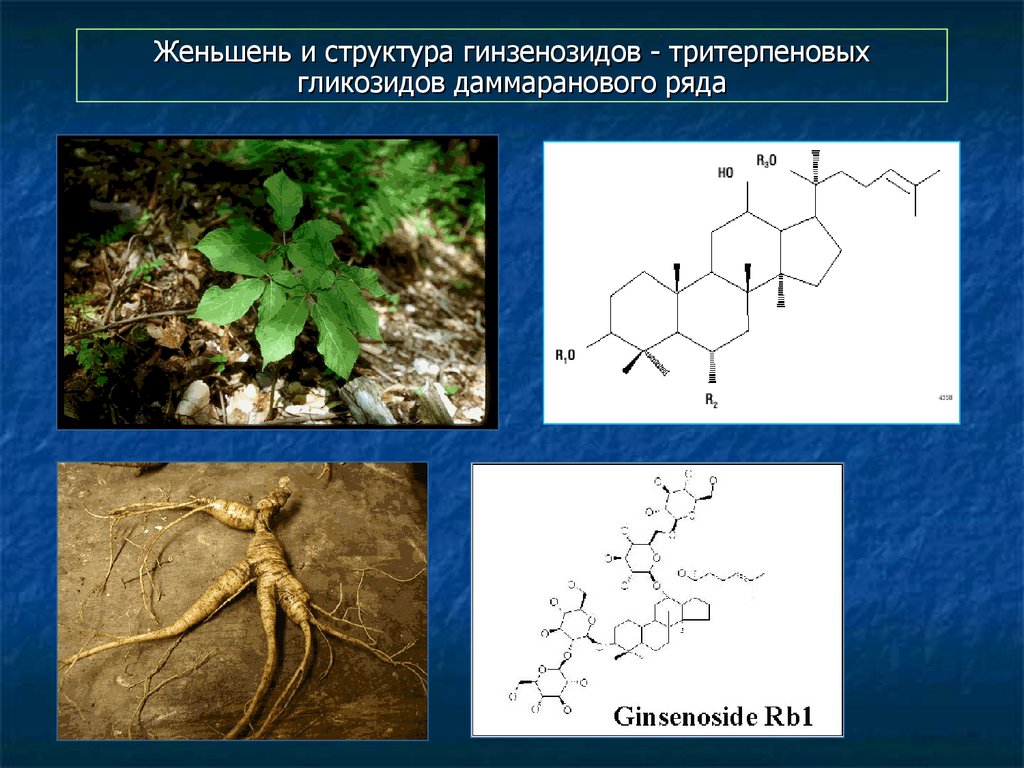
48. Женьшень и структура гинзенозидов - тритерпеновых гликозидов даммаранового ряда
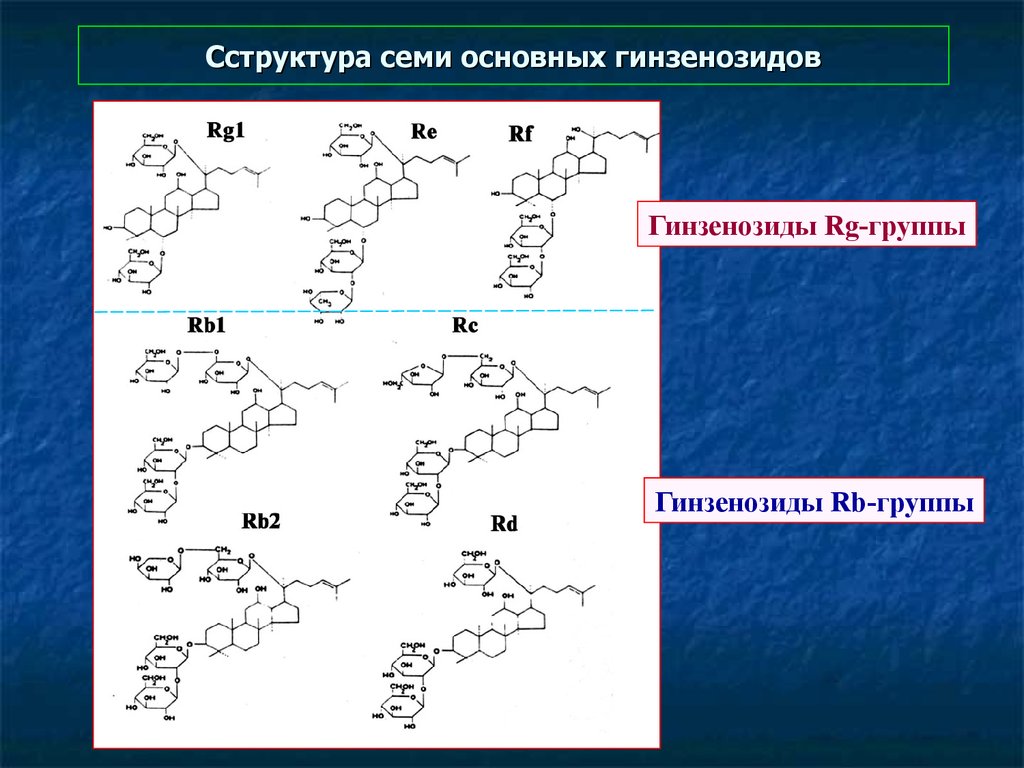
49. Cструктура семи основных гинзенозидов
Гинзенозиды Rg-группыГинзенозиды Rb-группы
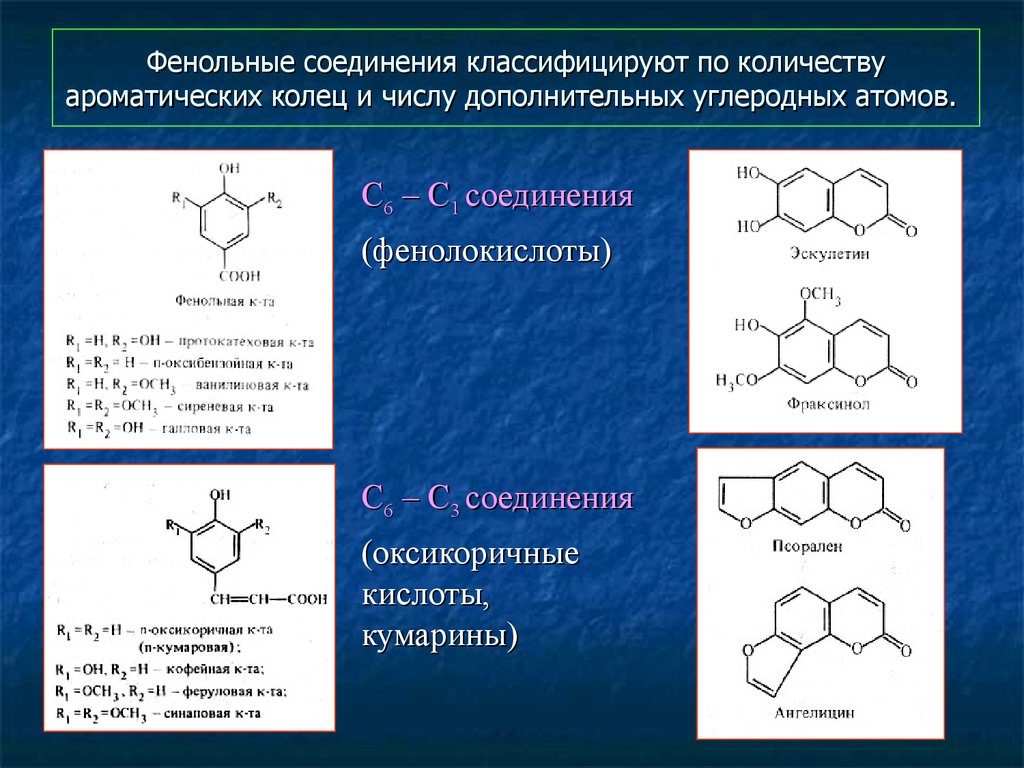
50. Фенольные соединения классифицируют по количеству ароматических колец и числу дополнительных углеродных атомов.
С6 – С1 соединения(фенолокислоты)
С6 – С3 соединения
(оксикоричные
кислоты,
кумарины)
51. Вся радуга окраски цветков обусловлена гликозидами трех флавоноидов (проантоцианидинов) – но с модификациями…
52. Антоцианы – гликозиды антоцианидинов
Цвет антоциановопределяется многими
факторами…
53. Фенольные соединения тоже небесполезны…
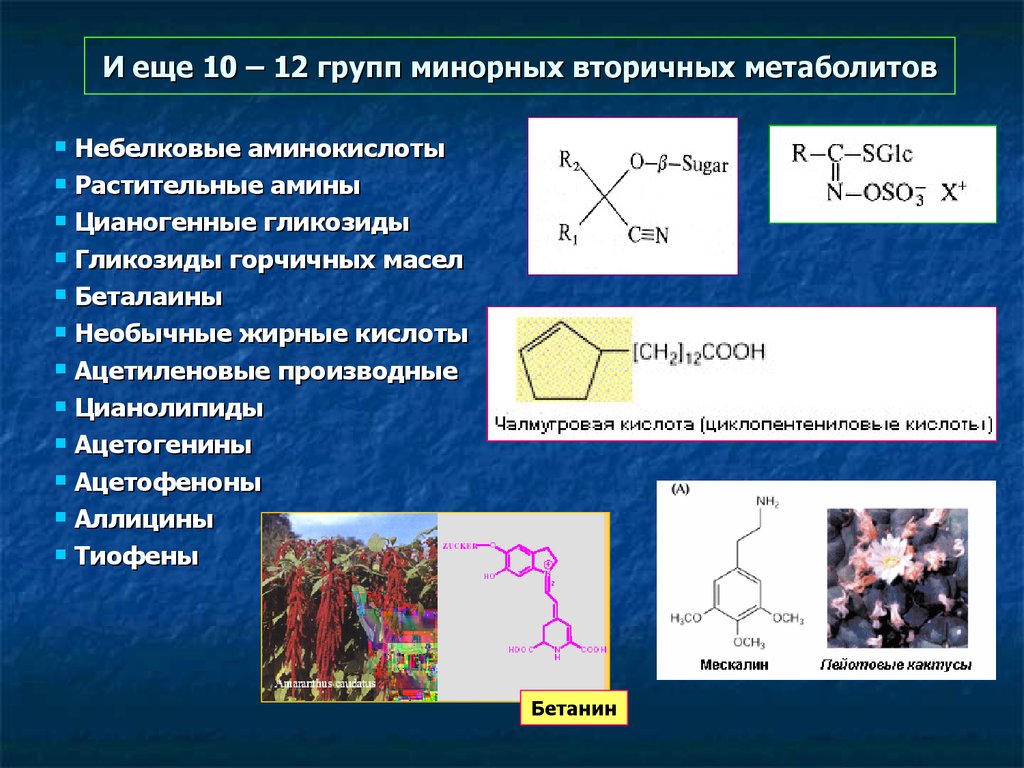
54. И еще 10 – 12 групп минорных вторичных метаболитов
Небелковые аминокислотыРастительные амины
Цианогенные гликозиды
Гликозиды горчичных масел
Беталаины
Необычные жирные кислоты
Ацетиленовые производные
Цианолипиды
Ацетогенины
Ацетофеноны
Аллицины
Тиофены
Бетанин
55. Небелковые аминокислоты
Более 500 представителей. Найдены прежде всего в растениях, хотя есть и в грибах.Присутствуют либо в свободном виде, либо в виде небольших конъюгатов.
Некоторые являются первичными метаболитами (орнитин, гомосерин, )
Часто – модификации белковых аминокислот
Классификация:
примеры
Нейтральные алифатические (5-гидроксинорлейцин, Crotolaria juncea )
Дикарбоновые (кислые)
(γ-метилен-L-глутаминовая кислота, земляной орех)
Основные
(γ-гидроксиогомоаргинин Lathyrus tinigitanus)
Серусодержащие
(S-метил-L-цистени Phaseolus vulgaris)
Селенсодержащие
(Se-метил-L-цистени Astragalus spp,)
Ароматические
(2,4-дигидрокси-метилфенилаланин, куколь посевной)
Гетероциклические (Мимозин, Mimosa pudica)
Ацетилированные
(N-ацетил-L-орнитин, широко распространен)
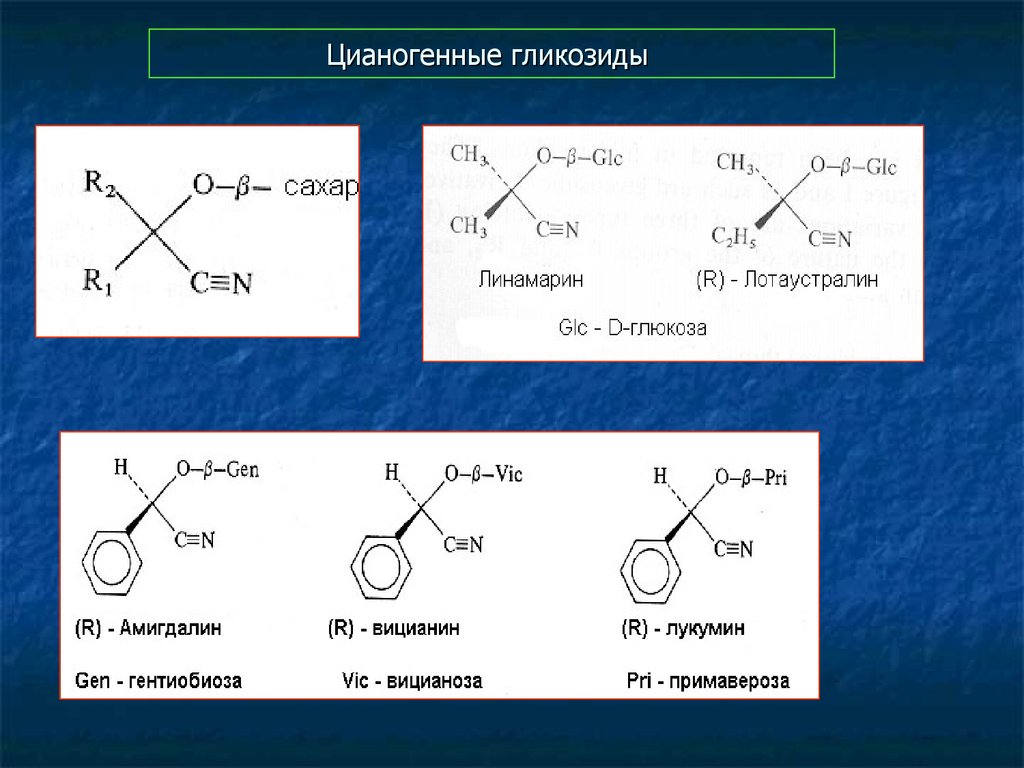
56. Цианогенные гликозиды
57. Глюкозинолаты
58. Беталаины
СахарАнтоциан (цианидин-гликозид)
Бетациаанин
59. Аллицины
60. Необычные жирные кислоты
61. Цианолипиды
Характерны для семействаSapindaceae, но найдены
также и у
Hippocastaneaceae и
Boraginaceae.
62. Ацетиленовые соединения
Чем отравили Сократа?Ядовитые полиацетилены веха болотного
Цикутотоксин
НО(СН2)3 -С≡С-С≡С-(СН=СН)3 -СН(ОН)-(СН2)2-СН3
Энантотоксин
НОСН2 -СН=СН-С≡С-С≡С-(СН=СН)2 -(СН2)2 -СН(ОН)-(СН2)2 -СН3
63. Еще один пример - необычные сахара
64. Как образуется это разнообразие структур? Общие принципы.
Предшественниками синтеза служат относительнонебольшое количество первичных метаболитов.
Синтез четко спланирован и обслуживается набором
специальных ферментов, причем некоторые из них
весьма специфичны, а некоторые – нет
Для многих групп вторичных метаболитов
существует несколько путей их синтеза. Часто этапы
синтеза дублированы в разных компартментах клетки
(например, пластиды – цитозоль).
65. Биохимический моделист-конструктор. 1 этап
Образуется «скелет» молекулы - "базовая" структура, наоснове которой затем формируются многочисленные варианты.
Принципы формирования «скелета» различны для разных групп
вторичных метаболитов.
Для изопреноидов – формирование гибких цепочек разной
длины - 10, 15, 20, 30, 40 атомов углерода (пренилтрансферазы),
а затем сворачивание их в разнообразные циклы (циклазы).
Для алкалоидов – формирование гетероциклов за счет
конденсации аминоальдегидов и/или аминокетонов,
получаемых из аминов (аминооксидазы), которые в свою
очередь формируются из аминокислот (декарбоксилазы)
66. Биохимический моделист-конструктор. 2 этап
«Декорирование» скелета: метилирование, ацилирование,десатурация, гидроксилирование, гликозилирование.
«Декорирование» может кардинально менять биологическую
активность молекулы.
У арабидопсиса в геноме:
Найдено более 300 (!) генов различных изоформ цитохрома
Р450. Трансгенные растения арабидопсиса и табака с двумя
чужеродными генами «цианогенных» цитохромов синтезировали
цианогенные гликозиды.
Найдены гены более 100 диоксигеназ. Диоксигеназы участвуют в
биосинтезе алкалоидов, флавонидов, гиббереллинов, этилена. Для
них характерна широкая субстратная специфичность возможность использовать разные субстраты и образовывать
несколько продуктов.
67. Биохимический моделист-конструктор. 2 этап
Ацилтрансферазы. У арабидопсиса – более 50 генов.Ацилтрансферазы вторичного метаболизма у разных видов
структурно близки и имеют консервативный гистидинсодержащий мотив. Структурно они также похожи на
ацилтрансферазы первичного метаболизма. Гены ацилрансфераз
в арабидопсисе собраны в кластеры на 5 хромосоме, тогда как
гены диоксигеназ разбросаны по геному
Метилтрансферазы. O-, C-, N-и S- метилтрансферазы,
метилируют флавониды, изопреноиды, алкалоиды, полиамины,
поликетиды. C-, N-и S- метилтрансферазы эволюционно не
связаны, О-метилтрансферазы представляют одну группу и
имеют консервативный SАМ-связывающий мотив.
Гликозилтрансферазы. O-, C-, S- гликозилтрансферазы.
68. Образование изохинолиновых алкалоидов. Формирование исходной структуры.
69. Образование изохинолиновых алкалоидов. Формирование «скелетов»
70. Образование индольных алкалоидов. Формирование «скелетов».
71. Синтез изопреноидов. Формирование исходных структур («цепочек»)
72. Образование изопреноидов: формирование «скелетов»
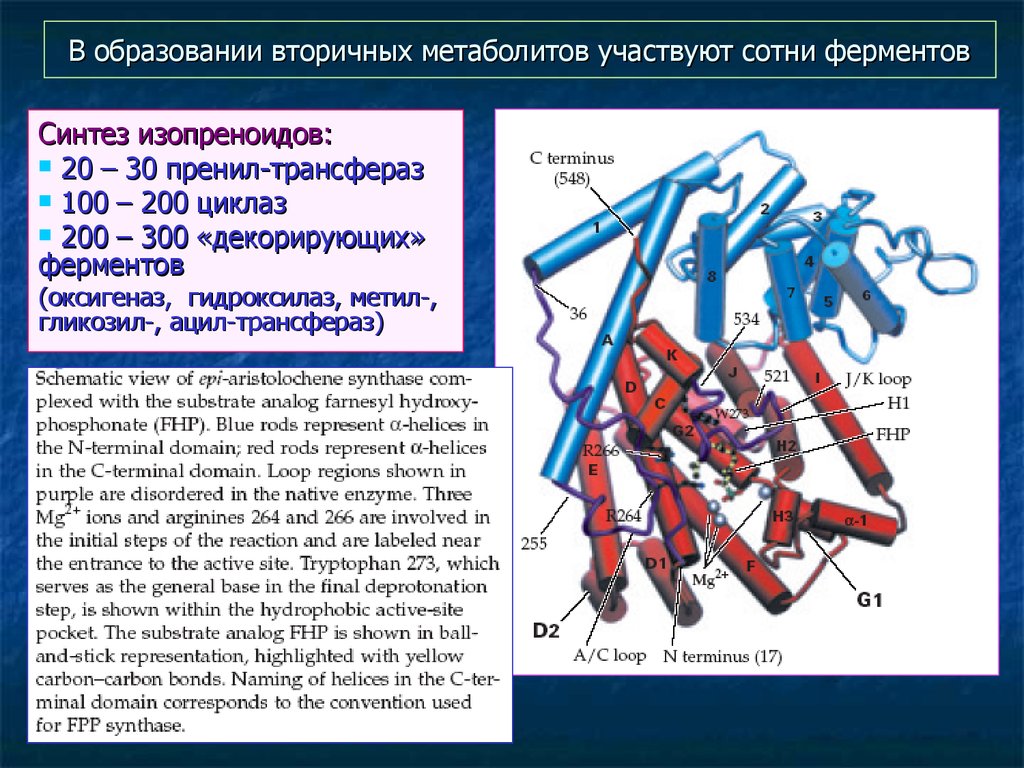
73. В образовании вторичных метаболитов участвуют сотни ферментов
Синтез изопреноидов:20 – 30 пренил-трансфераз
100 – 200 циклаз
200 – 300 «декорирующих»
ферментов
(оксигеназ, гидроксилаз, метил-,
гликозил-, ацил-трансфераз)
74.
Возможные пути биосинтеза летучих бензоидов ифенилпропаноидов в цветках петунии
OH
C
O
C
OH
O
CH2
O
OH
CH2
phenylpyruvic acid
B
BP
CH2
dehydrogenase
CO2
2-phenylethylamine
80OH
OH
phenylacetaldehyde
T
phenylethanol
O
O
CoA ligase
C
OH
hydration
* 2 *PAL
H5 PAL
H2O
*L-phenylalanine
*
trans-cinnamic acid
*
2
H5-Phe
GTase
retro-aldol
cleavage
O
O
CoA-SH
CoA-independent,
O
H3
2
lignin
OCH3
eugenol
OH
OCH3
isoeugenol
O-glucose
55 75 95 115
155
methylbenzoate
O
hydroxylase
benzoyl-glucose
OCH3
OH
OH
T
M
A
methylsalicylate
S
OH
salicylic acid
SA GTase
O
m/z
O
OH
salicyloyl-CoA
GTase
195
d5-labeled
OCH3
BA2H
non- -oxidative
155
O
O
benzaldehyde NAD NADH benzoic acid
3-hydroxy-3-phenyl
propionic acid
OH
flavonoids
OH
dehydrogenase
O
para-coumaric acid
C
0
BZL
H
CH3COO-
C4H
O-glucose
O
SCoA
O
benzoyl-CoA
CH3CO-SCoA
CoA-SH
benzylbenzoate
80
40
hydroxylase
thioesterase
CoA-SH
3-oxo-3-phenyl
propionyl-CoA
retro-aldol
cleavage
COOH
NH2
NH
2
cinnamoylglucose
C
thiolase
e
NADH
O
0BPBT
55 75 95 115
O
120
SCoA
CH3CO-SCoA
dehydrogenase
NAD
3-hydroxy-3-phenyl
propionyl-CoA
CoA-SH
O
OH
COOH
C
OH
C
oge
na s
enoyl-CoA
hydratase
CoA lig
ase
phe
tran nylala
sam nin
in a e
se
phenylalanine
decarboxylase
O
H2O
trans-cinnamoyl-CoA
SCoA
SCoA
C
ydr
C
deh
CO2
..
40
benzylalcohol
CoA-dependent, -oxidative
SCoA
unlabeled
thioesterase
CH2
phenyllactic acid
ase
CH2
H
O
T
O
C=O
BS
M
NH2
Relative Ion Intensity
CH2
Methylbenzoate
120
phenylethylbenzoate
este
r
C
O-glucose
OH
salicyloyl-glucose
195
m/z
75.
Пути синтеза бензоидов в цветках петунии ночью и днемСвет
толщина линии отражает интенсивность потока
Темнота
нет потока
очень слабый поток
Синтез бензойной кислоты из бензилбензоата является
светозависимым процессом.
Orlova et al. (2006) Plant Cell 18
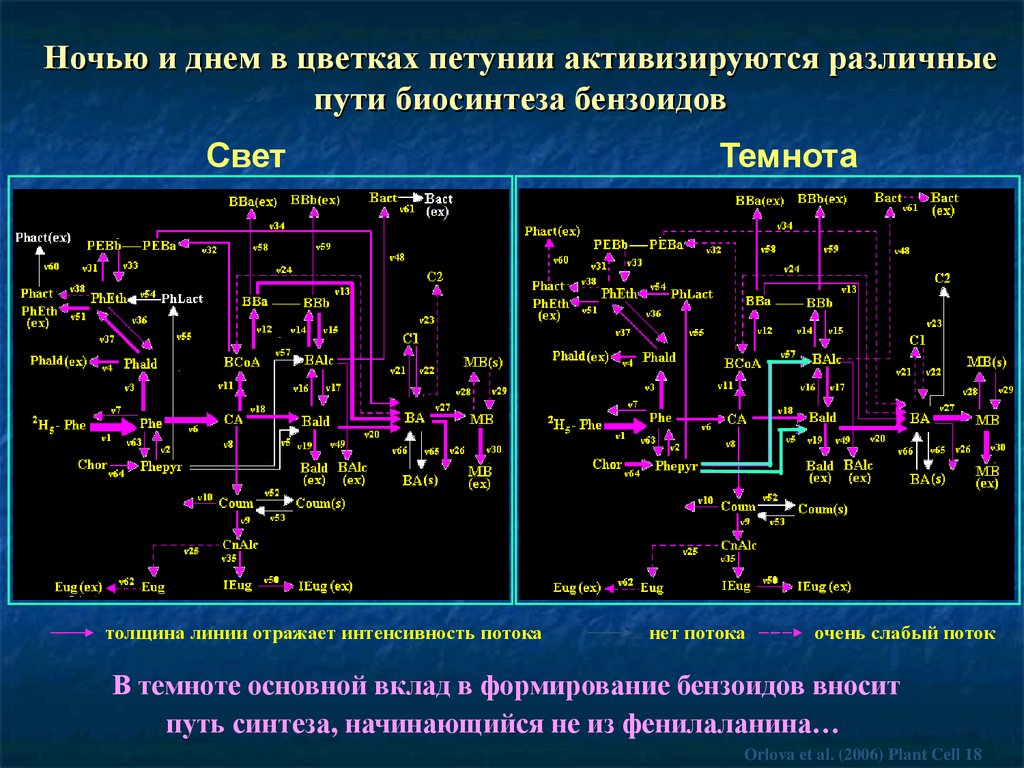
76.
Ночью и днем в цветках петунии активизируются различныепути биосинтеза бензоидов
Свет
толщина линии отражает интенсивность потока
Темнота
нет потока
очень слабый поток
В темноте основной вклад в формирование бензоидов вносит
путь синтеза, начинающийся не из фенилаланина…
Orlova et al. (2006) Plant Cell 18
77. Синтез и накопление вторичных метаболитов как правило, пространственно разделены
Внутриклеточное разделение:Синтез: цитозоль, ЭР, пластиды.
Накопление: вакуоль,
периплазматическое пространство
Флуоресценция стероидных
гликозидов в клетке
Dioscorea deltoidea in vitro
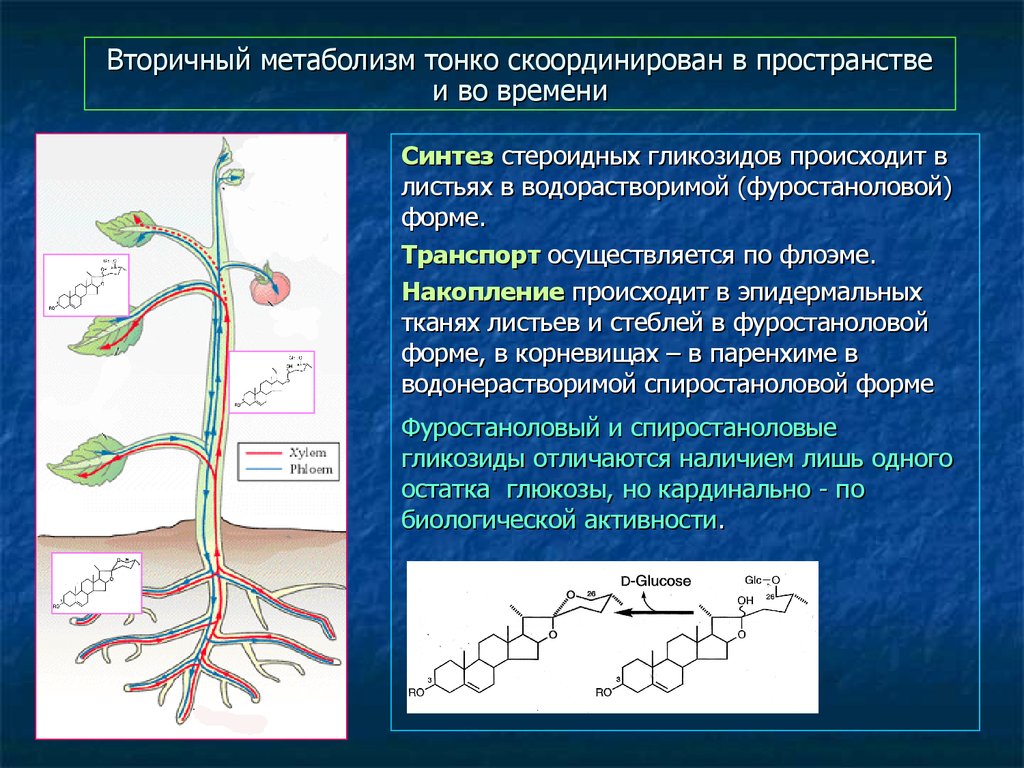
78. Вторичный метаболизм тонко скоординирован в пространстве и во времени
Синтез стероидных гликозидов происходит влистьях в водорастворимой (фуростаноловой)
форме.
Транспорт осуществляется по флоэме.
Накопление происходит в эпидермальных
тканях листьев и стеблей в фуростаноловой
форме, в корневищах – в паренхиме в
водонерастворимой спиростаноловой форме
Фуростаноловый и спиростаноловые
гликозиды отличаются наличием лишь одного
остатка глюкозы, но кардинально - по
биологической активности.
79. Локализация синтеза индольных алкалоидов Catharaynthus roseus
TDC (триптофандекарбоксилаза)
STR-1 (стриктозидин
синтаза локализованы в
клетках верхнего и
нижнего
эпидермиса листа.
D4H
(дезацетоксивиндолин –
гидроксилаза
DAT (деацетилвиндолин
4-О-ацетилтрансфераза)
– экспрессируются в
идиобластах и
млечниках листа.
TDC и STR-1 также
экспрессируются в в
протодерме корня и
кортикальных клетках
корня вокруг
апикальной меристемы.
Синтез идет только в
молодых листьях и
корнях.
80. Трихомы и железы листа стевии – синтез и выделение вторичных метаболитов
81. Зачем нужен вторичный метаболизм растению?
Основные точки зрения:Совсем не нужен (вторичные метаболиты – «отходы
производства»)
Вторичные метаболиты – запасные соединения
Вторичные метаболиты – защитные соединения
Вторичные метаболиты – «биохимические инструменты»
взаимодействия растения с окружающей средой
Но как это доказать ?































































 Биология
Биология








