Похожие презентации:
Неметаллы. Общие свойства
1.
В воздухе он главный газ,Окружает всюду нас.
Угасает жизнь растений
Без него, без удобрений.
В наших клеточках живет
Важный элемент …
В чем горят дрова и газ,
Фосфор, водород, алмаз?
Дышит чем любой из нас
АЗОТ
Каждый миг и каждый час?
Без чего мертва природа?
Правильно, без …
Удивить готов он нас Он и уголь, и алмаз,
Он в карандашах сидит,
КИСЛОРОДА
Потому что он — графит.
Грамотный народ поймет
То, что это …
УГЛЕРОД
2. Тема урока: «Общая характеристика неметаллов»
ТЕМА УРОКА:«ОБЩАЯ
ХАРАКТЕРИСТИКА
НЕМЕТАЛЛОВ»
3.
НЕМЕТАЛЛЫ - это химическиеэлементы, для атомов
которых характерна
способность принимать
электроны до завершения
внешнего уровня.
ЭЛЕМЕНТЫ
109
НЕМЕТАЛЛЫ
22
МЕТАЛЛЫ
87
4. 1.Неметаллы
1.НЕМЕТАЛЛЫОбщая характеристика
Кислород и кремний составляют 76% от массы
земной коры (О – 49%, Si – 27%)
C,H,O,N,P,S – биогенные элементы, составляют
98,5% от массы растений и 97,6% от массы тела
человека
5. Неметаллы
НЕМЕТАЛЛЫОбщая характеристика
В состав земной атмосферы входят простые и
сложные вещества, образованные элементаминеметаллами (N2-75,5%, O2-23,2%, а также
CO2,H2O и др.)
Водород – главный элемент Вселенной (Солнце
и другие звёзды, газовые облака и т.д.) Из
каждых 100 атомов на Земле 17 – это атомы
водорода.
6. 2.Распространенность химических элементов Неме
2.РАСПРОСТРАНЕННОСТЬХИМИЧЕСКИХ ЭЛЕМЕНТОВ
НЕМЕ
7.
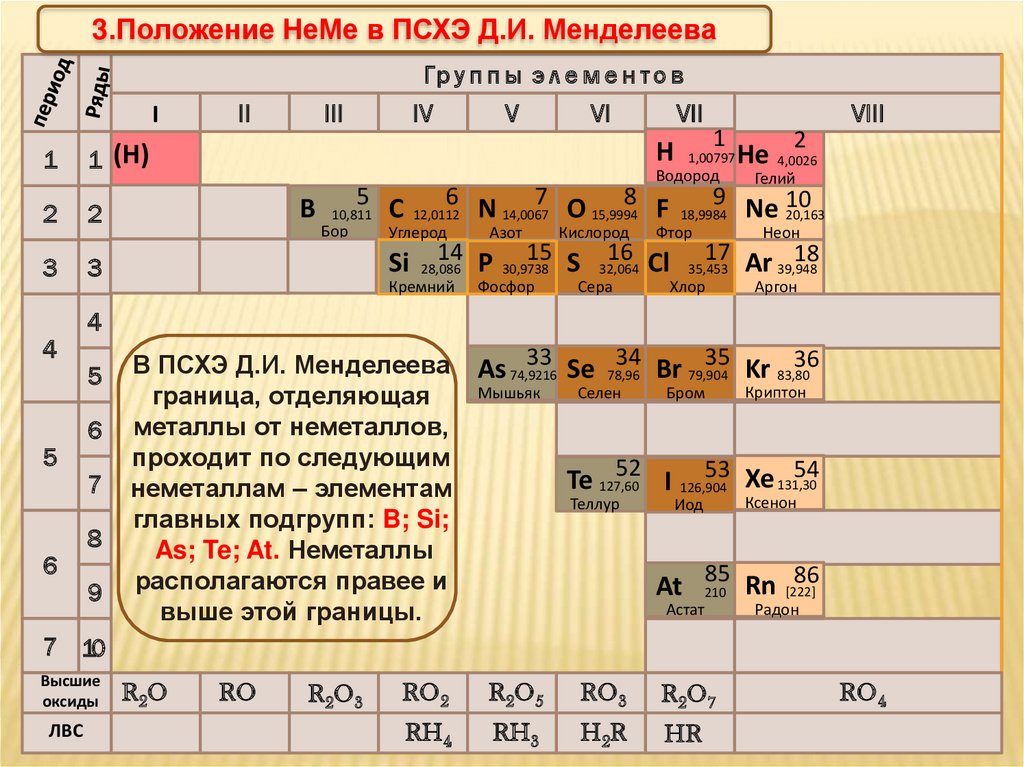
3.Положение НеМе в ПСХЭ Д.И. МенделееваГр у п п ы э л е м е н т о в
I
1
1 (H)
2
2
3
3
4
5
6
II
III
IV
V
VI
VII
Н
В
5
10,811
Бор
С
6
12,0112
Углерод
1
1,00797
Водород
7
8
N 14,0067
O 15,9994
F
Азот
14 Р
Si 28,086
Кремний
VIII
Кислород
15 S
30,9738
Фосфор
9
18,9984
Фтор
16 Cl
32,064
Сера
2
He 4,0026
Гелий
Ne 10
20,163
Неон
17 Ar 18
39,948
35,453
Хлор
Аргон
4
5
6
7
8
9
33
34
35
36
В ПСХЭ Д.И. Менделеева As 74,9216
Kr 83,80
Se 78,96
Br 79,904
Криптон
Мышьяк
Селен
Бром
граница, отделяющая
металлы от неметаллов,
проходит по следующим
52
53 Xe 131,30
54
Te
I
127,60
126,904
неметаллам – элементам
Ксенон
Теллур
Иод
главных подгрупп: B; Si;
As; Te; At. Неметаллы
86
располагаются правее и
At 85
210 Rn [222]
Радон
Астат
выше этой границы.
7 10
Высшие
оксиды
ЛВС
R2O
RO
R2O 3
RO2
R2O 5
RO3
R2O 7
RH4
RH3
H2R
HR
RO4
8.
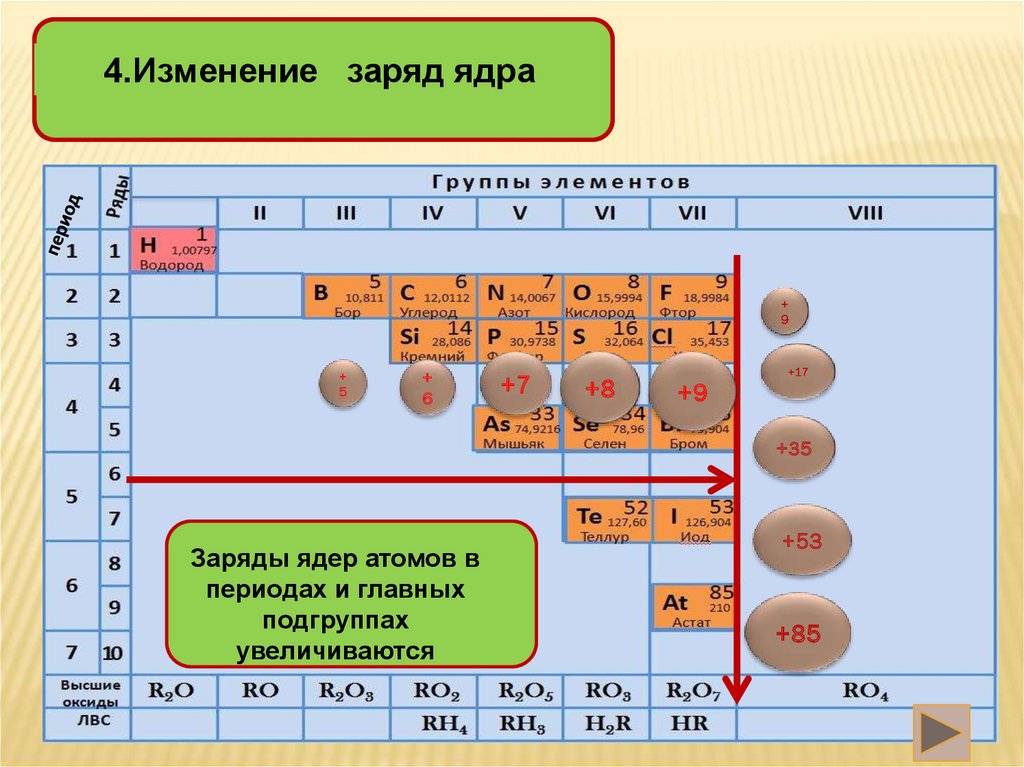
4.Изменение заряд ядра+
9
+
5
+
6
+7
+8
+9
+17
+35
Заряды ядер атомов в
периодах и главных
подгруппах
увеличиваются
+53
+85
9.
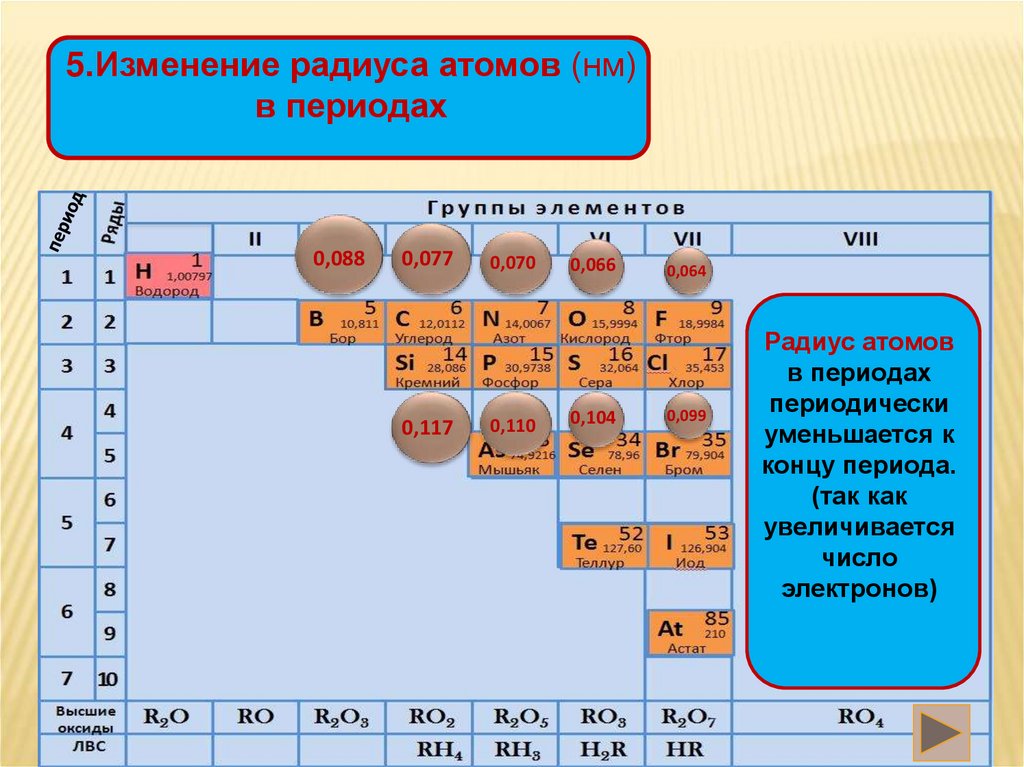
5.Изменение радиуса атомов (нм)в периодах
0,088
0,077
0,117
0,070
0,110
0,066
0,104
0,064
0,099
Радиус атомов
в периодах
периодически
уменьшается к
концу периода.
(так как
увеличивается
число
электронов)
10.
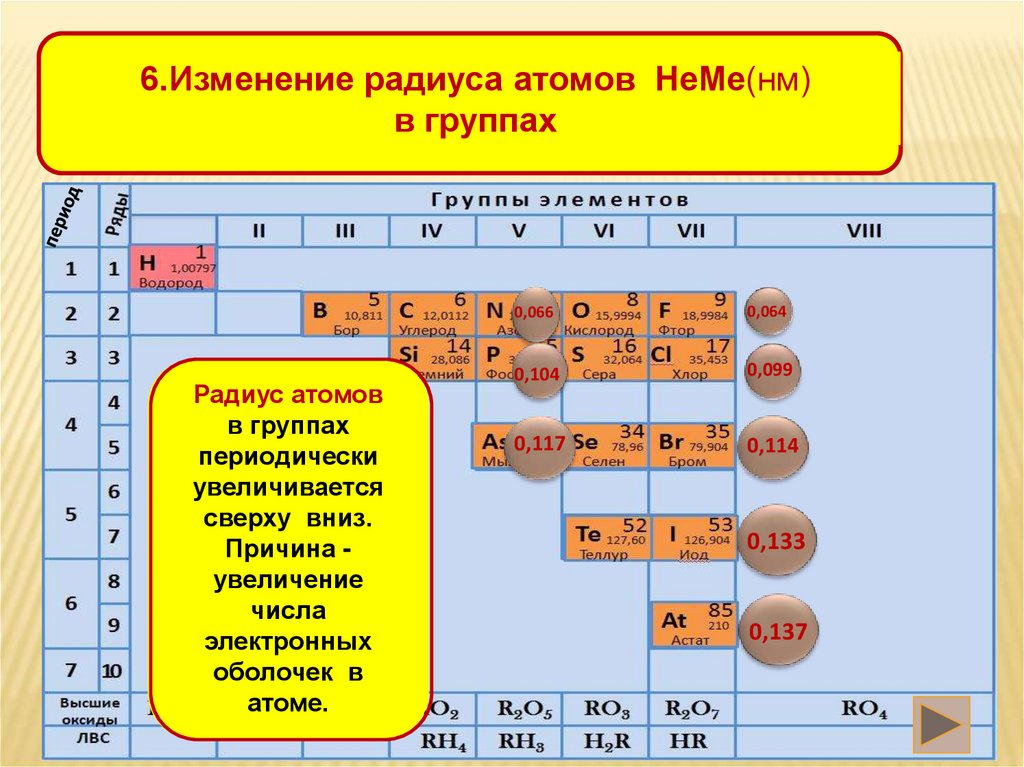
6.Изменение радиуса атомов НеМе(нм)в группах
Радиус атомов
в группах
периодически
увеличивается
сверху вниз.
Причина увеличение
числа
электронных
оболочек в
атоме.
0,066
0,064
0,104
0,099
0,117
0,114
0,133
0,137
11.
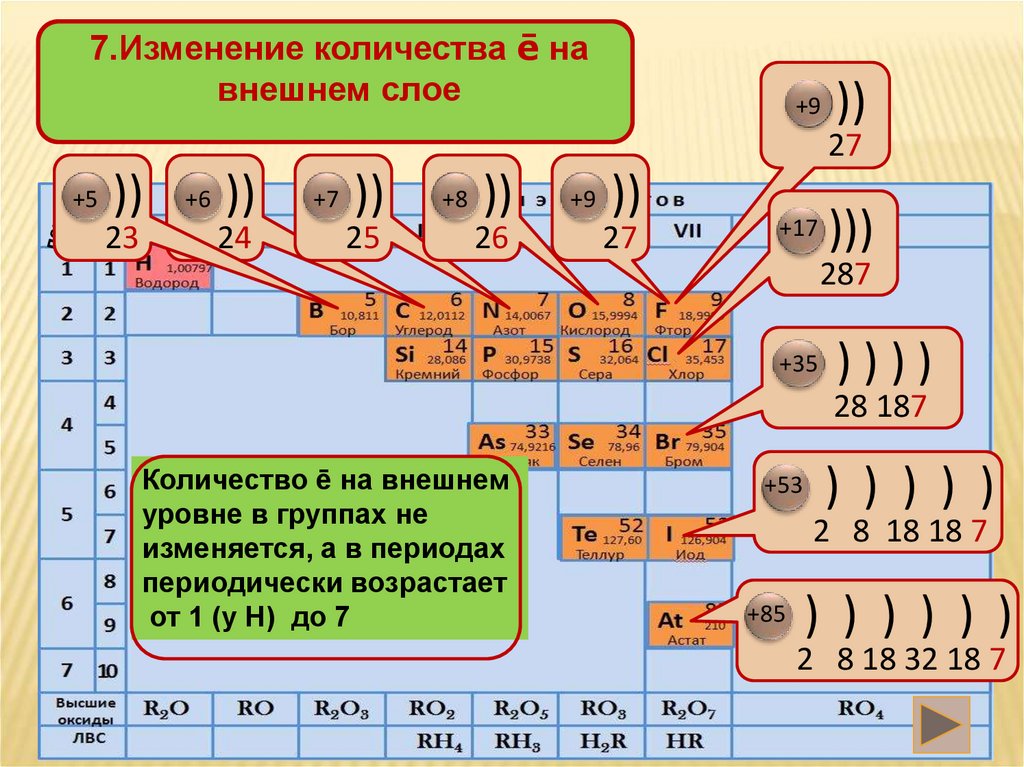
7.Изменение количества ē навнешнем слое
+9
))
27
+5
))
23
+6
))
24
+7
))
25
+8
))
26
+9
))
27
+17
)))
287
+35
))))
28 187
Количество ē на внешнем
уровне в группах не
изменяется, а в периодах
периодически возрастает
от 1 (у Н) до 7
+53
) ) ) ) )
2 8 18 18 7
+85
) ) ) ) ) )
2 8 18 32 18 7
12.
I1
2
3
4
1
Н
II
III
Группы элементов
V
VI
VII
IV
1
He 4,0032
1.008
Водород
B
2
5
10,811
Бор
C
Углерод
Si
3
6
12,011
14,00
Азот
14
28,086
Кремний
7
N
Р
6
O
8
15,998
Кислород
15
30,9738
Фосфор
S
Сера
16
32,064
9
F
18,998
Фтор
Cl
Хлор
ЛВС
10
Ne20,179
Неон
17
35,453
As
5
33
74,922
Se
Селен
78,96
Br
Бром
35
79,904
18
Ar 39,948
Аргон
Kr
36
83,80
Криптон
6
Te
7
Теллур
52
127,60
126,906
Xe131,30
54
85
Rn 86
53
I
Иод
Ксенон
8
At
9
Астат
7
Гелий
4
Мышьяк
5
VIII
1
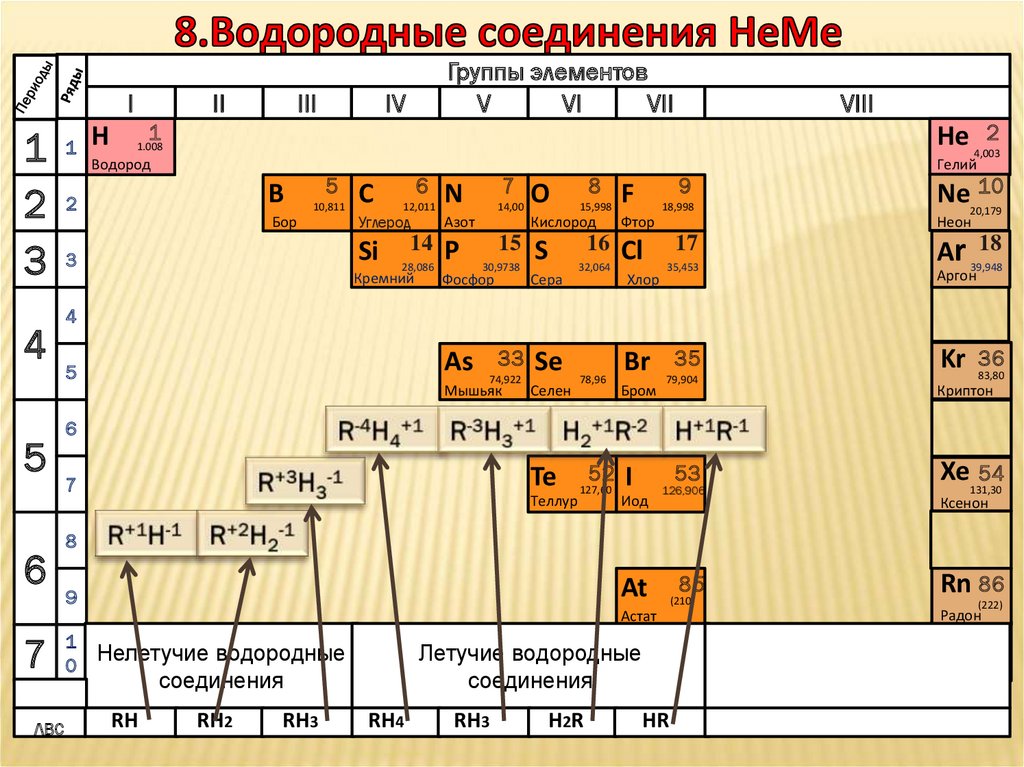
Нелетучие водородные
0
Летучие водородные
соединения
соединения
RH
RH2
RH3
RH4
RH3
H2 R
HR
(210)
(222)
Радон
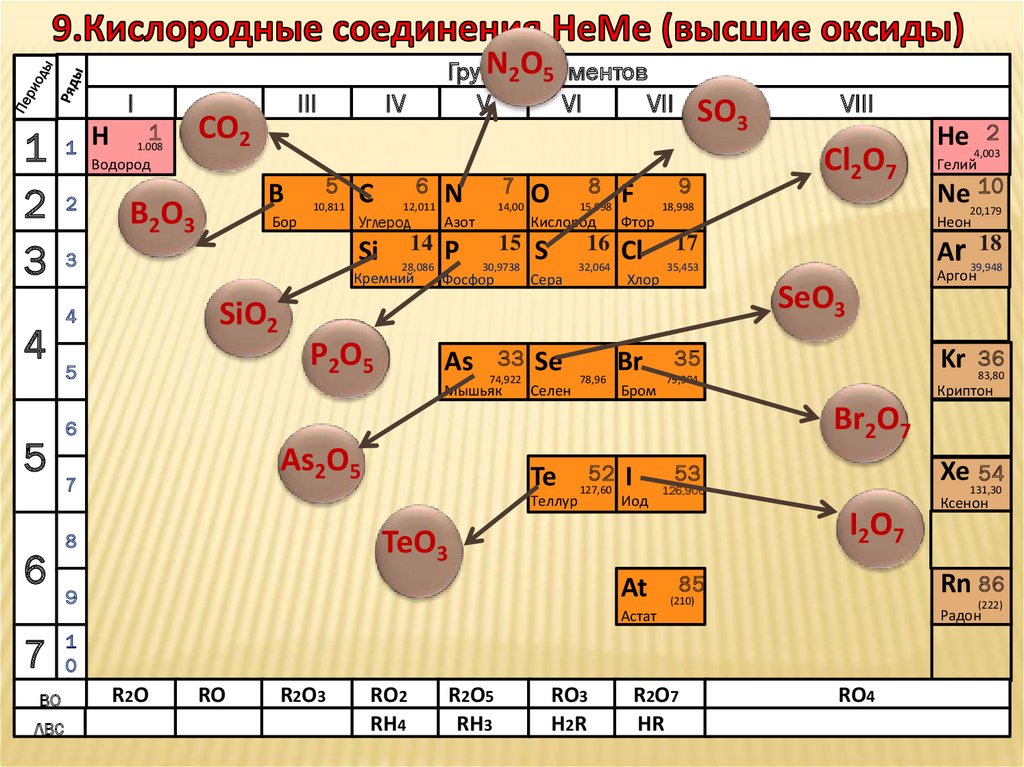
13.
I1
2
3
4
1
2
Н
II
1
1.008
III
CO2
Водород
B
B2O3
N2Oэлементов
Группы
5
V
VI
VII
IV
5
10,811
Бор
C
Углерод
Si
3
6
12,011
14
28,086
Кремний
7
N
14,00
Азот
Р
6
15,998
Кислород
15
30,9738
Фосфор
16
S
Сера
32,064
F
9
P2O5
5
As
33
74,922
Se
Селен
78,96
VIII
Cl2O7
18,998
Фтор
Cl
Хлор
Br
Бром
17
ВО
ЛВС
Гелий
10
Ne20,179
18
Ar 39,948
35,453
Аргон
SeO3
35
Kr
79,904
36
83,80
Криптон
Br2O7
6
As2O5
7
Te
Теллур
52
127,60
Иод
126,906
I2O7
TeO3
8
At
9
Xe131,30
54
53
I
85
(222)
Радон
1
0
R2 O
RO
R 2 O3
RO2
RH4
R 2 O5
RH3
RO3
H2 R
R 2 O7
HR
Ксенон
Rn 86
(210)
Астат
7
He 4,0032
Неон
SiO2
4
Мышьяк
5
8
O
SO3
RO4
14.
10.Выводы:Изменение св-в
НеМе в главной
подгруппе:
1.число электронов на
внешнем слое не
изменяется
2.радиус атома
увеличивается
3.ЭО уменьшается
4.окислительные свойства
уменьшаются
5.НеМе св-ва уменьшаются
Изменение св-в
НеМе в периоде
1.радиусы атомов уменьш.
2.число электронов на
внешнем слое уменьш.
3.
электроотрицательность
увеличивается
4.окислительные свойства
увеличиваются
5.НеМе св-ва
увеличиваются
15.
Самостоятельная работа1.Назовите распределение е на
оболочках у:серы, фтора, хлора , брома
S 286
Cl 2 8 7
F 27
Br 2 8 18 7
2.У какого из элементов ярче
выражены НеМе свойства и почему:
а) As - N
б) Cl - S
а) N – меньше радиус атома (больше
значение электроотрицательности)
б) Cl - меньше радиус атома, больше
валентных электронов ( больше
значение ЭО)
16.
11.НАХОЖДЕНИЕ НЕМЕТАЛЛОВ В ПРИРОДЕВ свободном виде НеМе могут быть :
Газообразные:
Фтор-F₂ , хлор-Cl₂ , кислород-O₂ , азот-N₂ ,
водород -H₂ , инертные газы-8 гр,главная
подгр
Твёрдые: иод I₂, астат, сера, селен, теллур,
фосфор, мышьяк, углерод, кремний, бор,
Жидкие состоянии существует (при
комнатной температуре
бром- Br₂.
Распространёнными являются
кислород, кремний, водород;
редкими — мышьяк, селен, иод.
17.
Ребята,Ребята,берегите
берегите
зрение!
зрение!
18.
12.Ф
И
З
И
Ч
Е
С
К
И
Е
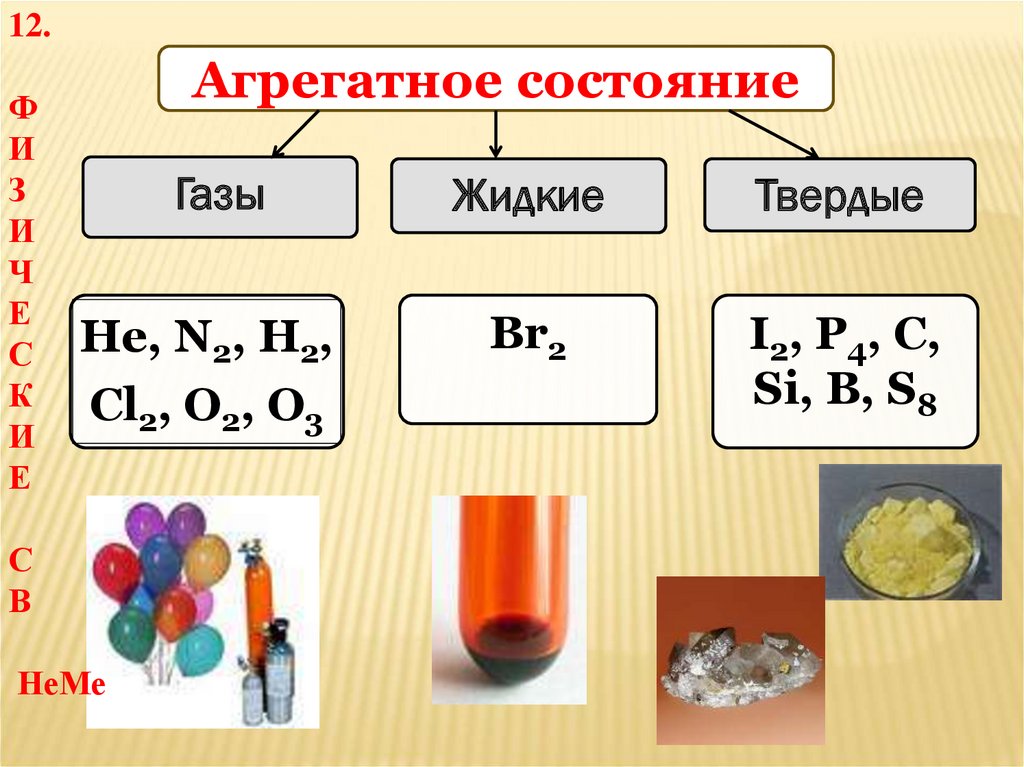
Агрегатное состояние
Газы
Жидкие
Твердые
Не, N2, Н2,
Cl2, O2, O3
Br2
I2, P4, C,
Si, B, S8
С
В
НеМе
19. ЦветА неметаллов
ЦВЕТА НЕМЕТАЛЛОВЧЕРНЫЙ
БЕЛЫЙ
ФОСФОР
ФОСФОР
ГРАФИТ
ЖЕЛТО-ЗЕЛЕНЫЙ
ХЛОР
20. ЦветА неметаллов
ЦВЕТА НЕМЕТАЛЛОВКРАСНЫЙ
ФОСФОР
ЖЕЛТЫЙ
ФИОЛЕТОВЫЙ
СЕРА
ЙОД
БЕСЦВЕТНЫЙ
УГЛЕРОД
21.
Чаще неметаллы находятся вхимически связанном виде:
вода, минералы, горные породы,
различные соли силикаты, фосфаты, сульфиды.
сульфид свинца
силикат натрия
22.
13.Блиц-опрос1.Какого газа ( по объему) больше всего
в атмосфере Земли ?
АЗОТА
2.Какого элемента-неметалла ( по
массе) больше всего в литосфере?
КИСЛОРОДА
3.Атомов какого элемента-неметалла
(по массе) больше всего в живых
организмах ?
КИСЛОРОДА
23.
1.Гость из космоса пришел, в воздухе приют себенашел
ВОДОРОД
2.В доме выше всех живем, вдвоем тепло и свет даем.
ВОДОРОД И ГЕЛИЙ
3.Он безжизненным зовется, но жизнь без него не
создается
АЗОТ
4.Красив в кристаллах и парах, на детей наводит
страх.
ЙОД
5.Из горы кусочек вынули, в деревянный ствол
задвинули.
ГРАФИТ(С) В КАРАНДАШЕ
6.Гордиться уголек невзрачный негорючим братом, и
братом прозрачным.
АЛМАЗ, ГРАФИТ
24.
7.Прокаленный уголек дышать пожарникупомог.
АКТИВИРОВАННЫЙ УГОЛЬ
8.Белый воздуха боится, покраснел чтоб
сохраниться.
БЕЛЫЙ И КРАСНЫЙ ФОСФОР
9.Хоть многие вещества превращает в яд, в
химии она достойна всяческих наград.
СЕРА
10.Какой неметалл является лесом?
БОР
11.Какие химические элементы утверждают,
что могут другие вещества рождать?
ВОДОРОД, КИСЛОРОД, УГЛЕРОД
25.
14.ХИМИЧЕСКИЕ СВОЙСТВА НЕМЕТАЛЛОВОкислительные свойства
простых веществ неметаллов:
1. Реагируют с металлами
2K + S⁰ = K₂S⁻²
3Ca + N₂⁰ = Ca₃N₂⁻³
2Fe + 3 Cl₂⁰ = 2 FeCl⁻₃
2. Реагируют с водородом
H₂ + S⁰ = H₂S⁻²
3N₂⁰ + H₂ = 2N⁻³H₃
3H₂ + WO₃ = 3H₂O + W
3. Реагируют с некоторыми сложными
веществами
C⁻⁴H⁺₄ + 2 O⁰₂ = C⁺⁴O₂⁻² + 2 H₂⁺O⁻²
2 KI⁻ + Cl₂⁰ = 2 KCl⁻ + I₂⁰
26.
Самостоятельная работа1.Допишите уравнения реакций :
Na + Br₂ → ?
2Na + Br₂⁰ = 2 NaBr⁻
Mg + P → ?
3Mg + 2P⁰ = Mg₃P₂⁻³
Na + Si → ?
4Na + Si⁰ = Na₄Si⁻⁴
H₂ + Cl ₂ → ?
H₂ + Cl₂⁰ = 2HCl⁻
P + Cl₂ → ? 2P + 5Cl₂⁰ = 2PCl₅⁻
27.
Самостоятельная работа2.Допишите уравнения реакций :
Si + F₂→
Si + 2F₂ = SiF₄
H₂ + WO₃ →
3H₂ + WO₃ = 3H₂O + W
Li + N₂ →
6Li + N₂ = 2Li₃N
28.
15.Т Е С Т1.Неметаллы, расположенные в порядке
усиления их неметалличности, - это
1) азот, углерод, бор
2) сера, хлор, фтор
3) фтор, кислород, хлор
4) бор, кремний, водород
2. Неметаллические свойства элементов
в ряду: углерод- азот- кислород-фтор:
1) не изменяются
2)усиливаются
3)ослабевают
4) изменяются периодически
29.
15.Т Е С Т3. Ковалентная полярная связь
образуется в соединении:
1) NaCl
2) NH₃ 3) P₄
4) BaCl₂
5.Простое вещество сера-S реагирует с
каждым из веществ ряда:
1) HCl, Na, O₂
2) Mg, O₂, H₂
3) K, Zn, Na₂SO₄
4) Al, H₂O, O₂
30.
16.Р Е Б У С ЫЙОД
КРЕМНИЙ
31.
АЗОТУГЛЕРОД
32.
«Острова»о. Грусти
о.Тревоги
о.Просветления
о.Бермудский
треугольник






















 Химия
Химия








