Похожие презентации:
Гемоглобин и миоглобин. Протеомика. Переваривание белков. Лекция 3
1. Лекция 3. Гемоглобин и миоглобин. Протеомика. Переваривание белков
2.
1. Миоглобин и гемоглобин. Гемоглобин: структура,свойства, виды, возрастные изменения
качественного и количественного состава в крови.
Гемоглобин АIС и его клиническое значение.
2. Производные гемоглобина. Аномальные
гемоглобины. Серповидно-клеточная анемия и
талассемия.
3. Конформационные изменения и кооперативные
взаимодействия субъединиц гемоглобина. Эффект
Бора. Роль 2,3–бисфосфоглицерата.
4. Роль протеомики в оценке патологических
состояний. Понятие об азотистом балансе.
Переваривание и всасывание пищевых белков.
Протеиназы желудочно-кишечного тракта: пепсин,
гастриксин, ренин, трипсин, химотрипсин,
экзопептидазы. Гастроинтестинальные гормоны,
их роль.
5. Бактериальное расщепление невсосавшихся в
кишечнике аминокислот.
3. 1. Миоглобин и гемоглобин. Гемоглобин: структура, свойства, виды, возрастные изменения качественного и количественного состава
вкрови. Гемоглобин АIС и его
клиническое значение
4.
• К группе гемопротеинов относятсягемоглобин и его производные,
миоглобин, хлорофиллсодержащие
белки и ферменты (вся цитохромная
система, каталаза и пероксидаза). Все
они содержат в качестве небелкового
компонента структурно сходные
железо- (или магний) порфирины, но
различные по составу и структуре
белки, обеспечивая тем самым
разнообразие их биологических
функций.
5.
• Гемоглобин в качестве белковогокомпонента содержит глобин, а
небелкового – гем.
• Видовые различия гемоглобина
обусловлены глобином, в то время как
гем одинаков у всех видов гемоглобина.
• Атом железа расположен в центре
гема-пигмента, придающего крови
характерный красный цвет.
6.
• Основу структуры простетическойгруппы большинства гемосодержащих
белков составляет порфириновое
кольцо, являющееся в свою очередь
производным тетрапиррольного
соединения – порфирина.
• Последний состоит из четырех
замещенных пирролов, соединенных
между собой метиновыми мостиками
(—СН=).
• Незамещенный порфирин называется
порфином.
7.
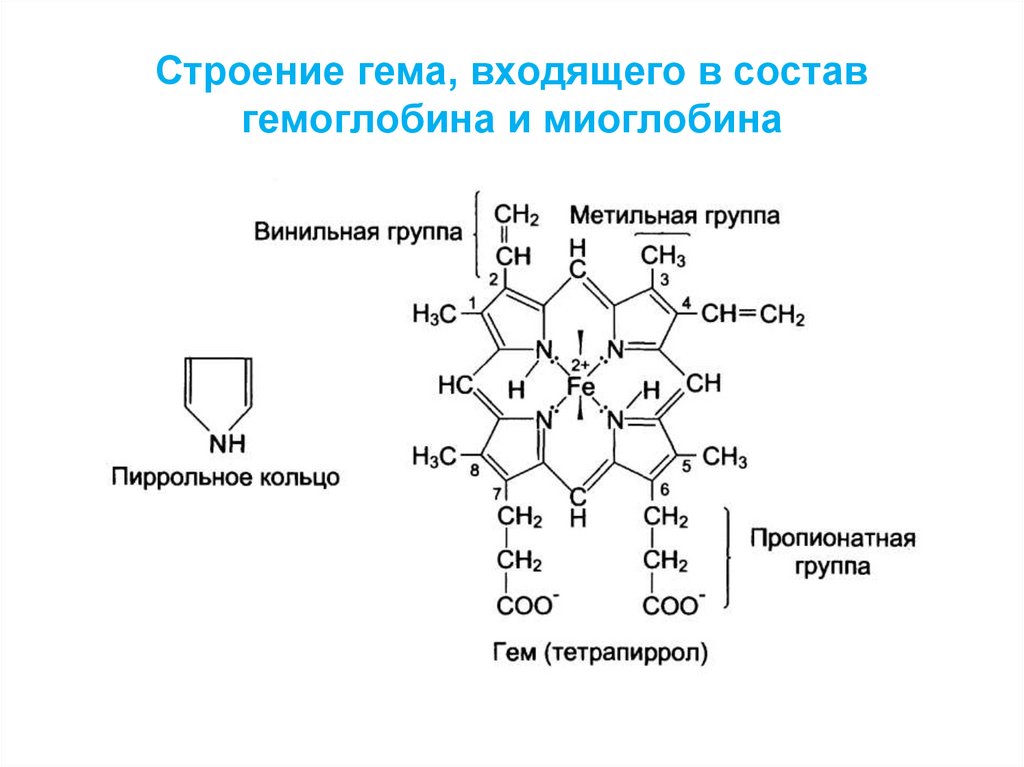
• В молекуле гема порфин представлен ввиде протопорфирина IX, содержащего
четыре метильные группы (—СН3), две
винильные группы (—СН=СН2) и два
остатка пропионовой кислоты.
Протопорфирин, присоединяя железо,
превращается в гем.
• Гем в виде гем-порфирина является
простетической группой не только
гемоглобина и его производных, но и
миоглобина, каталазы, пероксидазы
и цитохромов b, с и c1.
8.
• Модель третичнойструктуры молекулы
миоглобина (по Дж.
Кендрью).
Латинскими буквами
обозначены
структурные
домены, красным
цветом – гем.
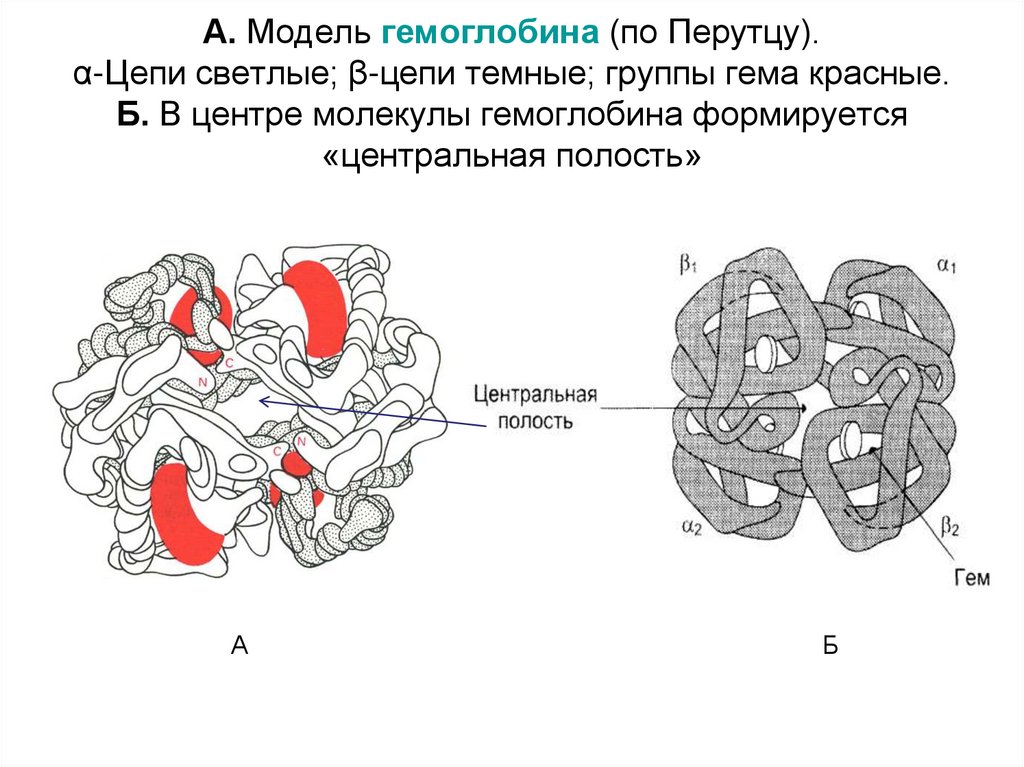
9. А. Модель гемоглобина (по Перутцу). α-Цепи светлые; β-цепи темные; группы гема красные. Б. В центре молекулы гемоглобина
формируется«центральная полость»
А
Б
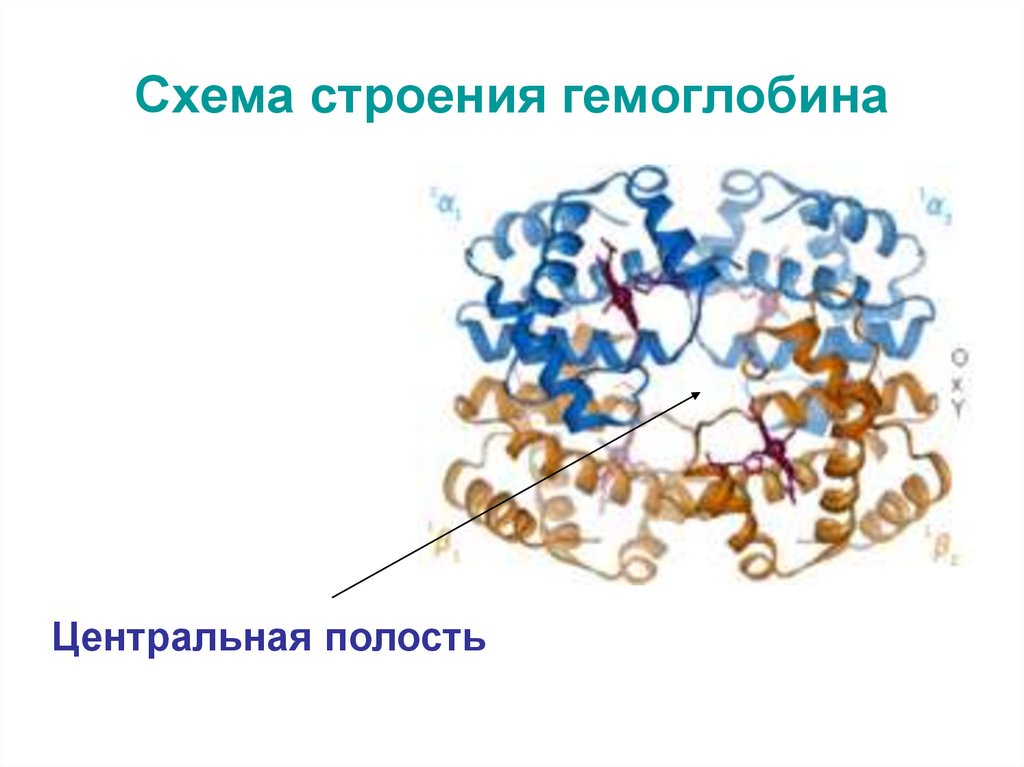
10. Схема строения гемоглобина
Центральная полость11. Строение гема, входящего в состав гемоглобина и миоглобина
12.
• Миоглобин – содержится в красныхмышцах и участвует в запасании
кислорода. В условиях интенсивной
мышечной работы, когда парциальное
давление кислорода в ткани падает, О2
освобождается из комплекса с
миогобином и используется в
митохондриях клеток для получения
необходимой для работы мышц
энергии.
13.
Гемоглобины – структурно-родственные белки,находящиеся в эритроцитах позвоночных. Они
выполняют две важные биологические
функции:
1) переносят О2 из легких к периферическим тканям;
2) переносят СО2 и протоны от периферических
тканей к дыхательным органам для последующего
выведения из организма.
Гемоглобин связывает четыре молекулы кислорода
на тетрамер (по одной на гем в каждой
субъединице); особенно важным отличием его от
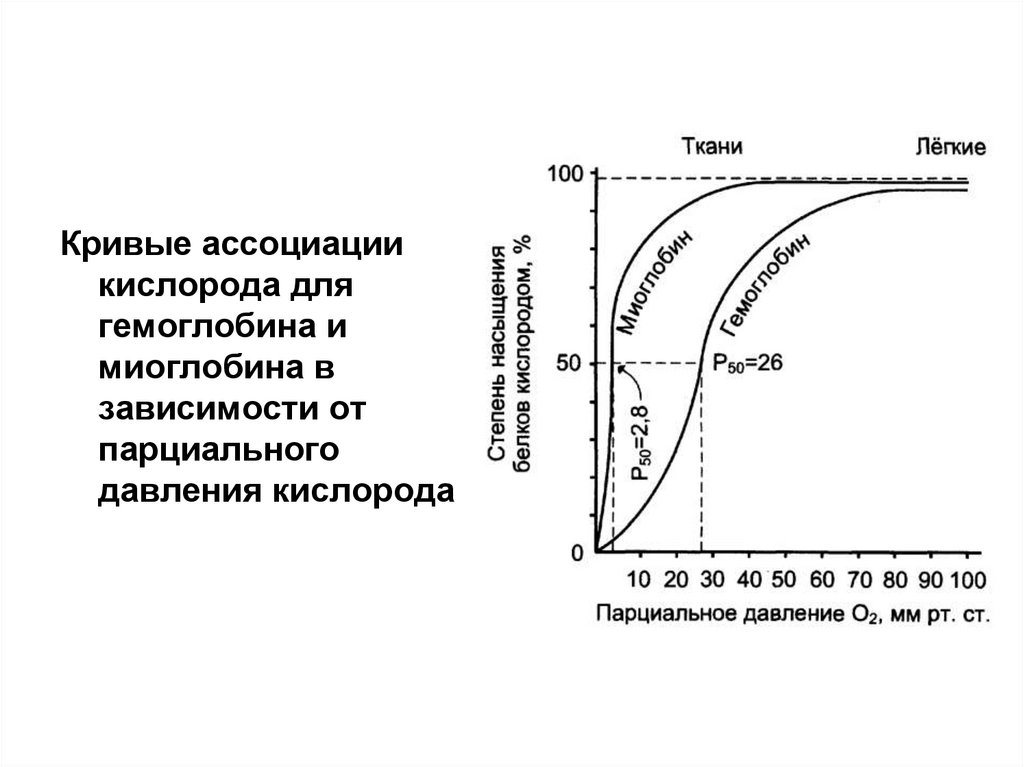
миоглобина является характерная кривая
насыщения кислородом, которая имеет
сигмоидную форму.
14.
Кривые ассоциациикислорода для
гемоглобина и
миоглобина в
зависимости от
парциального
давления кислорода
15.
Наиболее распространенные гемоглобины имеютследующую тетрамерную структуру:
• НЬА (нормальный гемоглобин взрослого человека) – α2β2.
Это основной гемоглобин взрослого организма, составляет
около 98% от общего количества гемоглобина;
• HbA2 (минорный гемоглобин взрослого человека) – α2δ2 Он
находится в организме взрослого человека в меньшей
концентрации, на его долю приходится около 2% общего
гемоглобина;
• Гемоглобин АIc – гемоглобин А, модифицированный
ковалентным присоединением к нему глюкозы
(гликозилированный гемоглобин);
• Эмбриональный гемоглобин – синтезируется в
эмбриональном желточном мешке через несколько недель
после оплодотворения – ξ2ε2. Через 2 недели после
формирования печени плода в ней начинает
синтезироваться гемоглобин F;
• HbF (фетальный гемоглобин) – α2γ2;
• HbS (гемоглобин при серповидно-клеточной анемии) – α2S2.
16. 2. Производные гемоглобина. Аномальные гемоглобины. Серповидно-клеточная анемия и талассемия
2. Производныегемоглобина. Аномальные
гемоглобины. Серповидноклеточная анемия и
талассемия
17.
Мутантные (М) гемоглобины человекаМутации генов, кодирующих α- и β-цепи, могут
существенным образом сказываться на их
биологической функции.
Известно несколько сот мутантных гемоглобинов
человека (в большинстве случаев функционально
активных), и о некоторых из них, отличающихся
сильным изменением биологических функций, речь
пойдет ниже.
Патологическое состояние, при котором мутация
вызывает изменение биологической функции
гемоглобина, называют гемоглобинопатией.
18. Гемоглобин при серповидноклеточной анемии
В гемоглобине S остаток Glu A2(6)βзамещен на Val.
Остаток А2 (Glu или Val) располагается на
поверхности молекулы гемоглобина и
контактирует с водой, и замещение
полярного остатка Glu на неполярный Val
приводит к появлению на поверхности βсубъединицы «липкого участка».
19. Различия в строении молекул гемоглобинов
12 3
4 5
6 7 8
• Hb A: Вал-Гис-Лей-Тре-Про-Глу-Глу-Лиз…
• Hb S: Вал-Гис-Лей-Тре-Про-Вал-Глу-Лиз…
20.
Этот липкий участок присутствует как воксигенированном, так и в
дезоксигенированном гемоглобине S (в
гемоглобине А он отсутствует).
На поверхности дезоксигенированного
гемоглобина существует
комплементарный участок, способный
прочно связываться с липким участком βсубъединицы, тогда как в
оксигенированном гемоглобине этот
участок маскируется другими группами.
21.
Когда гемоглобин S переходит вдезоксигенированное состояние, его липкий
участок связывается с комплементарным
участком на другой молекуле
дезоксигенированного гемоглобина.
Происходит полимеризация
дезоксигемоглобина S и его осаждение в
виде длинных волокон.
Волокна дезоксигемоглобина S механически
деформируют эритроцит, придавая ему
серповидную форму, что приводит к лизису
клеток и множеству вторичных клинических
проявлений.
22. Ассоциация молекул дезоксигемоглобина S
23.
Другая важная группа нарушений, связанных саномалиями гемоглобина – талассемии.
Для них характерна пониженная скорость
синтеза α-цепей гемоглобина (α-талассемия)
или β-цепей (β-талассемия). Это приводит к
анемии, которая может принимать очень
тяжелую форму. В последние годы достигнут
ощутимый прогресс в выяснении
молекулярных механизмов, ответственных за
развитие талассемии.
24. 3. Конформационные изменения и кооперативные взаимодействия субъединиц гемоглобина. Эффект Бора. Роль 2,3–бисфосфоглицерата
3. Конформационныеизменения и кооперативные
взаимодействия
субъединиц гемоглобина.
Эффект Бора. Роль 2,3–
бисфосфоглицерата
25. Кооперативные изменения конформации гемоглобина
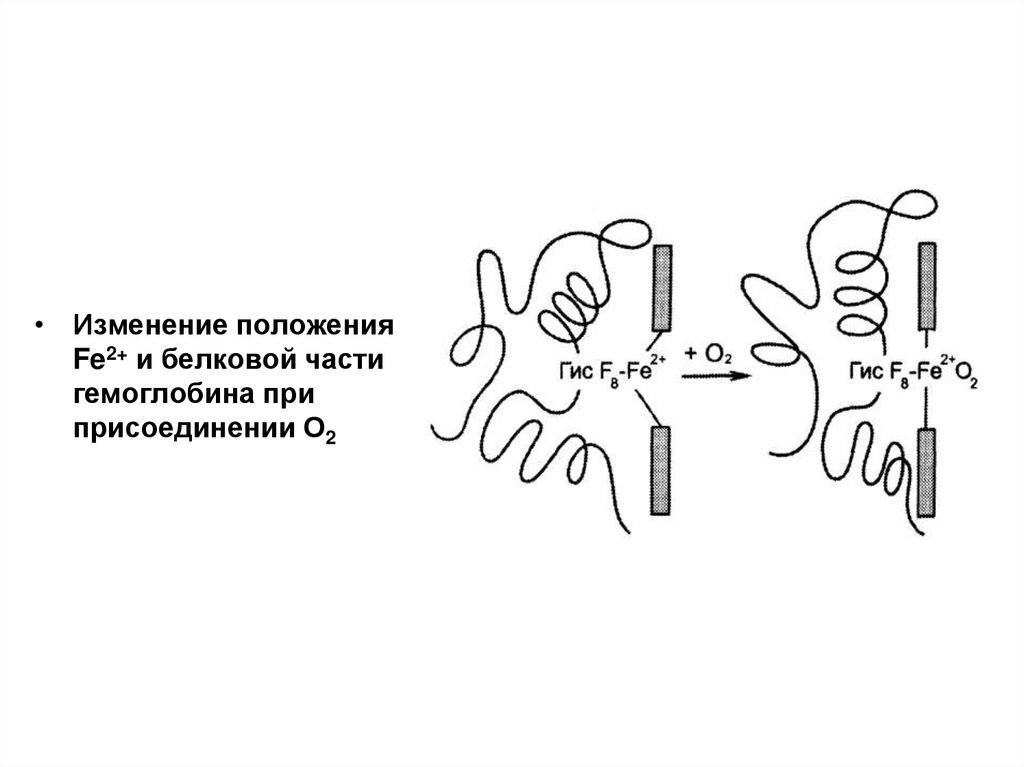
В дезоксигемоглобине благодаря ковалентнойсвязи с белковой частью атом Fe2+ выступает
из плоскости гема в направлении Гис F8.
Присоединение О2 к атому Fe2+ одного
протомера вызывает его перемещение в
плоскость гема, за ним перемещаются
остаток Гис F8 и полипептидная цепь, в
состав которой он входит.
Т.к. протомер связан с остальными
протомерами, а белки обладают
конформационной лабильностью, происходит
изменение конформации всего белка.
26.
• Изменение положенияFe2+ и белковой части
гемоглобина при
присоединении О2
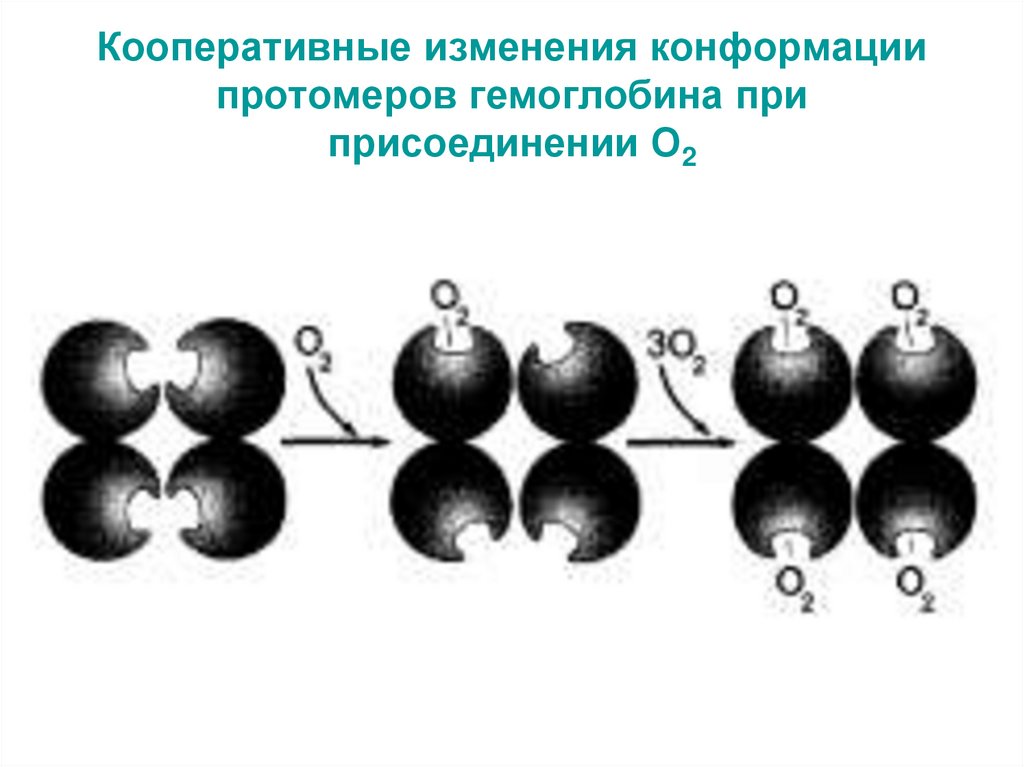
27. Кооперативные изменения конформации протомеров гемоглобина при присоединении О2
28. Перенос Н+ и СО2 с кровью. Эффект Бора. А – влияние концентрации СО2 и Н+ на высвобождение О2 из комплекса с гемоглобином в
тканях (эффект Бора); Б – оксигенированиедезоксигемоглобина в лёгких, образование и выделение СО2.
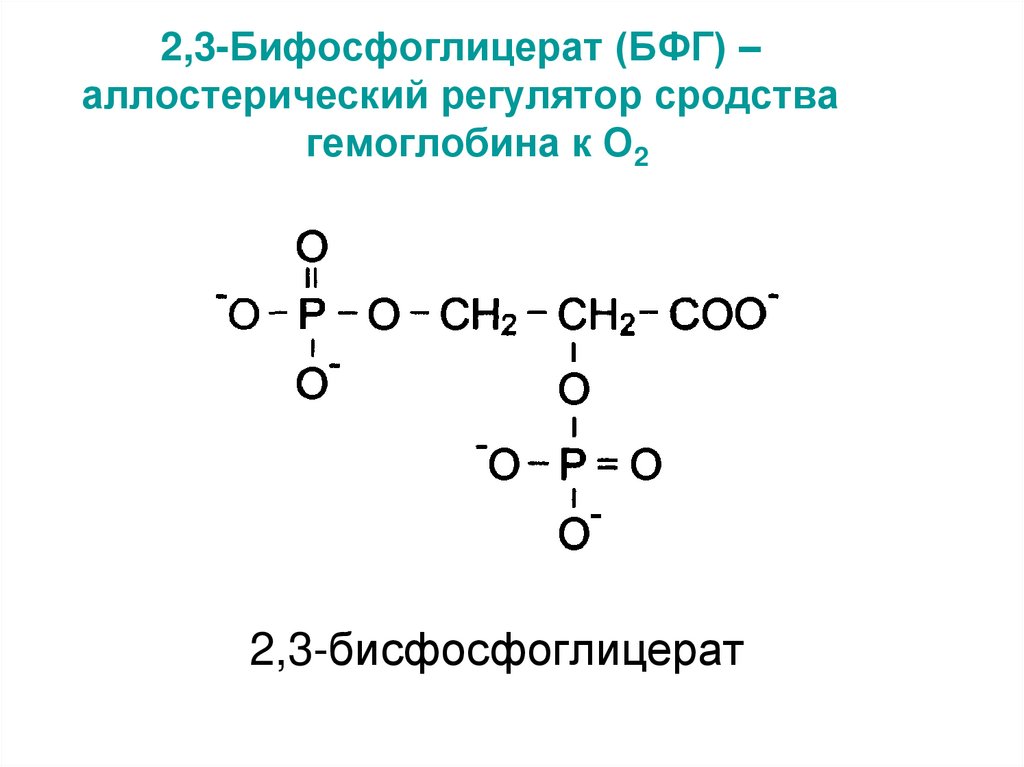
29. 2,3-Бифосфоглицерат (БФГ) – аллостерический регулятор сродства гемоглобина к О2
2,3-бисфосфоглицерат30.
ТканиНb(О2)4
+
БФГ
↔
Лёгкие
Нb-БФГ
+
4О2
31. 4. Роль протеомики в оценке патологических состояний. Понятие об азотистом балансе. Переваривание и всасывание пищевых белков.
Протеиназыжелудочно-кишечного тракта:
пепсин, гастриксин, ренин,
трипсин, химотрипсин,
экзопептидазы.
Гастроинтестинальные гормоны,
их роль
32. Протеомика – наука, основным предметом изучения которой являются белки, их функции и взаимодействия в живых организмах, в том
числе –в человеческом.
33.
Основная задача протеомики – количественныйанализ экспрессии белков в клетках в зависимости от
их типа, состояния или влияния внешних условий.
Протеомика осуществляет сравнительный анализ больших
групп белков – от всех белков, вовлеченных в тот или иной
биологический процесс до полного протеома.
Преимуществом протеомики перед геномикой является тот
факт, что наличие какого-либо гена в геноме не означает,
что с него производится транскрипция, а наличие
транскрипта не означает, что с него происходит
трансляция, а даже если происходит, то транскрипт не
позволяет однозначно говорить о структуре белка, его
созревании и локализации.
34. Азотистый баланс означает разность между общим количеством азота, поступившим в организм человека (или другой организм), и
общим количествомэкскретируемого азота.
35. Если азота поступает больше, чем экскретируется, говорят, что данный индивидуум имеет положительный азотистый баланс. Примеры:
период роста ибеременности. Азотистый баланс
положителен как у здорового
растущего ребенка, так и у
здоровой беременной женщины.
36. Взрослый человек в норме находится в состоянии азотистого равновесия: потребление азота уравновешивается его выделением в
составефекалий и мочи.
37. В состоянии отрицательного азотистого баланса количество выделяемого азота превышает количество азота, потребляемого
организмом.Важным примером служат больные,
потребляющие недостаточное
количество азота с пищей (например, при
квашиоркоре). Такое же состояние
наблюдается при прогрессирующих
формах рака и в ряде случаев в
послеоперационном периоде.
38. Переваривание пищевых белков
Переваривание белков, входящих всостав пищи, происходит в различных
отделах ЖКТ с участием протеиназ.
39. Пепсин
Основная пищеварительная функция желудказаключается в том, что в нем начинается
переваривание белка.
Пепсин продуцируется главными клетками в виде
неактивного зимогена, пепсиногена.
Пепсиноген активируется в пепсин ионами Н+,
которые отщепляют защитный полипептид,
«раскрывая» активный пепсин, а также самим
пепсином, вызывающим быструю активацию
дополнительных молекул пепсиногена
(аутокатализ).
40.
• Пепсин преобразует денатурированный белок впротеозы и затем в пептоны —большие
полипептидные производные. Он представляет
собой эндопептидазу, поскольку осуществляет
гидролиз пептидных связей в составе главной
полипептидной структуры, а не N- или С-концевых
последовательностей, что характерно для
экзопептидаз.
• Пепсин специфически атакует пептидные связи,
образуемые с участием ароматических аминокислот
(например, тирозина) или дикарбоновых аминокислот
(например, глутамата).
41.
Гастриксин – протеолитический фермент(катализирующий расщепление белка пищи)
желудочного сока, проявляющий максимальную
активность при pH, равном 3,0-3,5. Гастриксин по
своим функциям и эволюции в желудке близок к
пепсину, поэтому иногда называется пепсин С или
парапепсин II и относится к изопепсинам.
Профермент гастриксина – прогастриксин –
секретируется главными клетками фундальных
желёз дна, тела и интермедиальной зоны желудка,
а также клетками пилорических желёз и
активируется, также как и профермент пепсина
пепсиноген, соляной кислотой желудочного сока.
42.
Гастриксин, в отличие от пепсина,протеолетически активен в менее кислой
среде. Гастриксин является вторым по
объёму после пепсина среди содержащихся в
желудочном соке протеолитических
ферментов. Количество гастриксина в
желудочном соке здорового взрослого
человека составляет 20-50 % от количества
пепсина.
Гастриксин вместе с пепсином обеспечивают
до 95 % всей протеолитической активности
желудочного сока.
43.
Реннин (химозин, сычужный фермент). Этотфермент вызывает створаживание молока.
Он чрезвычайно важен для процессов
пищеварения у младенцев, поскольку
предотвращает быстрый выход молока из
желудка.
В присутствии кальция реннин вызывает
необратимые изменения казеина молока,
превращая его в параказеин, который затем
подвергается действию пепсина. В желудке
взрослых людей реннин, по-видимому,
отсутствует.
Реннин используется при производстве сыра.
44. Трипсин, химотрипсин и эластаза
Протеолитическое действие панкреатическогосекрета обусловливается тремя эндопептидазами
– трипсином, химотрипсином и эластазой,
которые расщепляют белки и полипептиды,
поступающие из желудка, с образованием
полипептидов, пептидов или тех и других.
Трипсин специфически действует на пептидные
связи, образуемые основными аминокислотами,
химотрипсин – на связи между остатками
незаряженных аминокислот (например,
ароматических), в то время как эластаза вопреки
своему названию обладает довольно широкой
специфичностью, расщепляя связи, примыкающие
к остаткам малых аминокислот, таких, как глицин,
аланин и серии.
45.
Все три фермента секретируются в видезимогенов. Активация трипсиногена
осуществляется другим протеолитическим
ферментом, энтерокиназой, секретируемой
слизистой кишечника.
Она гидролизует лизиновую пептидную связь в
зимогене, высвобождая малый полипептид,
что приводит к разворачиванию молекулы в
активный трипсин.
Образовавшийся трипсин действует не только
на новые молекулы трипсиногена, но и на
другие зимогены панкреатического секрета –
химотрипсиноген, проэластазу и
прокарбоксипептидазу – с высвобождением
соответственно химотрипсина, эластазы и
карбоксипептидазы.
46. Карбоксипептидаза
Дальнейшее расщепление полипептидов,образовавшихся под действием
эндопептидаз, осуществляет
экзопептидаза – карбоксипептидаза,
которая атакует С-концевую пептидную
связь, высвобождая одиночные
аминокислоты.
47. Переваривание секретом кишечника
Кишечный сок, секретируемый железами Бруннера иЛиберкюна, также содержит пищеварительные
ферменты, в число которых входят:
1) аминопептидаза, представляющая собой экзопептидазу,
которая гидролизует пептидные связи за N-концевыми
аминокислотами полипептидов и олигопептидов;
дипептидазы различной специфичности, некоторые из них
могут находиться внутри кишечного эпителия; они
завершают расщепление дипептидов до свободных
аминокислот;
2) специфические дисахаридазы и олигосахаридазы, такие,
как α-глюкозидаза (мальтаза), удаляющая единичные
глюкозные остатки из α1→4-связанных олигосахаридов и
дисахаридов начиная с нередуцирующих концов,
изомальтаза (а-декстриназа), которая гидролизует 1→6связи α-декстринов; β-галактозидаза (лактаза), удаляющая
галактозу из лактозы; сахараза, гидролизующая сахарозу, и
трегалаза. расщепляющая трегалозу;
48. Переваривание секретом кишечника
3) фосфатаза, удаляющая фосфат из некоторыхорганических фосфатов (гексозофосфаты и
глицерофосфат) и из нуклеотидов пищевого
происхождения или образующихся из нуклеиновых
кислот в результате их переваривания нуклеазами;
4) полинуклеотидазы, которые расщепляют нуклеиновые
кислоты на нуклеотиды;
5) нуклеозидазы (нуклеозидфосфорилазы),
катализирующие фосфоролиз нуклеозидов с
образованием свободных азотистых оснований и
пентозофосфатов;
6) кишечный секрет, по-видимому, содержит также
фосфолипазу, которая действует на фосфолипиды с
образованием глицерола, жирных кислот, фосфорной
кислоты и оснований, таких, как холин.
49. Всасывание аминокислот и белка
В нормальных условиях пищевые белки почтиполностью расщепляются на составляющие
их аминокислоты, которые затем быстро
всасываются в кишечнике.
Возможно, что некоторые гидролитические
процессы (например, в случае дипептидов)
полностью завершаются в кишечной стенке.
Потребность животных в белке может с
успехом удовлетворяться скармливанием
полной смеси аминокислот.
50. Изменения белкового состава организма
1. Изменение белкового состава клеток впроцессе их дифференцировки.
2. Наследственные протеинопатии.
3. Приобретённые протеинопатии.
51. 5. Бактериальное расщепление невсосавшихся в кишечнике аминокислот
52. Процессы гниения и брожения в кишечнике
Большая часть потребленной пищивсасывается в тонком кишечнике. Остальная
часть попадает в толстый кишечник. Именно
здесь происходит значительное всасывание
воды и полужидкое кишечное содержимое
постепенно становится более твердым. В
этот период проявляется бактериальная
активность.
В ходе вызываемых бактериями процессов
брожения и гниения образуются различные
газы, такие, как СО2, метан, водород, азот и
сероводород, а также уксусная, молочная и
масляная кислоты.
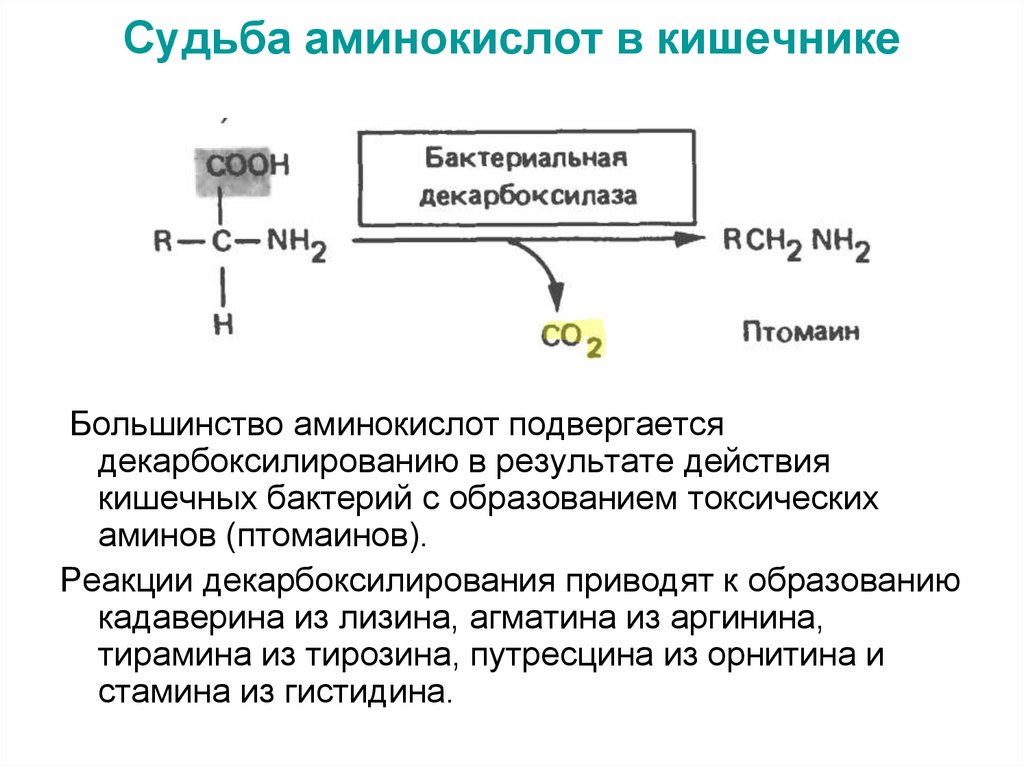
53. Судьба аминокислот в кишечнике
Большинство аминокислот подвергаетсядекарбоксилированию в результате действия
кишечных бактерий с образованием токсических
аминов (птомаинов).
Реакции декарбоксилирования приводят к образованию
кадаверина из лизина, агматина из аргинина,
тирамина из тирозина, путресцина из орнитина и
стамина из гистидина.
54.
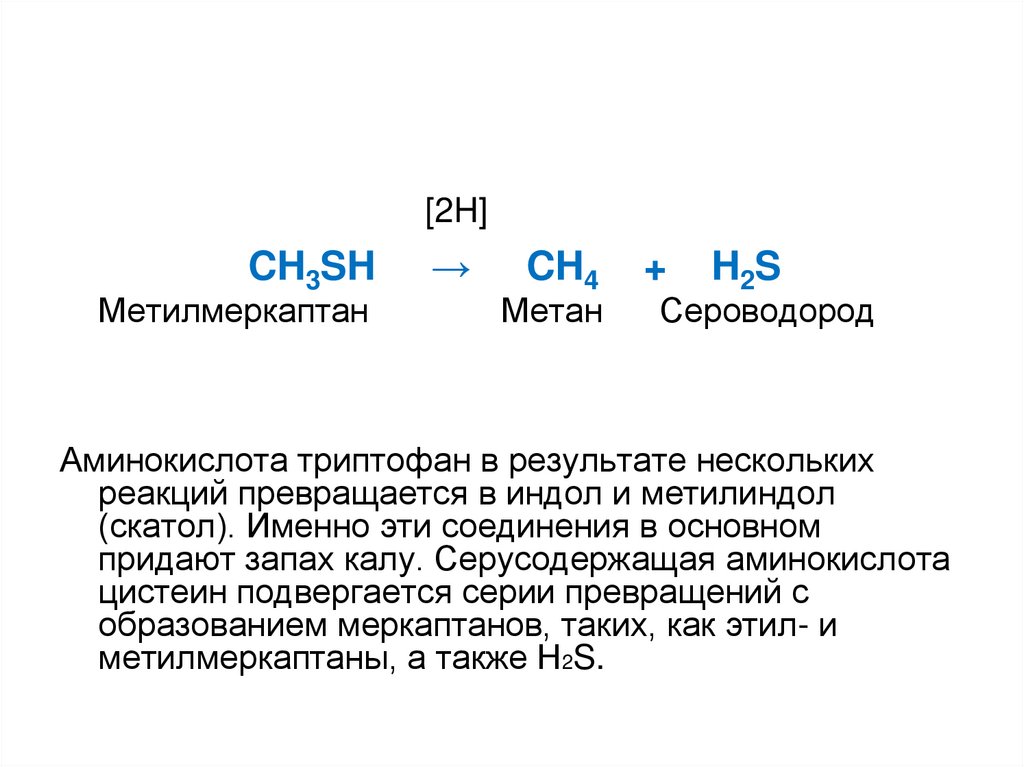
[2H]CH3SH
Метилмеркаптан
→
CH4
Метан
+
H2 S
Сероводород
Аминокислота триптофан в результате нескольких
реакций превращается в индол и метилиндол
(скатол). Именно эти соединения в основном
придают запах калу. Серусодержащая аминокислота
цистеин подвергается серии превращений с
образованием меркаптанов, таких, как этил- и
метилмеркаптаны, а также H2S.
55. Превращение аминокислот в толстом кишечнике
56. Кишечные бактерии
Кишечный микробоценоз может составлятьзначительную часть (до 25%) сухого веса кала.
У травоядных, пища которых состоит большей
частью из целлюлозы, бактерии кишечника или
рубца играют важную роль в пищеварении,
поскольку они расщепляют полисахариды и тем
самым способствуют их всасыванию. Кроме того,
эти бактерии осуществляют синтез незаменимых
аминокислот и витаминов.
Для людей кишечный микробоценоз не столь важен,
как для травоядных. Однако бактериальная
активность вносит определенный полезный вклад
в питание человека, ибо с ней связан синтез
витаминов К и В12, а возможно, и других
витаминов группы В, которые далее усваиваются
организмом.















































 Биология
Биология








