Похожие презентации:
Основания и их свойства
1.
Основания и их свойства2.
3.
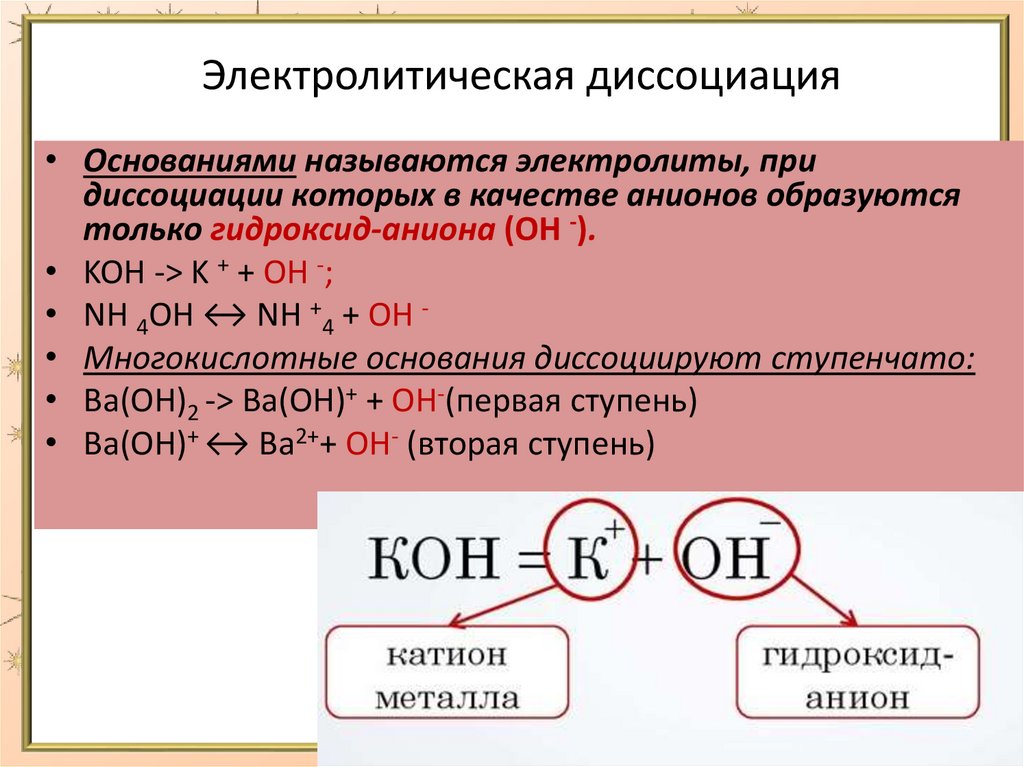
Электролитическая диссоциация• Основаниями называются электролиты, при
диссоциации которых в качестве анионов образуются
только гидроксид-аниона (OH -).
• KOH -> K + + OH -;
• NH 4OH ↔ NH +4 + OH • Многокислотные основания диссоциируют ступенчато:
• Ba(ОН)2 -> Bа(ОН)+ + OH-(первая ступень)
• Ba(OH)+ ↔ Ba2++ OH- (вторая ступень)
4.
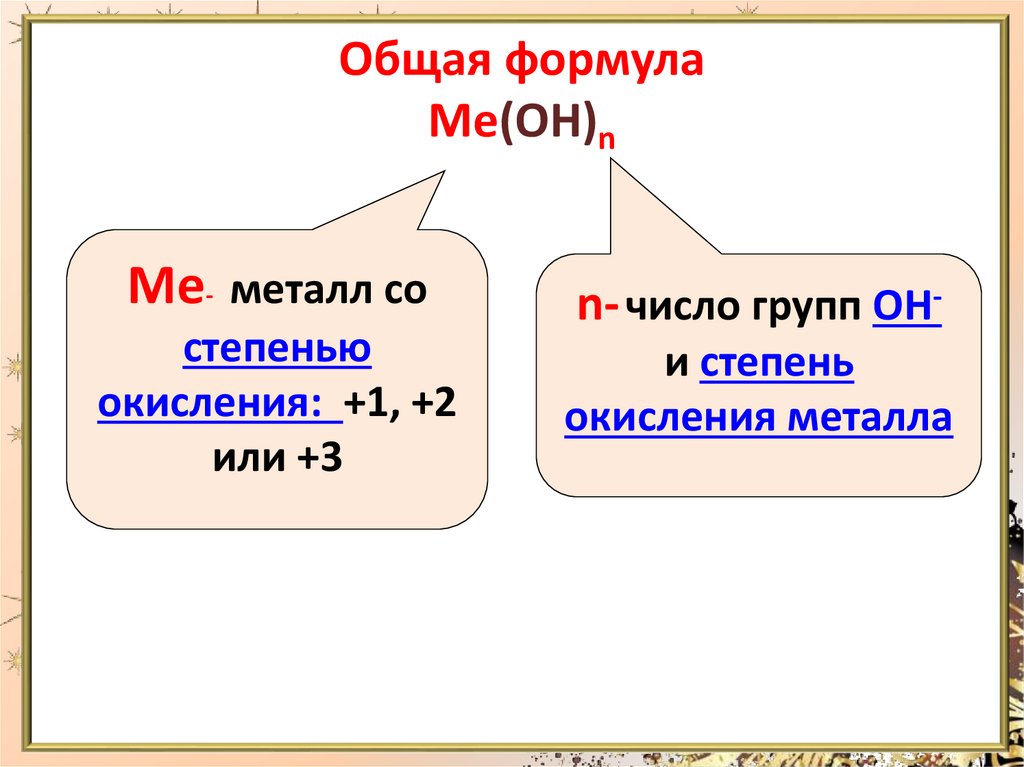
Общая формулаМе(ОН)n
Ме- металл со
степенью
окисления: +1, +2
или +3
n- число групп ОНи степень
окисления металла
5.
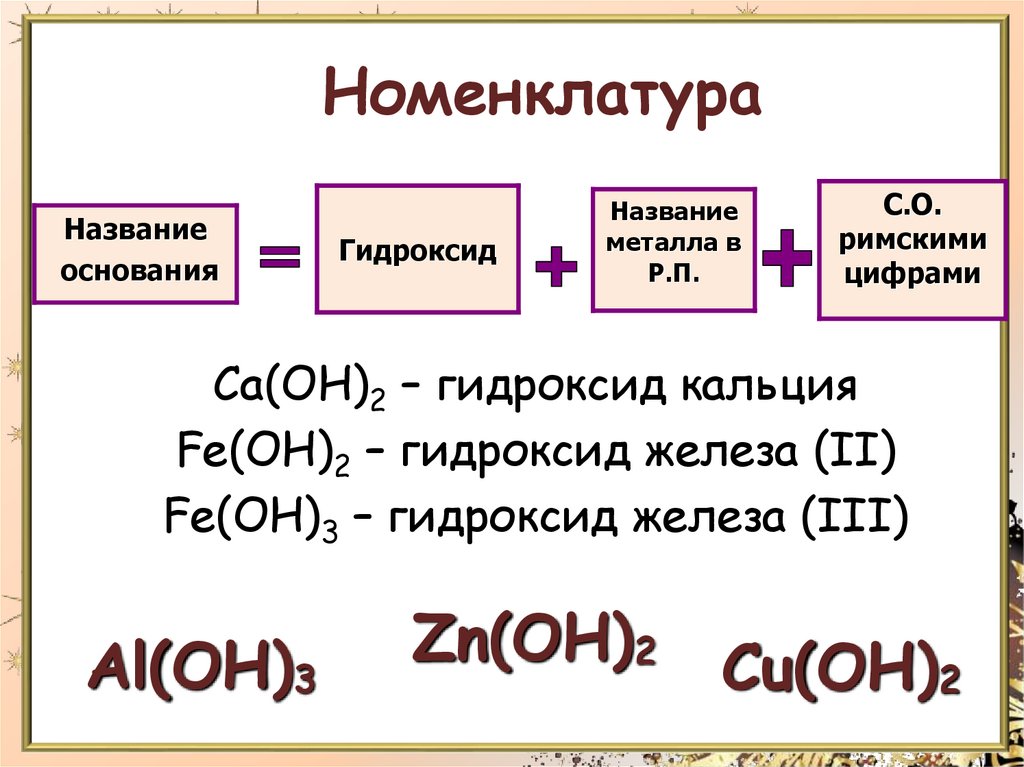
НоменклатураНазвание
основания
Гидроксид
Название
металла в
Р.П.
С.О.
римскими
цифрами
Ca(OH)2 – гидроксид кальция
Fe(OH)2 – гидроксид железа (II)
Fe(OH)3 – гидроксид железа (III)
Al(OH)3
Zn(OH)2
Cu(OH)2
6.
7.
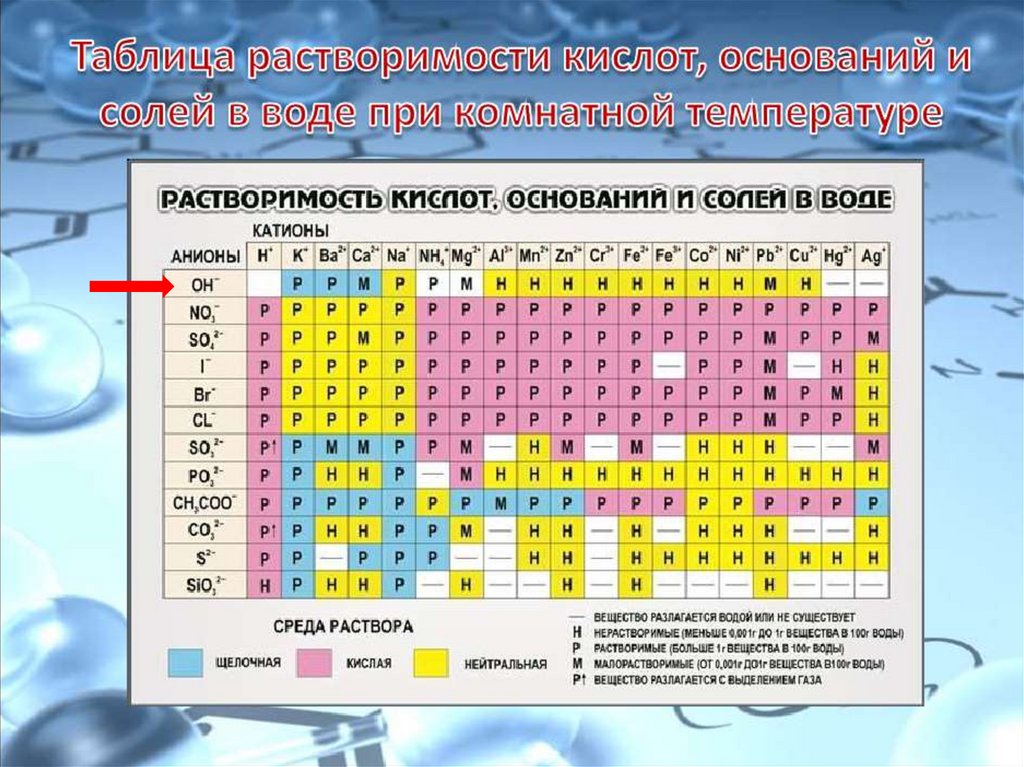
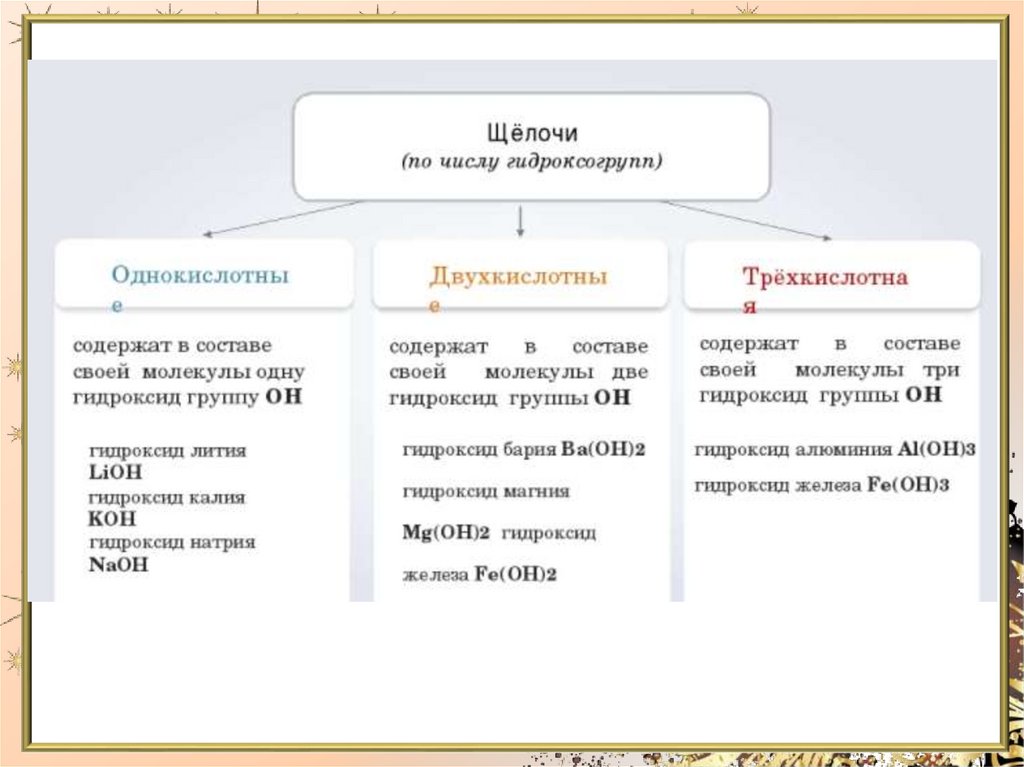
Классификация основанийОснования
Растворимые
(Щелочи)
Нерастворимые
8.
ЩелочиНерастворимые
основания
KOH
LiOH
Ca(OH)2
Mn(OH)2
Fe(OH)3
Al(OH)3












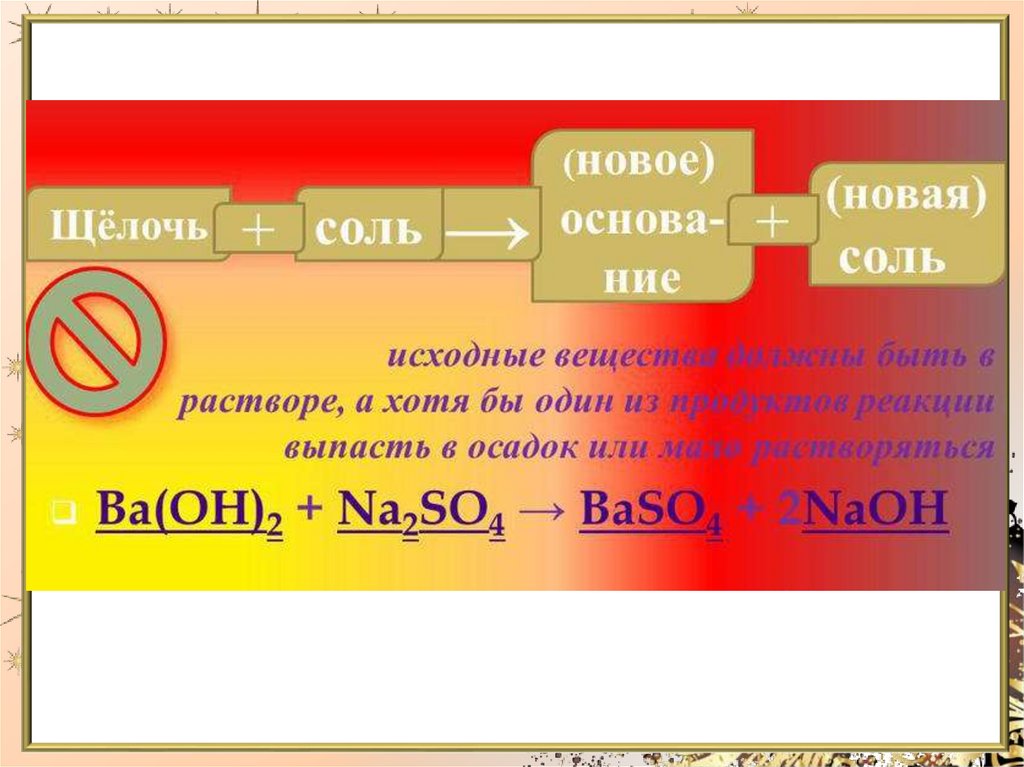


 Химия
Химия








