Похожие презентации:
Основания и их свойства
1.
Основания и их свойства2.
Проверка. Ответы:1 вариант
2 вариант
• HCl
• Н2SO4
2HCl + BaCO3 = BaCl2 + CO2+ H2O
2H+ +2Cl- + Ba2+ + CO32- =Ba2+ +2Cl- +CO2+H2O
2H+ + CO32- = CO2+ H2O
Н2SO4 + Ba(OH)2 = BaSO4+ 2H2O
2Н+ + SO42- + Ba2+ + 2OH- = BaSO4 + 2H2O
3.
Основания (гидроксиды)Основания – электролиты, при диссоциации которых в качестве
анионов образуются только гидроксид-ионы ОН-
4.
Номенклатура оснований(правила составления химических названий)
Пример:
NaOH – гидроксид (чего?) натрия
Fe2+ (OH)2 – гидроксид железа (II)
Fe 3+ (OH)3 – гидроксид железа (III)
5.
Тривиальные названия (разговорные)NaOH
KOH
• Гидроксид натрия
• Едкий натр, Каустическая сода
• Гидроксид калия
• Едкое кали
6.
Тривиальные названия• Гидроксид кальция
Ca(OH)2
•Гашеная известь – М
• Известковая вода – Р
• Известковое молоко - взвесь
7.
8.
Выполнить задания• Карточка 2
9.
Ответы• Карточка 2
Распознать основания:
1. CH3OH
2. CrPO4
3. H2SiO3
4. CsOH
10.
Ответы2. Составить формулы оснований,
образованных следующими металлами,
назвать их:
•К
- KOH
• Al
- Al(OH)3
• Ca
- Ca(OH)2
• Cu (II) - Cu(OH)2
11.
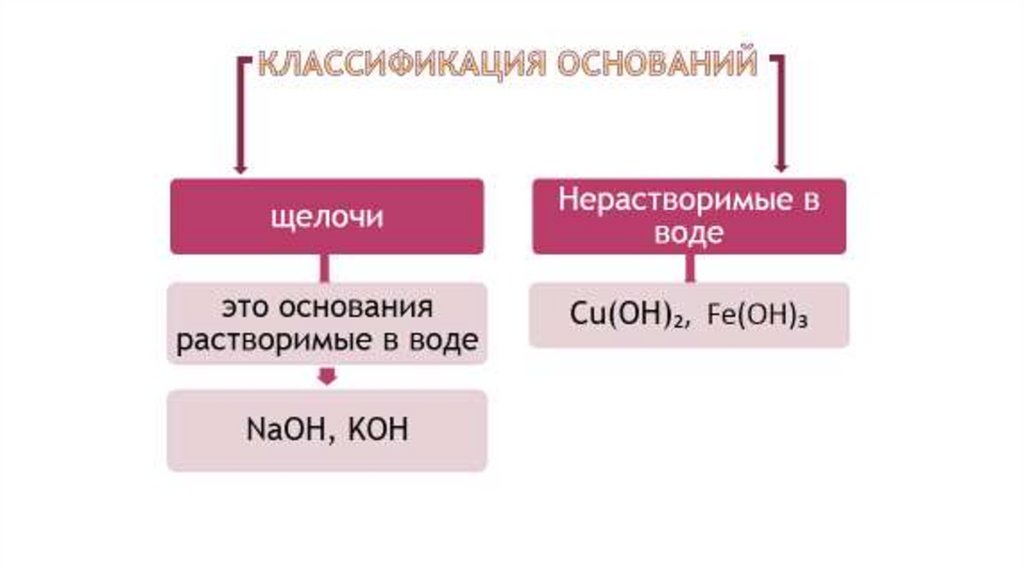
Ответы3. Выберите из предложенных веществ основания и
запишите их в два столбика по признаку растворимости:
CaO Al(OH)3 HCl KOH Na2SO4 MgO
Ba(OH)2 H2SO4
N2O5 NaOH HNO3
Cu(OH)2
MgCO3 Fe(OH)3
Щелочи
Нерастворимые
KOH
Al(OH)3
Ba(OH)2
Cu(OH)2
NaOH
Fe(OH)3
12.
ОБЖщелочи
• Разъедают кожу и слизистые
ткани
• Все работы проводить в очках
и резиновых перчатках
• При попадании на кожу
промывать проточной водой.
Затем обратиться за
медицинской помощью.
13.
Химические свойства оснований.1 задание: Прилить к р-ру КOH + р-р фенолфталеина
1) свойство:
2 задание: Прилить к р-ру КOH + р-р HCl
3 задание: а) Прилить к р-ру КOH + р-р FeCl3
14.
Запись в тетради:1 свойство: изменяет окраску индикатора
KOH + фенолфталеин = малиновый цвет раствора
Почему?
Потому, что KOH = K+ + OHВывод: щелочи диссоциируют на гидроксид-ионы,
которые изменяют окраску индикаторов.
15.
2. Написать уравнение реакцииCu(OH)2 + HNO3→
В чем суть реакции?
Какие ионы «встретились»?
16.
3. Написать уравнение реакцииNaOH + Zn(NO3)2 →
В чем суть реакции?
Какие ионы «встретились»?
17.
Кислотные оксиды – им соответствуют кислотыN2O5
СO2
18.
4)свойство: Щелочь + Кислотный оксид = Соль + Вода
(оксид неметалла)
- это реакция обмена
2NaOH + N2O5 = 2NaNO3 + H2O
• Эта реакция, на первый взгляд, не похожа на
привычный обмен, поэтому вызывает трудности.
• Как ее правильно написать?
19.
• Сначала под формулой кислотного оксида пишемформулу соответствующей кислоты.
NaOH + N2O5 =
(HNO3) азотная кислота
• Затем кислотный остаток из этой кислоты отправляем в
соль, уравниваем реакцию:
• 2NaOH + N2O5 = 2NaNO3 + H2O
(HNO3) нитрат натрия
20.
5) свойство: нерастворимые основания разлагаются принагревании
Cu(OH)2 = CuO + H2O
21.
• Какие ионы определяют свойства растворовоснований?
22.
5. Написать уравнение реакций разложенияFe(OH)3 =
Zn(OH)2 =
23.
Получение основанийпросмотр: mmlab.chemistry.527.oms






















 Химия
Химия








