Похожие презентации:
ИК-спектроскопия
1.
ИК-СПЕКТРОСКОПИЯ2.
Приборы и представление данныхК самописцу
М2
S2
2
М6
М4
P
S4
S
.
1
М1
Источник излучения
М5
М7
S3
S1
М3
М8
Приемник
Д
3.
Приборы и представление данныхДостоинства приборов классической схемы:
■ простота конструкции;
■ относительная дешевизна.
Недостатки:
■ невозможность регистрации слабых сигналов из-за малого
отношения сигнал-шум, что сильно затрудняет работу в
далекой ИК области;
■ сравнительно невысокая разрешающая способность (до
0,1 см-1);
■ длительная (в течение нескольких минут) регистрация
спектров.
4.
Основы метода ИК-Фурьеспектроскопии■ В ИК-Фурье-спектрометрах с образцом
взаимодействует интерферирующая волна, в отличие
от дисперсионных приборов, в которых энергия
взаимодействия находится в строго определенном
диапазоне длин волн.
■ Интерферирующая волна продуцируется в
интерферометре, наиболее распространенным из
которых является интерферометр Майкельсона.
■ Для контроля работы интерферометра, сбора и
хранения данных и, самое главное, проведения
преобразования Фурье используется ЭВМ. Кроме
того, с помощью компьютера проводится
последующая обработка спектра.
5.
Принципиальная схема Фурьеинтерферометра1 – движущееся
зеркало;
2 – неподвижное
зеркало;
3 – разделитель
луча
6.
Приборы и представление данныхДостоинства фурье-спектрометра:
■ высокое отношение сигнал-шум;
■ возможность работы в широком диапазоне длин волн без
смены диспергирующего элемента;
■ быстрая (за секунды и доли секунд) регистрация спектра;
■ высокая разрешающая способность (до 0,001 см-1);
■ возможность обработки спектров.
Недостатки:
■ сложность изготовления
■ высокая стоимость.
7.
Кюветы■ С помощью кювет, изготовленных из KBr, NaCl,
LiF, можно регистрировать ИК-спектры
газообразных, жидких и твердых веществ.
■ Галогениды щелочных металлов прозрачны в
обычно используемом диапазоне инфракрасного
излучения, однако поверхности изготовленных из
них кювет легко повреждаются влагой,
содержащейся в образце или в атмосфере, и
водные растворы исследовать нельзя.
■ Для водных растворов используют стекла из CaF2.
8.
Способы введения образцовв ИК-спектрометр
1. Растворы веществ наиболее удобны для получения
спектров, так как в этом случае отсутствуют
межмолекулярные взаимодействия.
■ В качестве растворителей используют соединения
простейшей структуры, спектр которых состоит из
минимального числа полос, например CHCl3 или
наиболее часто – CCl4, который прозрачен выше 1300
см–1, и сероуглерод, практически прозрачный ниже
1300 см–1. Последовательно растворив вещество в том
и другом растворителе, удается записать весь ИКспектр.
■ Для растворов применяют цилиндрические кюветы
толщиной 0,1–1,0 мм с окнами из солевых пластин.
■ Необходимый для заполнения кюветы объем раствора
0,1–1,0 мл при концентрации 0,05–10 %.
9.
Способы введения образцовв ИК-спектрометр
2. Тонкие пленки (< 0,01 мм) жидкого вещества,
помещенные между солевыми пластинами,
удерживаемыми капиллярными силами.
■ Тонкие пленки твердого вещества готовят следующим
образом. Образец растворяют в подходящем
быстроиспаряющемся растворителе и выливают на
подложку из стекла KBr и сушат. Можно регулировать
необходимую толщину пленки, а растворитель брать в
минимальном количестве.
10.
Способы введения образцовв ИК-спектрометр
3. Пасты, приготовляемые тщательным растиранием
твердого образца с вазелиновым маслом и
помещаемые в виде тонкого слоя между солевыми
пластинами.
■ Само вазелиновое масло, являющееся смесью
углеводородов, интенсивно поглощает в области
~2900 см–1 и ~1400 см–1.
■ Иногда для приготовления паст используются жидкий
парафин (нуйол) или гексахлорбутадиен-1,3,
прозрачный выше 1600 см–1 и в области 1250–1500
см–1, т.е. в тех интервалах частот, в которых поглощает
вазелиновое масло.
11.
Способы введения образцовв ИК-спектрометр
4. Твердые вещества в виде тонкого порошка (0,5–1 мг),
тщательно перетирают с порошком бромида калия
(~100 мг) ( <2 %-ный твердый раствор) в течение 40
мин, и затем спрессованные в специальном
устройстве под давлением до ~4,5·108 Па в тонкую
пластину.
■ Таблетка из KBr – это наилучший вариант.
■ Эта операция сравнительно трудоемка и требует
принятия мер, предотвращающих попадание влаги в
таблетку (красная лампа), однако регистрируемый
таким путем спектр совершенно свободен от полос
поглощения растворителя.
12.
ИНФРАКРАСНАЯСПЕКТРОСКОПИЯ
Некоторые рекомендации по
использованию ИК-спектров
для идентификации органических
соединений
13.
Рекомендации■ Следует обратить внимание на то, всю ли область
ИК-поглощения охватывает рассматриваемый
спектр.
■ Если спектр снят в интервале от 4000 см–1 до
650 см–1, то его называют полным.
■ Такой спектр позволяет получить максимальную
информацию о строении соединения.
14.
РекомендацииОбращаем внимание на метод приготовления образца
исследуемого соединения для записи спектра.
■ В качестве образца используют либо само вещество,
либо его растворы или пасты.
■ Снятие спектров индивидуально чистых веществ обычно
ограничено жидкими веществами, хотя при наличии
специальных кювет можно работать с парами и
расплавами.
■ В этих случаях все полосы поглощения, наблюдаемые в
спектре, принадлежат исследуемому соединению.
■ Техника прессования анализируемого вещества в
таблетках KBr полностью отвечает данному соединению.
15.
Рекомендации■ При использовании растворов и паст некоторые участки
спектра оказываются закрытыми полосами поглощения
растворителя или компонента, на основе которого
готовят пасту.
■ Обычно для твердых веществ используют пасты в
вазелиновом масле и в этом случае из спектра следует
исключить полосы поглощения вазелинового масла
2900–2800, 1460, 1380 см–1.
16.
Анализ ИК-спектра■ Анализ ИК-спектра целесообразно начинать с
коротковолновой части (область высоких частот). В
области 3650–3200 см–1 наблюдается поглощение,
обусловленное валентными колебаниями связей О–Н и
N–Н гидроксильной и аминогрупп.
■ О–Н. Валентное колебание νО–Н, одно из наиболее
характерных для ИК-спектра, образует интенсивную
полосу в области 3600–3200 см–1.
17.
Валентные колебания■ В ИК-спектрах таких
растворов свободная
гидроксильная
группа спиртов
проявляется в
области
3620–3610 см–1.
■ В фенолах
свободные О–Н
проявляются с еще
большей
интенсивностью, чем
в спиртах, но имеют
меньшую частоту
(3615–3600 см–1).
бензиловый спирт
фенол
18.
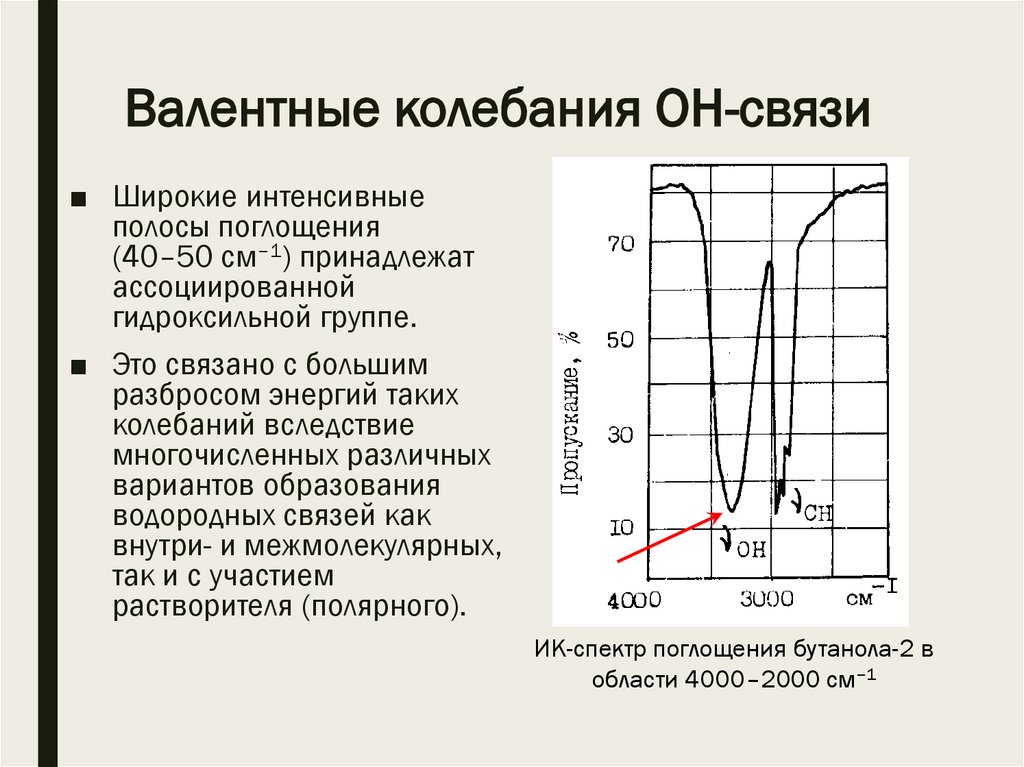
Валентные колебания ОН-связи■ Широкие интенсивные
полосы поглощения
(40–50 см–1) принадлежат
ассоциированной
гидроксильной группе.
■ Это связано с большим
разбросом энергий таких
колебаний вследствие
многочисленных различных
вариантов образования
водородных связей как
внутри- и межмолекулярных,
так и с участием
растворителя (полярного).
ИК-спектр поглощения бутанола-2 в
области 4000–2000 см–1
19.
Валентные колебания ОН-связи■ Водородная связь изменяет
силовую постоянную связи
О–Н и, следовательно,
приводит к уменьшению
частоты колебаний.
■ Характер поглощения
ассоциированной
гидроксильной группы зависит
от природы соединения.
■ Так, в спектрах алифатических
спиртов поглощение
ассоциированной ОН-группы
проявляется в виде широкой
интенсивной полосы
поглощения при
3400–3200 см–1.
ИК-спектр поглощения бутанола-2 в
области 4000–2000 см–1
20.
Валентные колебания ОН-связи■ В фенолах поглощение ОНгруппы сильно смещено в
область низких частот, так
что полосы поглощения,
обусловленные
валентными колебаниями
С–Н-связей, проявляются в
виде пиков на фоне
интенсивного поглощения
фенольного гидроксила.
ИК-спектр поглощения фенола в
области 4000–2000 см–1
21.
Валентные колебания ОН-связи■ Еще больше изменяется
характер поглощения
гидроксильной группы, когда
она входит в состав
карбоксильной функции.
■ В этом случае димеры
карбоновых кислот
поглощают в области 3300–
2500 см–1, причем
поглощение проявляется в
виде широкой интенсивной
полосы, на фоне которой
могут выступать полосы
поглощения С–Н валентных
колебаний.
ИК-спектр поглощения
изовалерьяновой кислоты в
области 4000–2000 см–1
22.
Валентные колебания ОН-связи■ И все же, необходимо специально подчеркнуть, для
большинства соединений, содержащих в своем составе
гидроксильную группу, характерно интенсивное
поглощение в области 3500–3200 см–1.
■ Слабая полоса в этой области скорее свидетельствует о
присутствии в веществе влаги (необходимо наличие
кристаллизационной воды дополнительно проверить по
полосе О–Н в области 1640–1615 см–1), чем ОН-группы,
причем она может быть обусловлена также появлением
первых обертонов валентных колебаний карбонильной
группы ( С=О = 3550–3200 см–1).
23.
Валентные колебания NН-связи■ Наличие в соединении
первичной или вторичной
аминогруппы вызывает
поглощение также в области
3500–3200 см–1.
■ Число полос определяется
степенью замещения у азота,
так для NH2-группы в ИКспектре наблюдаются две
полосы
( asN–H 3500 и sN–H 3400
см–1).
ИК-спектр поглощения анилина в
области 4000–2800 см–1 (10 %
раствор в CСl4)
24.
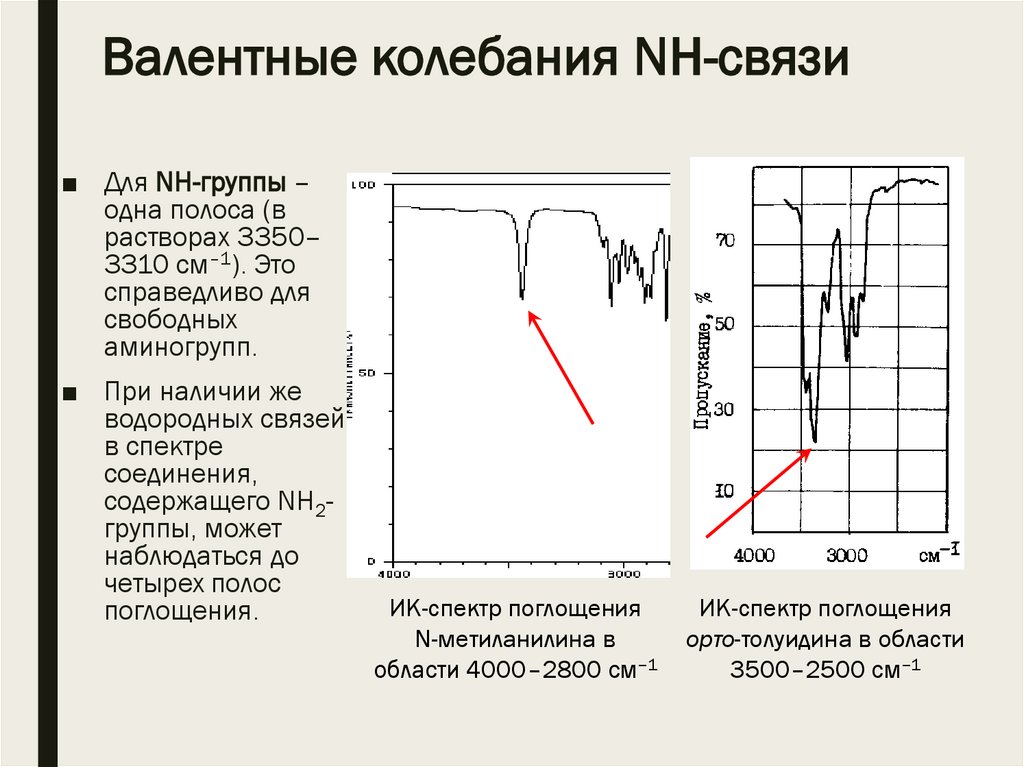
Валентные колебания NН-связи■ Для NH-группы –
одна полоса (в
растворах 3350–
3310 см–1). Это
справедливо для
свободных
аминогрупп.
■ При наличии же
водородных связей
в спектре
соединения,
содержащего NH2группы, может
наблюдаться до
четырех полос
поглощения.
ИК-спектр поглощения
N-метиланилина в
области 4000–2800 см–1
ИК-спектр поглощения
орто-толуидина в области
3500–2500 см–1
25.
Валентные колебания NН-связи■ Первичные соли аминов
(–NH3+) в твердых растворах
дают широкую полосу средней
интенсивности в области
3350–3150 см–1, в растворе
– у них проявляются две
полосы: 3380 и 3280 см–1.
ИК-спектр поглощения
тетраметилхлорид аммония в
области 4000–2800 см–1 (в
пленке)
26.
Валентные колебания NН-связи■ В спектрах первичных амидов
карбоновых кислот в разбавленных
растворах проявляются полосы
умеренной интенсивности ( asN–H
3540–3480 и sN–H 3420–3380 см–
1).
■ Водородная связь в спектрах
амидов в твердом состоянии
смещает asN–H и sN–H
соответственно в область
3350 см–1 и 3200 см–1 с
уменьшением интенсивности.
ИК-спектр поглощения
ацетамида в области 4000–2800
см–1 (в KBr)
27.
Валентные колебания NН-связи■ У вторичных амидов проявляется
полоса для транс- 3450 см–1 и для
цис-конформации 3430 см–1.
■ В ассоциатах имеются две полосы,
одна (3100–3070 см–1) присутствует и
в цис- и транс-изомере, другая
индивидуальна – для цис- 3180–3140
см–1, для транс- 3330–3270 см–1
■ Если в соединении присутствует
гидроксильная и аминогруппы, то
интерпретация спектра в этой области
затруднена и неоднозначна.
ИК-спектр поглощения
N-метилцетамида в области 4000–2700 см–1 (в
пленке)
28.
Валентные колебания CН-связи■ Поглощение в области 3340–2800 см–1 обусловлено
валентными колебаниями С–Н-связей.
■ Для ациклических и ненапряженных –1
циклических структур
С–Н имеют следующие значения (см ):
СН3 asС–Н = 2975–2950 (с.)
sС–Н = 2885–2860 (с.)
СН2 asС–Н = 2940–2915 (с.)
sС–Н = 2870–2845 (с.)
СН С–Н = 2900–2880 (сл.) практически не используются.
■ Асимметричные полосы несколько более интенсивнее, чем
симметричные.
■ Полосы характеристичны, но малоинформативны, т.к. в
веществе обычно осуществляются разные колебания С–Н,
которые, кроме того, могут взаимодействовать между
собой, тем самым образуя полосу со слабо выраженными
максимумами.
29.
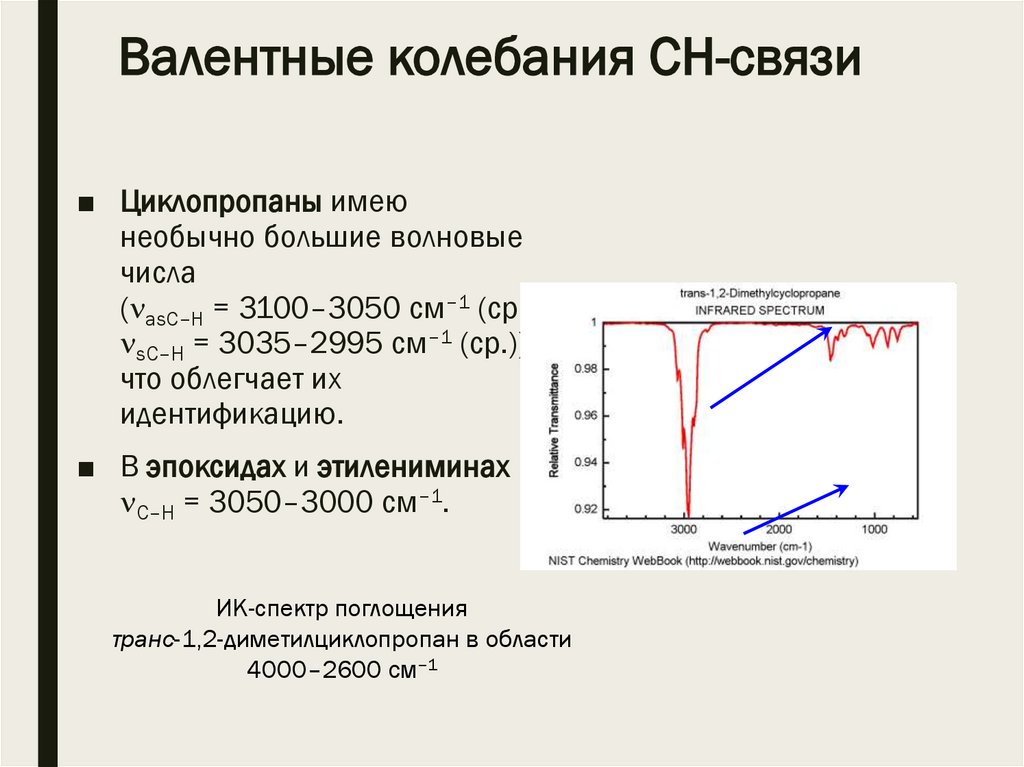
Валентные колебания CН-связи■ Циклопропаны имею
необычно большие волновые
числа
( asС–Н = 3100–3050 см–1 (ср.),
sС–Н = 3035–2995 см–1 (ср.)),
что облегчает их
идентификацию.
■ В эпоксидах и этилениминах
С–Н = 3050–3000 см–1.
ИК-спектр поглощения
транс-1,2-диметилциклопропан в области
4000–2600 см–1
30.
Валентные колебания CН-связи■ Для –OCH3-группы
характерны полосы
поглощения
sС–Н 2830–2815 см–1
в алифатических
и ~2850 см–1 в
ароматических
соединениях.
ИК-спектр поглощения
2-метоксибутан в области 4000–
2600 см–1 (в пленке)
ИК-спектр поглощения
п-метиланизола в области
4000–2700 см–1 (в пленке)
31.
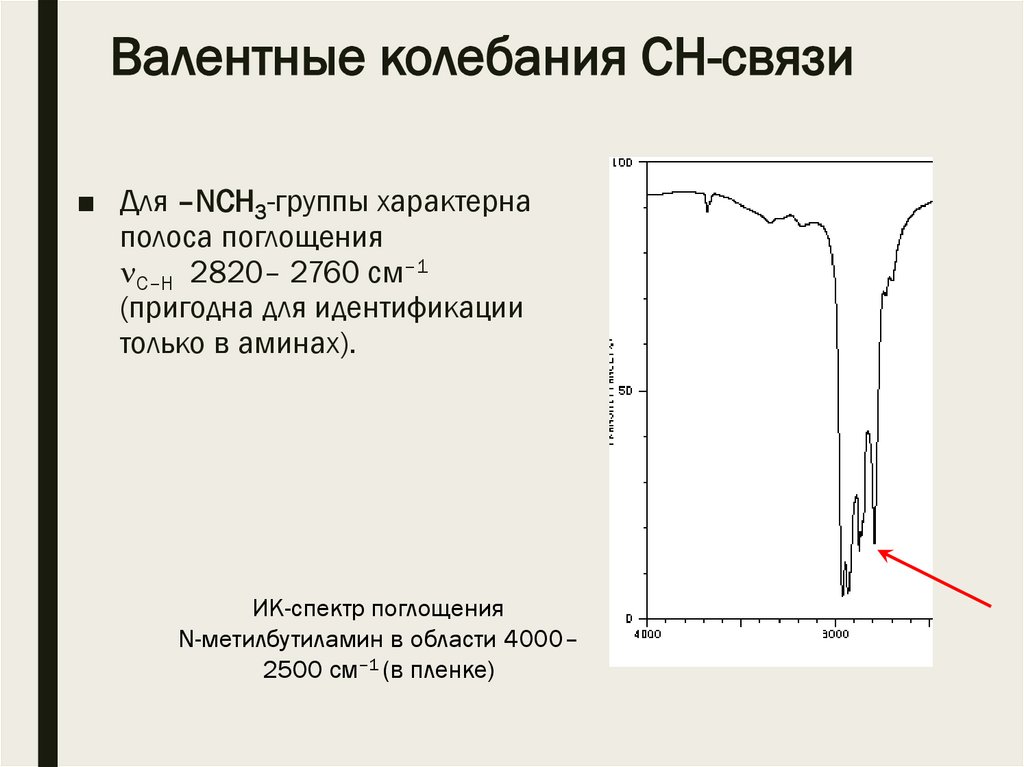
Валентные колебания CН-связи■ Для –NCH3-группы характерна
полоса поглощения
С–Н 2820– 2760 см–1
(пригодна для идентификации
только в аминах).
ИК-спектр поглощения
N-метилбутиламин в области 4000–
2500 см–1 (в пленке)
32.
Валентные колебания CН-связи■ Для определения структуры вещества эти полосы могут
показаться полезными только в том случае, если в
соединении мало атомов водорода (например,
полигалогеналканы).
■ Отсутствие полос в данной области является убедительным
доказательством отсутствием в веществе атомов водорода
при насыщенных углеродных атомах.
■ В спектрах алкилгалогенидов под влиянием соседнего
атома галогена полосы валентных колебаний в метильных
или метиленовых группах сдвигаются и максимумы этих
полос обычно лежат выше 3000 см–1 (до 3058 см–1 у
иодидов и до 3005 см–1 у фторидов).
■ Более полярные заместители снижают интенсивность
полос.
33.
Валентные колебания CН-связи■ Валентные колебания
sp2-С–Н-связи (алкены,
ароматические соединения)
проявляются при
3100–3000 см–1:
=СН2 asС–Н = 3095–3075 (ср.)
sС–Н = 2975 (ср.)
=СН С–Н = 3045–3010 (ср.)
дифференцировать
циси трансне удается
ИК-спектр поглощения
пентена-1 в области 4000–2600 см–1
(в пленке)
34.
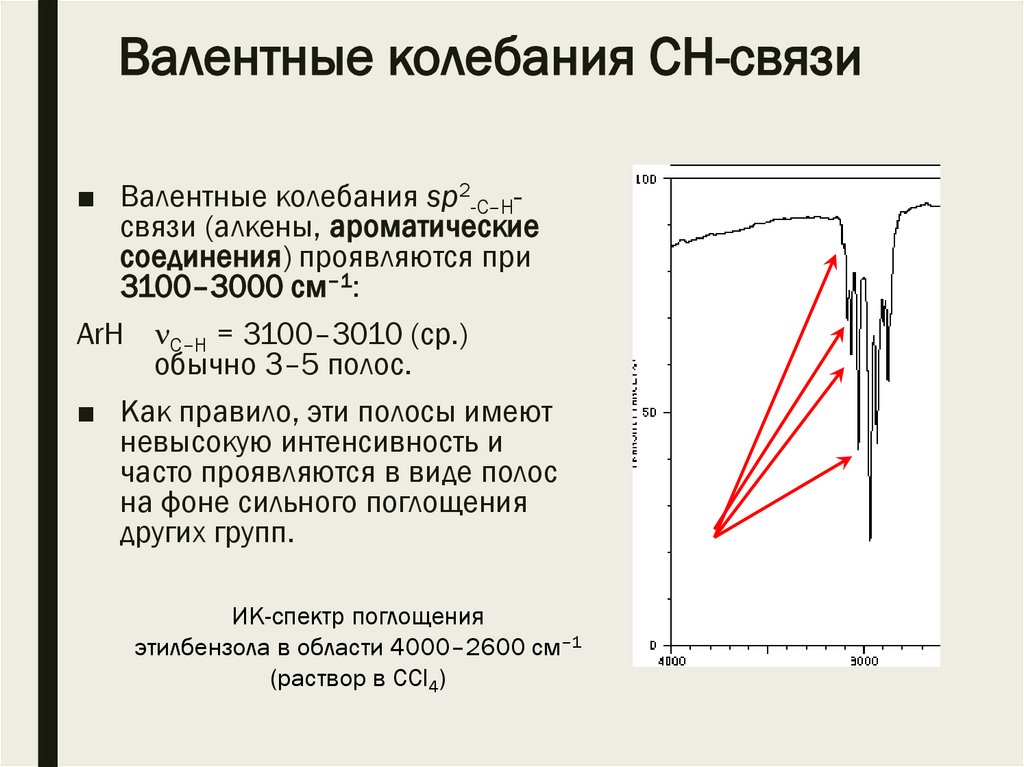
Валентные колебания CН-связи■ Валентные колебания sp2-С–Нсвязи (алкены, ароматические
соединения) проявляются при
3100–3000 см–1:
ArН С–Н = 3100–3010 (ср.)
обычно 3–5 полос.
■ Как правило, эти полосы имеют
невысокую интенсивность и
часто проявляются в виде полос
на фоне сильного поглощения
других групп.
ИК-спектр поглощения
этилбензола в области 4000–2600 см–1
(раствор в CCl4)
35.
Валентные колебания CН-связи■ Специфическим поглощением
обладают алкины: валентные
колебания sр-С–Н-связей
проявляются при 3310–3300 см–1
в виде узкой полосы с обычно
умеренной интенсивностью.
■ Следует обратить внимание, что в
этом диапазоне поглощают группы
–OH и –NH.
ИК-спектр поглощения
пентина-1 в области 4000–2600 см–1 (в
пленке)
36.
Валентные колебания CН-связи■ Для альдегидов полоса С–Н
составляет 2880–2650 см–1 и
проявляется обычно в виде
дублета ( С–Н и обертон или
составная часть) средней или
малой интенсивности (2880–
2800 и 2780–2650 см–1 (как
правило слабее).
ИК-спектр поглощения
пропаналя в области 4000–2600 см–1
(раствор в CCl4)































 Физика
Физика








