Похожие презентации:
Соли как производные кислот и оснований
1. Соли как производные кислот и оснований.
2. Цель и задачи урока.
Цель урока: выяснить почему соли являютсяпроизводными кислот и оснований.
Задачи урока:
1.Дать определение солей.
2. Рассмотреть состав и название солей.
3. Продолжить обучение школьников определять
степени окисления в сложных соединениях.
4. Научить, составлять формулы солей.
5. Познакомить учащихся с классификацией солей.
6. Познакомить с некоторыми свойства солей.
3.
5.такое
основные
оксиды,
4. Что
1.
2.
3.
Какие
классы
кислоты?
оксиды?
основания?
веществ
вы знаете?
кислотные оксиды, амфотерные?
4.
5.
6. ТЕСТ
1. Определите ряд формул состоящихтолько из:
кислотных оксидов ( I вариант)
основных оксидов: (II вариант)
а) Na2 O, N2O, CuO;
б) CO2, P2O5, Cl2O7;
в) MgO, BaO, K2O;
г) Li2O, CaO, CO.
7. ТЕСТ
2. Выберите из списка веществ формулы:только кислот (I вариант), формулы
только оснований (II вариант):
а) НСI, AICI3, CO2, H2SO4
б) H2SO4, HCI, HNO3, HF
в) NaOH, BaCI2, CO, Ca(OH)2
г) AI(OH)3, NaOH, KOH, Ba(OH)2
8. ТЕСТ
3. Выберите формулу оксида серы (IV) – Iвариант
Выберите формулу оксида углерода (II) –
II вариант:
а)H2S б) CO
в) HNO3
г) ZnO д) SO2
9. ТЕСТ
4. * Выберите формулу серной кислоты –I вариант
* Выберите формулу сернистой кислоты –
II вариант
а) H2SiO3 б) H2SO4 в) H2SO3 г) H2S
10. ТЕСТ
5. * Выберите формулу гидроксида калия –I вариант
* Выберите формулу гидроксида кальция II вариант
а) Ba(OH)2, б) NaOH в) KOH г) Ca(OH)2
11. ТЕСТ
6. * Выберите формулы растворимого вводе основания – I вариант
* Выберите формулы нерастворимого в
воде основания – II вариант
а)Cu(OH)2 б) KOH в) LiOH г) AI(OH)3
12. ТЕСТ
7. * Выберите формулы, в которыхлакмус меняет свой цвет
на красный – I вариант
* Выберите формулы, в которых лакмус
меняет свой цвет на синий – II вариант
а) НСI б) H2SO4 в) NaOH г) KOH
13. Ответы к тесту.
I вариант1. б
2. б
3. д
4. б
5. в
6. б, в
7. а, б
II вариант
1. в
2. г
3. б
4. в
5. г
6. а, г
7. в, г
14. Критерии оценивая.
Оценка«5» - одна ошибка
Оценка «4» - две ошибки
Оценка «3» - три ошибки
Оценка «2» - четыре
ошибки и больше.
15.
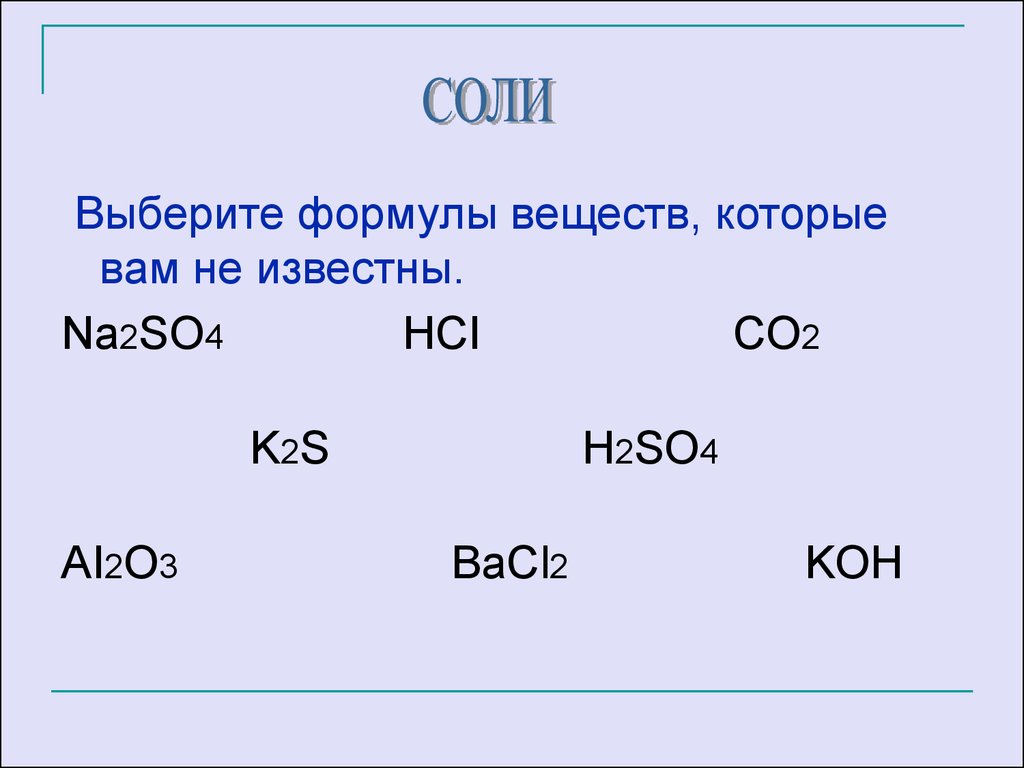
Выберите формулы веществ, которыевам не известны.
Na2SO4
HCI
CO2
K2S
AI2O3
H2SO4
ВаCl2
KOH
16.
Чем объединены и чем отличаютсяперечисленные соединения:
Na2SO4
K2S
ВаCl2
Cu(NO3)2
CaSiO3
K3PO4
17.
Cоли –это сложные вещества,
состоящие из атомов
металла и кислотного остатка.
18.
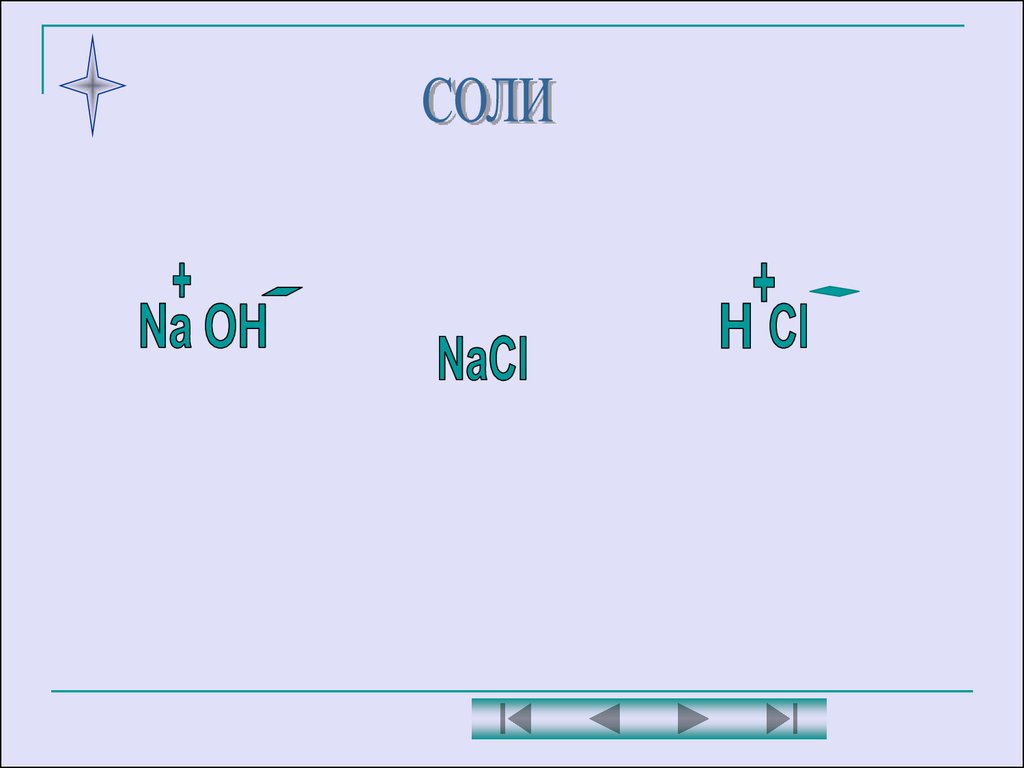
19. Соли
С уверенностью можно сказать, что, по крайнеймере, одно химическое соединение в довольно
чистом виде имеется в каждом доме, в каждой
семье. Это – поваренная соль или как ее
называют химики – хлорид натрия NaCl.
20. Соли
Гипс –кристаллогидрат
сульфата кальция
СаSO4 * 2H2O
21. Соли
Из мрамора(СаСО3) сделан
дворец в Индии
Тадж- Махал
22. Соли
Кристаллогидратсульфата меди (II)
СuSO4* 5H2O
Безводный сульфат
меди(II)
23. Соли
* Кристаллогидратжелеза или
железный купорос
FeSO4* 7H2O
* Сульфат магния –
горькая
английская соль
MgSO4
24. Лабораторная работа «Знакомство с образцами солей»
Название Агрегатноевещества состояние
Цвет Запах Формула Растворим. в
воде
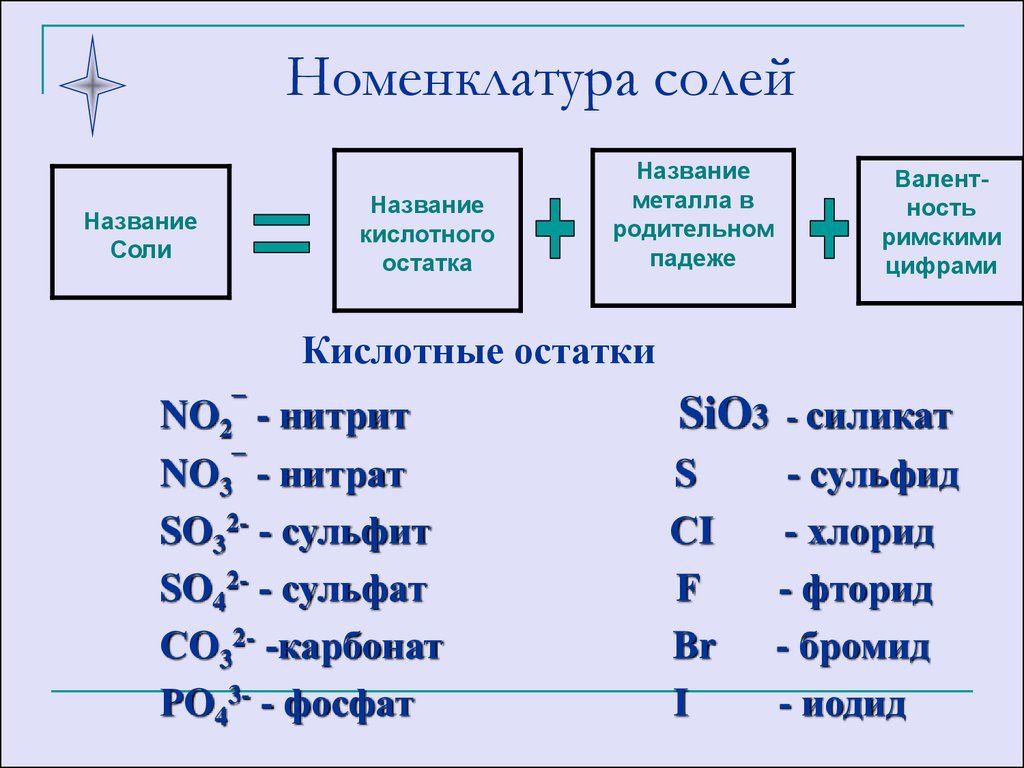
25. Номенклатура солей
НазваниеСоли
Название
кислотного
остатка
Название
металла в
родительном
падеже
Валентность
римскими
цифрами
Кислотные остатки
NO2¯ - нитрит
NO3¯ - нитрат
SO32- - сульфит
SO42- - сульфат
СO32- -карбонат
РO43- - фосфат
SiO3 - силикат
S
СI
F
Br
I
- сульфид
- хлорид
- фторид
- бромид
- иодид
26. Составить формулу сульфата алюминия:
Составьте формулы:сульфата натрия,
сульфата кальция,
сульфата железа(III).
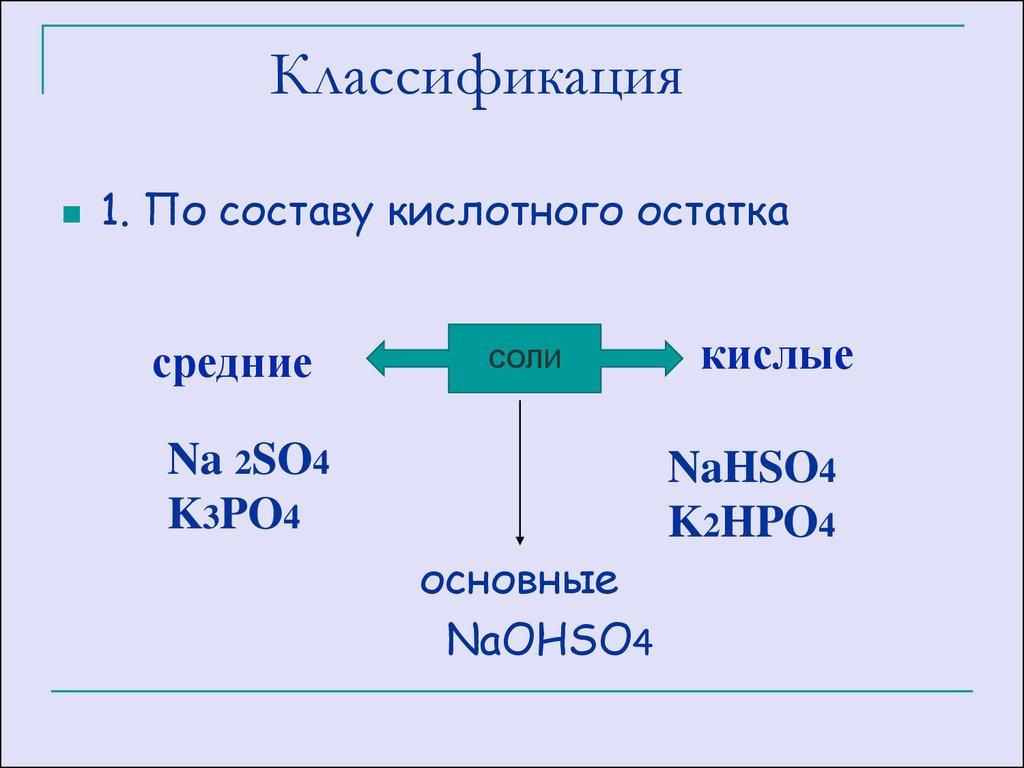
27. Классификация
1. По составу кислотного остаткасредние
СОЛИ
Na 2SO4
K3PO4
кислые
NaHSO4
K2HPO4
основные
NaOHSO4
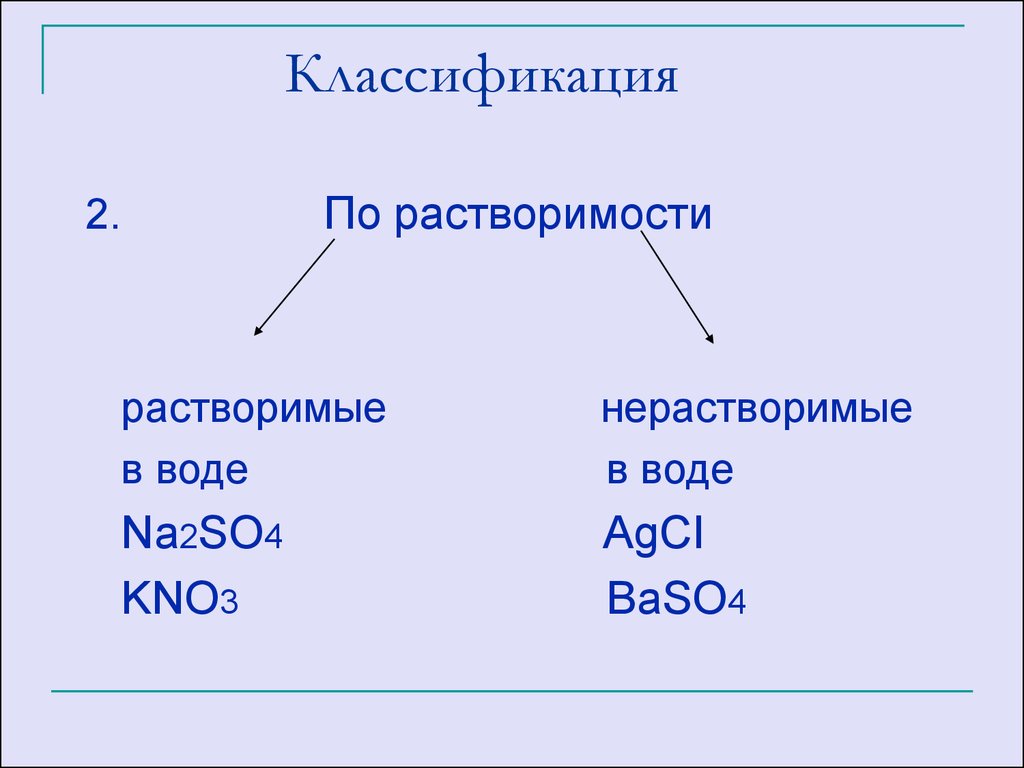
28. Классификация
По растворимости2.
растворимые
в воде
нерастворимые
в воде
Na2SO4
KNO3
AgCI
BaSO4
29. ЗАКРЕПЛЕНИЕ
Дать названиявеществам:
Ca(NO3)магния,
3.2.Составить
солей:
2, K2SO3,
1.формулы
Что такое
соли?нитрита
Li2силиката
CO3, CuSO
натрия,
фосфатарастворимость
кальция.
4. Определить
этих веществ.
30. Домашнее задание:
§21, Упр.2, 3,наизусть названия солей на примере
солей натрия.
























 Химия
Химия