Похожие презентации:
Физические и химические явления. Закон сохранения массы веществ. Уравнения химических реакций. Типы химических реакций
1. Физические и химические явления. Закон сохранения массы веществ. Уравнения химических реакций. Типы химических реакций.(8 класс)
Титович Е.Н.2. Тема урока: Физические и химические явления, Химические реакции Цель урока: Познакомить с признаками физических и химических явлений, науч
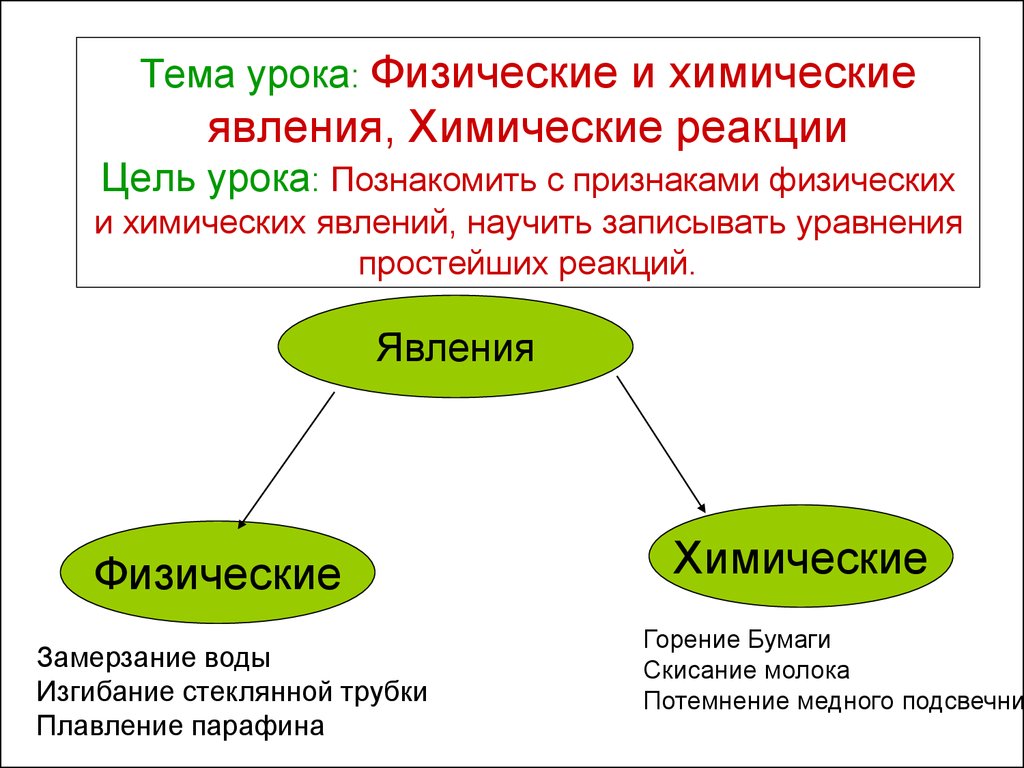
Тема урока: Физические и химическиеявления, Химические реакции
Цель урока: Познакомить с признаками физических
и химических явлений, научить записывать уравнения
простейших реакций.
Явления
Физические
Замерзание воды
Изгибание стеклянной трубки
Плавление парафина
Химические
Горение Бумаги
Скисание молока
Потемнение медного подсвечни
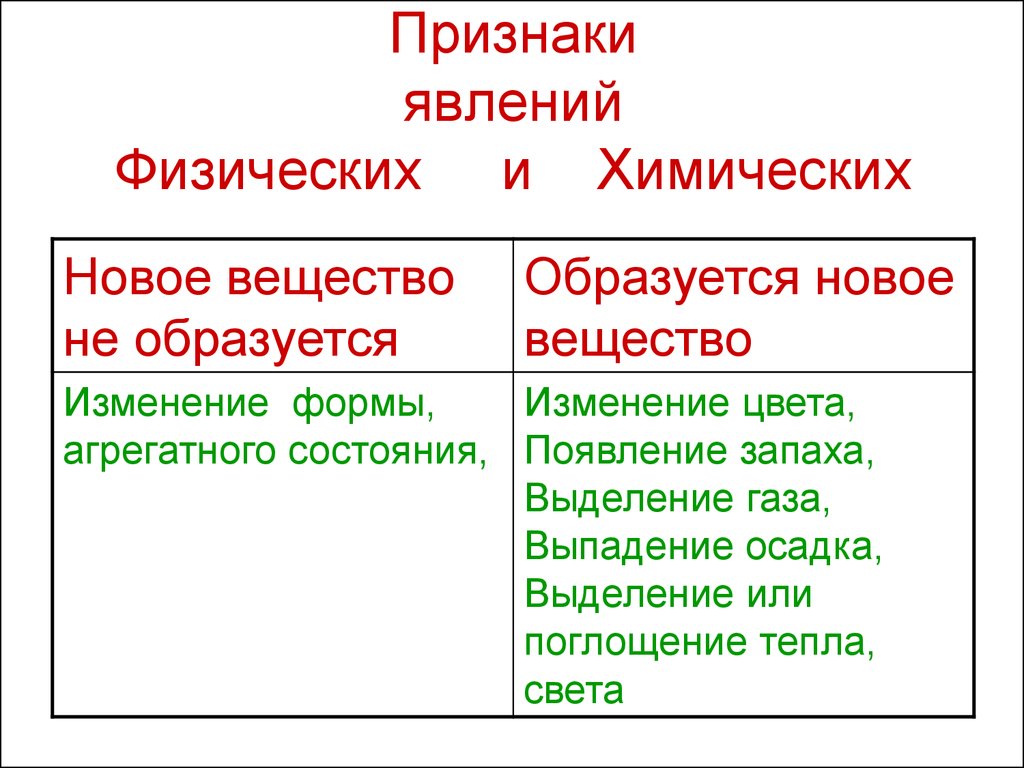
3. Признаки явлений Физических и Химических
Новое веществоне образуется
Образуется новое
вещество
Изменение формы,
Изменение цвета,
агрегатного состояния, Появление запаха,
Выделение газа,
Выпадение осадка,
Выделение или
поглощение тепла,
света
4.
5.
6. Закон сохранения массы веществ,уравнения химических реакций
М.В. ЛомоносовРоберт Бойль
А.Л. Лавуазье
А
7.
8. Уравнения химических реакций
Химическое уравнение- условнаязапись химической реакции с помощью
химических формул и коэффициентов
С+О2=СО2
+5 -2
4Р+ 5О2= 2 P2 O 5
-2
+3
4 AL+3 O2 = 2 Al O 3
2
Mg+CL2=
AL+S=
9. Запишите уравнения реакций, подтвердите расчётом закон сохранения массы веществ
Запишите уравнения реакций,
подтвердите расчётом закон
сохранения массы веществ
Ca+ O2=
Mg+ N2=
AL+ CL2=
H2O= H2 +…
AL + HCl = AlCL3 + …
Ag2O= Ag + …
Na+ Cl2 =
K+ S =
CO+ Fe2O3 = CO2+ …
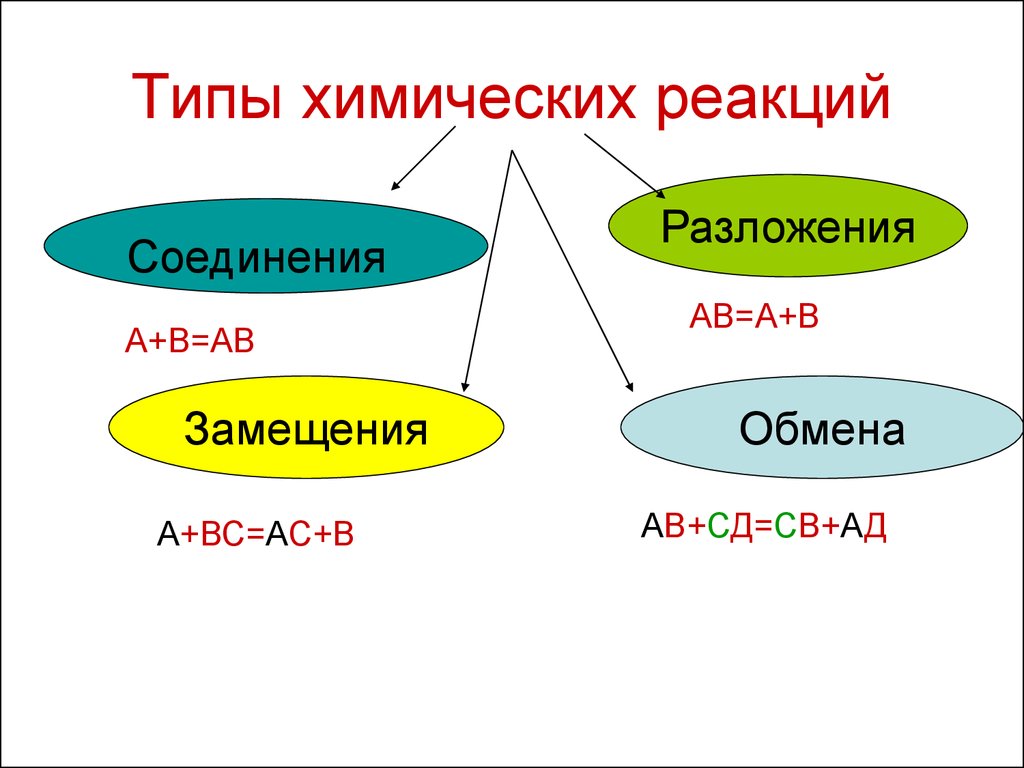
10. Типы химических реакций
СоединенияА+В=АВ
Замещения
А+ВС=АС+В
Разложения
АВ=А+В
Обмена
АВ+СД=СВ+АД
11.
12.
13. Закончить уравнения реакций и определить их тип
K+ N2=AL+ Fe3O4= … + …
Ba+ O2=
KOH+ ALCL3= AL(OH)3+….
HgO= O2 + …
SO2+ O2= SO3
Na2O+ H2O=
Mg+ H3PO4= Mg3(PO4)2 +…
Для первого и второго уравнения подтвердить расчётом
закон сохранения массы веществ
14. Запишите уравнения реакций между:
1 серной кислотой и гидроксидом алюминия2 оксидом кальция и ортофосфорной кислотой
3 сульфатом алюминия и гидроксидом натрия
4 сульфатом меди(II) и алюминием
5 карбонатом кальция и азотной кислотой
6 нитратом железа(III) и гидроксидом калия
7 оксидом железа(III) и алюминием
8 алюминием и соляной кислотой
9 хлоридом бария и сульфатом натрия
10 сернистой кислотой и гидроксидом калия
15. Самостоятельная работа
В-1В-2
Закончите уравнения реакций, расставьте
коэффициенты, укажите тип реакции.
АL+O2=
Mg+ HCL=MgCL2+…
K2O+HCL= KCL+…
Ag2O=Ag+…
Na+O2=
BaO+HCL=BaCL2+…
H2O=H2+…
C+CuO=CO2+…
•Для последнего уравнения
подтвердите расчётом закон
сохранения массы веществ.











 Химия
Химия








