Похожие презентации:
Метаболизм холестерола (2 курс)
1.
МЕТАБОЛИЗМ ХОЛЕСТЕРОЛА2 КУРС , БАКАЛАВРИАТ
КАФЕДРА БИОХИМИИ
БИОЛОГИЧЕСКИЙ ФАКУЛЬТЕТ
Подготовила: Пинковская Екатерина
Викторовна
2022
2.
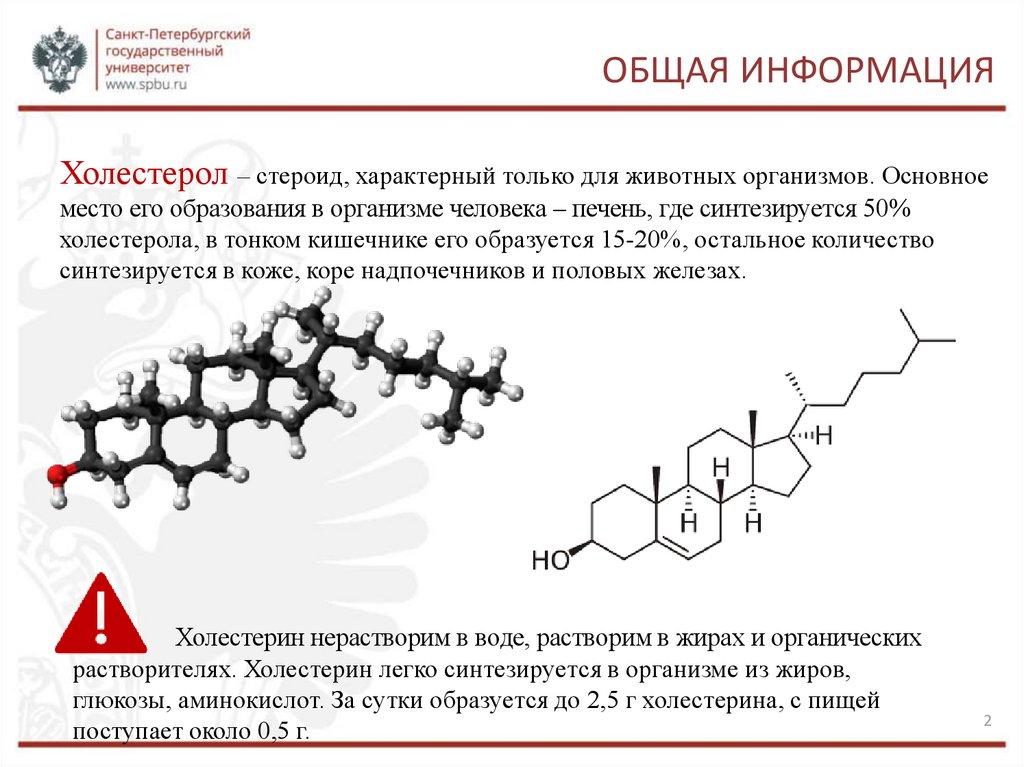
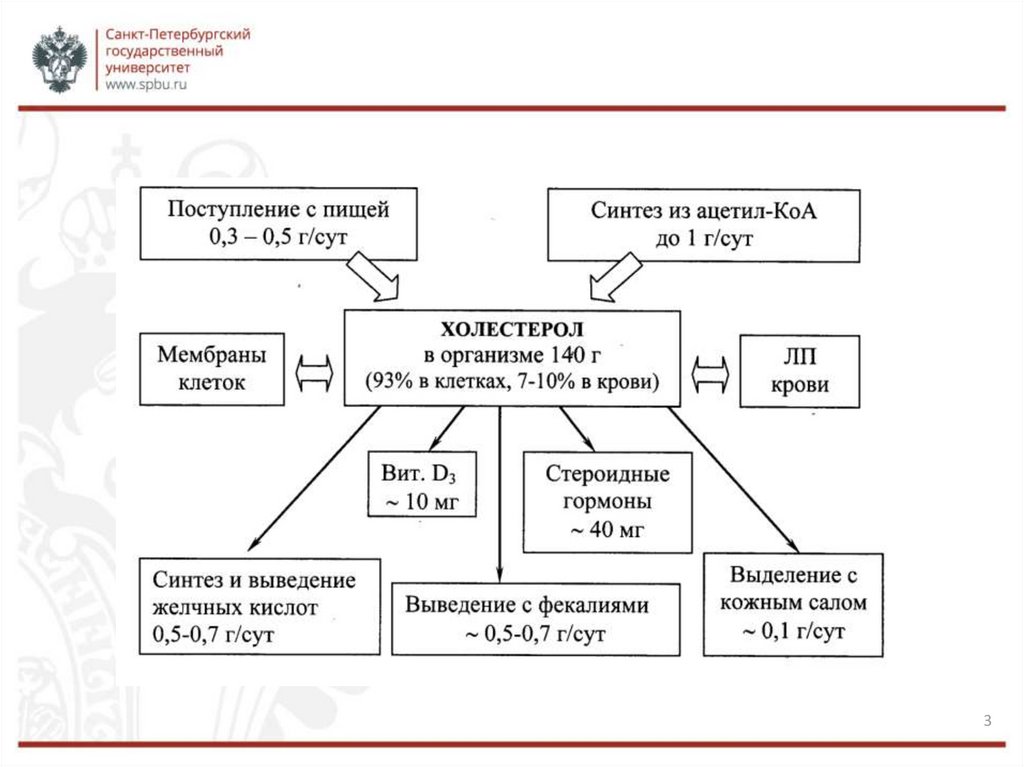
ОБЩАЯ ИНФОРМАЦИЯХолестерол – стероид, характерный только для животных организмов. Основное
место его образования в организме человека – печень, где синтезируется 50%
холестерола, в тонком кишечнике его образуется 15-20%, остальное количество
синтезируется в коже, коре надпочечников и половых железах.
Холестерин нерастворим в воде, растворим в жирах и органических
растворителях. Холестерин легко синтезируется в организме из жиров,
глюкозы, аминокислот. За сутки образуется до 2,5 г холестерина, с пищей
поступает около 0,5 г.
2
3.
34.
ОБЩАЯ ИНФОРМАЦИЯХолестерин обеспечивает устойчивость клеточных мембран
в широком интервале температур.
Он необходим для выработки витамина D, выработки
надпочечниками различных стероидных гормонов (включая
кортизол, альдостерон, половые гормоны: эстрогены,
прогестерон, тестостерон), жёлчных кислот.
4
5.
56.
ОБЩАЯ ИНФОРМАЦИЯИзбыток холестерина (гиперхолестеринемия)
приводит к атеросклерозу сосудов, при
котором, например, может произойти
холестериновая эмболия.
6
7.
78.
БИОСИНТЕЗ8
9.
БИОСИНТЕЗПроисходит в цитозоле клеток. Это один из
самых длинных метаболических путей в
организме человека.
9
10.
БИОСИНТЕЗЦепь биосинтеза холестерина, включающая в себя несколько
ступеней:
1. Превращение трёх молекул активного ацетата в пятиуглеродный мевалонат.
2. Превращение мевалоната в активный изопреноид —
изопентенилпирофосфат.
3. Образование тридцатиуглеродного изопреноида сквалена из шести молекул
изопентенилдифосфата.
4. Циклизация сквалена в ланостерин.
5. Последующее превращение ланостерина в холестерин.
10
11.
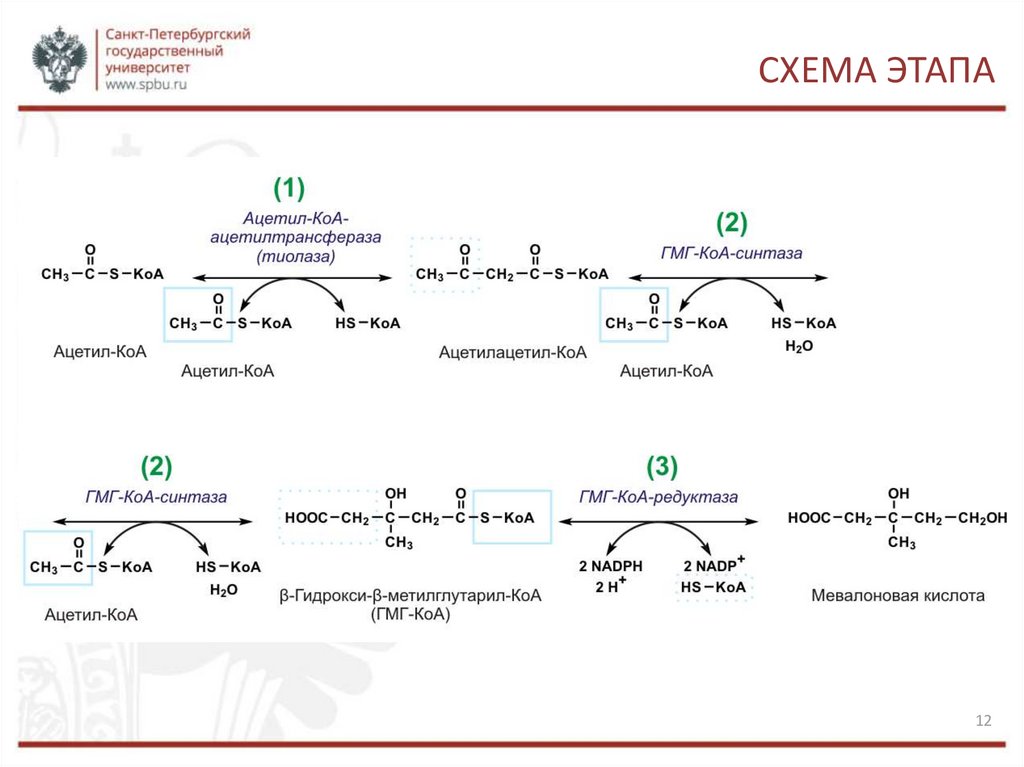
СИНТЕЗ МЕВАЛОНАТАСинтез мевалоната протекает в три этапа.
1. Образование ацетоацетил-КоА из двух молекул ацетил-КоА с помощью тиолазного
фермента ацетоацетилтрансферазы. Реакция обратима. Происходит в цитозоле.
2. Образование β-гидрокси-β-метилглутарил-КоА из ацетоацетил-коА с третьей
молекулой ацетил-КоА с помощью гидроксиметилглутарил-КоА-синтазы (ГМГ-КоАсинтазы). Реакция также обратима. Происходит в цитозоле.
3. Образование мевалоната восстановлением ГМГ и отщеплением HS-KoA с помощью
НАДФ-зависимой гидроксиметилглутарил-КоА-редуктазы (ГМГ-КоА-редуктаза).
Происходит в гЭПР. Это первая практически необратимая реакция в цепи биосинтеза
холестерина, а также она лимитирует скорость биосинтеза холестерина. Отмечены
суточные колебания синтеза этого фермента. Активность его увеличивается при
введении инсулина и тиреоидных гормонов, снижается при голодании, введении
глюкагона, глюкокортикоидов.
11
12.
СХЕМА ЭТАПА12
13.
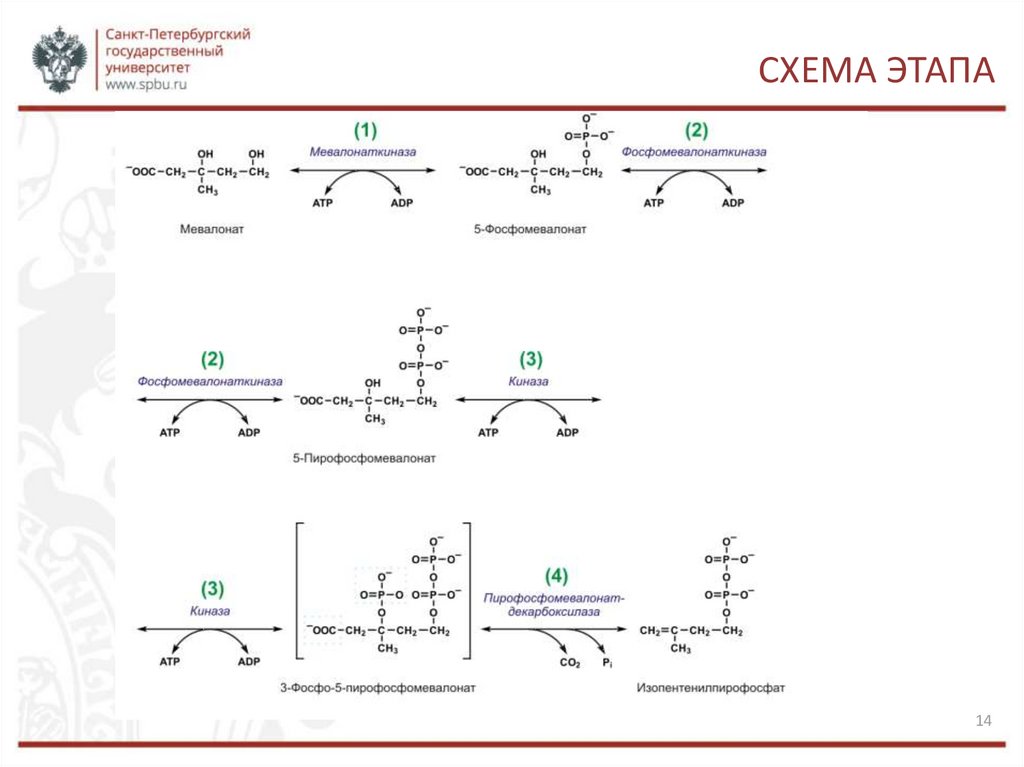
СИНТЕЗ ИЗОПЕНТЕНИЛПИРОФОСФАТА1, 2. Вначале мевалоновая кислота дважды фосфорилируется с
помощью АТФ: до 5-фосфомевалоната, а затем до 5пирофосфомевалоната.
3. 5-пирофосфомевалонат фосфорилируется по 3 атому углерода,
образуя нестабильный промежуточный продукт — 3-фосфо-5пирофосфомевалонат.
4. Последний декарбоксилируется и дефосфорилируется, образуется
изопентенилпирофосфат.
13
14.
СХЕМА ЭТАПА14
15.
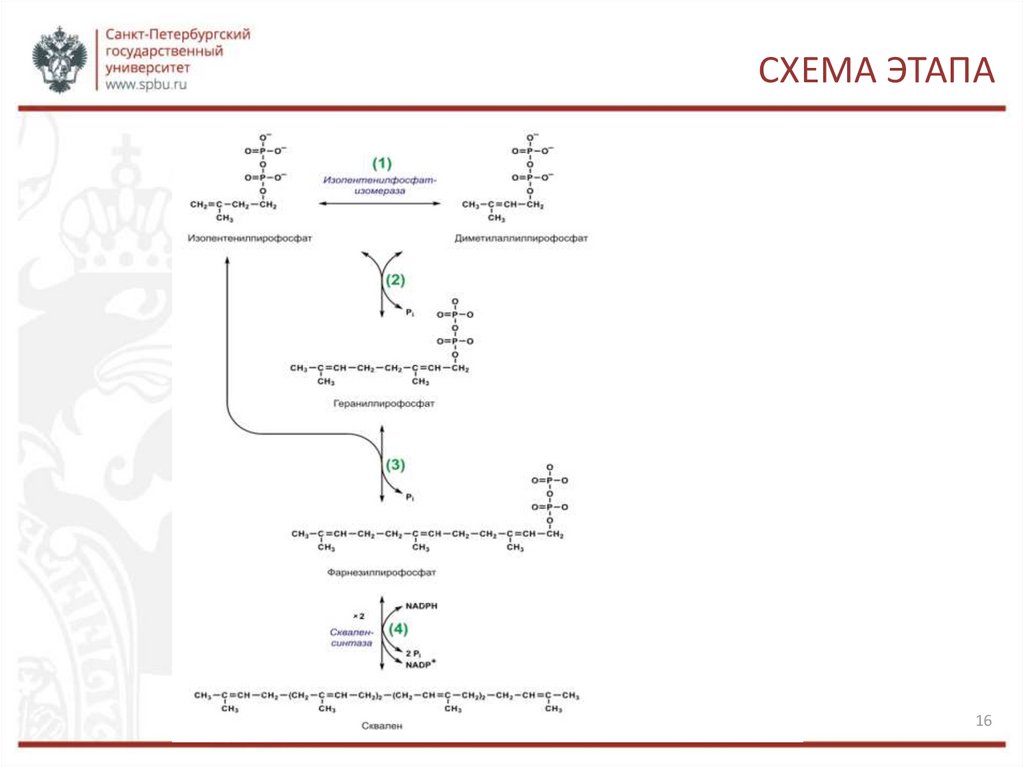
СИНТЕЗ ИЗОПЕНТЕНИЛДИФОСФАТА1. Изопентенилпирофосфат изомеризуется в диметилаллилпирофосфат.
2. Конденсация изопентенилпирофосфата (С5) с диметилаллилпирофосфатом (С5) и
образование геранилпирофосфата (С10). При этом высвобождается молекула
пирофосфата.
3. Конденсация изопентенилпирофосфата (С5) с геранилпирофосфатом (С10).
Образуется фарнезилпирофосфат (С15) и высвобождается ещё одна молекула
пирофосфата.
4. Конденсация двух молекул фарнезилпирофосфата (С15) «голова-к-голове» и
образование сквалена (С30). Реакция проходит с затратой НАДФН, и высвобождаются
две молекулы пирофосфата. Молекулы фарнезилпирофосфата конденсируются концами,
несущими пирофосфатные группы. Сначала отщепляется одна пирофосфатная группа и
образуется промежуточный прескваленпирофосфат. Он, в свою очередь,
восстанавливается с помощью НАДФН. Второй пирофосфат уходит. Образуется
сквален.
5. Начиная со сквалена, продукты пути биосинтеза холестерина нерастворимы в водной
среде и участвуют в дальнейших реакциях, будучи связанными со стеринпереносящими
белками (СПБ).
15
16.
СХЕМА ЭТАПА16
17.
СИНТЕЗ ЛАНОСТЕРИНА1. Под действием скваленэпоксидазы образуется эпоксид сквалена
2. Затем эпоксид сквалена циклизуется в ланостерин. При этом метильная группа у
С14 переносится на С13, а метильная группа у С8 — на С14.
17
18.
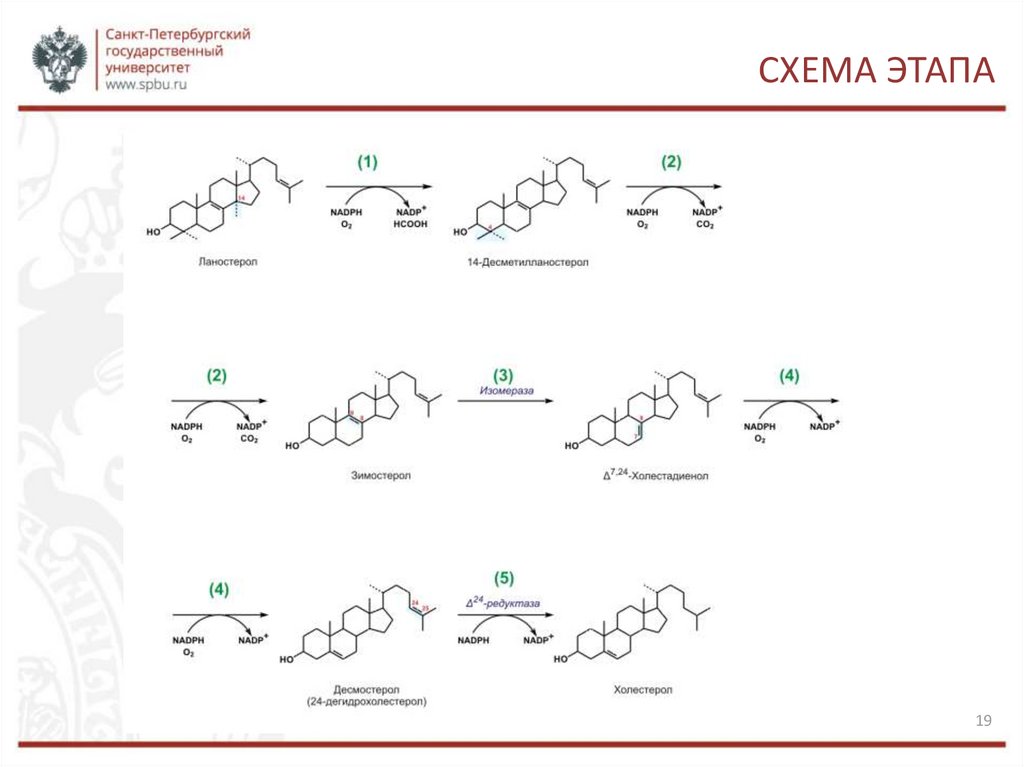
СИНТЕЗ ХОЛЕСТЕРОЛАЛаностерин превращается в мембранах гладкого эндоплазматического
ретикулума в холестерин.
1.Метильная группа при С14 окисляется, и образуется 14-десметилланостерин.
2. Затем удаляются ещё два метила при С4, и образуется зимостерол.
3. Далее двойная связь C8=С9 перемещается в положение С8=С7 и образуется
Δ7,24-холестадиенол.
4. Двойная связь далее перемещается в положение С5=С6,образуется
десмостерол.
5. После чего в боковой цепи восстанавливается двойная связь, и образуется
холестерин.
(Восстановление двойной связи в боковой цепи может, однако, происходить и на
предшествующих стадиях биосинтеза холестерола.)
18
19.
СХЕМА ЭТАПА19
20.
ДРУГИЕ ПУТИ СИНТЕЗАУ некоторых организмов при синтезе стероидов могут
встречаться другие варианты реакций (например,
немевалонатный путь образования пятиуглеродных молекул).
20
21.
РЕГУЛЯЦИЯ СИНТЕЗА ХОЛЕСТЕРОЛА1. Фосфорилирование/дефосфорилирование ГМГ-КоА-редуктазы.
Инсулин стимулирует дефосфорилирование ГМГ-КоА-редуктазы,
переводя её тем самым в активное состояние. Следовательно, в
абсорбтивный период синтез ХС увеличивается. В этот период
увеличивается и доступность исходного субстрата для синтеза – ацетилКоА. Глюкагон оказывает противоположное действие: через
протеинкиназу А стимулирует фосфорилирование ГМГ-КоА-редуктазы,
переводя её в неактивное состояние. В результате синтез ХС в
постабсорбтивном периоде и при голодании ингибируется.
21
22.
РЕГУЛЯЦИЯ СИНТЕЗА2. Ингибирование синтеза ГМГ-КоА-редуктазы. ХС (конечный продукт
метаболического пути) снижает скорость транскрипции гена ГМГ-КоАредуктазы, подавляя таким образом собственный синтез, аналогичный эффект
вызывают и жёлчные кислоты.
22
23.
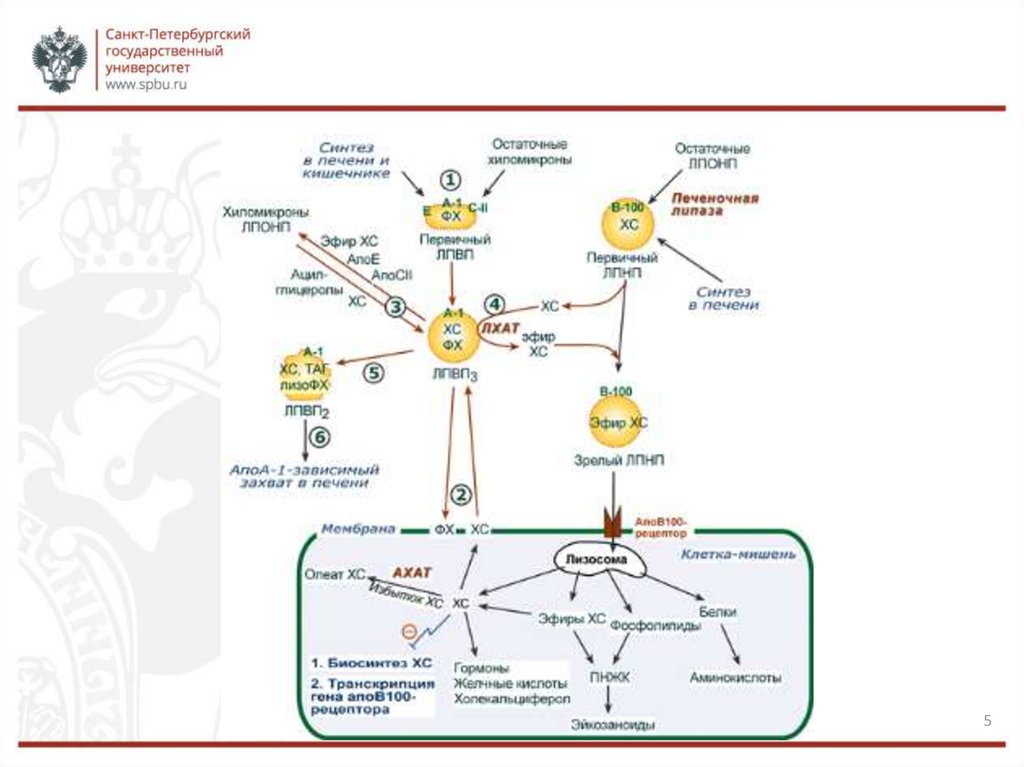
ТРАНСПОРТ ХОЛЕСТЕРОЛАТранспорт холестерола кровью осуществляется в составе ЛП. ЛП
обеспечивают поступление в ткани экзогенного ХС, определяют его
потоки между органами и выведение из организма. Если количество ХС,
поступающего в клетку, превышает её потребность, то синтез рецепторов
ЛПНП подавляется, что уменьшает поток ХС из крови. При снижении
концентрации свободного ХС в клетке, наоборот, синтез рецепторов
активируется. В регуляции синтеза рецепторов ЛПНП участвуют
гормоны: инсулин, трийодтиронин и половые гормоны увеличивают
образование рецепторов, а глюкокортикоиды – уменьшают.
В так называемом «обратном транспорте холестерола», т.е. пути,
обеспечивающем возвращение ХС в печень, основную роль играют
ЛПВП.
23
24.
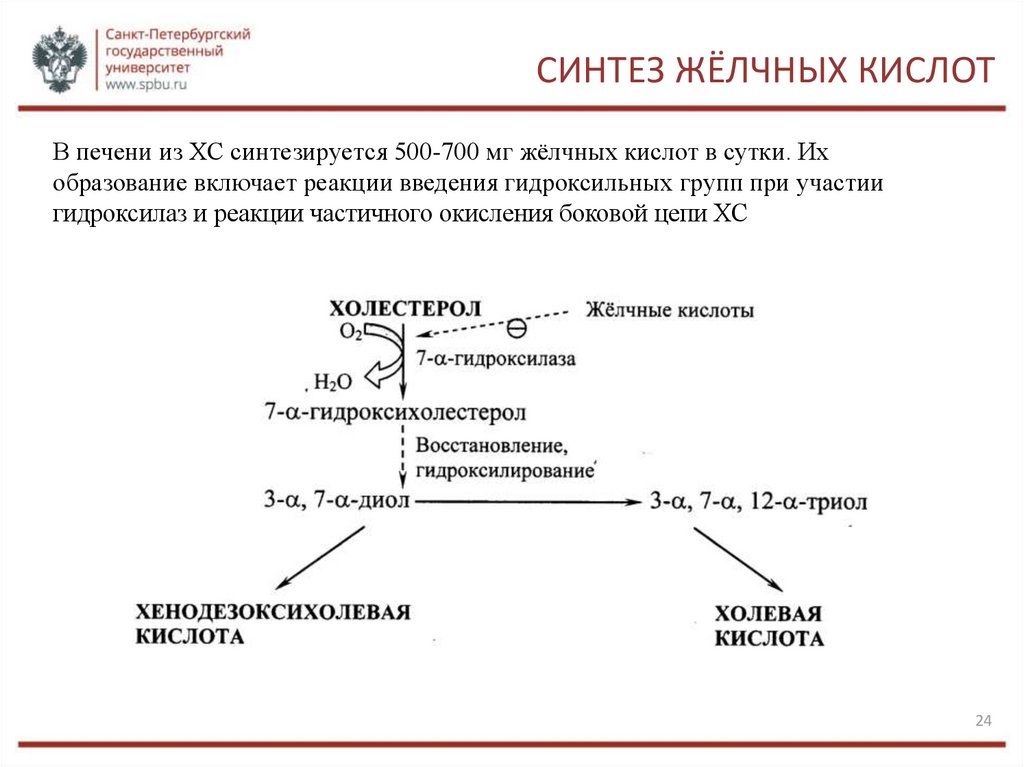
СИНТЕЗ ЖЁЛЧНЫХ КИСЛОТВ печени из ХС синтезируется 500-700 мг жёлчных кислот в сутки. Их
образование включает реакции введения гидроксильных групп при участии
гидроксилаз и реакции частичного окисления боковой цепи ХС
24
25.
ПРЕЗЕНТАЦИЯ•Биологическая химия», Берёзов Т. Т., Коровкин Б. Ф.]
•Кольман Я., Рём К.-Г., «Наглядная биохимия», пер. с нем., М., «Мир», 2009.
•Марри Р., Греннер Д., Мейес П., Родуэлл В., «Биохимия человека». М., «Мир»,
1993.
•https://studfile.net/preview/7225225/page:75/
25
26.
Спасибоза внимание!
Санкт-Петербургский
государственный университет
spbu.ru
















 Химия
Химия








