Похожие презентации:
Липиды. Метаболизм. (Лекция 9)
1. ЛЕКЦИЯ № 9
ФГБОУ ВО УГМУ Минздрава РоссииКафедра биохимии
Дисциплина: Биохимия
ЛЕКЦИЯ № 9
Липиды.
Метаболизм
Лектор: Гаврилов И.В.
Факультет: лечебно-профилактический,
Курс: 2
Екатеринбург, 2016г
2. Жирные кислоты
• Жирными кислотами (ЖК) - называютсякарбоновые кислоты, которые образуются
при гидролизе омыляемых липидов.
• В основном к жирным кислотам относятся
высшие карбоновые кислоты (содержащие 12
и более атомов С).
• Высшие ЖК водонерастворимыми, они
транспортируются в крови с помощью
альбуминов, а в клетках - с помощью Zбелков.
3.
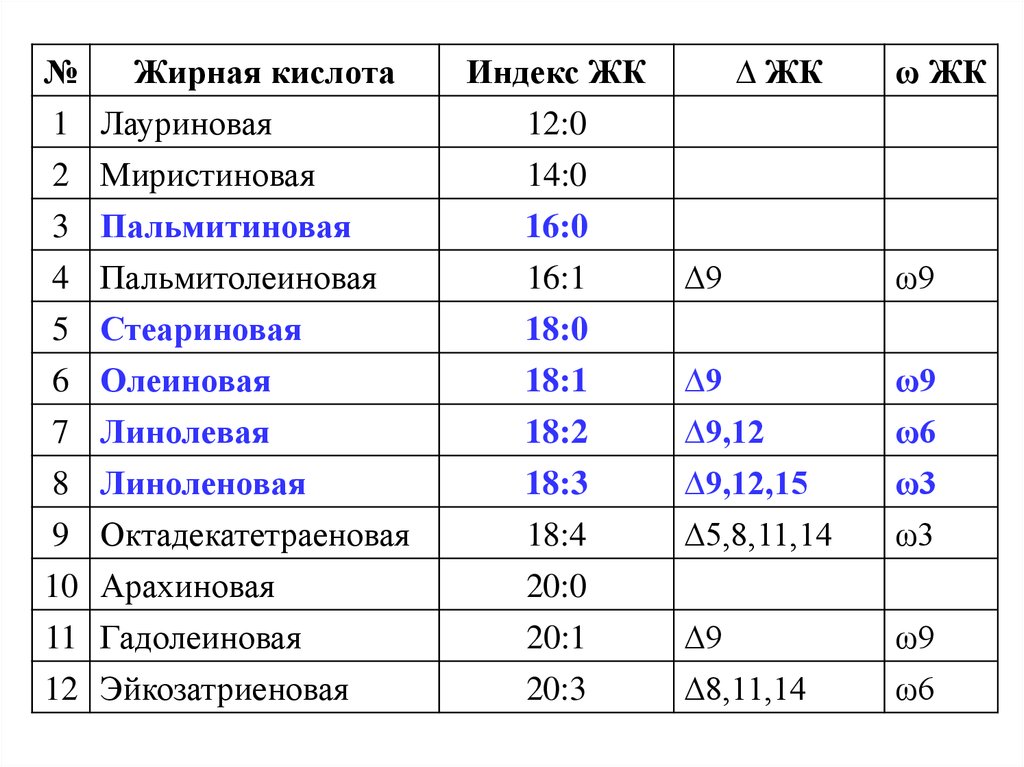
№Жирная кислота
1 Лауриновая
2 Миристиновая
Индекс ЖК
12:0
14:0
∆ ЖК
ω ЖК
3 Пальмитиновая
4 Пальмитолеиновая
5 Стеариновая
16:0
16:1
18:0
∆9
ω9
6 Олеиновая
18:1
∆9
ω9
7 Линолевая
8 Линоленовая
18:2
18:3
∆9,12
∆9,12,15
ω6
ω3
9 Октадекатетраеновая
10 Арахиновая
18:4
20:0
∆5,8,11,14
ω3
11 Гадолеиновая
12 Эйкозатриеновая
20:1
20:3
∆9
∆8,11,14
ω9
ω6
4.
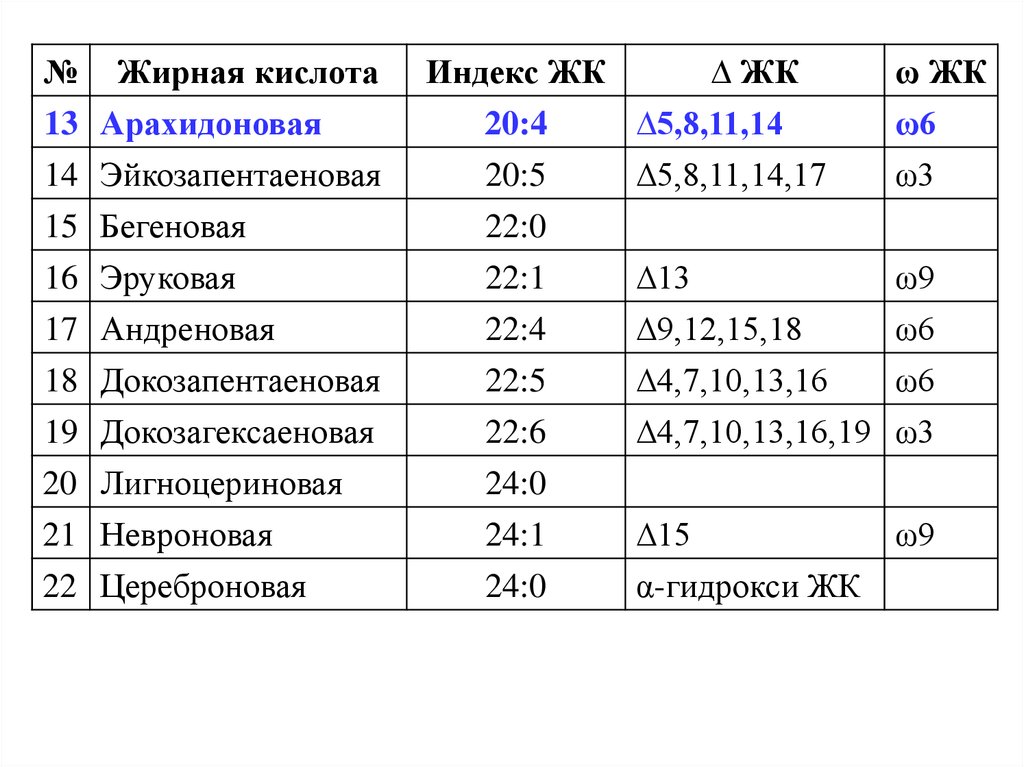
№ Жирная кислота13 Арахидоновая
14 Эйкозапентаеновая
Индекс ЖК
∆ ЖК
20:4
∆5,8,11,14
20:5
∆5,8,11,14,17
ω ЖК
ω6
ω3
15 Бегеновая
16 Эруковая
17 Андреновая
22:0
22:1
22:4
∆13
∆9,12,15,18
ω9
ω6
18 Докозапентаеновая
22:5
∆4,7,10,13,16
ω6
19 Докозагексаеновая
20 Лигноцериновая
22:6
24:0
∆4,7,10,13,16,19 ω3
21 Невроновая
22 Цереброновая
24:1
24:0
∆15
ω9
α-гидрокси ЖК
5. Биологическое значение ЖК
1.2.
3.
полиеновые ЖК (арахидоновая,
эйкозапентаеновая, эйкозатриеновая)
используются для синтеза БАВ – эйкозаноидов
(простагландинов, простациклинов, тромбоксанов,
лейкотриенов, липоксинов).
ЖК окисляются в аэробных условиях с
образованием АТФ;
ЖК являются структурным компонентом
омыляемых липидов: восков, глицеролипидов,
сфинголипидов, эфиров холестерина.
6. АНАБОЛИЗМ ЖИРНЫХ КИСЛОТ
• Источником ЖК в организме являются синтетическиепроцессы, омыляемые липиды и пища.
• ЖК, которые синтезируются в организме, называются
заменимыми. Значительная их часть образуется в
печени, в, меньшей степени — в жировой ткани и
лактирующей молочной железе.
• ЖК, которые не синтезируются в организме, но
необходимы для него называются незаменимыми.
Единственным источником незаменимых ЖК
является пища. Они образуют понятие витамин F
(линолевая, линоленовая и арахидоновая).
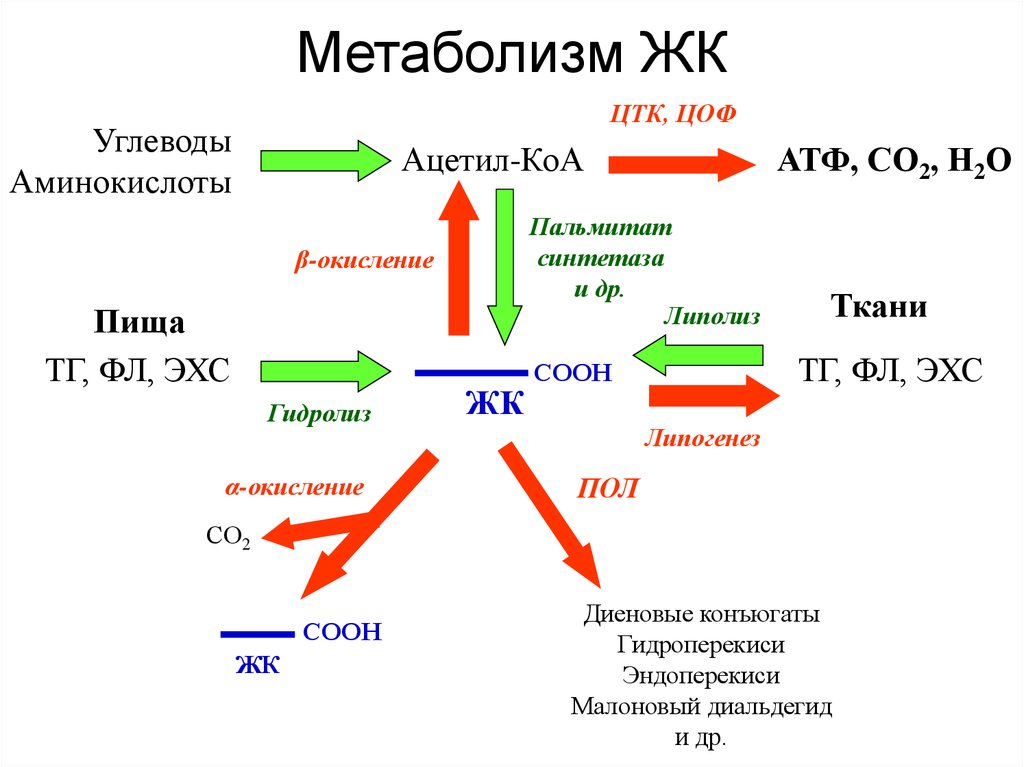
7. Метаболизм ЖК
ЦТК, ЦОФУглеводы
Аминокислоты
Ацетил-КоА
Пальмитат
синтетаза
и др.
Липолиз
β-окисление
Пища
ТГ, ФЛ, ЭХС
Гидролиз
α-окисление
АТФ, СО2, Н2О
ЖК
Ткани
ТГ, ФЛ, ЭХС
СООН
Липогенез
ПОЛ
СО2
СООН
ЖК
Диеновые конъюгаты
Гидроперекиси
Эндоперекиси
Малоновый диальдегид
и др.
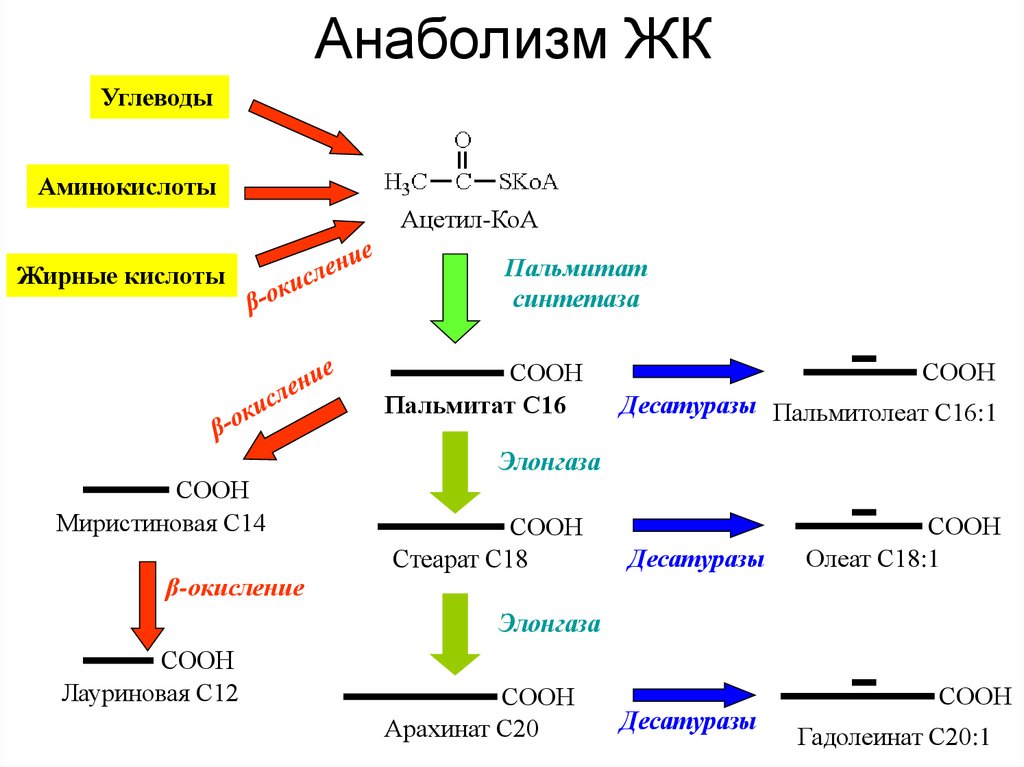
8. Анаболизм ЖК
УглеводыАминокислоты
Ацетил-КоА
Жирные кислоты
Пальмитат
синтетаза
СООН
Пальмитат С16
СООН
Миристиновая С14
β-окисление
СООН
Десатуразы Пальмитолеат С16:1
Элонгаза
СООН
Стеарат С18
Десатуразы
СООН
Олеат С18:1
Элонгаза
СООН
Лауриновая С12
СООН
Арахинат С20
Десатуразы
СООН
Гадолеинат С20:1
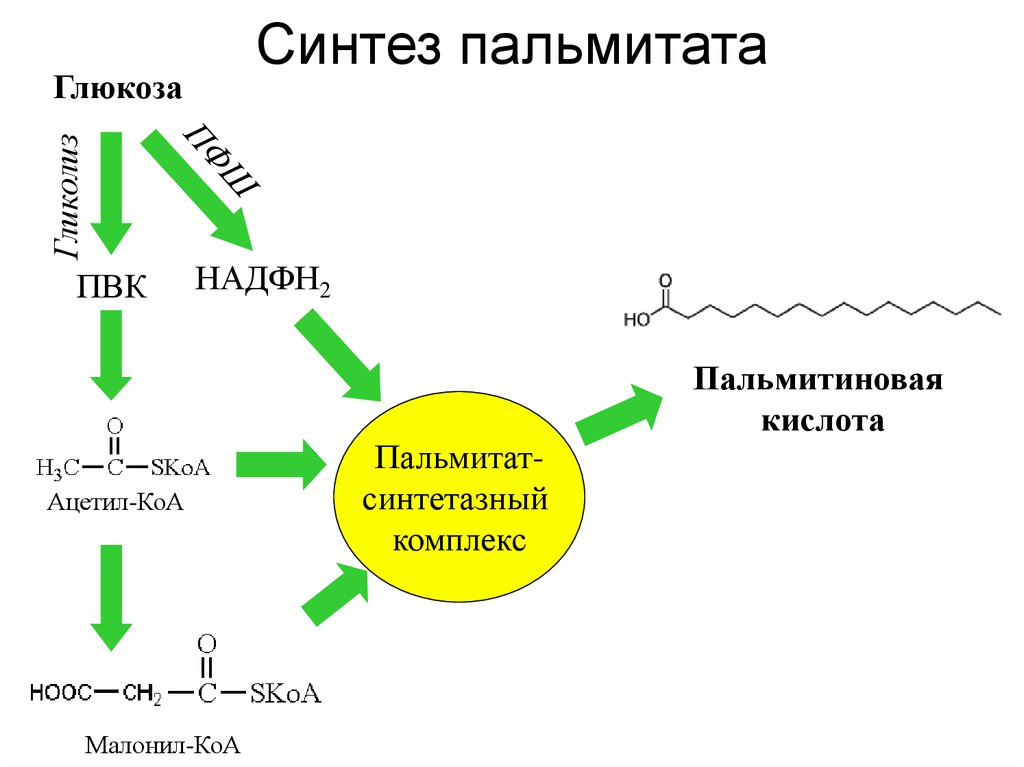
9. Синтез пальмитата
ГликолизГлюкоза
ПВК
НАДФН2
Ацетил-КоА
Малонил-КоА
Пальмитатсинтетазный
комплекс
Пальмитиновая
кислота
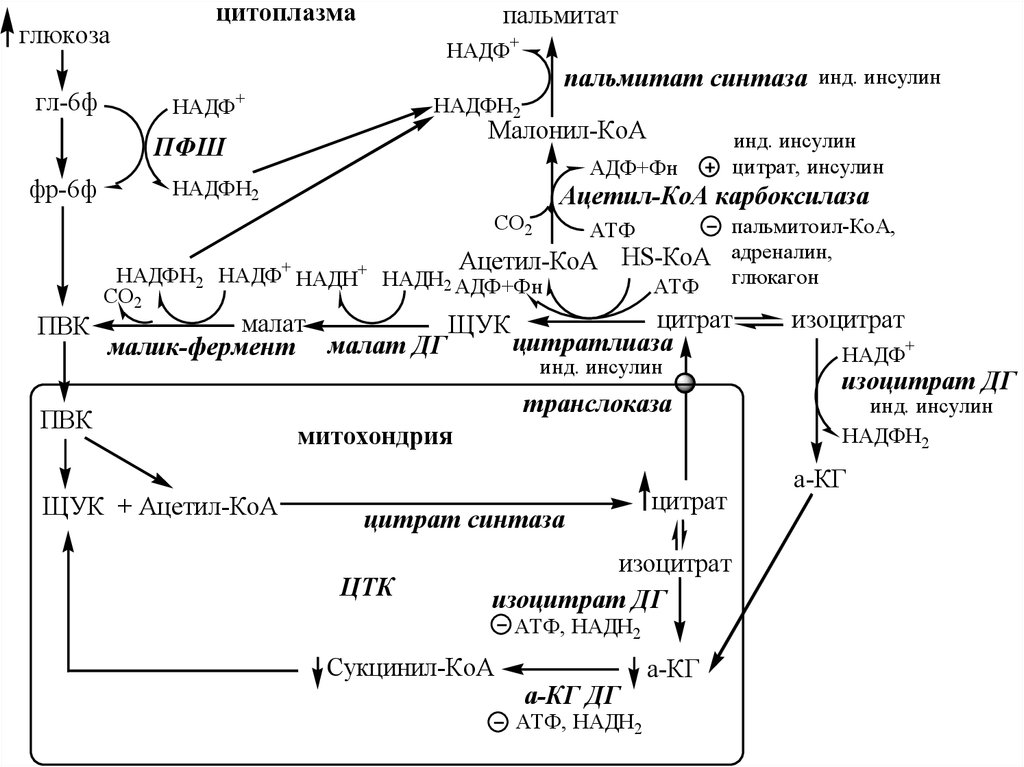
10.
глюкозагл-6ф
цитоплазма
пальмитат
НАДФ+
пальмитат синтаза инд. инсулин
НАДФ+
НАДФН2
Малонил-КоА
ПФШ
фр-6ф
АДФ+Фн
НАДФН2
Ацетил-КоА карбоксилаза
СО2
АТФ
Ацетил-КоА HS-КоА
ПВК
инд. инсулин
цитрат, инсулин
НАДФН2 НАДФ+ НАДН+ НАДН2
АДФ+Фн
СО2
АТФ
пальмитоил-КоА,
адреналин,
глюкагон
цитрат
малат
ЩУК
цитратлиаза
малик-фермент малат ДГ
инд. инсулин
ПВК
ЩУК + Ацетил-КоА
транслоказа
митохондрия
цитрат синтаза
ЦТК
цитрат
изоцитрат
изоцитрат ДГ
АТФ, НАДН2
Сукцинил-КоА
а-КГ ДГ
АТФ, НАДН2
а-КГ
изоцитрат
НАДФ+
изоцитрат ДГ
инд. инсулин
НАДФН2
а-КГ
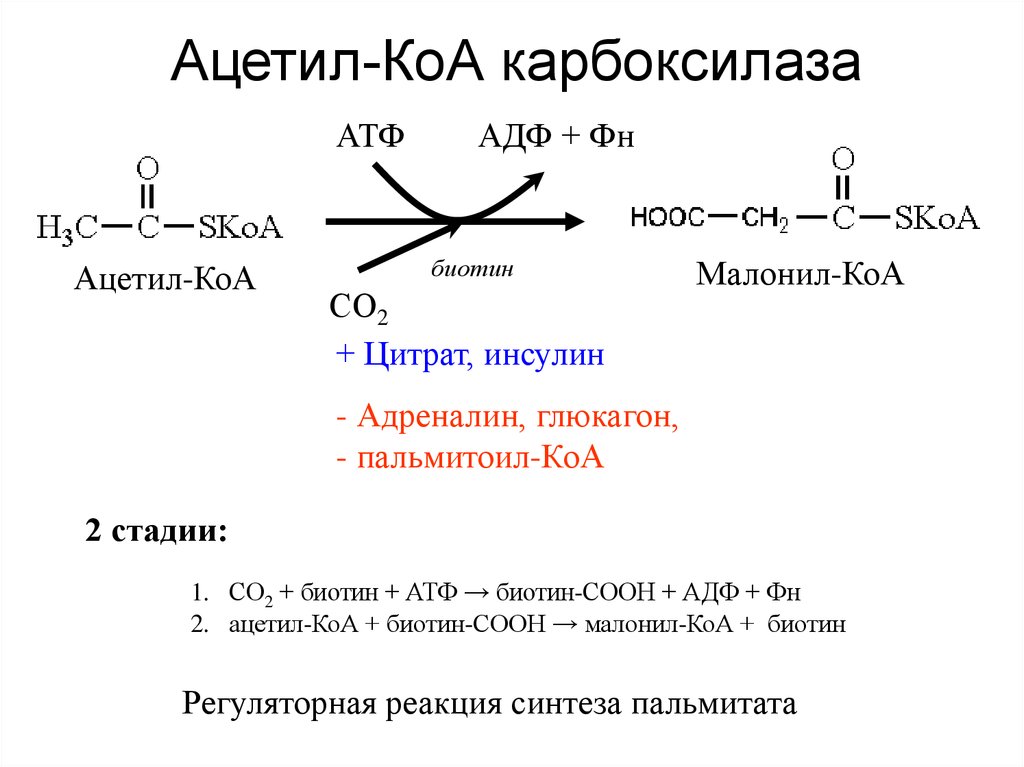
11. Ацетил-КоА карбоксилаза
АТФАцетил-КоА
АДФ + Фн
биотин
СО2
+ Цитрат, инсулин
Малонил-КоА
- Адреналин, глюкагон,
- пальмитоил-КоА
2 стадии:
1. СО2 + биотин + АТФ → биотин-СООН + АДФ + Фн
2. ацетил-КоА + биотин-СООН → малонил-КоА + биотин
Регуляторная реакция синтеза пальмитата
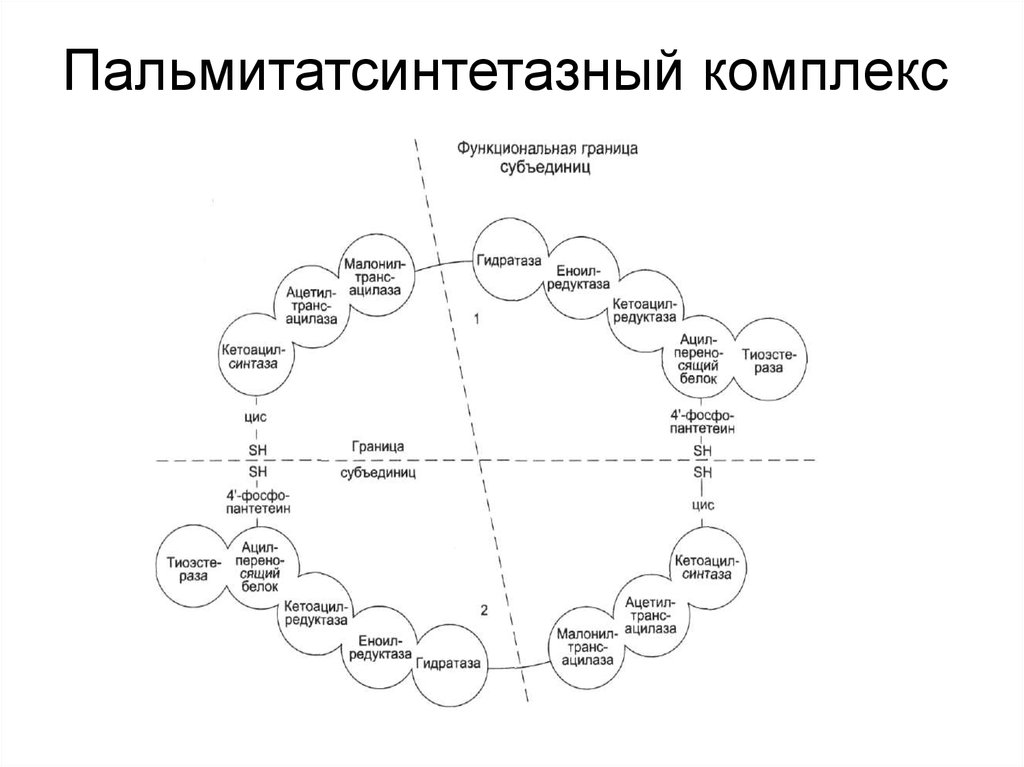
12. Пальмитатсинтетазный комплекс
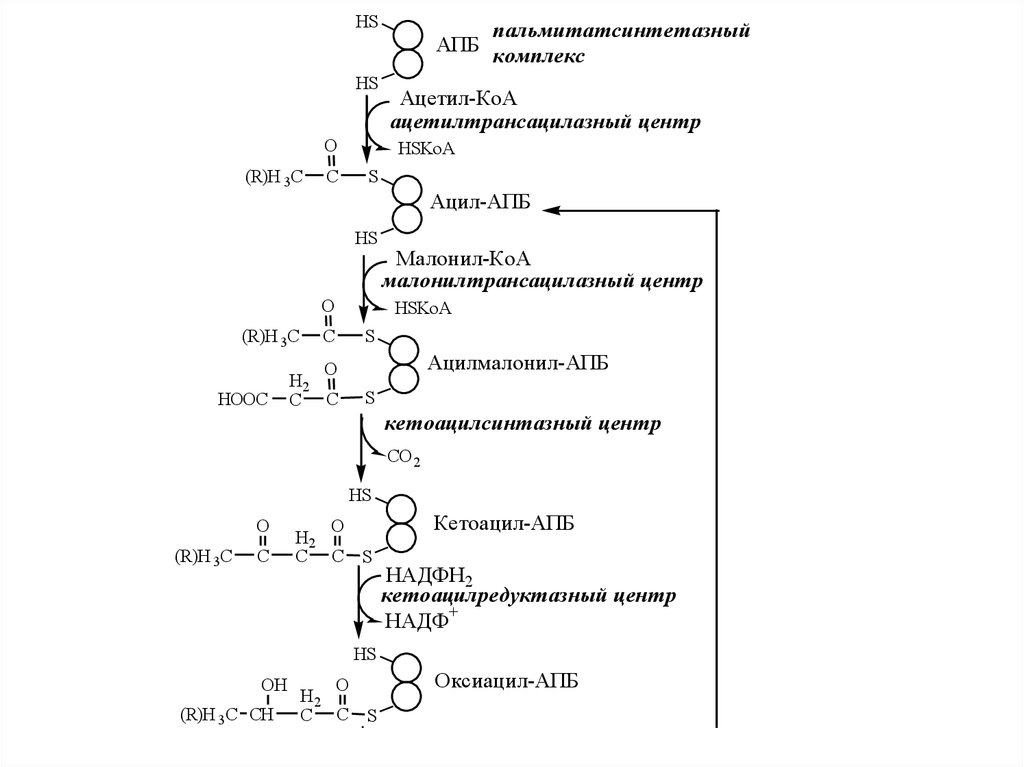
13.
HSАПБ
HS
O
(R)H 3C
C
Ацетил-КоА
ацетилтрансацилазный центр
НSKoA
S
Ацил-АПБ
HS
O
(R)H 3C
C
Малонил-КоА
малонилтрансацилазный центр
НSKoA
S
Ацилмалонил-АПБ
O
HOOC
пальмитатсинтетазный
комплекс
H2
C C
S
кетоацилсинтазный центр
СО 2
HS
О
(R)H 3C
C
Кетоацил-АПБ
O
H2
C C S
НАДФН2
кетоацилредуктазный центр
НАДФ+
HS
ОH
(R)H 3C CH
O
H2
C C S
Оксиацил-АПБ
гидратазный центр
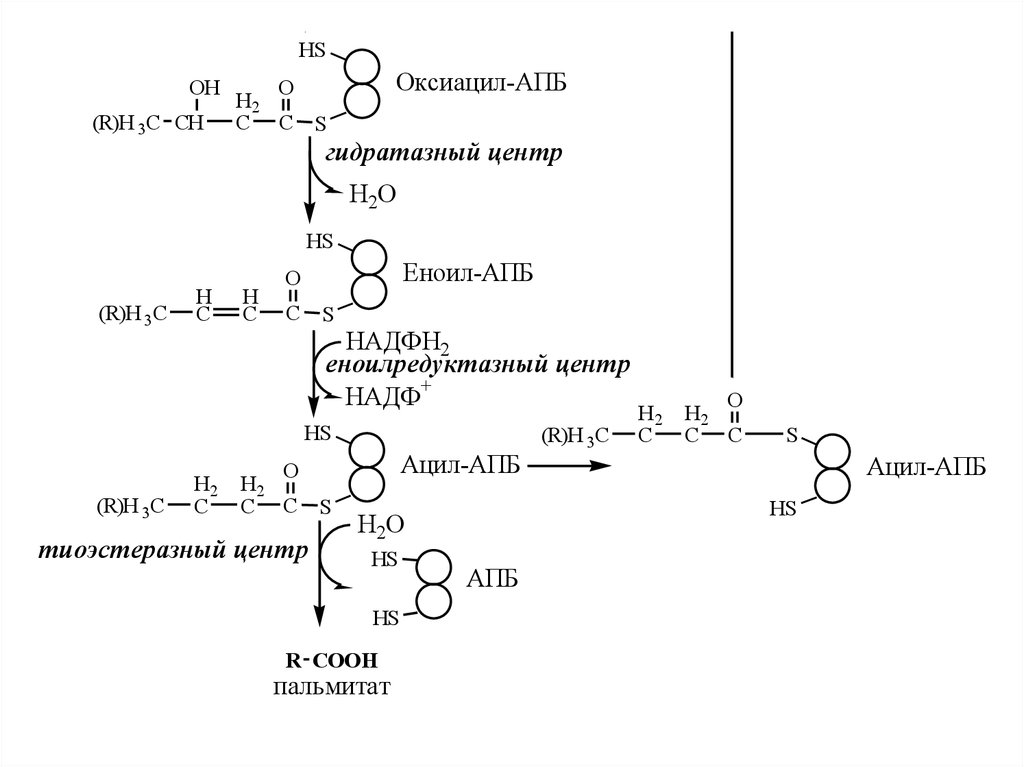
14.
НАДФ+HS
ОH
(R)H 3C CH
Оксиацил-АПБ
O
H2
C C S
гидратазный центр
Н2О
HS
(R)H 3C
H
C
H
C
Еноил-АПБ
O
C S
НАДФН2
еноилредуктазный центр
НАДФ+
HS
(R)H 3C
H2
C
O
H2
C C S
тиоэстеразный центр
Ацил-АПБ
HS
R CООН
пальмитат
O
H2
C C
S
Ацил-АПБ
HS
Н2О
HS
(R)H 3C
H2
C
АПБ
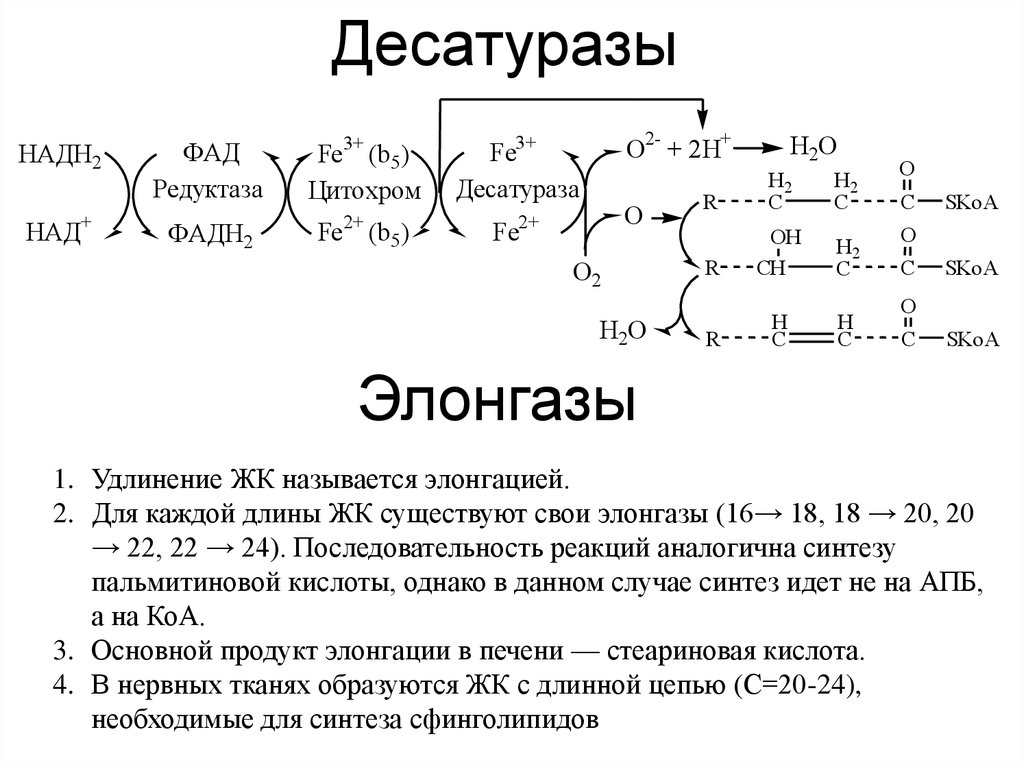
15. Десатуразы
НАДН2НАД+
ФАД
Редуктаза
Fe3+ (b5)
Цитохром
Fe3+
Десатураза
ФАДН2
Fe2+ (b5)
Fe2+
O2- + 2H+
O
O2
H2O
H2O
R
H2
C
H2
C
R
OH
CH
R
H
C
O
C
SKoA
H2
C
O
C
SKoA
H
C
O
C
SKoA
Элонгазы
1. Удлинение ЖК называется элонгацией.
2. Для каждой длины ЖК существуют свои элонгазы (16→ 18, 18 → 20, 20
→ 22, 22 → 24). Последовательность реакций аналогична синтезу
пальмитиновой кислоты, однако в данном случае синтез идет не на АПБ,
а на КоА.
3. Основной продукт элонгации в печени — стеариновая кислота.
4. В нервных тканях образуются ЖК с длинной цепью (С=20-24),
необходимые для синтеза сфинголипидов
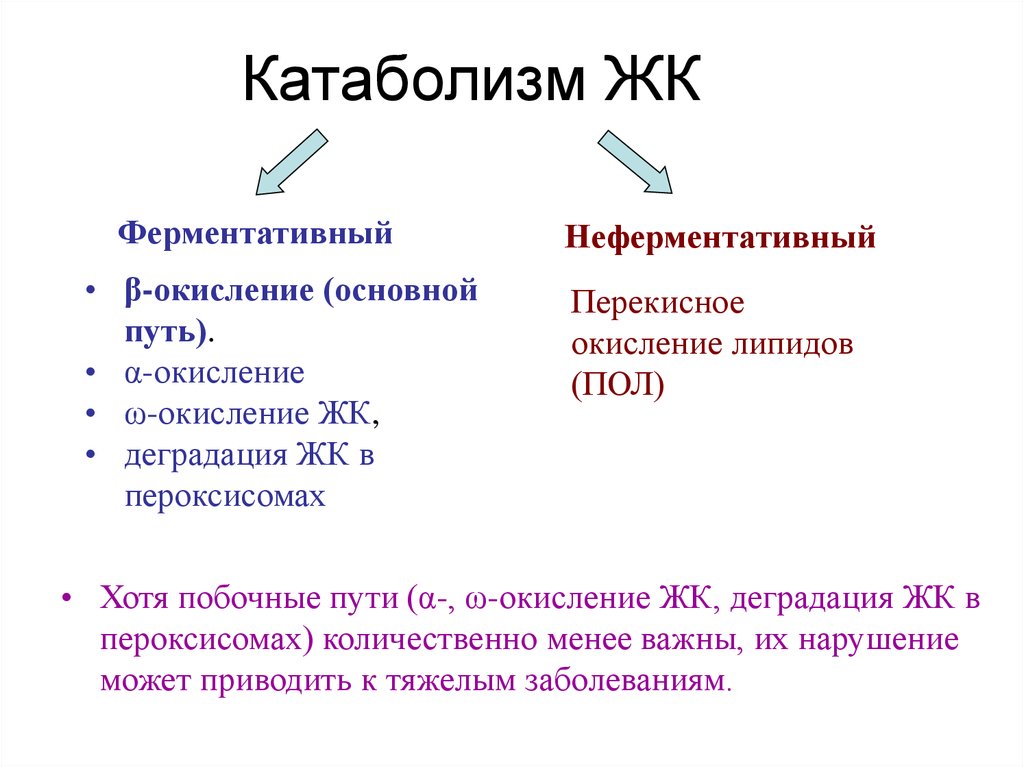
16. Катаболизм ЖК
Ферментативный• β-окисление (основной
путь).
• α-окисление
• ω-окисление ЖК,
• деградация ЖК в
пероксисомах
Неферментативный
Перекисное
окисление липидов
(ПОЛ)
• Хотя побочные пути (α-, ω-окисление ЖК, деградация ЖК в
пероксисомах) количественно менее важны, их нарушение
может приводить к тяжелым заболеваниям.
17.
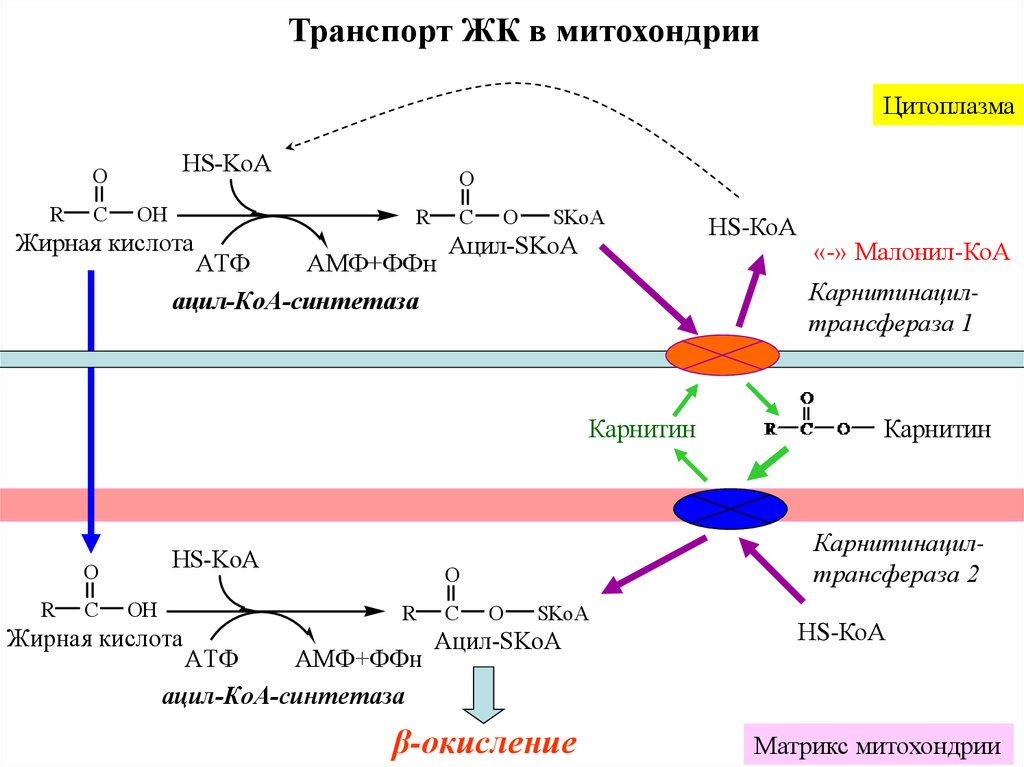
Транспорт ЖК в митохондрии• ЖК с короткой и средней цепью (от 4 до 12 атомов С) могут
проникать в матрикс митохондрий путём диффузии. Активация
этих ЖК происходит ацил-КоА синтетазами в матриксе
митохондрий.
• ЖК с длинной цепью, сначала активируются в цитозоле (ацилКоА синтетазами на внешней мембране митохондрий), а затем
переносятся в матрикс митохондрий специальной транспортной
системой с помощью карнитина.
•Карнитин поступает с пищей или
синтезируется из лизина и
метионина с участием витамина С.
L-карнитин
18.
Транспорт ЖК в митохондрииЦитоплазма
HS-KoA
O
R
C
OH
Жирная кислота
O
R
C
АТФ
АМФ+ФФн
ацил-КоА-синтетаза
O
SKoA
Ацил-SKoA
O
R
C
OH
Жирная кислота
АТФ
АМФ+ФФн
ацил-КоА-синтетаза
C
Карнитин
Карнитинацилтрансфераза 2
O
R
«-» Малонил-КоА
Карнитинацилтрансфераза 1
Карнитин
HS-KoA
НS-КоА
O
SKoA
Ацил-SKoA
β-окисление
НS-КоА
Матрикс митохондрии
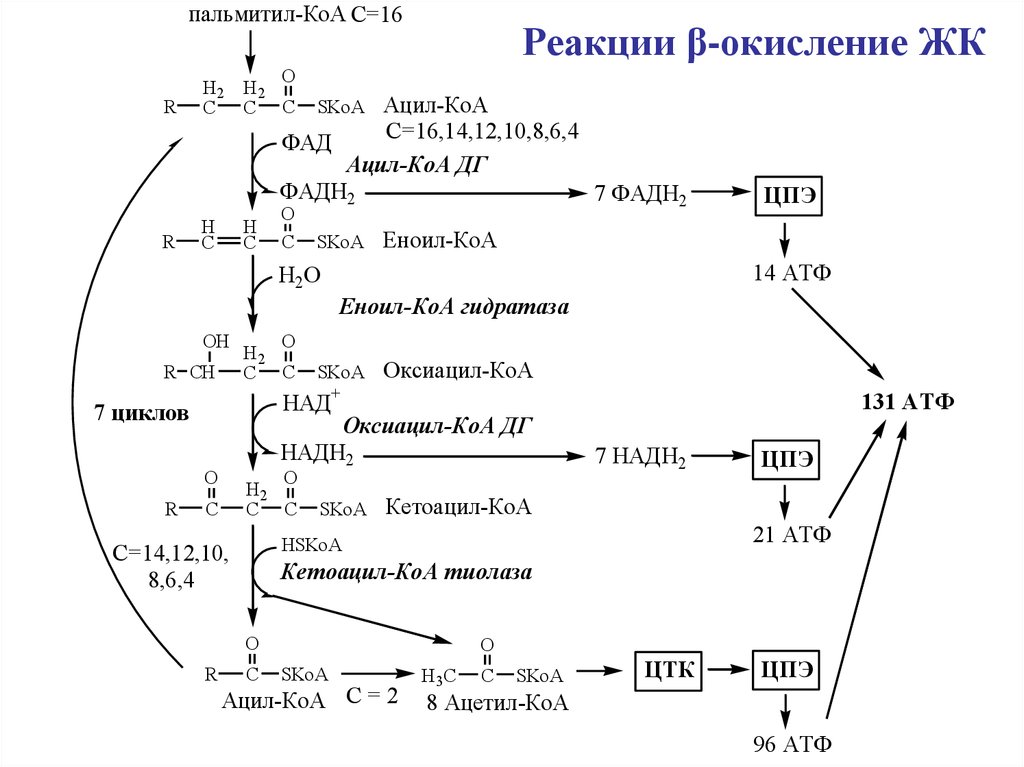
19.
пальмитил-КоА C=16R
H2
C
O
H2
C C
Реакции β-окисление ЖК
SKoA Ацил-КоА
C=16,14,12,10,8,6,4
Ацил-КоА ДГ
ФАДН2
7 ФАДН2
ФАД
R
H
C
H
C
O
C
ЦПЭ
SKoA Еноил-КоА
14 АТФ
Н2О
Еноил-КоА гидратаза
ОН
R CН
O
H2
C C
НАД+
7 циклов
Оксиацил-КоА ДГ
НАДН2
О
R
SKoA Оксиацил-КоА
O
H2
C C
C
7 НАДН2
ЦПЭ
SKoA Кетоацил-КоА
21 АТФ
НSKoA
C=14,12,10,
8,6,4
Кетоацил-КоА тиолаза
O
R
131 АТФ
C
O
SKoA
Ацил-КоА C = 2
H3C
C
SKoA
ЦТК
ЦПЭ
8 Ацетил-КоА
96 АТФ
20.
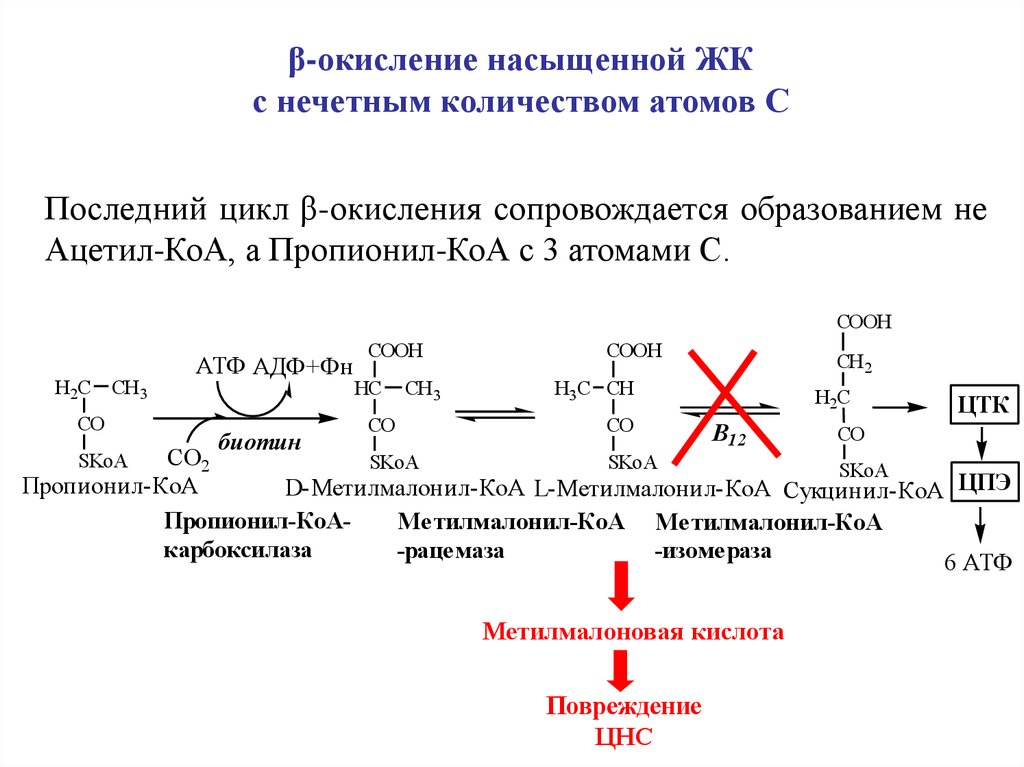
β-окисление насыщенной ЖКс нечетным количеством атомов С
Последний цикл β-окисления сопровождается образованием не
Ацетил-КоА, а Пропионил-КоА с 3 атомами С.
COOH
H2C
CH 3
CO
АТФ АДФ+Фн
биотин
COOH
HC
CO
CH 3
COOH
CH 2
H3C CH
CO
H2C
В12
CO
ЦТК
CO2
SKoA
SKoA
SKoA
Пропионил-КоА
D-Метилмалонил-КоА L-Метилмалонил-КоА Сукцинил-КоА ЦПЭ
Пропионил-КоАМетилмалонил-КоА Метилмалонил-КоА
карбоксилаза
-рацемаза
-изомераза
6 АТФ
SKoA
Метилмалоновая кислота
Повреждение
ЦНС
21. Регуляция
β-окисление активируют: глюкагон, адреналин, ЖК, НАД+,АДФ:
Голод, физическая нагрузка → ↑ глюкагон, ↑ адреналин →
липолиз ТГ в адипоцитах → ↑ ЖК в крови → ↑ β-окисление в
аэробных условиях в мышцах, печени → ↑АТФ;
↑АТФ, ↑НАДH2
↑Ацетил-КоА → ↑ цитрат, ↑ЖК → ↓ гликолиз → ↑ экономию
глюкозы для нервной ткани, эритроцитов и т.д.
β-окисление ингибируют: инсулин, НАДH2, АТФ.
Пища → ↑ инсулин → ↑ гликолиз → ↑ Ацетил-КоА → ↑ синтез
малонил-КоА и ЖК, ↑ малонил-КоА →
↓ карнитинацилтрансферазы I в печени → ↓ транспорт ЖК в
матрикс митохондрий → ↓ ЖК в матриксе → ↓ β-окисление
ЖК
22.
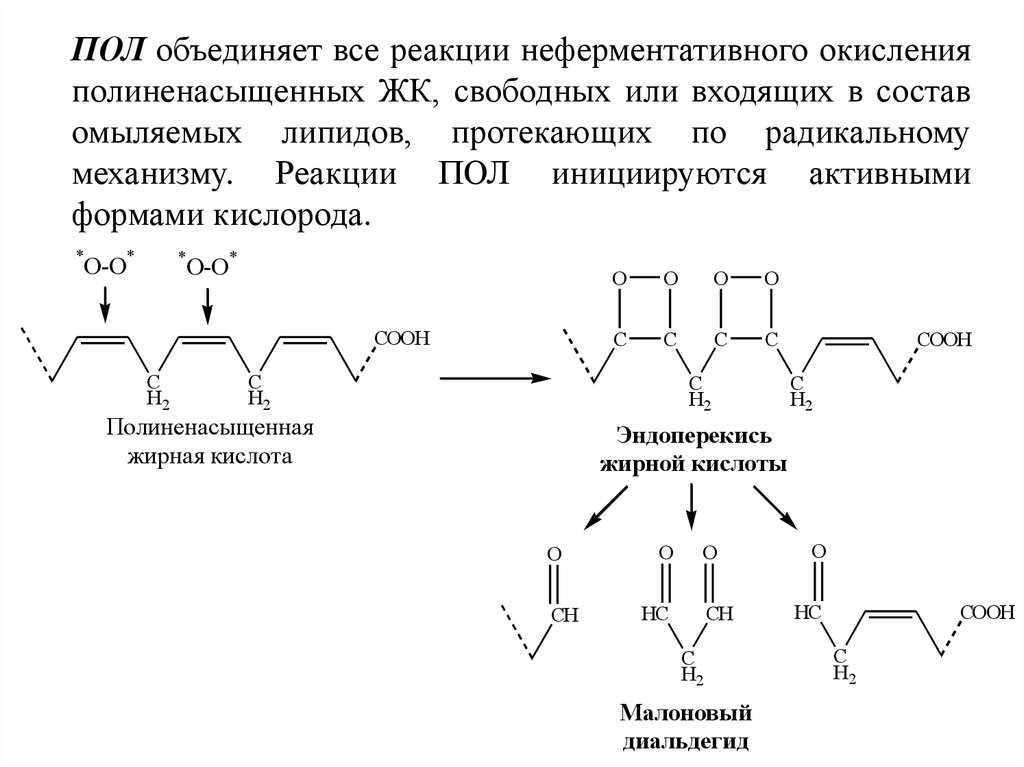
ПОЛ объединяет все реакции неферментативного окисленияполиненасыщенных ЖК, свободных или входящих в состав
омыляемых липидов, протекающих по радикальному
механизму. Реакции ПОЛ инициируются активными
формами кислорода.
*
O-O*
*
O-O*
СООН
C
H2
O
O
O
O
С
С
С
С
C
H2
C
H2
Полиненасыщенная
жирная кислота
СООН
C
H2
Эндоперекись
жирной кислоты
O
CH
O
O
HC
СH
C
H2
Малоновый
диальдегид
O
HС
СООН
C
H2
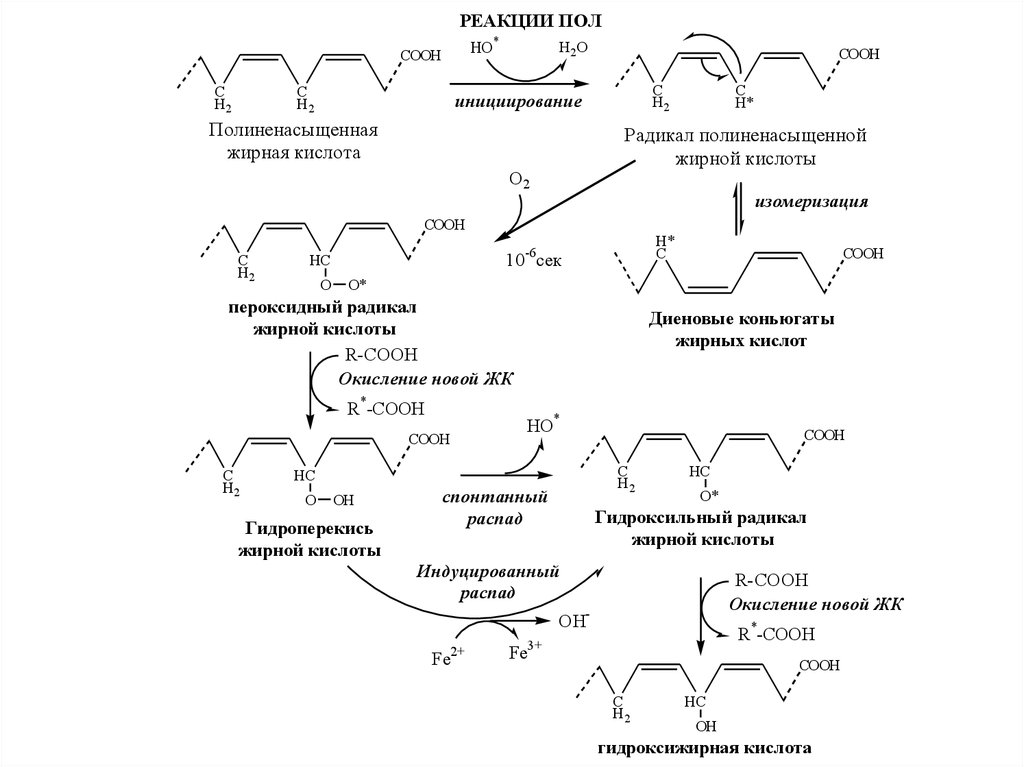
23.
РЕАКЦИИ ПОЛHО*
СООН
C
H2
C
H2
H2O
СООН
C
H2
инициирование
Полиненасыщенная
жирная кислота
Радикал полиненасыщенной
жирной кислоты
О2
изомеризация
СООН
C
H2
O
H*
C
10-6сек
HC
R*-COOH
СООН
Диеновые коньюгаты
жирных кислот
HO*
OH
Гидроперекись
жирной кислоты
СООН
C
H2
HC
O
COOH
O*
пероксидный радикал
жирной кислоты
R-COOH
Окисление новой ЖК
C
H2
C
H*
спонтанный
распад
HC
O*
Гидроксильный радикал
жирной кислоты
Индуцированный
распад
R-COOH
Окисление новой ЖК
OHFe2+
R*-COOH
Fe3+
СООН
C
H2
HC
OH
гидроксижирная кислота
24.
Регуляция ПОЛПроцессы ПОЛ усиливаются при избытке катехоламинов (стресс), гипоксии, ишемии
(при реоксигенации), повышенном содержании активных форм О2, снижении
антиоксидантной защиты, повышенном содержании ненасыщенных жирных
кислот.
Активация ПОЛ происходит при воспалении и характерна для многих заболеваний:
дистрофии мышц (болезнь Дюшенна), болезни Паркинсона, атеросклерозе,
развитии опухолей.
Физиологическое значение реакций ПОЛ:
1. модифицируют физико-химические свойства биомембран: увеличивают их
проницаемость.
2. регулируют активность мембранных ферментов, реакции окислительного
фосфорилирования.
3. участвуют в контроле клеточного деления.
4. Участвует в адаптации организма.
Повышение активности ПОЛ приводит к:
1. разрушению, фрагментации клеточных мембран, повреждению и гибели клеток.
2. модификации ЛП, особенно ЛПНП. Они становятся «липкими», легче проникают в
сосудистую стенку, хорошо захватываются макрофагами, что ускоряет развитие
атеросклероза.
3. накоплению продуктов ПОЛ, многие из которых токсичны, канцерогенены и
мутагенены (МДА).
4. ускорению процессов старения организма.
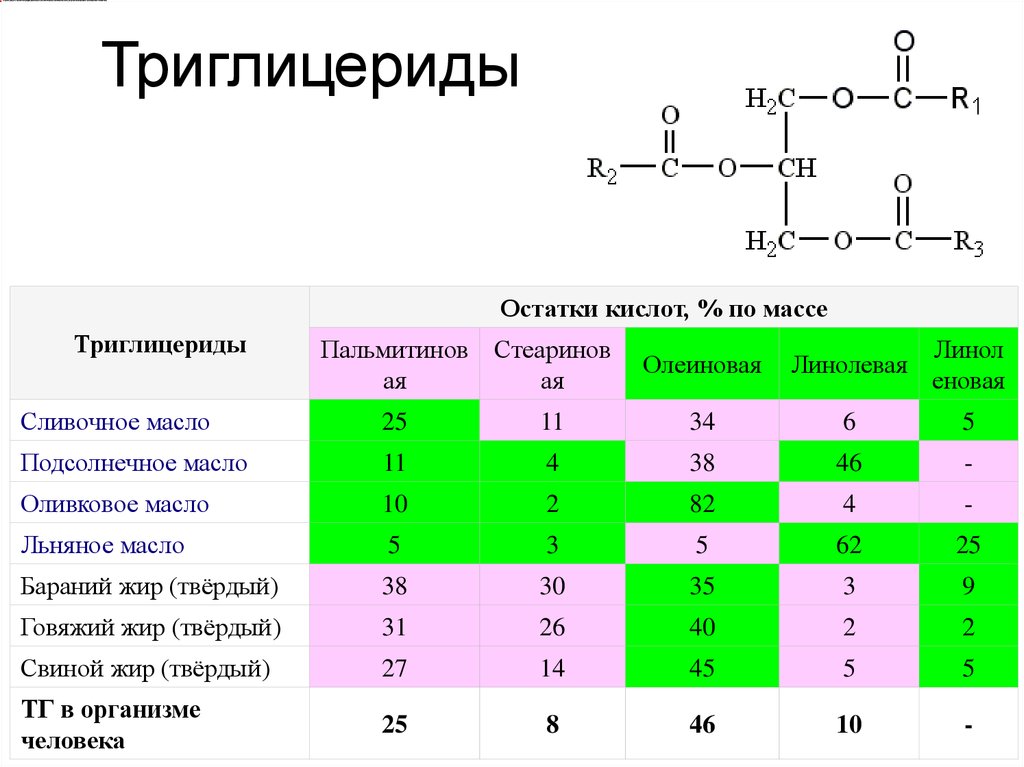
25. Триглицериды
Остатки кислот, % по массеТриглицериды
Пальмитинов Стеаринов
ая
ая
Олеиновая
Линолевая
Линол
еновая
Сливочное масло
25
11
34
6
5
Подсолнечное масло
11
4
38
46
-
Оливковое масло
10
2
82
4
-
Льняное масло
5
3
5
62
25
Бараний жир (твёрдый)
38
30
35
3
9
Говяжий жир (твёрдый)
31
26
40
2
2
Свиной жир (твёрдый)
27
14
45
5
5
ТГ в организме
человека
25
8
46
10
-
26. Жировая ткань
Жировая ткань – это разновидность соединительной ткани,составляет 15-20% веса мужчин и 20-25% веса женщин.
Как и любая ткань, она состоит из клеток (адипоциты,
макрофаги, тучные клетки и т.д.) и межклеточного вещества.
Межклеточное вещество в жировой ткани представлено
небольшим количеством волокон (коллагена и эластина) и
основного вещества (гликозаминогликаны, протеоликаны).
Белая жировая ткань
• Есть везде. Основные жировые
отложения имеются под кожей (в
подкожножировой клетчатке), и вокруг
внутренних органов, преимущественно в
области живота (висцеральный жир).
27. функции
Синтез липидов из углеводов
запасающая (95% ТГ в жировой ткани, 5% - во
внутренних органах и костях), накопление витаминов А,
Д, Е
теплоизоляционная;
механическая защита органов и тканей;
эндокринная (секреция: лептина, эстрогенов,
ангиотензиногена, интерлейкина-6, ФНО-α);
Антибактериальная защита (комплементарные
факторы: адипсин, комплемент С3, фактор В)
Регуляция воспаления (α1-кислый гликопротеин,
гаптоглобин)
пассивное обезвреживание (депонирование)
токсичных веществ
Участие в водно-солевом обмене
Обеспечивает поддержание гомеостаза
28. Химический состав
65-85% - ТГ,22% - вода,
5,8% белок,
15 ммоль/кг калий.
Из жирных кислот
42—51% - олеиновая (18:1),
22—31% пальмитиновая (16:0),
5—14% пальмитоолеиновая (16:1),
3—5 % миристиновая,
1—5 % линолевая
29. ОСОБЕННОСТИ МЕТАБОЛИЗМА АДИПОЦИТА БЕЛОЙ ЖИРОВОЙ ТКАНИ
• Энергетический обмен медленный, анаэробный,потребляет мало кислорода. Энергия АТФ тратится
на транспорт жирных кислот через клеточные
мембраны (с участием карнитина).
• Белковый обмен низкий, белки синтезируются
адипоцитами преимущественно для собственных
нужд. На экспорт синтезируются лептин, белки
острой фазы воспаления (α1-кислый гликопротеин,
гаптоглобин), компоненты системы комплимента
(адипсин, комплемент С3, фактор В), интерлейкины.
• Углеводный обмен. Невысокий, преобладает
катаболизм.
• Липидный обмен - интенсивно идут реакции
липолиза и липогенеза.
30. Бурая жировая ткань
• Мало у взрослого человека, много уноворожденного
• Локализована около почек и
щитовидной железы.
• Смешанная жировая ткань: между
лопатками, на грудной клетке и плечах.
31. Функция бурой жировой ткани
• термогенез• «взрывной» липолиз
32. ОСОБЕННОСТИ МЕТАБОЛИЗМА БУРОЙ ЖИРОВОЙ ТКАНИ
1. потребляет много кислорода2. активно окисляет глюкозу и жирные кислоты
3. энергетический обмен высокий (низкий синтез
АТФ, 2 реакции в гликолизе,1 в ц. Кребса), в
основном энергия в виде тепла
(несократительный термогенез)
4. разобщение в митохондриях белком
термогенином (РБ-1) процессов окисления и
фосфорилирования
5. Характерен феномен «взрывного липолиза»
6. Термогенез активируется при переохлаждении,
излишке липидов в крови, под действием
лептина.
33. Липогенез – синтез липидов
34.
1. Моноацилглицероловый путь синтеза ТГ и ФЛТолько в энтероцитах
HS-KoA
O
R
C
OH
Жирная кислота
O
R
АТФ
АМФ+ФФн
ацил-КоА-синтетаза
C
O
SKoA
Ацил-SKoA
Ацилтрансфераза
2-МГ + Ацил~КоА → 1,2-ДГ + HS-КоА,
1,2-ДГ + Ацил~КоА → ТГ + HS-КоА
1,2-ДГ + ЦДФ-холин → лецитин + ЦМФ
1,2-ДГ + ЦДФ-этаноламин → кефалин + ЦМФ
В клетках слизистой оболочки тонкой кишки синтезируются в основном
видоспецифичные ТГ. Однако при поступлении с пищей ТГ с необычными жирными
кислотами, например бараньего жира, в адипоцитах появляются ТГ, содержащие
кислоты, характерные для бараньего жира (насыщенные разветвлённые жирные
кислоты).
35.
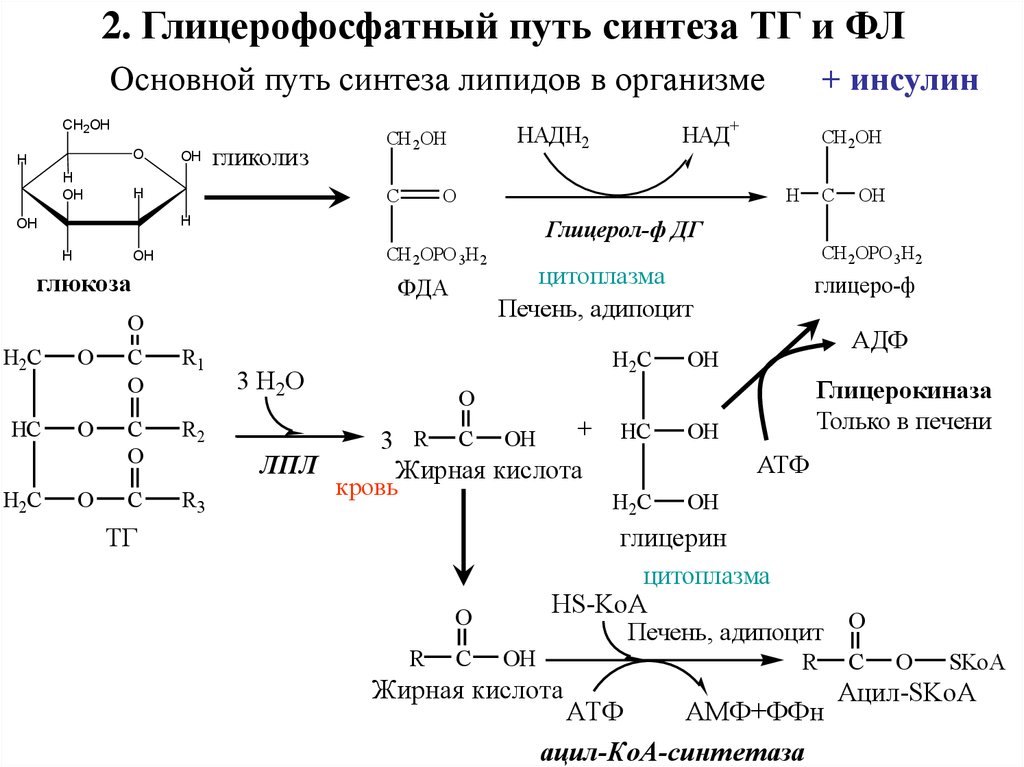
2. Глицерофосфатный путь синтеза ТГ и ФЛОсновной путь синтеза липидов в организме
CH2OH
O
H
H
OH
OH
гликолиз
С
H
H
CH 2OPO 3H2
OH
ФДА
O
HC
H2C
O
O
O
С
O
R1
С
O
R2
С
R3
С
Глицерол-ф ДГ
глюкоза
H2C
CH 2OH
H
O
H
OH
НАД+
НАДН2
CH 2OH
+ инсулин
3 Н2О
CH 2OPO 3H2
цитоплазма
Печень, адипоцит
H2C
OH
HC
OH
глицеро-ф
АДФ
Глицерокиназа
Только в печени
O
+
3 R C OH
ЛПЛ
Жирная кислота
кровь
ТГ
C
АТФ
H2C
OH
глицерин
цитоплазма
HS-KoA
Печень, адипоцит O
O
R
OH
OH
Жирная кислота
R
АТФ
АМФ+ФФн
ацил-КоА-синтетаза
C
O
SKoA
Ацил-SKoA
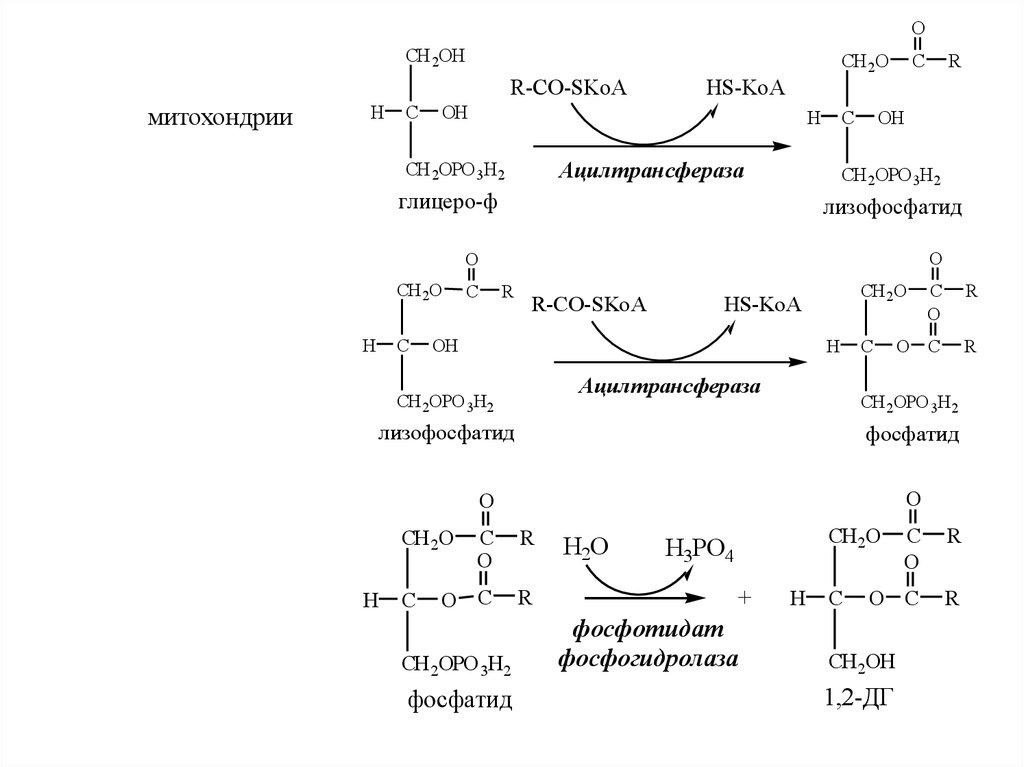
36.
OCH 2OH
R-CO-SKoA
митохондрии
H
С
CH 2O
HS-KoA
OH
H
С
Ацилтрансфераза
CH 2OPO 3H2
C
OH
CH 2OPO 3H2
глицеро-ф
лизофосфатид
O
O
CH 2O
H
С
C
R
R-CO-SKoA
CH 2O
HS-KoA
OH
H
Ацилтрансфераза
CH 2OPO 3H2
С
С
R
O C
R
фосфатид
O C
R
O
C
O
CH 2OPO 3H2
R
фосфатид
O
H
C
O
CH 2OPO 3H2
лизофосфатид
CH 2O
R
Н2О
CH 2O
Н3РО4
+
фосфотидат
фосфогидролаза
H
С
C
O
R
O C
R
CH 2OH
1,2-ДГ
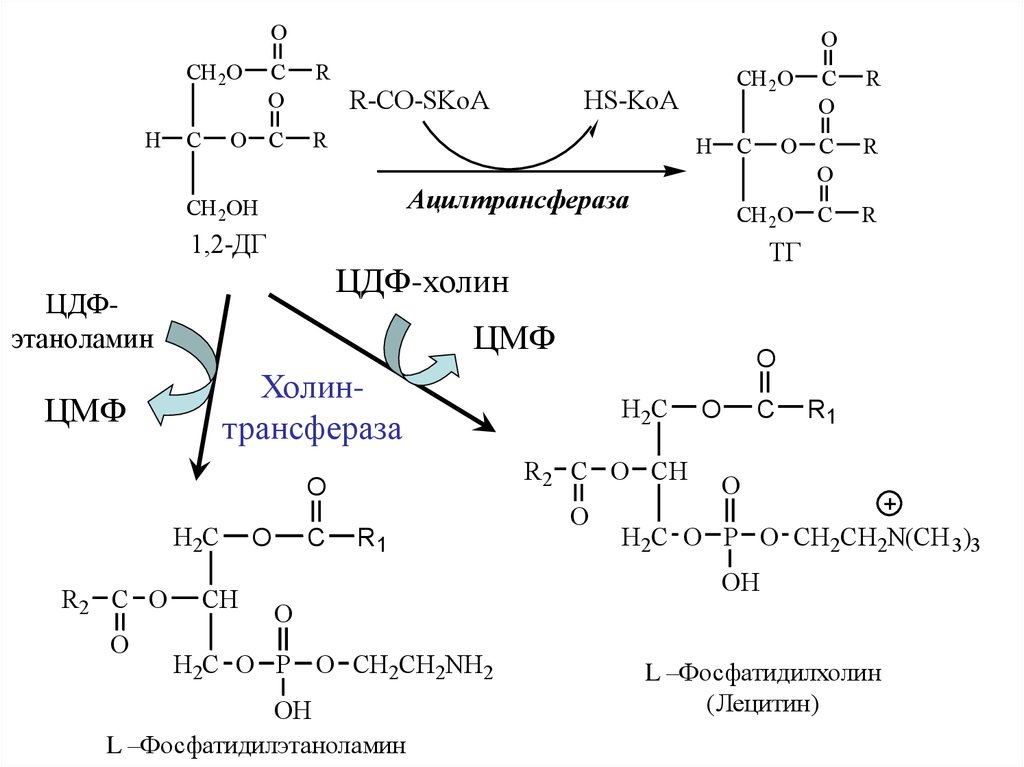
37.
OCH 2O
H
C
O
C
O
R
O C
R
R-CO-SKoA
CH 2O
HS-KoA
H
Ацилтрансфераза
CH 2OH
ЦМФ
H2C
O
CH
O
C
H2 C
R2 C O CH
O
R1
R
C
R
O
Холинтрансфераза
ЦМФ
O C
O
ТГ
ЦДФ-холин
ЦДФэтаноламин
R
CH 2O
1,2-ДГ
R2 C O
C
C
O
O
O
C
R1
O
H2C O P O CH2CH2N(CH 3)3
OH
O
H2C O P O CH2CH2NH2
OH
L –Фосфатидилэтаноламин
L –Фосфатидилхолин
(Лецитин)
38. Липолиз – распад липидов
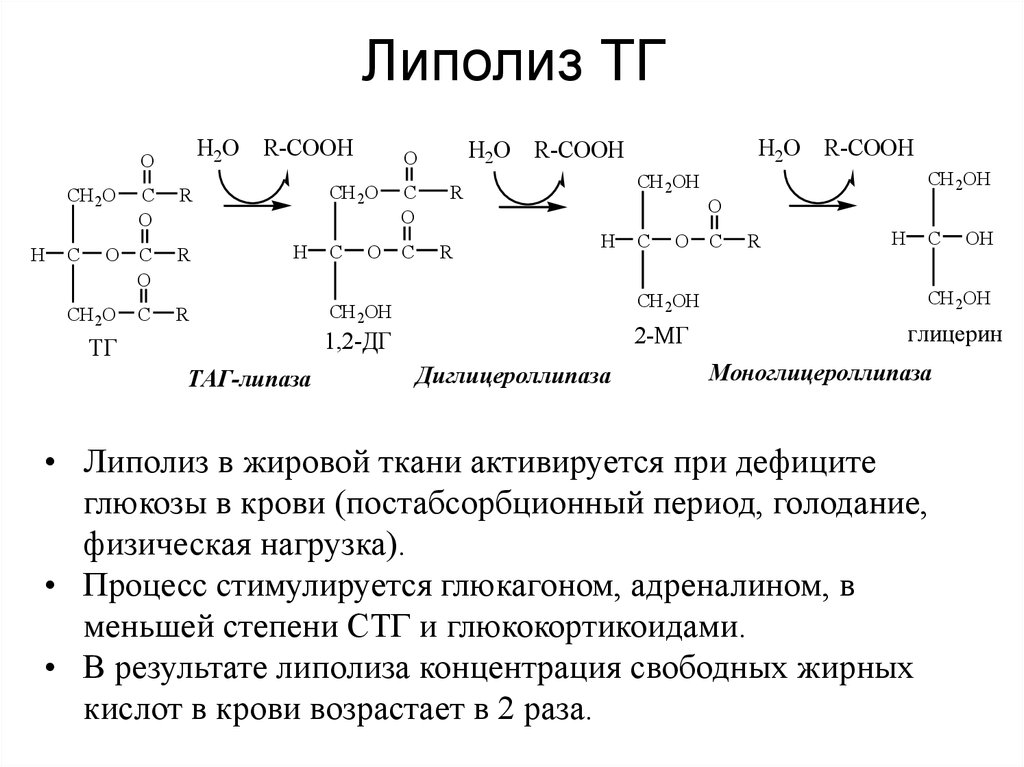
39. Липолиз ТГ
Н2О R-COOHO
CH 2O
H
C
C
O
R
O C
O
R
CH 2O
C
CH 2O
H
R
C
C
O
O C
CH 2OH
R
R
H
ТАГ-липаза
C
2-МГ
Диглицероллипаза
CH 2OH
O
O C
CH 2OH
CH 2OH
1,2-ДГ
ТГ
Н2О R-COOH
Н2О R-COOH
O
R
H
C
OH
CH 2OH
глицерин
Моноглицероллипаза
• Липолиз в жировой ткани активируется при дефиците
глюкозы в крови (постабсорбционный период, голодание,
физическая нагрузка).
• Процесс стимулируется глюкагоном, адреналином, в
меньшей степени СТГ и глюкокортикоидами.
• В результате липолиза концентрация свободных жирных
кислот в крови возрастает в 2 раза.
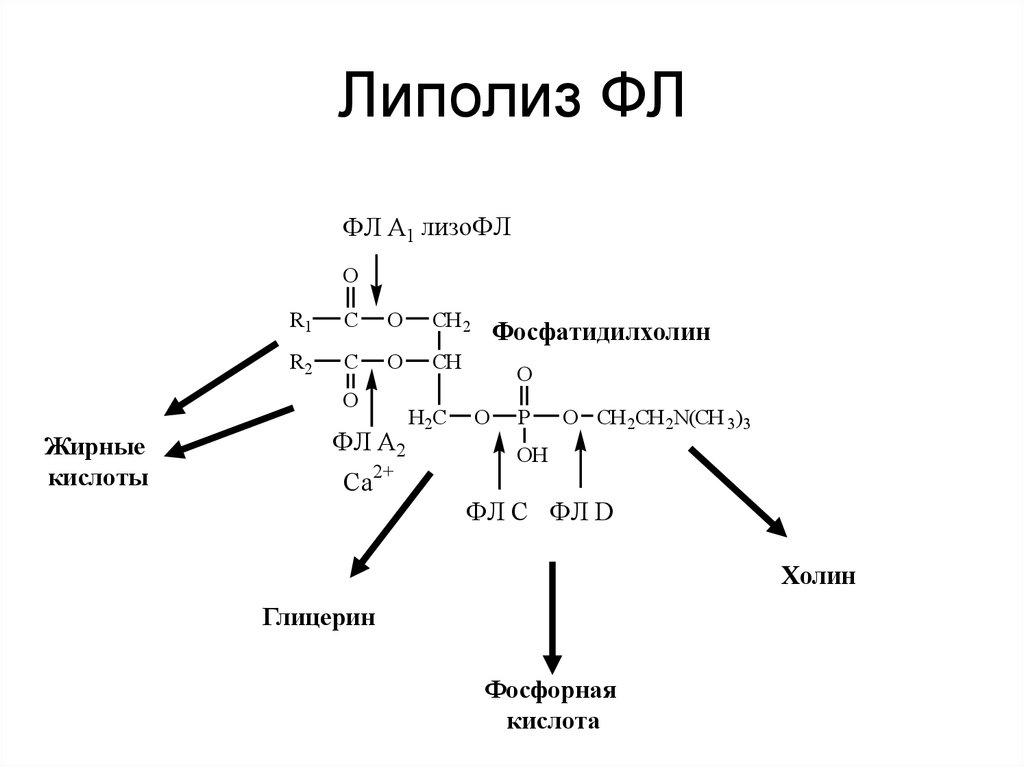
40. Липолиз ФЛ
ФЛ А1 лизоФЛO
R1
C
O
CH 2
R2
C
O
CH
O
Жирные
кислоты
ФЛ А2
2+
H2C
Фосфатидилхолин
O
O
P
O CH 2CH 2N(CH 3)3
OH
Ca
ФЛ C ФЛ D
Холин
Глицерин
Фосфорная
кислота
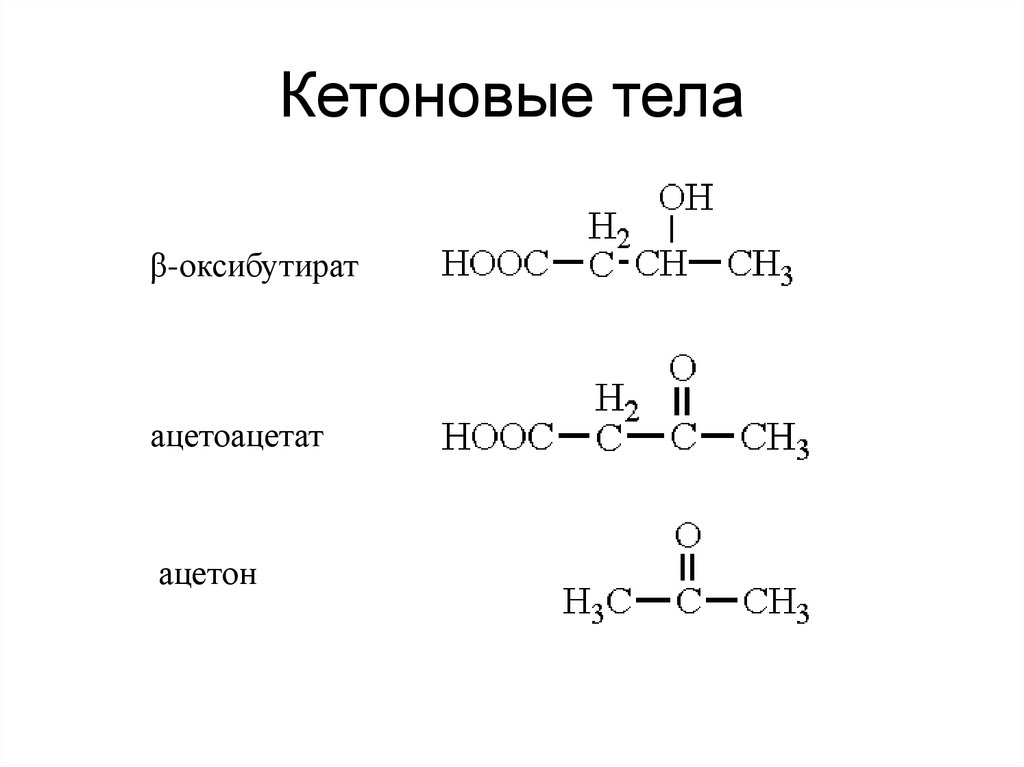
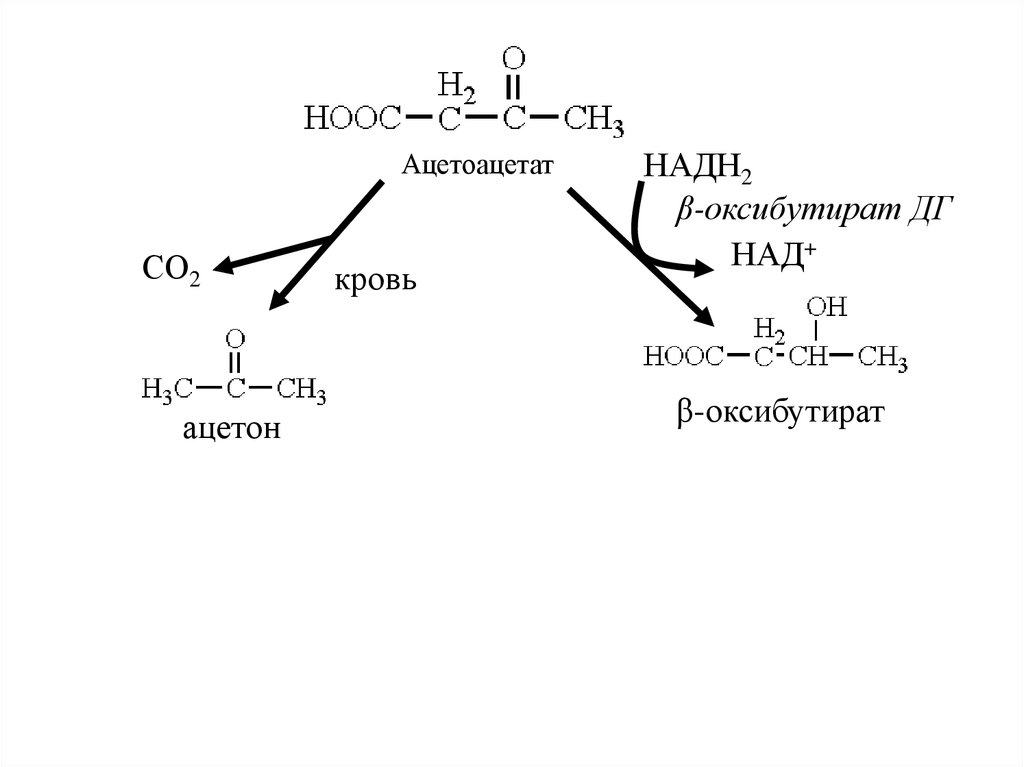
41. Кетоновые тела
β-оксибутиратацетоацетат
ацетон
42. Биологическое значение КТ
1. КТ - топливные молекулы, окисление β-гидроксибутирата доСО2 и Н2О обеспечивает синтез 26 АТФ. Окисление КТ, как и
ЖК сберегает глюкозу, что имеет большое значение в
энергоснабжении аэробных тканей при голодании и
физических нагрузках, когда возникает дефицит глюкозы.
2. Для нервной ткани КТ имеют исключительное значение, так
как в отличие от мышц и почек, нервная ткань практически не
использует ЖК в качестве источника энергии (ЖК не проходят
гематоэнцефалический барьер).
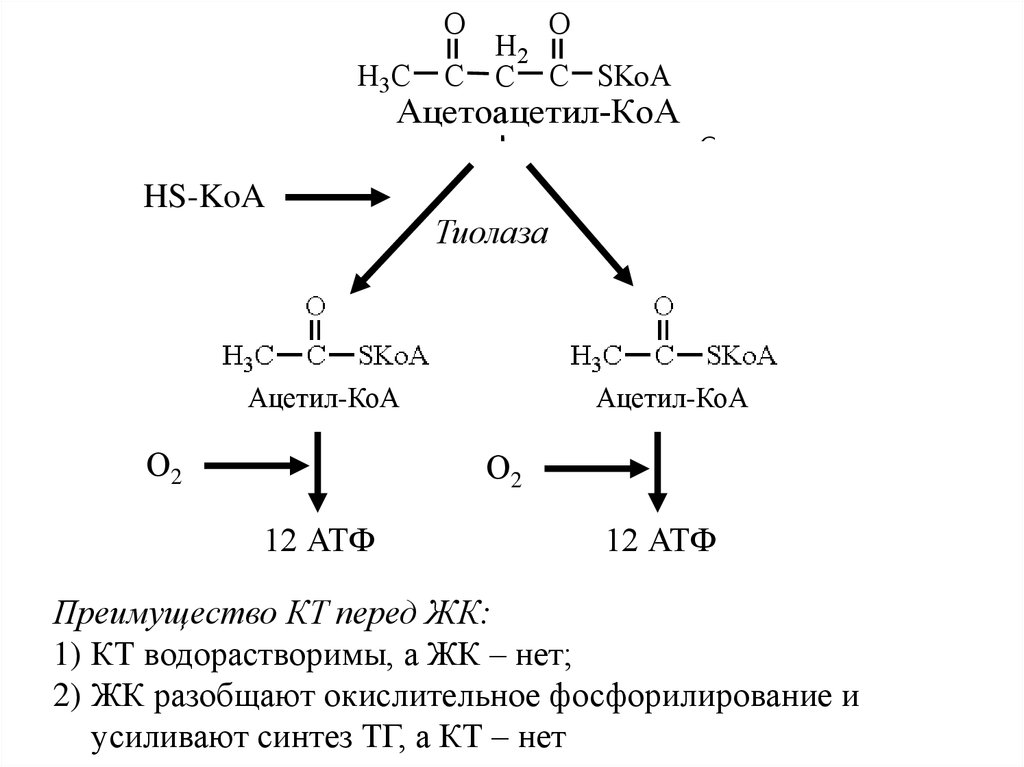
3. Преимущество КТ перед ЖК:
1) КТ водорастворимы, а ЖК – нет;
2) ЖК разобщают окислительное фосфорилирование и
усиливают синтез ТГ, а КТ – нет.
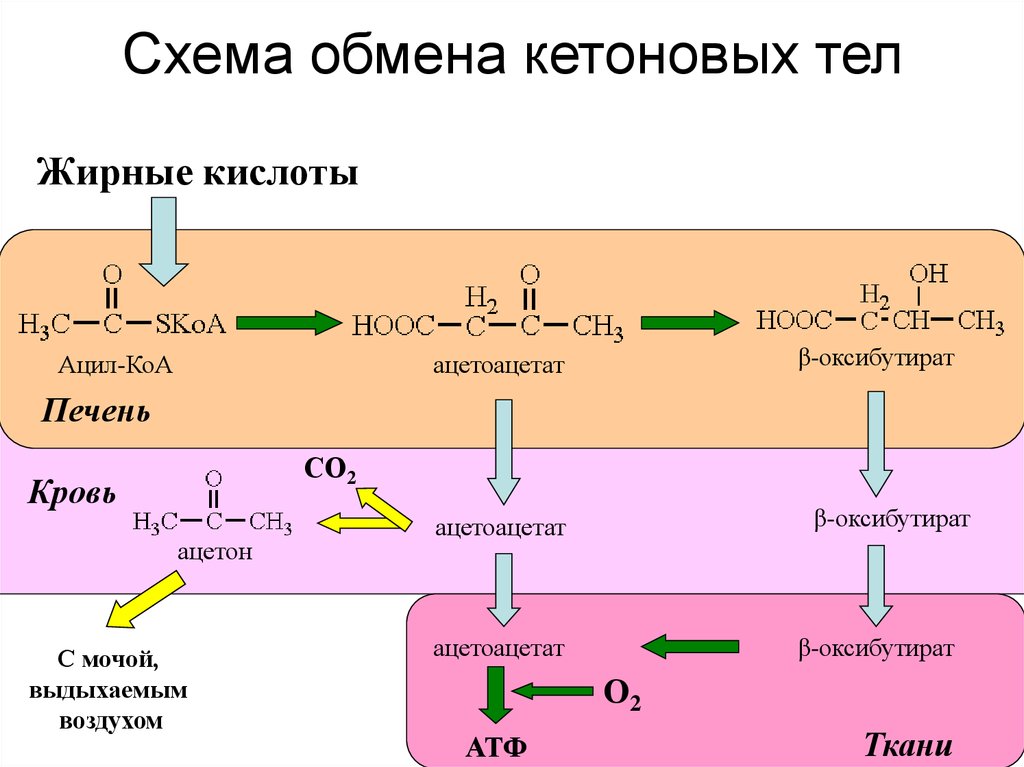
43. Схема обмена кетоновых тел
Жирные кислотыАцил-КоА
β-оксибутират
ацетоацетат
Печень
СО2
Кровь
ацетон
С мочой,
выдыхаемым
воздухом
β-оксибутират
ацетоацетат
ацетоацетат
β-оксибутират
О2
АТФ
Ткани
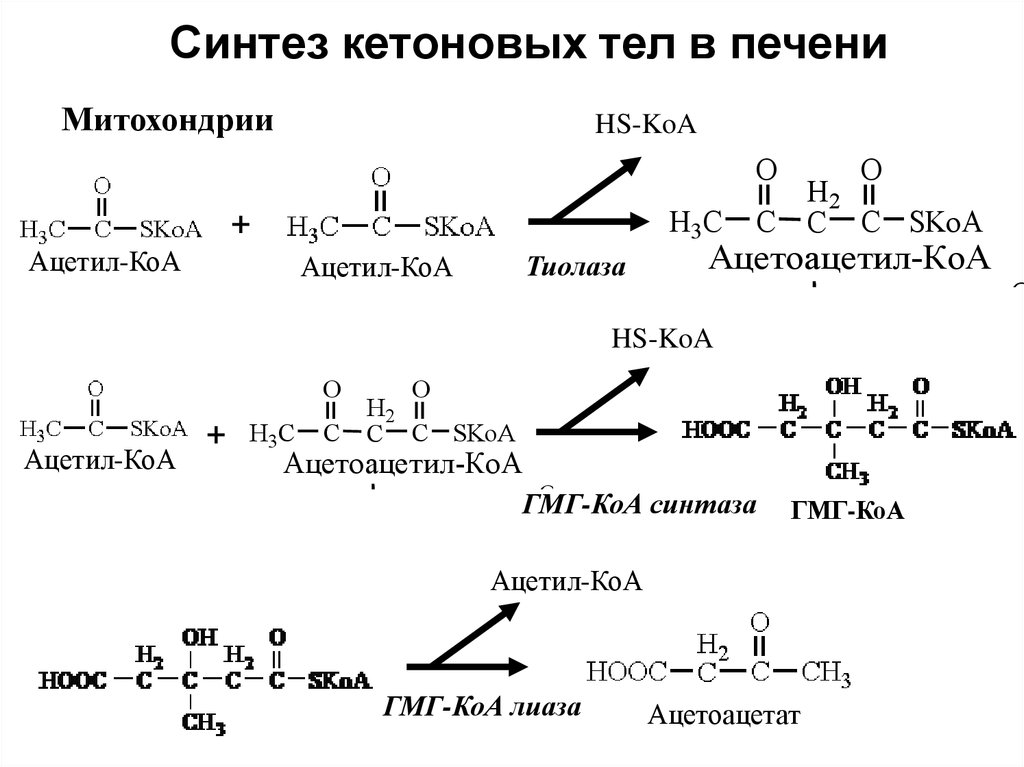
44. Синтез кетоновых тел в печени
глюкагонH3Cтел
C в
SKoA
Синтез кетоновых
печени
тиолаза
Ацетил-КоА
Ацетил-КоА
глюкагон
Митохондрии
HS-KoA
НАДН2
O
Печень
O
К
H3C b-окисление
C SKoA
+
ировая
Ацетил-КоА
O
глюкагон
+
Ацетил-КоА
НАД
Ацетил-КоА
кань
H3C C SKoA
тиолаза
л-КоА
Ацетил-КоА
лицеринглюкагон
ЖК
-окисление
юкагон
+
Ацетил-КоА
НАД
O
C
+
H3C
O
ЖК
H2
C
O
ХС
HS-KoA инд. ЖК
етон
неферH2
ХС
мента- HOOC C
глюкагон
тивно
O
H3C
инд. ЖК
C
O
Ацети
OH
O
C SKoA
CH 3
ГМГ-КоА
ГМГ-КоА лиаза
H2
C C SKoA
ГМГ-КоА лиаза
CH 3
C
H2
O
ГМГ-КоА
синтазаH2 ГМГ-КоА
HOOC C C C C SKoA
глюкагон
Ацетил-КоА
Ацетил-КоА
OH
H3C
ГМГ-КоА синтаза
Ацетоацетил-КоА
HS-KoA
CH 3 ГМГ-КоА синтаза
H2
C C SKoA
HS-KoA
HS-KoA
C SKoAHS-KoA
C
C
O
Ацетоацетил-КоА
Тиолаза
HS-KoA
НАДН2
H3C
HS-KoA
Ацетоацетат
O
H3C
C
Ацетил
45.
АцетоацетатСО2
ацетон
кровь
НАДН2
β-оксибутират ДГ
НАД+
β-оксибутират
46.
ровьКатаболизм кетоновых тел
3АТФ
НАД+
НАДН2
O
Печень
ЦТК
β-оксибутират ДГ
HАцетоацетат
β-оксибутират
3C C SKoA
Ацетил-КоА
O
глюкагон
ЦТК H3C C SKoA
тиолаза
АТФ
АДФ + Фн
Ацетил-КоА
Ацетил-КоА
глюкагон
HS-KoA
Сукцинил-КоА Сукцинат
НАДН2
O
O
b-окисление
H2
C C SKoA
H3C C
ировая
+
Ацетоацетил-КоА
НАД
Ацетоацетат
кань
O
лицерин Сукцинил-КоА-ацетоацетат-КоА-трансфераза
H3C C
HS-KoA
47.
НАДН2O
b-окисление
H3C
НАД+
C
O
H2
C C SKoA
Ацетоацетил-КоА
O
HS-KoA
Тиолаза
ГМГ-КоА синтаза
HS-KoA
ЖК
HS-KoA инд. ЖК
ХС
HOOC
Ацетил-КоА
глюкагон
OH
H2
C C
H3C
C SKoA
Ацетил-КоА
O
H2
C C SKoA
Ацетил-КоА
CH 3
ГМГ-КоА
О2
O
ГМГ-КоА лиаза
H12
C SKoA
12 АТФ
3C АТФ
Ацетил-КоА
Преимущество КТ перед ЖК:O
H2 – нет;
1) КТ водорастворимы, а ЖК
C C CH
3
2) ЖК разобщаютHOOC
окислительное
фосфорилирование
и
Ацетоацетат
усиливают синтез ТГ,
а КТ – нет
О2
48. Нормы
Содержание КТ в крови:• 30 мг/л – норма;
• 300-500 мг/л – при голодании;
• 3-4 г/л – при сахарном диабете;
49. ХОЛЕСТЕРИН
Холестерин (ХС) — стероид, характерный только дляживотных организмов.
В сутки в организме синтезируется 1г ХС.
ХС синтезируется в печени (50%), тонком кишечнике (1520%), коже, коре надпочечников, половых железах.
С пищей поступает в сутки 0,3—0,5г ХС.
Биологическая роль ХС
входит в состав мембран клеток, увеличивает их
электроизоляционные свойства, придает жесткость и
прочность;
В мембране защищает полиненасыщенные ЖК от
окисления;
из ХС синтезируются жёлчные кислоты, стероидные
гормоны, витамин Д3
является компонентом желчи, участвует в
переваривании липидов.
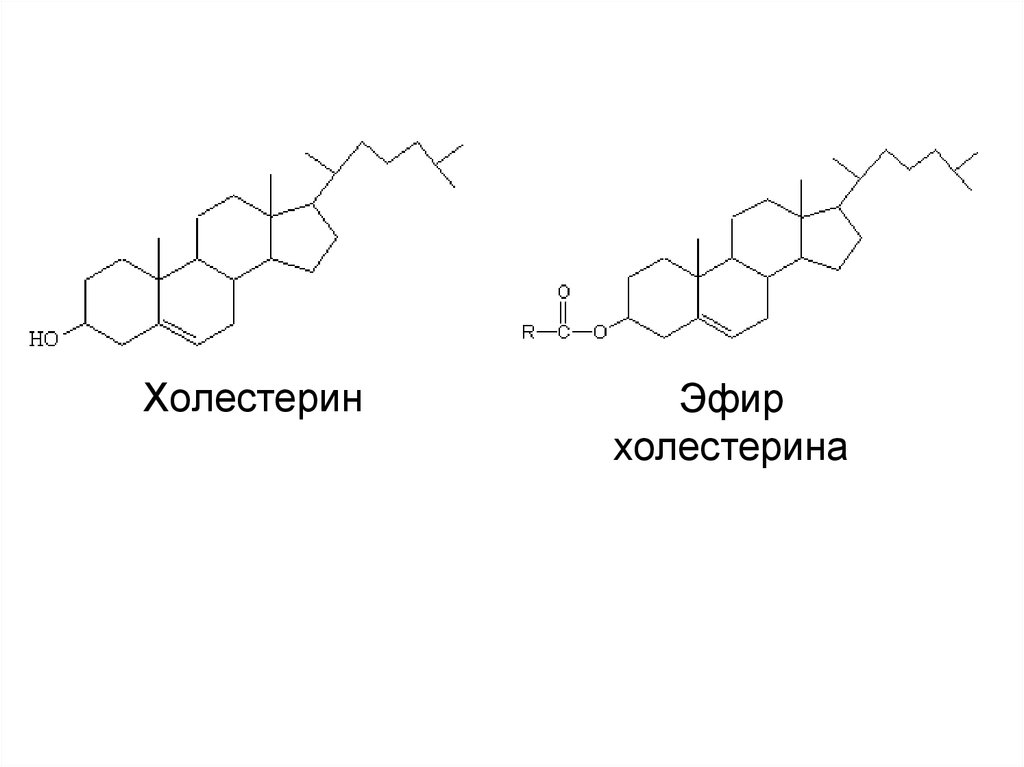
50. Холестерин
Эфирхолестерина
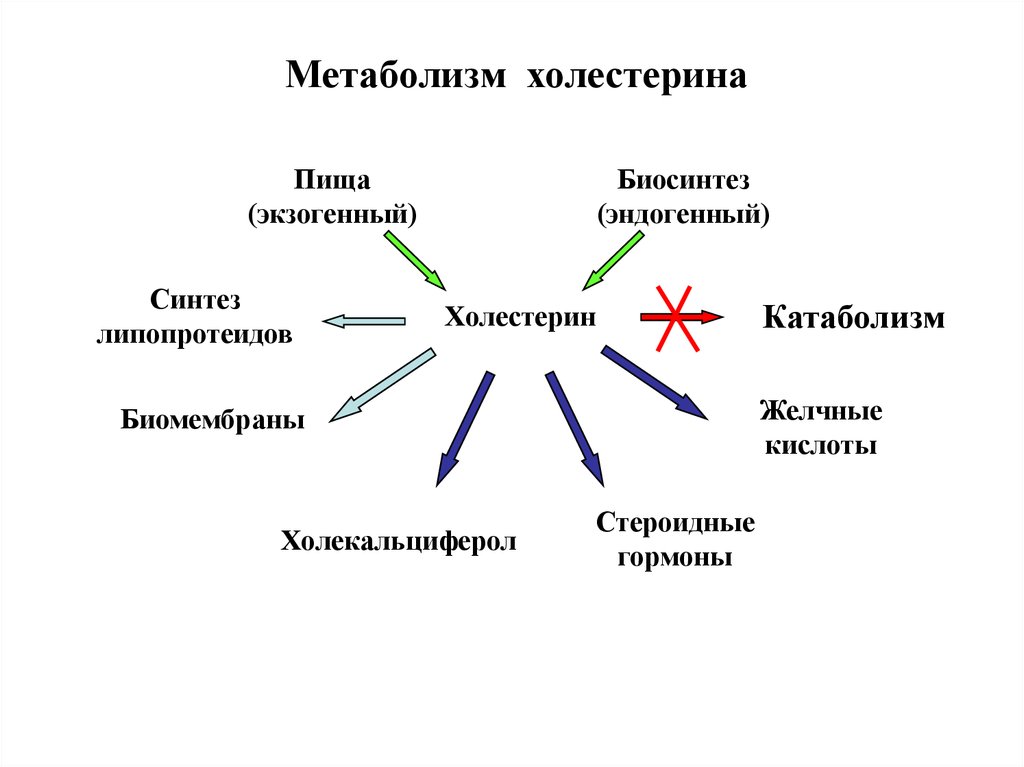
51. Холестерин
Метаболизм холестеринаПища
(экзогенный)
Синтез
липопротеидов
Биосинтез
(эндогенный)
Холестерин
Желчные
кислоты
Биомембраны
Холекальциферол
Катаболизм
Стероидные
гормоны
52. СИНТЕЗ ХС
происходит в цитозоле и ЭПР клеток.Это один из самых длинных метаболических путей в
организме человека (около 100 последовательных
реакций).
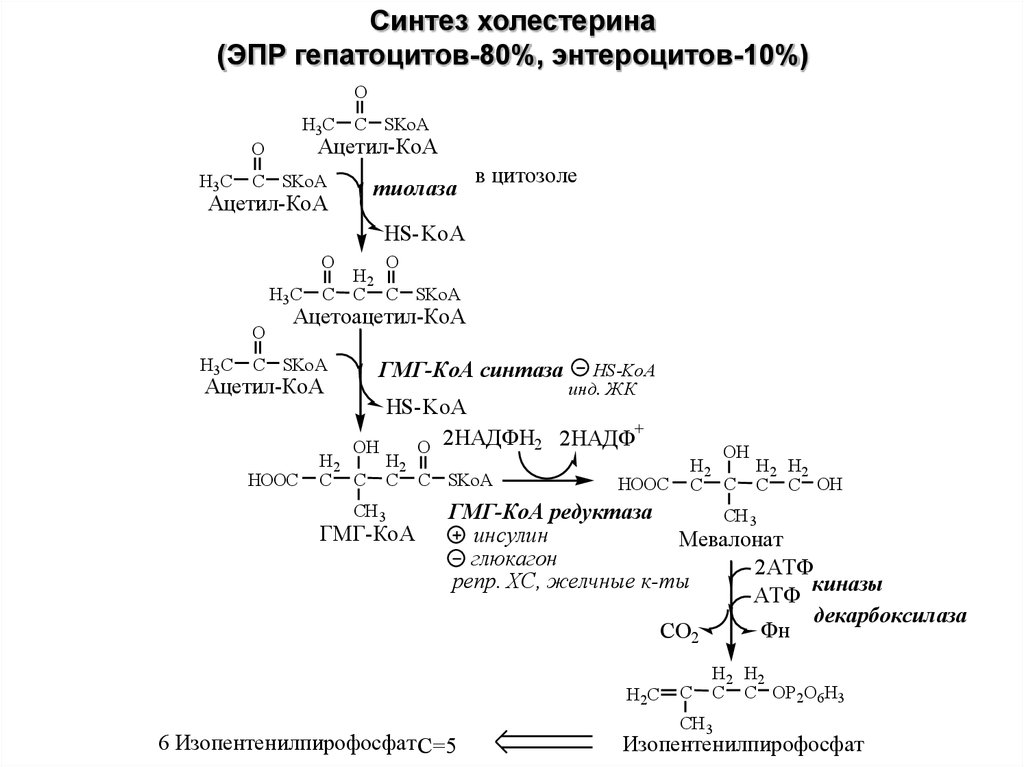
3 этапа:
I этап - образование мевалоната (мевалоновой
кислоты).
• Две молекулы ацетил-КоА конденсируются тиолазой с
образованием ацетоацетил-КоА;
• Гидроксиметилглутарил-КоА-синтаза (ГМГ-КоА)
присоединяет третий ацетильный остаток к
ацетоацетил-КоА с образованием ГМГ-КоА.
• ГМГ-КоА-редуктаза восстанавливает ГМГ-КоА до
мевалоната с использованием 2 молекул НАДФH2.
53.
II этап - образование сквалена• Мевалонат превращается в изопреноидную
структуру — изопентенилпирофосфат (5
атомов С);
• 2 изопентенилпирофосфата конденсируются в
геранилпирофосфат (10 атомов С);
• Присоединение изопентенилпирофосфата к
геранилпирофосфату дает
фарнезилпирофосфат (15 атомов С).
• 2 фарнезилпирофосфата конденсируются в
сквален (15 атомов С).
54.
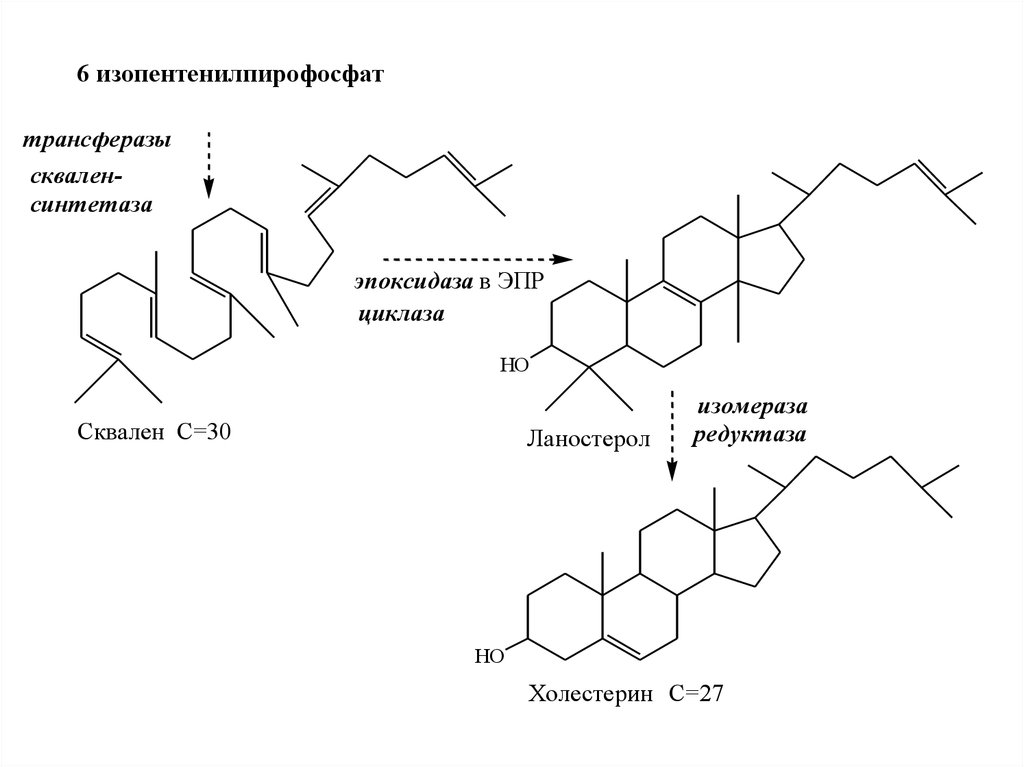
III этап - образование ХС• Сквален циклазой превращается в
ланостерин, (4 цикла и 30 атомов С).
• Далее происходит 20
последовательных реакций,
превращающих ланостерин в ХС (27
атомов С).
55.
Синтез холестерина(ЭПР гепатоцитов-80%, энтероцитов-10%)
O
H3C
Ацетил-КоА
O
H3C
C SKoA
C SKoA
тиолаза
Ацетил-КоА
в цитозоле
HS-KoA
O
H3C
O
H3C
O
H2
C C C SKoA
Ацетоацетил-КоА
C SKoA
Ацетил-КоА
HOOC
ГМГ-КоА синтаза
HS-KoA
инд. ЖК
HS-KoA
+
OH
O 2НАДФН2 2НАДФ
H2
C C
H2
C C SKoA
CH 3
ГМГ-КоА
HOOC
OH
H2
H2 H2
C C C C OH
ГМГ-КоА редуктаза
CH 3
инсулин
Мевалонат
глюкагон
2АТФ
репр. ХС, желчные к-ты
АТФ киназы
декарбоксилаза
Фн
СО2
H2C
6 Изопентенилпирофосфат С=5
C
H2 H2
C C OP 2O6H3
CH 3
Изопентенилпирофосфат
56.
H2C6 изопентенилпирофосфат
6 Изопентенилпирофосфат С=5
трансферазы
скваленсинтетаза
C
H2 H2
C C OP 2O6H3
CH 3
Изопентенилпирофосфат
эпоксидаза в ЭПР
циклаза
HO
Сквален С=30
Ланостерол
изомераза
редуктаза
HO
Холестерин С=27
57. Этерификация ХС
ХС образует с ЖК сложные эфиры (ЭХС),которые более гидрофобны, чем сам ХС.
В клетках эту реакцию катализирует
АХАТ(АцилКоА:ацилхолестеринтрансферазой):
ХС + Ацил-КоА → ЭХС + HSKoA
ЭХС формирует в цитоплазме липидные капли,
которые являются формой хранения ХС. По
мере необходимости ЭХС гидролизуются
холестеролэстеразой на ХС и ЖК.
ЭХС синтезируются в крови в ЛПВП под
действием ЛХАТ (лецитин:
холестеролацилтрансферазой):
ХС + лецитин → ЭХС + лизолецитин
58. Регуляция ключевого фермента синтеза ХС ГидроксиМетилГлутарил-КоА-редуктазы
• Инсулин через дефосфорилирование активируетфермент.
• Повышение концентрации ацетил-КоА стимулирует
синтез ХС.
• Синтез ХС активируется при питании углеводами и
снижается при голодании.
• Глюкагон через фосфорилирование ингибирует
фермент.
• ХС, желчные кислоты (в печени) репрессируют ген ГМГКоА-редуктазы.
59. Выведение ХС из организма
В сутки из организма выводится 1,0г - 1,3г ХС.С желчью (0,5 - 0,7 г/сут) - в виде жёлчных
кислот.
Часть ХС в кишечнике под действием ферментов
бактерий восстанавливается по двойной связи,
образуя холестанол и копростанол.
С кожным салом в сутки выделяется 0,1г ХС.




























 Биология
Биология Химия
Химия