Похожие презентации:
Аминокислоты
1. «Аминокислоты»
2.
Ход урока:1. Записать дату и тему урока.
2. Прочитать параграф 37,
посмотреть презентацию.
3. Записать: понятие
«Аминокислот», классификацию и
хим. свойства.
4. Работу выслать до
следующего урока.
3. Аминокислоты
N H2 – C H – C O O HR
Производные карбоновых кислот,
содержащие в своем составе одну или
несколько аминогрупп.
4. Аминокислоты
ПриродныеИх около 150, они были
обнаружены в живых
организмах, около 20 из
них входят в состав
белков. Половина этих
аминокислот –
незаменимые
(не синтезируются
в организме человека),
они поступают с пищей.
Синтетические
Получают кислотным
гидролизом белков
либо из карбоновых
кислот, воздействуя на
них галогеном
и, далее, аммиаком.
5. Некоторые важнейшие α-аминокислоты общей формулы NH2 - CH - COOH R
Некоторые важнейшие α-аминокислоты общейформулы
Аминокислота
Глицин
NH2 - CH - COOH
R
Сокращенное
Радикал
обозначение
Gly
–Н
Аланин
Ala
CH3
Фенилаланин
Phe
CH2–C6H5
Валин
Val
–СH(CH3)2
Лейцин
Leu
–CH2–CH(CH3)2
Серин
Ser
–CH2OH
6. Номенклатура
По систематической номенклатуре названияаминокислот образуются из названий соответствующих
кислот прибавлением приставки амино- и указанием
места расположения аминогруппы по отношению
к карбоксильной группе.
7. Номенклатура
Часто используется другой способ построения названийаминокислот, согласно которому к тривиальному
названию карбоновой кислоты добавляется приставка
амино- с указанием положения аминогруппы буквой
греческого алфавита.
8. Изомерия аминокислот
углеродногоскелета ;
положения функциональных групп ;
межклассовая (нитросоединения);
оптическая.
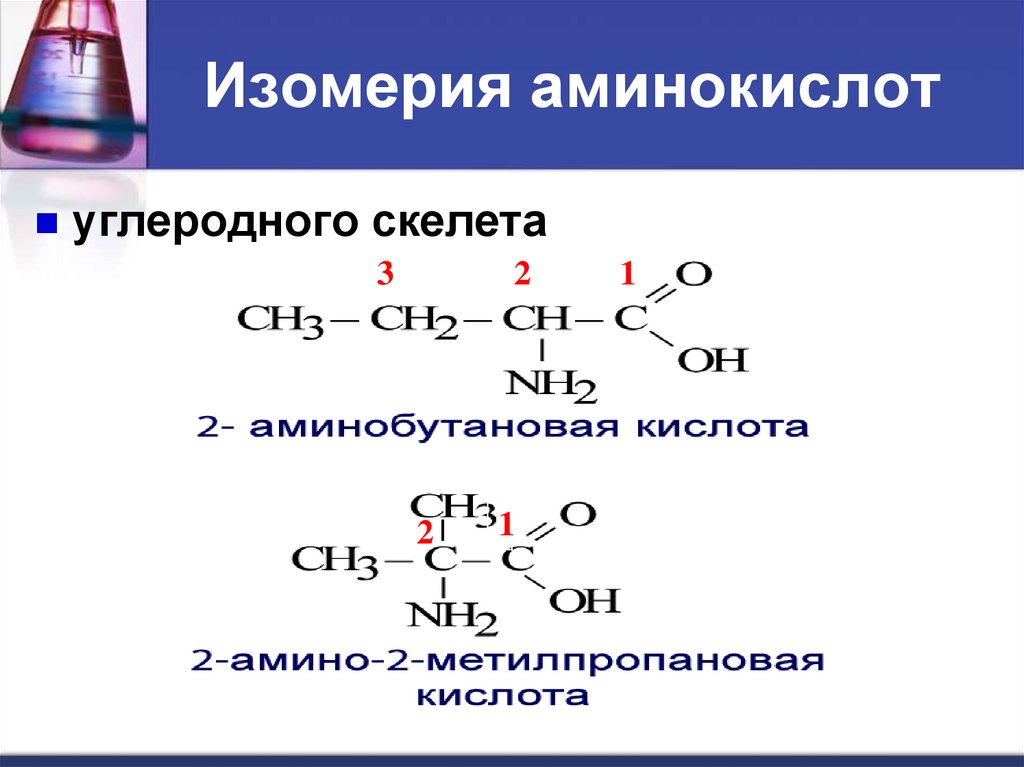
9. Изомерия аминокислот
углеродного скелета3
2
2
1
1
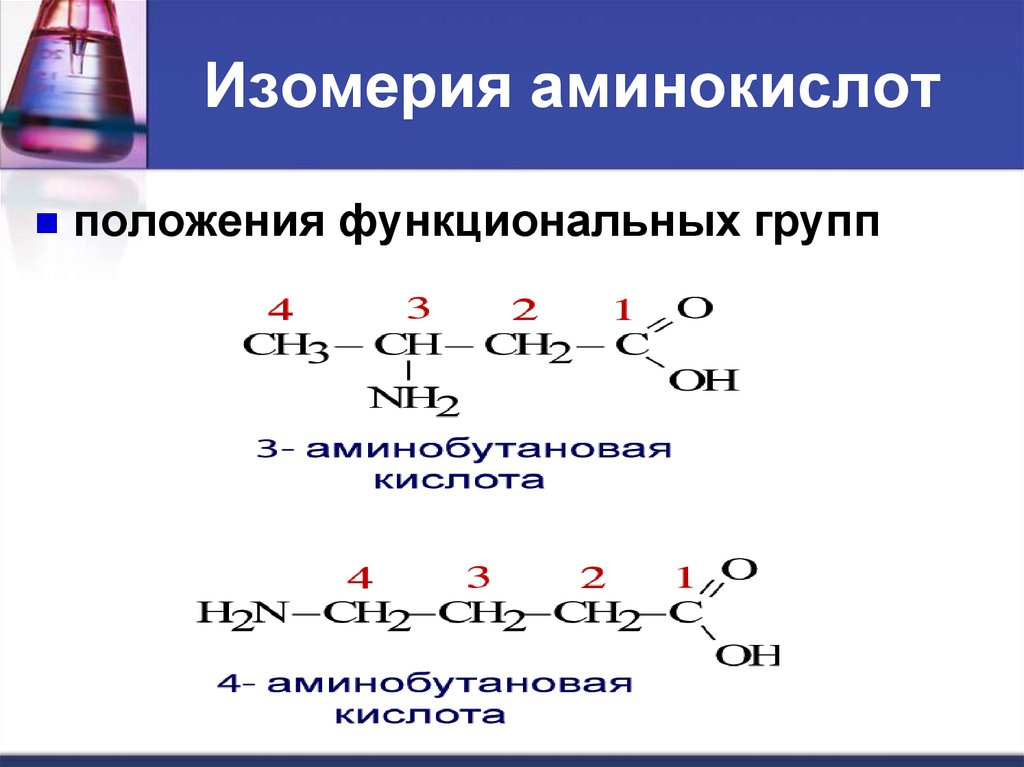
10. Изомерия аминокислот
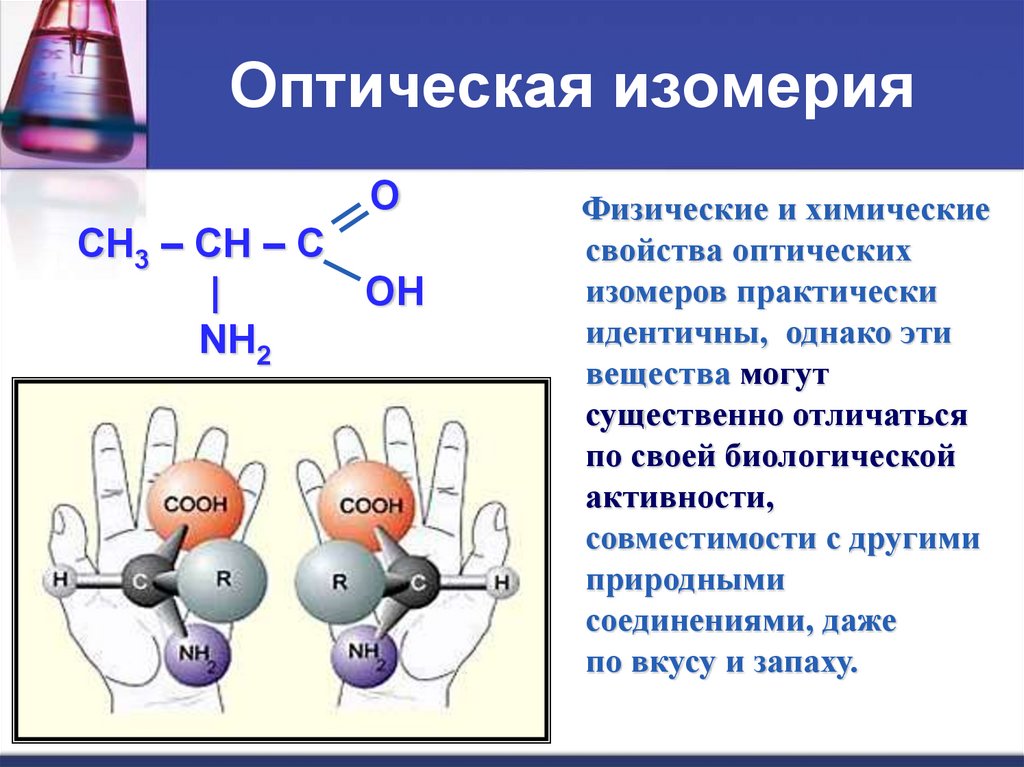
положения функциональных групп11. Оптическая изомерия
OCH3 – CH – C
|
OH
NH2
2- аминопропановая кислота
Физические и химические
свойства оптических
изомеров практически
идентичны, однако эти
вещества могут
существенно отличаться
по своей биологической
активности,
совместимости с другими
природными
соединениями, даже
по вкусу и запаху.
12. Физические свойства
Аминокислотыбесцветные;
кристаллические;
хорошо растворимы в воде, но нерастворимы
в эфире;
в зависимости от R могут быть сладкими,
горькими или безвкусными;
обладают оптической активностью;
плавятся с разложением при температуре выше
200º.
13. Химические свойства
Наличие аминои карбоксильной группопределяет двойственность
химических свойств
аминокислот.
Амфотерность (от греч.
amphуteros – «и тот и другой») –
способность некоторых веществ
в зависимости от условий
проявлять либо кислотные,
либо основные свойства;
амфотерные вещества иногда
называют амфолитами.
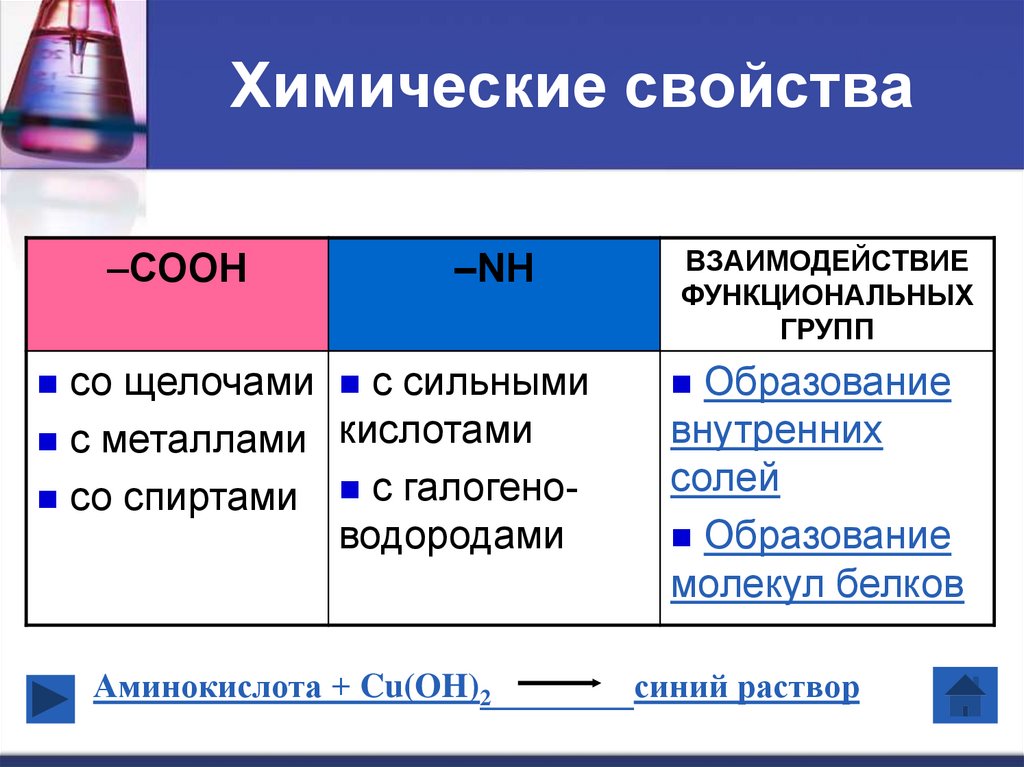
14. Химические свойства
–СООН–NH
со щелочами с сильными
с металлами кислотами
со спиртами с галогеноводородами
Аминокислота + Cu(OH)2
ВЗАИМОДЕЙСТВИЕ
ФУНКЦИОНАЛЬНЫХ
ГРУПП
Образование
внутренних
солей
Образование
молекул белков
синий раствор
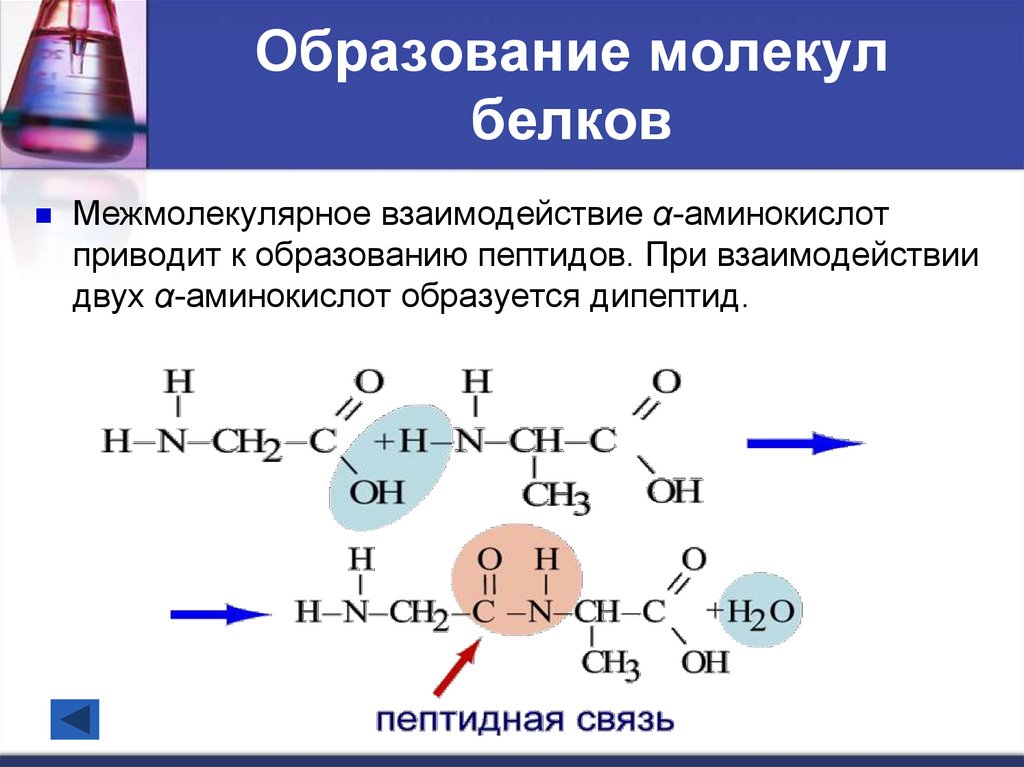
15. Образование молекул белков
Межмолекулярное взаимодействие α-аминокислотприводит к образованию пептидов. При взаимодействии
двух α-аминокислот образуется дипептид.
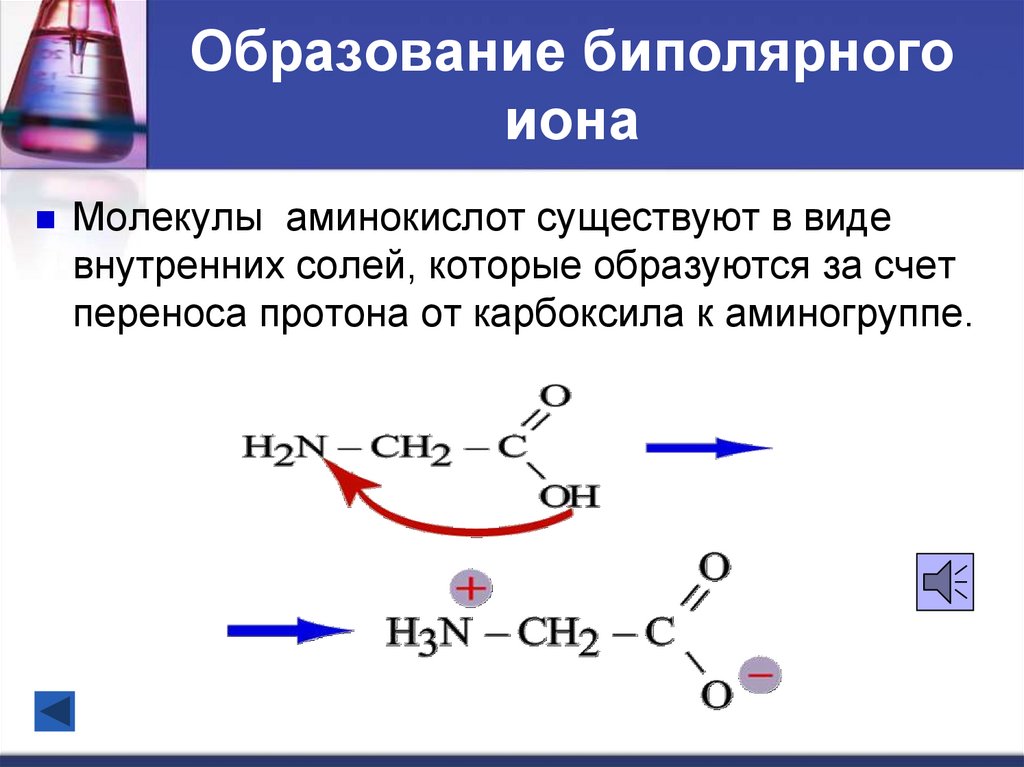
16. Образование биполярного иона
Молекулы аминокислот существуют в видевнутренних солей, которые образуются за счет
переноса протона от карбоксила к аминогруппе.
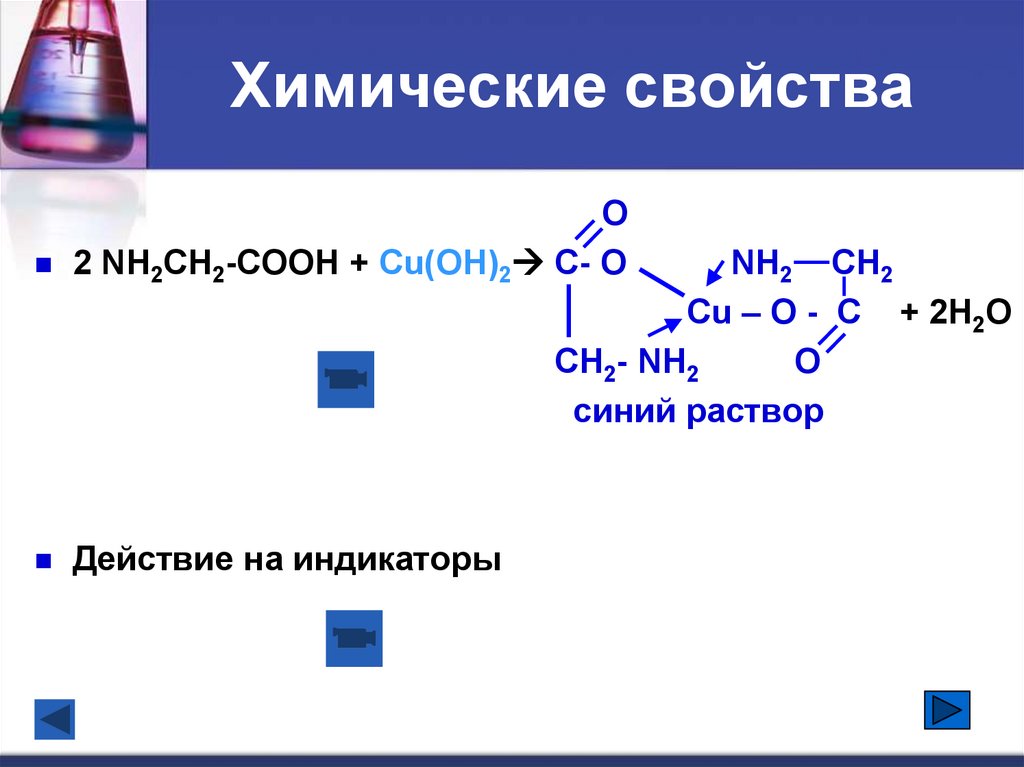
17. Химические свойства
O2 NH2CH2-COOH + Cu(OH)2 C- O
Действие на индикаторы
NH2 CH2
Cu – O - C + 2H2O
CH2- NH2
O
синий раствор
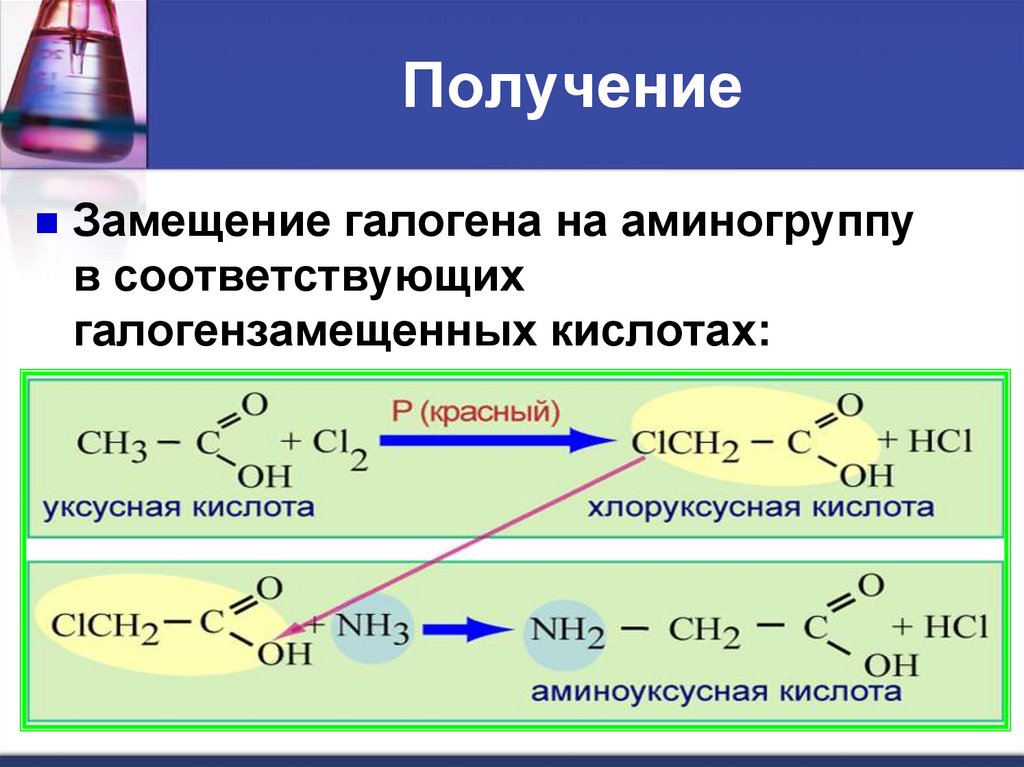
18. Получение
Замещение галогена на аминогруппув соответствующих
галогензамещенных кислотах:
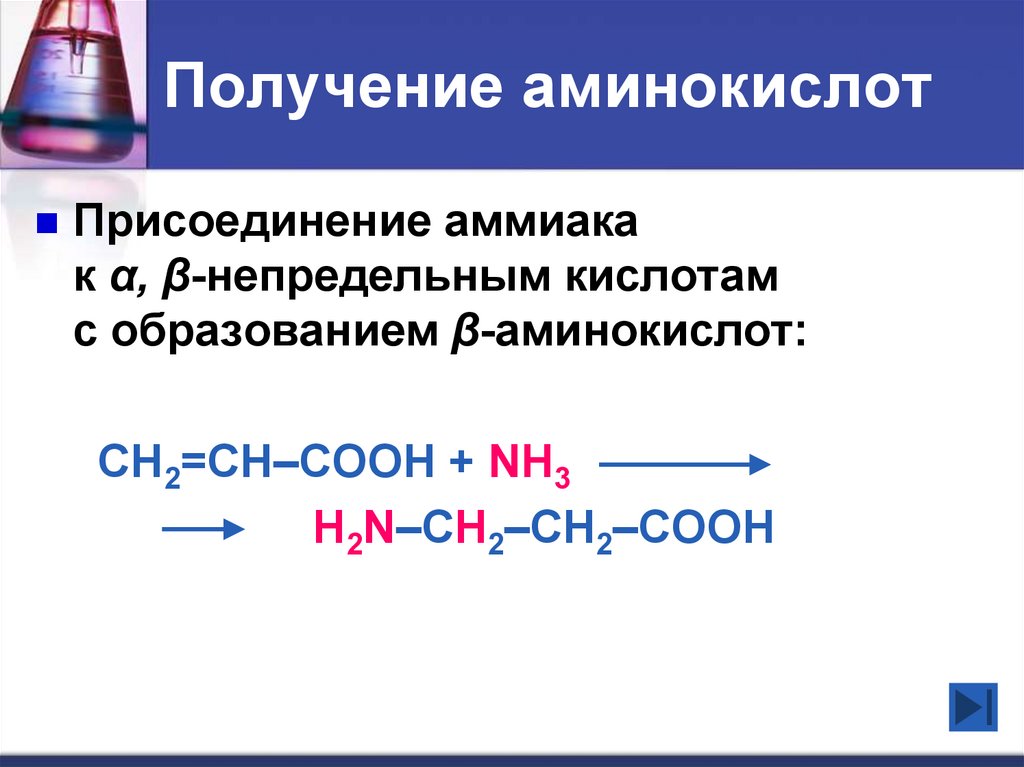
19. Получение аминокислот
Присоединение аммиакак α, β-непредельным кислотам
с образованием β-аминокислот:
CH2=CH–COOH + NH3
H2N–CH2–CH2–COOH










 Химия
Химия








