Похожие презентации:
Влияние факторов окружающей среды на метаболизм человека. Биохимия печени (лекция10)
1.
Лекция10:Влияние факторов окружающей
среды на метаболизм человека.
Биохимия печени.
Дисциплина: Биологическая химия
для специальности 32.05.01 Медико-профилактическое дело
ИФОИТМ ТГМУ
Разработаны – доц. О. А. Артюкова
Лектор – доц. В.И. Янькова
2.
Основные вопросы лекции:• Влияние факторов окружающей среды на метаболизм человека.
• Биохимия печени.
• Функция печени в обезвреживании эндогенных и экзогенных
токсических веществ.
• Микросомальное окисление, роль цитохрома Р450.
• Желтухи.
• Биохимические маркеры заболеваний печени
(АСТ, АЛТ, билирубин, гипераммониемия).
3.
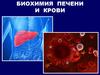
Печень - самый крупный из паренхиматозных органов.Печень состоит из 300 млрд. клеток,
80% составляют гепатоциты.
Масса печени достигает 1,5 кг,
(2 - 3% от массы тела).
На печень приходится 20 - 30%
потребляемого организмом О2.
Клетки печени занимают
центральное место в
реакциях метаболизма.
4.
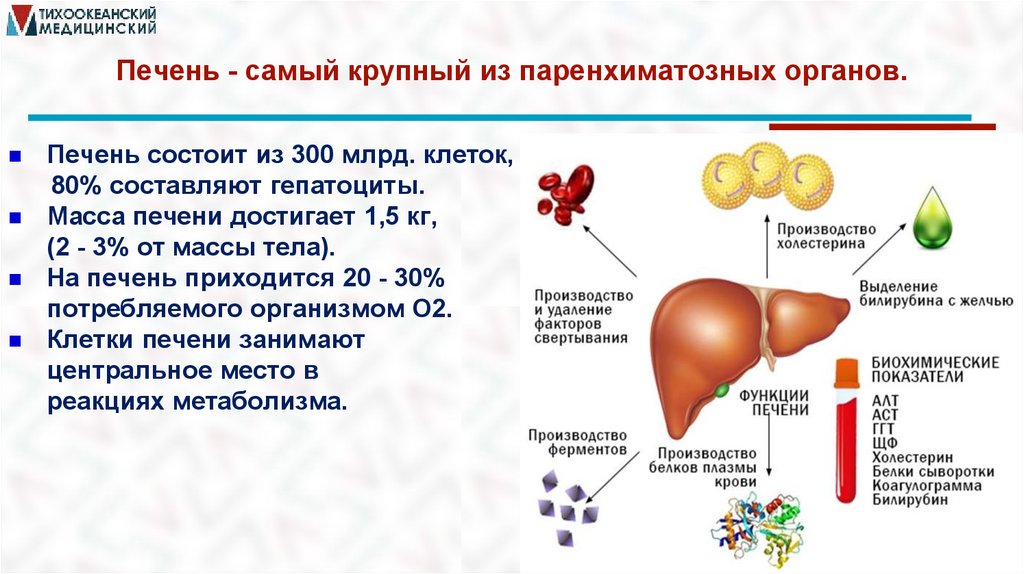
Печень выполняет ряд ключевых функций:Метаболическая - принимает и распределяет
вещества, поступающие из ЖКТ.
Депонирующая - накопление гликогена, белков, ТАГ,
витаминов, гормонов, минеральных веществ,
макроэргических соединений и структурных блоков,
необходимые для синтеза сложных макромолекул.
Секреторная – биосинтез и секреция в кровь белков,
липопротеинов, глюкозы, кетоновых тел и др.
Желчеобразующая (участие в переваривании жиров).
Антитоксическая (инактивация токсических веществ).
Экскреторная - выведение веществ эндо- и экзогенного
происхождения с желчью (более 40 соединений).
Гомеостатическая - поддержание гомеостаза, обеспечивает
синтез, накопление и выделение в кровь метаболитов.
5.
Печень выполняет ряд ключевых функций:6.
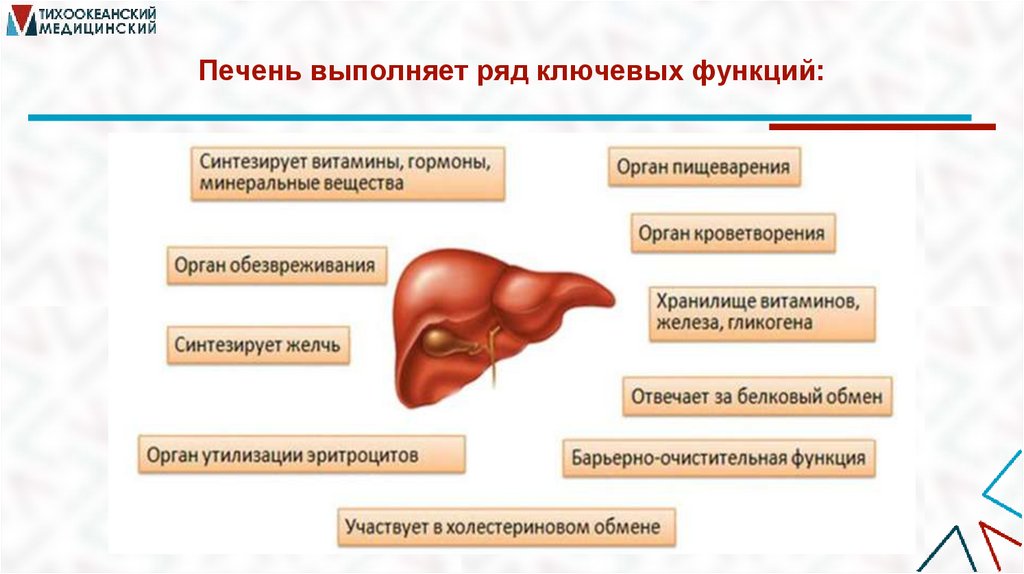
Разнообразные функции печени требуют особого строения.Артериальная кровь проходит к центру
печеночной дольки по разветвленной сети
капилляров между рядами гепатоцитов,
называемой синусоидами.
Вдоль синусоид располагаются
клетки РЭС – клетки Купфера.
В зонах соприкосновения мембран 2-х
или более гепатоцитов формируются
желчные канальцы. На периферии они
сливаются в более крупные желчные ходы.
Поверхность печеночной капиллярной сети
достигает 400 м и обеспечивает прохождение
через печень около 2000 л крови в сутки.
7.
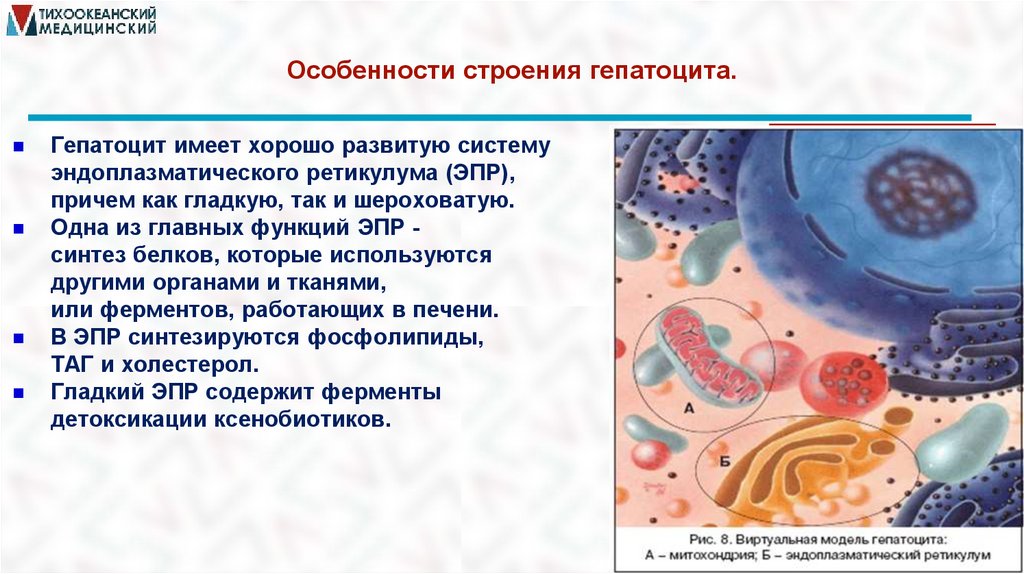
Особенности строения гепатоцита.Гепатоцит имеет хорошо развитую систему
эндоплазматического ретикулума (ЭПР),
причем как гладкую, так и шероховатую.
Одна из главных функций ЭПР синтез белков, которые используются
другими органами и тканями,
или ферментов, работающих в печени.
В ЭПР синтезируются фосфолипиды,
ТАГ и холестерол.
Гладкий ЭПР содержит ферменты
детоксикации ксенобиотиков.
8.
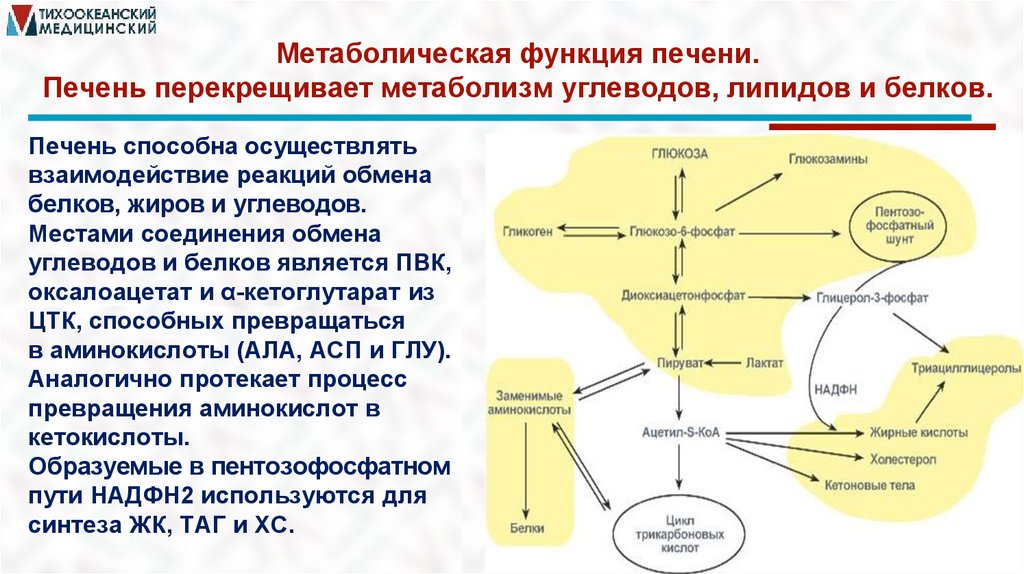
Метаболическая функция печени.Печень перекрещивает метаболизм углеводов, липидов и белков.
Печень способна осуществлять
взаимодействие реакций обмена
белков, жиров и углеводов.
Местами соединения обмена
углеводов и белков является ПВК,
оксалоацетат и α-кетоглутарат из
ЦТК, способных превращаться
в аминокислоты (АЛА, АСП и ГЛУ).
Аналогично протекает процесс
превращения аминокислот в
кетокислоты.
Образуемые в пентозофосфатном
пути НАДФН2 используются для
синтеза ЖК, ТАГ и ХС.
9.
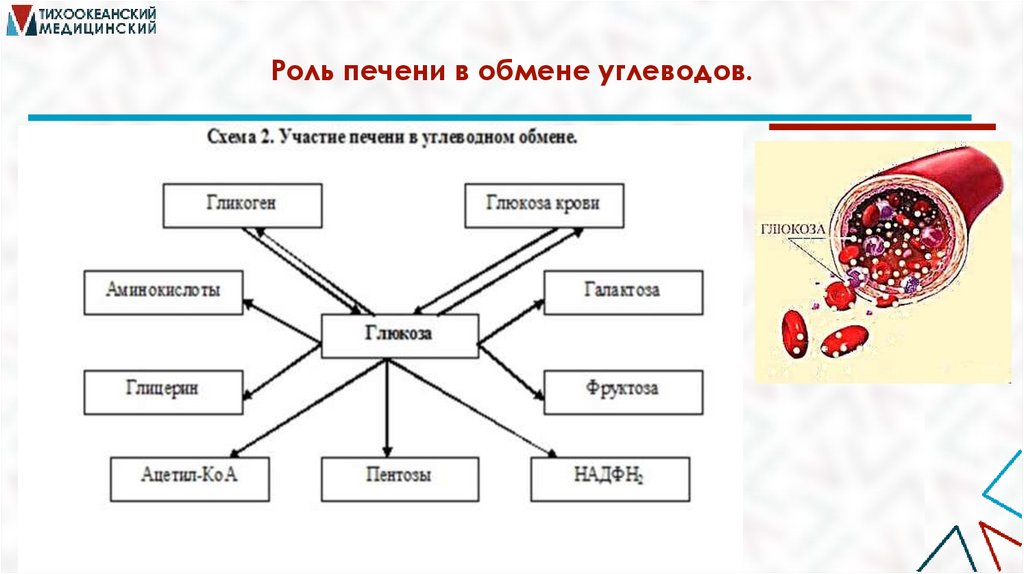
Роль печени в обмене углеводов.10.
Печень играет ведущую роль в поддержании оптимальной концентрацииглюкозы в крови (глюкостатическая функция печени).
После приема углеводной пищи
(концентрация глюкозы в крови воротной
вены достигает 20 ммоль/л)
печень тратит ее следующим образом:
10 % - на синтез гликогена,
60 % - на окислительный распад,
30 % - на синтез жирных кислот.
Благодаря синтезу и распаду гликогена печень поддерживает концентрацию
глюкозы в крови. При кратковременном голодании происходит гликогенолиз.
При длительном голодании источником глюкозы крови является глюконеогенез.
Печень осуществляет взаимопревращение сахаров,
т.е. превращение гексоз (фруктозы, галактозы) в глюкозу.
Реакции пентозофосфатного пути обеспечивают наработку НАДФН2,
необходимого для синтеза ЖК, ХС И ТАГ из глюкозы.
11.
Печени принадлежит ведущая роль в метаболизме липидов.12.
Печени принадлежит ведущая роль в метаболизме липидов.Жирные кислоты синтезируются
в печени из ацетил-КоА. Затем они
включаются в состав ТАГ и ФЛ, которые
поступают в кровь в форме ЛПОНП.
При избытке глюкозы в гепатоцитах
происходит синтез ЖК и ТАГ.
При дефиците глюкозы в печени
активируется β-окисление жирных
кислот.
В печени синтезируются кетоновые тела.
Сердечная мышца, ЦНС и др. органы в
условиях голодания в качестве
источника энергии могут использовать
эти соединения, а не глюкозу.
13.
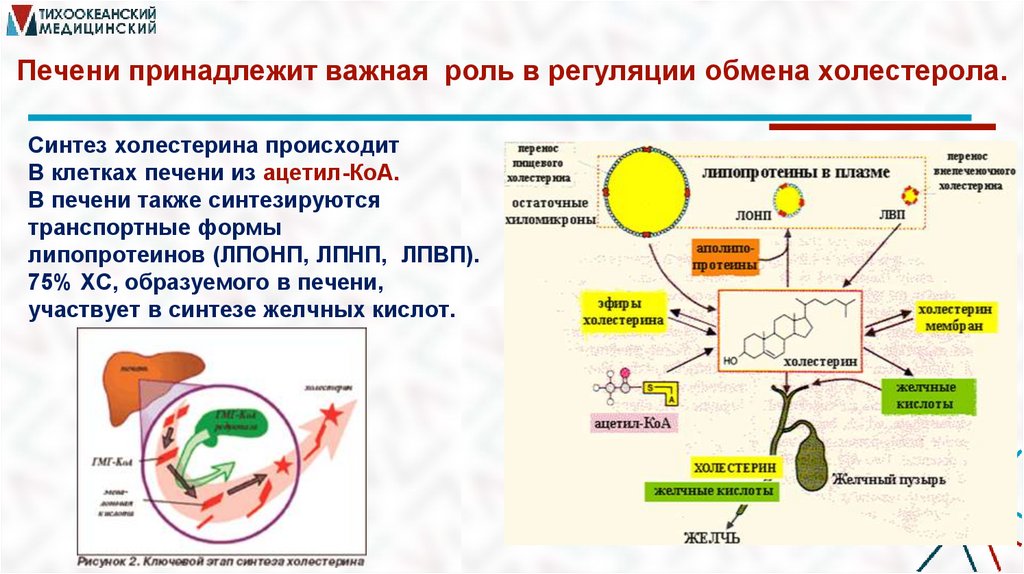
Печени принадлежит важная роль в регуляции обмена холестерола.Синтез холестерина происходит
В клетках печени из ацетил-КоА.
В печени также синтезируются
транспортные формы
липопротеинов (ЛПОНП, ЛПНП, ЛПВП).
75% ХС, образуемого в печени,
участвует в синтезе желчных кислот.
14.
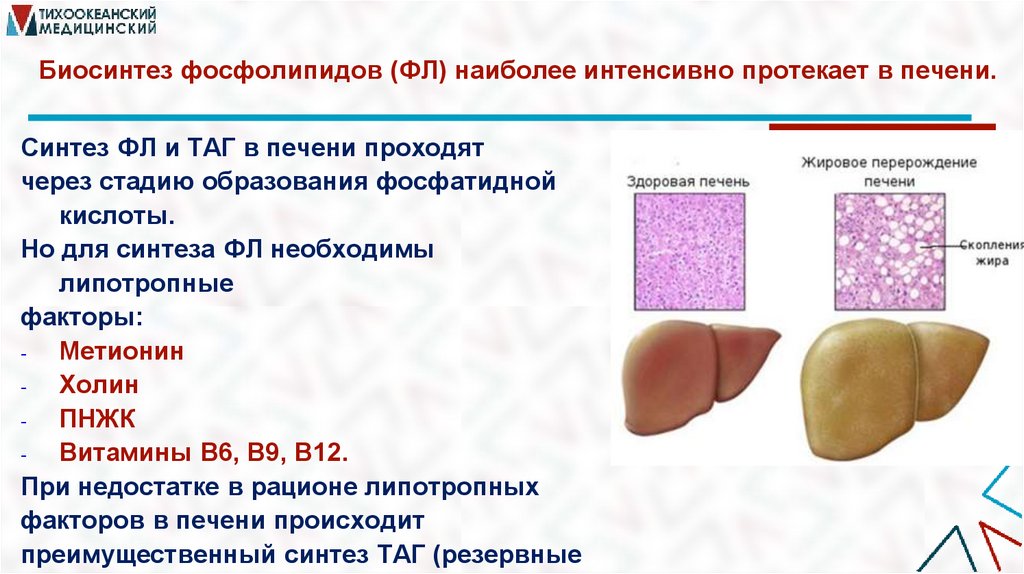
Биосинтез фосфолипидов (ФЛ) наиболее интенсивно протекает в печени.Синтез ФЛ и ТАГ в печени проходят
через стадию образования фосфатидной
кислоты.
Но для синтеза ФЛ необходимы
липотропные
факторы:
Метионин
Холин
ПНЖК
Витамины В6, В9, В12.
При недостатке в рационе липотропных
факторов в печени происходит
преимущественный синтез ТАГ (резервные
15.
Печень занимает центральное место в обмене аминокислот.В клетках печени имеется
уникальный набор ферментов,
катализирующих специфические
реакции аминокислот,
в ней активно протекают
процессы их химической
модификации
(трансаминирование,
дезаминирование,
трансметилирование).
Происходят реакции синтеза
из аминокислот холина, креатина
и других азотсодержащих
соединений.
16.
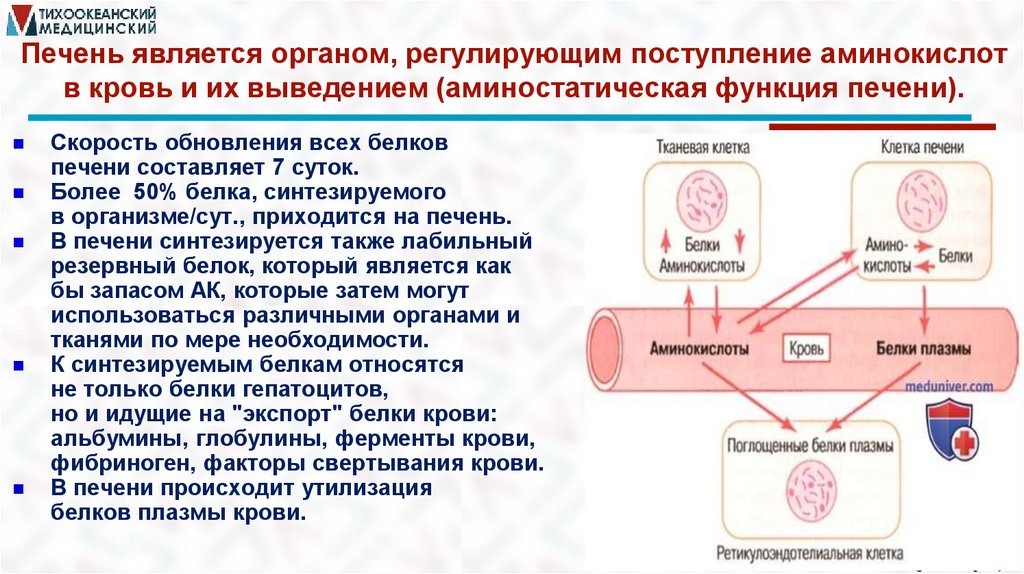
Печень является органом, регулирующим поступление аминокислотв кровь и их выведением (аминостатическая функция печени).
Скорость обновления всех белков
печени составляет 7 суток.
Более 50% белка, синтезируемого
в организме/сут., приходится на печень.
В печени синтезируется также лабильный
резервный белок, который является как
бы запасом АК, которые затем могут
использоваться различными органами и
тканями по мере необходимости.
К синтезируемым белкам относятся
не только белки гепатоцитов,
но и идущие на "экспорт" белки крови:
альбумины, глобулины, ферменты крови,
фибриноген, факторы свертывания крови.
В печени происходит утилизация
белков плазмы крови.
17.
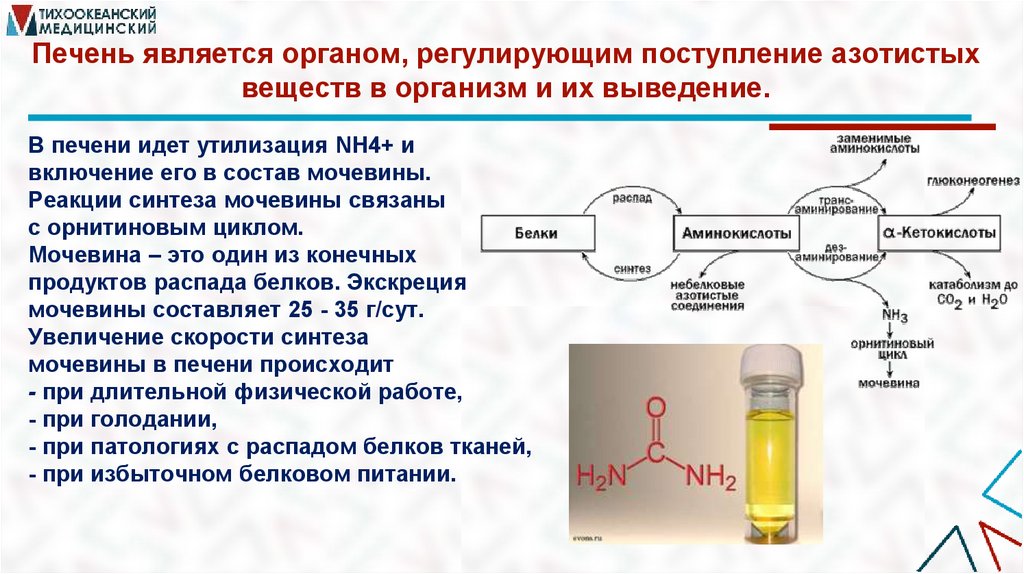
Печень является органом, регулирующим поступление азотистыхвеществ в организм и их выведение.
В печени идет утилизация NH4+ и
включение его в состав мочевины.
Реакции синтеза мочевины связаны
с орнитиновым циклом.
Мочевина – это один из конечных
продуктов распада белков. Экскреция
мочевины составляет 25 - 35 г/сут.
Увеличение скорости синтеза
мочевины в печени происходит
- при длительной физической работе,
- при голодании,
- при патологиях с распадом белков тканей,
- при избыточном белковом питании.
18.
Депонирующая функция печени.● Печень служит местом депонирования энергетических
резервов организма
(6% массы печени – запас гликогена).
● Печень служит местом депонирования
минеральных веществ (15% Fe, содержащегося в организме)
● Печень служит местом депонирование витаминов
(A, D, K, В9, B12 и др.).
19.
Токсин — это любое химическое вещество,которые нарушает функцию клетки или разрушает ее структуру.
Из окружающей среды токсические элементы мигрируют в различные экосистемы
и по пищевым цепям, достигая больших концентраций в растениях и животных,
попадают с пищей в организм человека. Проникновение вредных веществ в
организм человека может осуществляться непосредственно из воды и воздуха.
Ксенобиотики — любые чуждые для организма вещества, способные нарушать
течение биологических процессов. Ксенобиотики, попадая в организм, либо
проявляют нежелательные эффекты, либо вследствие биотрансформации в
печени образуют более токсичные метаболиты.
Категории токсичных веществ:
тяжелые металлы;
стойкие органические загрязнители:
(растворители, формальдегид, пестициды,
гербициды, лекарства, алкоголь и др.);
токсины, выделяемые микробами, грибами;
продукты распада белка.
20.
Антитоксическая функция печени.Печень — орган, который, помимо остальных
своих функций, обезвреживает токсичные
вещества. Часть из них поступают извне, а другие
вырабатываются внутри организма.
Фильтрация крови — одна из функций печени
(скорость - 2 л/мин).
Важнее всего фильтровать кровь, которая
поступает из ЖКТ, потому что она перегружена
токсинами (продукты гниения белка в кишечнике,
продукты работы иммунной системы).
Если печень функционирует нормально,
то в процессе фильтрации она удаляет
из кровотока до 99% токсичных веществ.
21.
Обезвреживание ксенобиотиков протекает в печени непрерывно.Ксенобиотики, как правило, гидрофобны и
токсичны. Печень связывает и обезвреживает
токсичные вещества с помощью специальных
ферментных систем.
Для снижения токсичности и повышения
растворимости ксенобиотики подвергаются
реакциям детоксикации, которые протекают
в две фазы:
I фаза - гидрофобное вещество химически
модифицируется и становится растворимым;
II фаза - реакция конъюгации.
После превращений в печени модифицированное
соединение направляется либо в желчь и далее в
фекалии, либо в кровь и мочу.
22.
Первая фаза обезвреживания обязательна для гидрофобныхвеществ, т. к. они могут накапливаться в тканях, богатых липидами
(жировая клетчатка, мембраны, нервная система).
В I фазе токсичные вещества подвергаются таким изменениям, как
гидроксилирование, восстановление, сульфоокисление, дезаминирование и др.
В мембранах эндоплазматического ретикулума (ЭПР) гепатоцитов локализована
система микросомального окисления, отвечающая за течение I фазы
обезвреживания. Реакции I фазы превращают ксенобиотик в более полярный
метаболит путем введения функциональной группы (-ОН, -NH2 -SH).
Если эти метаболиты полярны, они могут легко экскретироваться.
23.
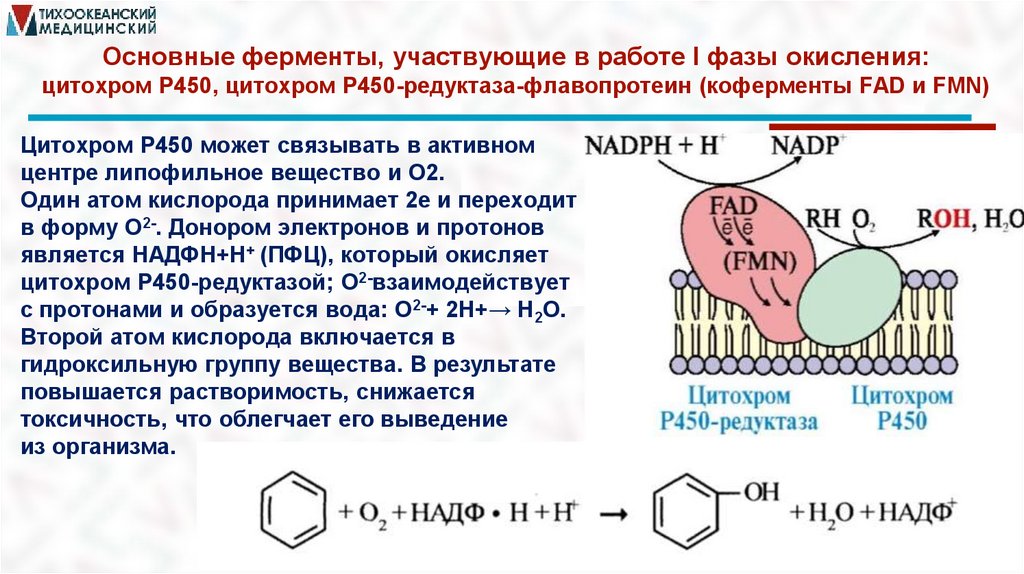
Основные ферменты, участвующие в работе I фазы окисления:цитохром Р450, цитохром Р450-редуктаза-флавопротеин (коферменты FAD и FMN)
Цитохром Р450 может связывать в активном
центре липофильное вещество и О2.
Один атом кислорода принимает 2е и переходит
в форму О2-. Донором электронов и протонов
является НAДФН+Н+ (ПФЦ), который окисляет
цитохром Р450-редуктазой; О2-взаимодействует
с протонами и образуется вода: О2-+ 2Н+→ Н2О.
Второй атом кислорода включается в
гидроксильную группу вещества. В результате
повышается растворимость, снижается
токсичность, что облегчает его выведение
из организма.
24.
Цитохром Р450 обладает относительной субстратной специфичностью.Известно много изоформ цит. Р450, каждая из них может
взаимодействовать со сходными по строению
ксенобиотиками (экзо-, и эндогенные вещества).
Цит.Р450 участвует в биотрансформации лекарств, которые
не могут быть выведены из организма в неизменном виде.
Активность разных изоформ цит. Р450 у разных людей
может отличаться во много раз. Это зависит от генетических
факторов, питания, содержания токсинов и др.
Поскольку активность ферментов системы цит.Р450
отличается, то разными оказываются
и индивидуальный терапевтический эффект,
и индивидуальный риск заболеваний.
Фаза I в печени тормозится с возрастом
(уменьшается ток крови через печень).
25.
II фаза обезвреживания – реакции коньюгации.Конъюгация - это присоединение к функциональным группам, образовавшимся
в первой фазе или уже имеющимся у ксенобиотиков, других молекул или групп,
увеличивающих гидрофильность и уменьшающих их токсичность.
Конъюгация может происходить с глицином, глюкуроновой кислотой,
сульфатом, ацетататом, метильной группой, глутатионом.
Участвуют ферменты трансферазы, которые присоединяют различные
конъюгаты к гидрофильным группам обезвреживаемых веществ. Полученный
продукт хорошо растворим и легко удаляется из организма с желчью и мочой.
26.
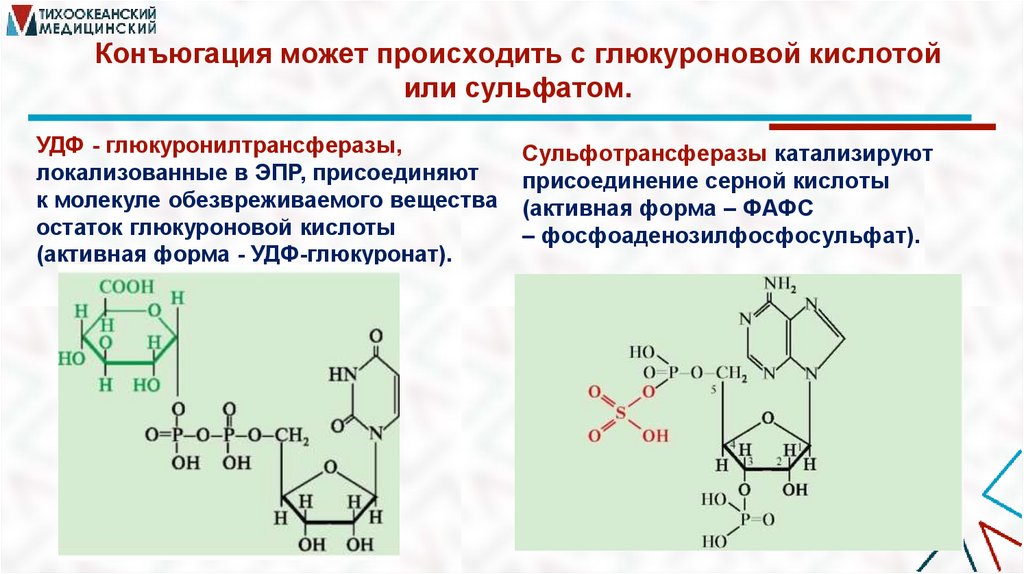
Конъюгация может происходить с глюкуроновой кислотойили сульфатом.
УДФ - глюкуронилтрансферазы,
локализованные в ЭПР, присоединяют
к молекуле обезвреживаемого вещества
остаток глюкуроновой кислоты
(активная форма - УДФ-глюкуронат).
Сульфотрансферазы катализируют
присоединение серной кислоты
(активная форма – ФАФС
– фосфоаденозилфосфосульфат).
27.
ОБЕЗВРЕЖИВАНИЕ ПРОДУКТОВ КАТАБОЛИЗМА АМИНОКИСЛОТВ КИШЕЧНИКЕ.
Индол образуется при гниении в кишечнике
триптофана, обладает гидрофобными и
токсичными свойствами.
Обезвреживается в печени в 2 этапа:
- образование индоксила;
- конъюгация индоксила с ФАФС,
образуется индоксилсерная кислота
(калиевая соль - животный индикан).
Анализ последнего в моче использовали
для оценки детоксикационной функции печени
28.
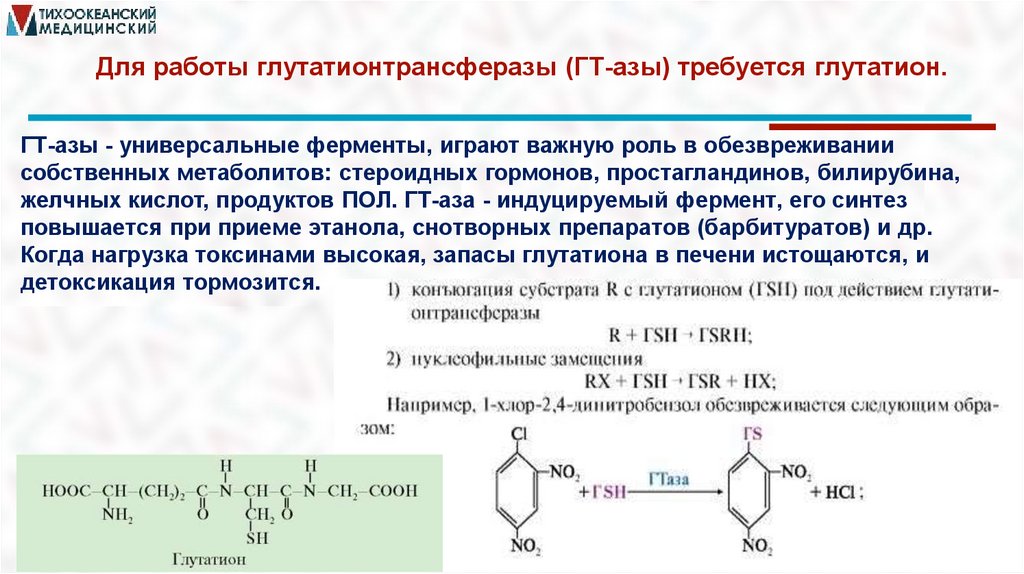
Для работы глутатионтрансферазы (ГТ-азы) требуется глутатион.ГТ-азы - универсальные ферменты, играют важную роль в обезвреживании
собственных метаболитов: стероидных гормонов, простагландинов, билирубина,
желчных кислот, продуктов ПОЛ. ГТ-аза - индуцируемый фермент, его синтез
повышается при приеме этанола, снотворных препаратов (барбитуратов) и др.
Когда нагрузка токсинами высокая, запасы глутатиона в печени истощаются, и
детоксикация тормозится.
29.
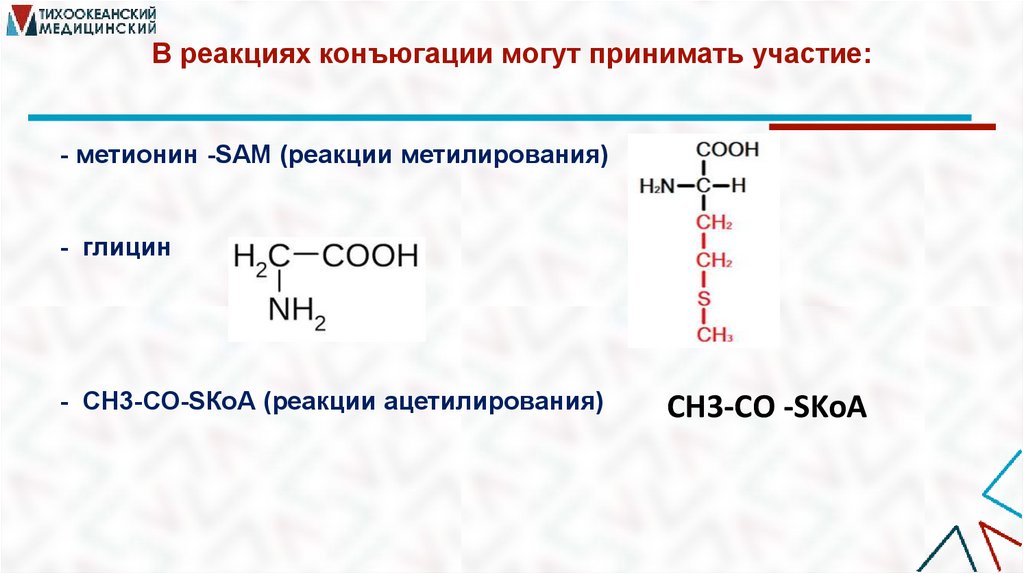
В реакциях конъюгации могут принимать участие:- метионин -SAM (реакции метилирования)
- глицин
- СН3-СО-SКоА (реакции ацетилирования)
СН3-СО -SKoA
30.
БИОТРАНСФОРМАЦИЯ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ.Действие на организм большинства
лекарств строго дозировано и
прекращается через определенное время
после их приема. Лекарственные
препараты подвергаются химической
модификации и в виде продуктов
экскретируются из организма.
31.
Обезвреживание тяжелых металлов в организме.Металлотионеины — семейство
низкомолекулярных белков с высоким
содержанием цистеина. Большие количества
этих белков синтезируется в печени и почках.
Металлотионеины способны связывать
физиологические (Zn, Cu, Se) и ксенобиотические
тяжёлые металлы (Cd, Hg, Ag, As, Pb и др.),
благодаря способности образовывать хелатные
соединения с ионами тяжелых металлов.
Также вывод тяжелых металлов из ЖКТ
осуществляется с помощью энтеросорбентов,
которые «вытягивают» токсичные вещества из
организма.
32.
МЕТАБОЛИЗМ И ОБЕЗВРЕЖИВАНИЕ ЭТАНОЛАЭндогенный этанол может синтезироваться в организме человека.
Источник – спиртовое брожение углеводов в клетках микрофлоры кишечника.
Экзогенный этанол поступает со спиртными напитками и
некоторыми пищевыми продуктами (соки, кефир, хлеб).
Экзогенный этанол быстро всасывается в желудке (20-30%) и в тонком кишечнике
(70-80%), достигая через 30-60 минут максимальной концентрации в крови.
Биологические эффекты экзогенного этанола многогранны:
мембранотропные, метаболические, наркотические, токсические и канцерогенные.
Метаболизм этанола начинается уже
в слизистой оболочке рта и
продолжается во многих органах,
но главным образом в печени
(до 70 - 95% окисляемого этанола).
33.
При малых и умеренных дозах этанол окисляется с участиемНAД-зависимых ферментов.
Токсическое действие оказывает продукт метаболизма этанола - ацетальдегид.
Ацетальдегид способен взаимодействовать с функциональными группами
(NH2, SH, ОН) белков, ферментов, рецепторов, глутатиона, нарушая их функции,
что может вызывать рак полости рта, глотки и мочевых путей.
Ацетальдегид ингибирует НAДH-дегидрогеназу и снижает способность
гемоглобина переносить кислород, что приводит к нарушению энергетического
обмена и синтеза АТФ.
34.
При употреблении больших количеств этанола индуцируетсяособая микросомальная этанолокисляющая система (МЭОС),
Главную роль в МЭОС играет цит. Р450 II Е1 - один из изоферментов цит. Р450.
В этой ситуации окисление этанола происходит следующим образом:
Цитохром Р450 II E не обладает абсолютной специфичностью
и может катализировать реакции с другими веществами,
в том числе лекарствами, вызывая их биотрансформацию.
У лиц, страдающих алкоголизмом, этанол увеличивает
активность цит. P450 путем индукции, поэтому
биотрансформация лекарств протекает более активно
и эффективность препаратов снижается.
35.
ХИМИЧЕСКИЙ КАНЦЕРОГЕНЕЗ.В основе химического канцерогенеза лежат повреждения
ДНК под действием химических канцерогенов.
● Канцерогенами могут быть как органические, так и неорганические молекулы, т.е.
канцерогенность не связана с какой-либо определенной структурной особенностью.
● Многие вещества (полициклические ароматические углеводороды,
ароматические амины, нитрозамины), которые содержатся в смоле,
табачном дыме, в загрязненном воздухе больших городов, в пищевых продуктах,
подвергнутых обжариванию на углях или копчению, сами не являются
канцерогенами, но превращаются в них, подвергаясь биотрансформации
в печени ферментами микросомального окисления.
● Известны сотни генов (протоонкогены),
мутации в которых могут способствовать
превращению нормальной клетки в опухолевую.
36.
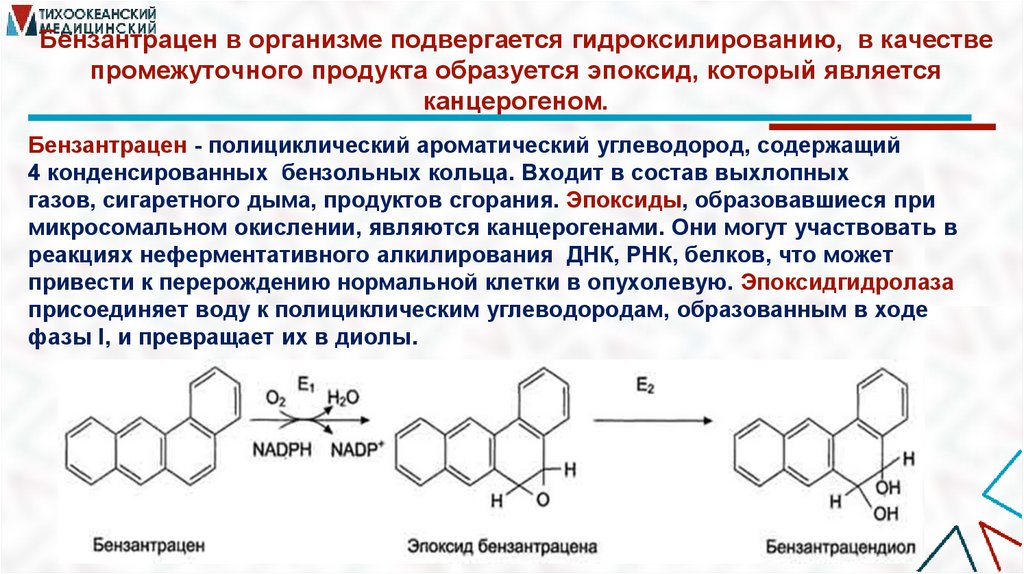
Бензантрацен в организме подвергается гидроксилированию, в качествепромежуточного продукта образуется эпоксид, который является
канцерогеном.
Бензантрацен - полициклический ароматический углеводород, содержащий
4 конденсированных бензольных кольца. Входит в состав выхлопных
газов, сигаретного дыма, продуктов сгорания. Эпоксиды, образовавшиеся при
микросомальном окислении, являются канцерогенами. Они могут участвовать в
реакциях неферментативного алкилирования ДНК, РНК, белков, что может
привести к перерождению нормальной клетки в опухолевую. Эпоксидгидролаза
присоединяет воду к полициклическим углеводородам, образованным в ходе
фазы I, и превращает их в диолы.
37.
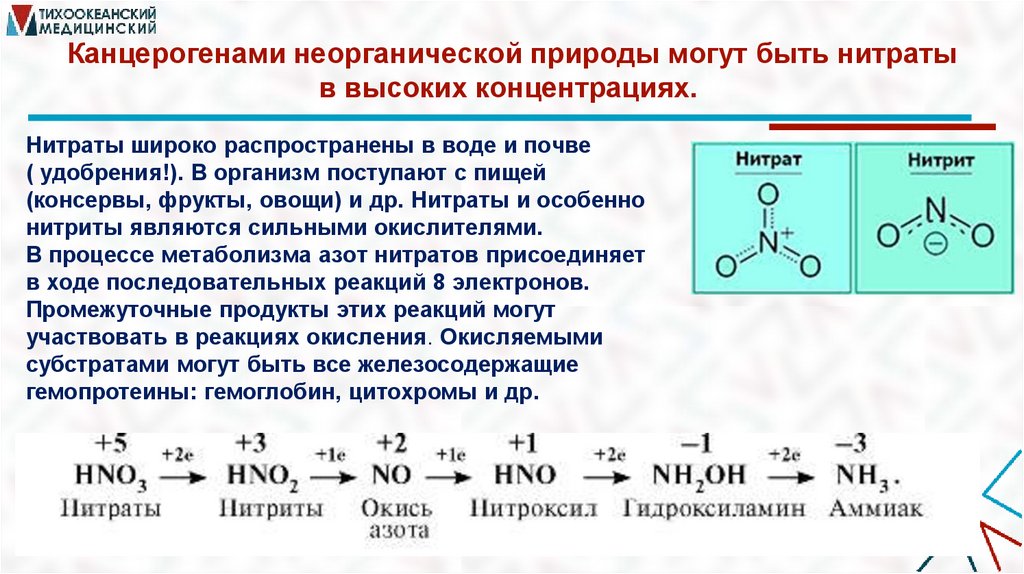
Канцерогенами неорганической природы могут быть нитратыв высоких концентрациях.
Нитраты широко распространены в воде и почве
( удобрения!). В организм поступают с пищей
(консервы, фрукты, овощи) и др. Нитраты и особенно
нитриты являются сильными окислителями.
В процессе метаболизма азот нитратов присоединяет
в ходе последовательных реакций 8 электронов.
Промежуточные продукты этих реакций могут
участвовать в реакциях окисления. Окисляемыми
субстратами могут быть все железосодержащие
гемопротеины: гемоглобин, цитохромы и др.
38.
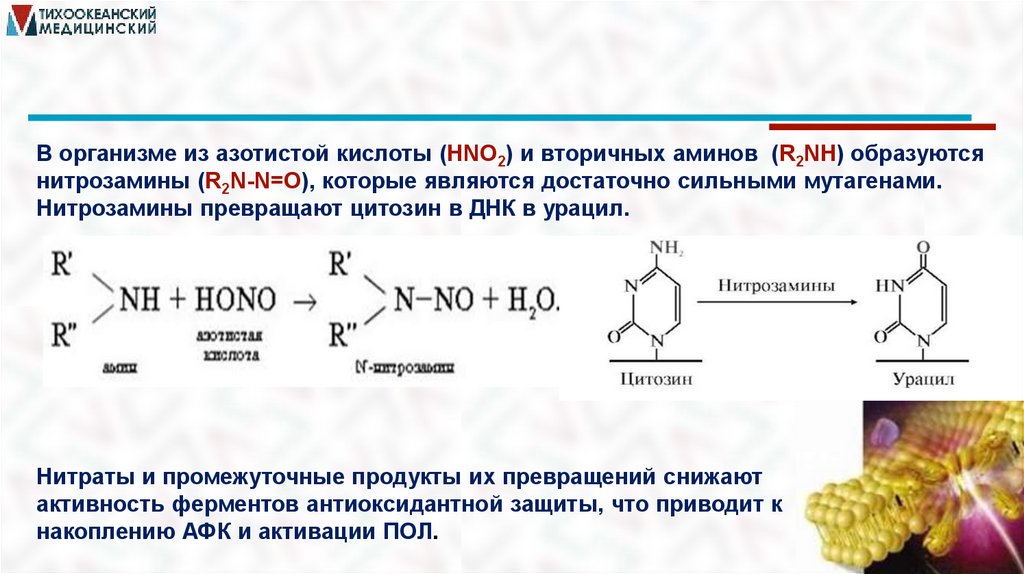
В организме из азотистой кислоты (HNO2) и вторичных аминов (R2NH) образуютсянитрозамины (R2N-N=O), которые являются достаточно сильными мутагенами.
Нитрозамины превращают цитозин в ДНК в урацил.
Нитраты и промежуточные продукты их превращений снижают
активность ферментов антиоксидантной защиты, что приводит к
накоплению АФК и активации ПОЛ.
39.
Ароматические амины – это вещества, которые используются впроизводстве анилиновых красителей и резиновой промышленности.
2-нафтиламин в печени в ходе I фазы
обезвреживания превращается в
канцероген 2-амино-1-нафтол.
Далее он конъюгирует с ФАФС и
превращается в нейтральный
продукт. При выведении с мочой
часть конъюгатов гидролизуется,
в результате чего снова образуется
канцероген, который может со
временем вызвать развитие рака
мочевого пузыря.
40.
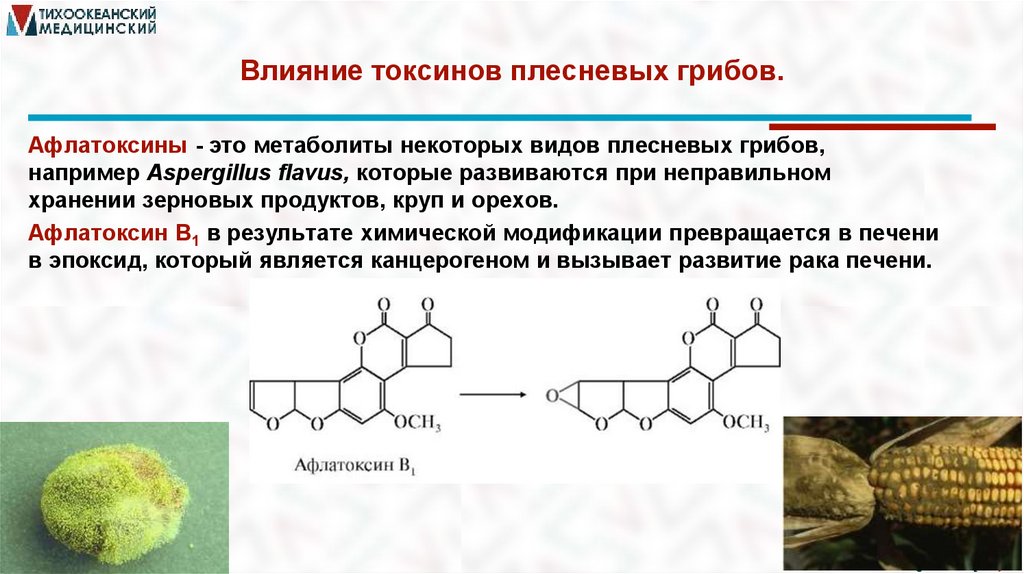
Влияние токсинов плесневых грибов.Афлатоксины - это метаболиты некоторых видов плесневых грибов,
например Aspergillus flavus, которые развиваются при неправильном
хранении зерновых продуктов, круп и орехов.
Афлатоксин В1 в результате химической модификации превращается в печени
в эпоксид, который является канцерогеном и вызывает развитие рака печени.
41.
Пигментный обмен в организме.Катаболизм гема и гемопротеинов.
Эритроциты имеют короткое
время жизни (120 дней),
при физиологических условиях в
организме человека ежесуточно
разрушается около 9 г гемопротеинов.
Распад гема происходит в ЭПР клеток
селезенки, костного мозга и печени.
Гем в составе гемоглобина окисляется
О2. В реакциях последовательно
происходит разрыв метинового мостика
между 1-м и 2-м пиррольными кольцами
гема с их восстановлением, отщеплением
железа и белковой части (глобина) и
образованием пигмента билирубина.
42.
Катаболизм гема в организме.Катаболизм гема происходит при участии
О2, гемоксигеназы (кофермент - НАДФН2).
Образуется биливердин (пигмент жёлто-зеленого
цвета).
Биливердин восстанавливается
биливердинредуктазой (кофермент - НАДФН2)
до билирубина (пигмент красно-желтого цвета).
У взрослого человека образуется ~ 250-350 мг/сут
билирубина (пигмент токсичен, нерастворим в воде).
Обезвреживание образованного в клетках РЭС
селезенки токсичного и гидрофобного билирубина
происходит в печени.
43.
Неконъюгированный (непрямой, свободный) билирубин.Билирубин, образованный в клетках РЭС селезенки, токсичный и плохо
растворимый в воде/крови, транспортируется в печень альбумином крови.
Эту фракцию билирубина называют неконъюгированный, непрямой
(не дает прямую реакцию с диазореактивом) или свободный билирубин.
Неконъюгированный билирубин легко растворяется в липидах мембран клеток
и проникает в митохондрии, разобщает дыхание и синтез АТФ, нарушает синтез
белка и др. Неконъюгированный билирубин проходит гемато-энцефалический
барьер (ГЭБ), когда его концентрация в плазме превышает уровень насыщения
альбумина, что отрицательно сказывается на состоянии ЦНС (энцефалопатия!).
44.
Конъюгированный(прямой, связанный) билирубин.
Реакции конъюгации билирубина происходят
в гепатоцитах. К билирубину присоединяются
2 молекулы глюкуроновой кислоты.
Катализируют процесс ферменты
УДФ – глюкуронилтрансферазы,
продуктом реакции является нетоксичный,
растворимый билирубиндиглюкуронид.
Эту форму (фракцию) билирубина называют
конъюгированный (прямой, связанный) билирубин.
Конъюгированный билирубин секретируется
в желчь и далее поступает в кишечник.
Небольшая часть прямого билирубина
может попадать в кровоток.
45.
В кишечнике билирубиндиглюкурониды гидролизуютсябактериальными ферментами.
В ЖКТ билирубин восстанавливается с образованием
бесцветных мезобилиногенов (уробилиногенов).
В толстой кишке ~ 15% мезобилиногенов
всасывается, попадает с кровью в печень,
где разрушается. При патологии печени
разрушения не происходит. Уробилиногены в моче показатель поражения гепатоцитов!
Большая часть мезобилиногенов окисляется до
пигмента коричневого цвета - стеркобилиногена
(стеркобилина) и удаляется с калом (200-300 мг/сут)
и с мочой (1-2 мг/сут). Стеркобилиноген в кишечнике
всасывается по системе геморроидальных вен,
попадает через почки в мочу и становится
пигментом мочи уробилином, влияющим на ее цвет.
46.
Диагностическое значение определения желчных пигментовв крови/моче.
Нормальная концентрация общего
билирубина в крови составляет
3,4 - 17,1 мкмоль/л.
Повышение концентрации общего
билирубина в крови – гипербилирубинемия.
При концентрации билирубина в крови
более 50 мкмоль/л, он диффундирует
в ткани, окрашивая их в жёлтый цвет.
Пожелтение тканей из-за отложения
в них билирубина называют желтухой.
47.
ЖелтухиНадпеченочная
(гемолитическая)
Печеночная
(паренхиматозная)
Подпеченочная
(механическая,
холестаз)
48.
Гемолитическая (надпеченочная) желтуха –результат интенсивного гемолиза эритроцитов.
Причины гемолиза: отравление, сепсис,
лучевая болезнь, несовместимость крови,
серповидно-клеточная анемия и др.
Способность печени образовывать глюкурониды
и выделять их в желчь в 3 - 4 раза превышает их
образование в физиологических условиях.
Гемолитическая желтуха развивается при
исчерпании резервных возможностей печени.
Диагностика:
Кровь: ↑ общий билирубин
↑ неконъюгированный (непрямой).
Кал интенсивно окрашен (↑ стеркобилины).
Моча интенсивно окрашена (↑ уробилины).
49.
Желтуха новорожденных – физиологическая желтуха.Желтуха у новорожденных детей наблюдается
в первые дни жизни ребёнка, может вызывать поражение
ЦНС.
Причиной повышения концентрации непрямого
билирубина в крови служит ускоренный гемолиз
эритроцитов и функциональная недостаточность
ферментов печени, ответственных за поглощение,
конъюгацию и секрецию прямого билирубина
(↓ активность УДФ-глюкуронилтрансферазы).
Методы коррекции желтухи новорожденных:
- фенобарбитал (индуктор синтеза цит. Р450)
- фототерапия (длина волны 620 нм)
- переливание крови.
50.
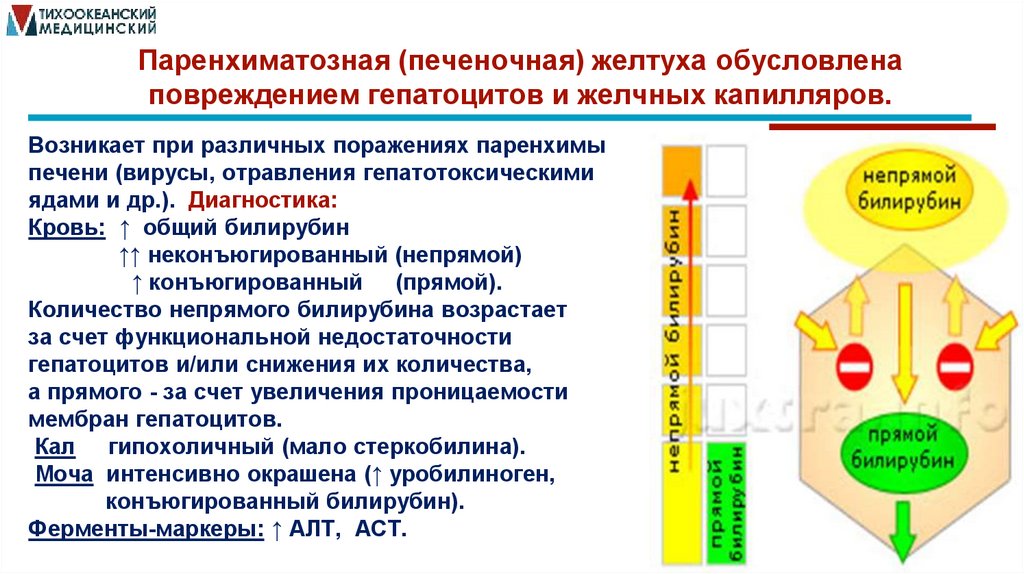
Паренхиматозная (печеночная) желтуха обусловленаповреждением гепатоцитов и желчных капилляров.
Возникает при различных поражениях паренхимы
печени (вирусы, отравления гепатотоксическими
ядами и др.). Диагностика:
Кровь: ↑ общий билирубин
↑↑ неконъюгированный (непрямой)
↑ конъюгированный (прямой).
Количество непрямого билирубина возрастает
за счет функциональной недостаточности
гепатоцитов и/или снижения их количества,
а прямого - за счет увеличения проницаемости
мембран гепатоцитов.
Кал гипохоличный (мало стеркобилина).
Моча интенсивно окрашена (↑ уробилиноген,
конъюгированный билирубин).
Ферменты-маркеры: ↑ АЛТ, АСТ.
51.
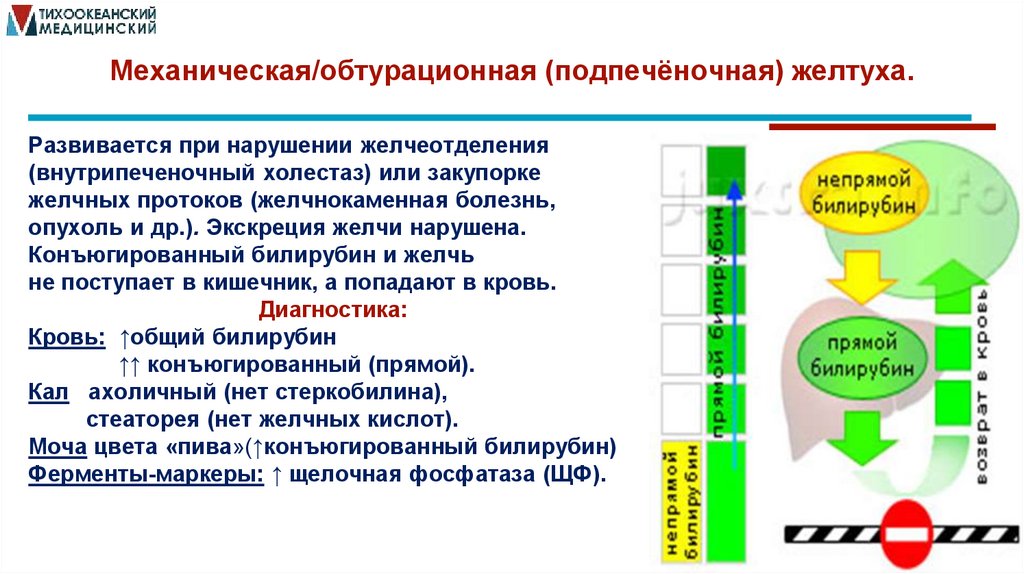
Механическая/обтурационная (подпечёночная) желтуха..Развивается при нарушении желчеотделения
(внутрипеченочный холестаз) или закупорке
желчных протоков (желчнокаменная болезнь,
опухоль и др.). Экскреция желчи нарушена.
Конъюгированный билирубин и желчь
не поступает в кишечник, а попадают в кровь.
Диагностика:
Кровь: ↑общий билирубин
↑↑ конъюгированный (прямой).
Кал ахоличный (нет стеркобилина),
стеаторея (нет желчных кислот).
Моча цвета «пива»(↑конъюгированный билирубин)
Ферменты-маркеры: ↑ щелочная фосфатаза (ЩФ).
52.
Значение определения желчных пигментов в диагностикетипа желтухи.
9. Обтурационная желтуха
(рак головки поджелудочной железы).
10. Паренхиматозная желтуха.
11. Гемолитическая желтуха.
цвет мочи (а) и кала (б).
Сыворотка крови
(желтая из-за высокого
содержания билирубина)



























 Медицина
Медицина