Похожие презентации:
Молекулярно-генетическая диагностика
1.
2.
Содержание:1. Общая информация. Что такое ПЦР. Этапы ПЦР анализа.
2. Виды транспортных сред.
3. Правила подготовки и забора материала для ПЦР диагностики. Хранение и транспортировка.
4. Фемофлор и Аднрофлор.
5. Правила забора материала на Covid 19.
6. Digene-Тест. Код 540.
7. Полиморфизмы генов системы свертывания. Код 593.
8. Полиморфизмы генов фолатного цикла. Код 598.
9. Полиморфизмы генов BRCA1 и BRCA2? Ассоциированные с риском развития рака молочной железы и других органов. Код 581.
10. Полиморфизмы генов, ассоцированные с риском развития артериальной гипертензии. Код 589.
11. Делеции локуса AZF Y-хромосомы. Код 580.
12. Часто допускаемые ошибки и как их избежать.
3.
Полимеразная цепная реакция (ПЦР, PCR) — метод молекулярной биологии,позволяющий добиться значительного увеличения малых концентраций
определённых фрагментов нуклеиновой кислоты (ДНК) в образце биологического
материала, в результате чего становится возможным их обнаружение.
Объект Полимеразной цепной реакции:
ДНК (дезоксирибонуклеиновая кислота) – носитель наследственной информации,
определяет структуру и функции живого организма. У ряда вирусов (например,
ВИЧ, ВГС) эту задачу выполняет РНК (рибонуклеиновая кислота).
•ДНК (РНК) есть у всех живых организмов.
•Каждый организм имеет специфичные (уникальные) участки молекулы ДНК или
РНК, отличающие его от других биологических видов.
•Цепи ДНК и РНК состоят из нуклеотидов, содержащих пять типов азотистых
оснований: аденина, гуанина, цитозина, тимина (ДНК), урацила (РНК),
образующих между собой пары по принципу комплементарности.
Комплементарность – способность азотистых оснований образовывать
водородные связи, обеспечивающие двухцепочечную структуру ДНК.
4.
Этапы ПЦР-анализа (аналитическая стадия исследования образца)Пробоподготовка: Предварительные процессы выделения ДНК и/или РНК из пробы для дальнейшего
проведения реакции. Происходит процесс разрушения клетки для высвобождения ДНК/РНК под
действием различных растворов, например, лизирующим раствором.
Амплификация: процесс увеличения малых концентраций участков ДНК в пробе, производится в
приборе (амплификаторе). В каждой микропробирке происходит процесс увеличения ДНК копий
микроорганизмов. Процесс амплификации может включать в себя различное количество циклов (Ct).
Цикл – время поддержания определенной температуры.
Если микроорганизм присутствует в пробе на экране прибора появляется графический результат на
каком-то из циклов.
Детекция: определение продуктов реакции после амплификации посредством измерения
интенсивности свечения флоофора (красителя) в микропробирке прибором (амплификатором).
Выявление копий ДНК микроорганизмов если таковы присутствуют в пробе.
Анализ результатов: комплекс мероприятий, направленных
последующей выдачей результатов пациенту.
на
правильное
заключение
с
5.
Виды транспортных сред:ДНК 8885 транспортный раствор.
Эппендорф с прозрачной жидкостью 2 мл.
Транспортная среда для исследований коды 500, 501,
502, 503, 504, 505, 506, 507, 508, 509, 511, 525, 526, 594
Транспортная раствор ТР- 100. Конусовидный
эппендорф с прозрачной жидкостью.
Транспортная среда для исследований ПЦР Ковид
коды 554, 550, 560.
Комплект реагентов для выделения ДНК «ПробаРапид». Конусовидный эппендорф с голубой
жидкостью. Предназначена для исследований коды
520, 521 Фемофлор, 522,523 Андрофлор, 545 ВПЧ
Квант-21.
Урогенитальный зонд тип А
Пробирка вакуумная с наполнителем К2-ЭДТА, Фиолетовая
крышка.
Предназначена для исследований крови методом ПЦР коды
524,528, 529, 532, 512, 513, 593.
Стерильный контейнер. Используется для сбора биологических
жидкостей, таких как Слюна, моча, эякулят, спиномозговая
жидкость методом ПЦР (НЕ МЕНЕЕ 1МЛ).
Стерильный контейнер с ложечкой. Используется для сбора кала
для исследований методом ПЦР (код 535 ПЦР Helicobacter pylori
в кале, код 9134 ПЦР острые кишечные инфекции) (1/2 чайной
ложки).
Набор для взятия цервикальных проб DNAPAP Cervical
Sampler™ (Digene-Тест)(Люм-набор)
6.
Исследуемый материал:Вирус Эпштейн-Бар
(вирус герпеса 4 типа
ВЭБ, ЭБВ, Epstein-Barr
virus, Human herpesvirus 4):
соскоб,
кровь,
синовиальная
жидкость
ликвор, слюна, мазки со
слизистой ротоглотки.
Герпетическая инфекция
(Herpes simplex viruse type
1-2, ВПГ): соскоб, кровь,
синовиальная
жидкость,
слюна, моча, эякулят.
Цитомегаловирусная
инфекция
(ЦМВ,
CMV,
Cytomegaloviruses,
вирус
герпеса 5 типа): соскоб,
кровь,
слюна,
спинномозговая,
синовиальная
жидкость,
эякулят.
Уреаплазмоз
(Ureaplasma urealyticum)соскоб, моча, эякулят,
синовиальная жидкость.
Кандидоз (Candida albicans):
соскоб, моча, эякулят.
Вирус гепатита В: кровь
Гонорея
(Neisseria gonorrhoeae) :
соскоб, секрет простаты,
эякулят, моча, синовиальная
жидкость.
Гарднереллез
(Gardnerella vaginalis):
соскоб, моча, эякулят.
Вирус гепатита С: Кровь.
Микоплазмоз
(Mycoplasma hominis,
Mycoplasma genitalum):
соскоб, моча, эякулят.
Хламидиоз
(Chlamydii trachomatis):
соскоб, моча, синовиальная
жидкость, эякулят.
Helicobacter pylori: кал
Трихомониаз
(Trichomonas vaginalis):
соскоб моча, эякулят.
Папилломавирусы:
Соскоб, моча, эякулят.
7.
Правила подготовки и забора биоматериала. Хранение и транспортировка.Урогенитальный мазок у женщин:
• В течение 48 часов до сдачи материала воздержаться от половых контактов.
• В течение 2-3 часов до сдачи материала не мочиться.
• За две недели необходимо прекратить прием антибиотиков, если применялся данный вид
лечения.
• Исключить местное применение лекарственных препаратов (включая противозачаточные
свечи), которые могут исказить результат, так как обладают антибактериальным действием.
• Накануне нельзя подмываться антибактериальным мылом, а также спринцеваться.
• Не рекомендуется сдавать материал во время менструации, (рекомендуется через 2 дня после её
окончания).
• Если накануне была кольпоскопия или влагалищное УЗИ, то следует отложить взятие
биоматериала на 48 часов*.
Порядок взятия: ввести гинекологическое зеркало во влагалище.
- Удалить ватным тампоном слизь и обработать шейку матки стерильным тампоном, смоченным
физиологическим раствором, далее обработать насухо.
1.Соскоб берется зондом тип А с заднего свода влагалища.
2.Соскоб эпителиальных клеток из цервикального канала: зонд тип А ввести в цервикальный
канал на глубину 0,5-1,5 см, собрать материал осторожными вращательными движениями.
3. Соскоб эпителиальных клеток из уретры: непосредственно перед взятием материала наружное
отверстие уретры обработать тампоном, смоченным стерильным физиологическим раствором.
- Ввести зонд тип А на глубину 1,0-1,5 см, собрать материал осторожными вращательными
движениями.
После взятия материала зонды погрузить в эппендорф с транспортной средой, несколько раз
повращать и удалить из него. Эппендорф плотно закрыть.
Если пациент одновременно сдает анализы на ВПЧ и ИППП:
Вначале забор материала производить на ВПЧ, затем на ИППП.
8.
Урогенитальный мазок у мужчин:• В течение 2–3 часа после мочеиспускания.
• За две недели необходимо прекратить прием антибиотиков, если применялся данный вид
лечения.
• Перед взятием мазка из уретры, головку полового члена обрабатывают стерильной
салфеткой.
Соскоб из уретры: зонд тип А ввести в уретру на глубину 2-3 см и несколькими
вращательными движениями собрать материал. При наличии обильных гнойных выделений
соскоб надо брать не позже, чем через 15 минут после мочеиспускания. После взятия
материала зонд опускают в транспортную среду эппендорф, ополаскивают, а затем удаляют из
пробирки.
Хранение.
Эппендорф с транспортной средой хранится до и после забора материала в холодильнике при
температуре +2 +80С. Повторной заморозке материал не подлежит!!!
Транспортировка: при температуре +2 +8 С.
Если пациент одновременно сдает анализы на ВПЧ и
ИППП: Вначале забор материала производить на ВПЧ,
затем на ИППП.
Эякулят: сдаётся в стерильный контейнер, который в течение 1 часа доставляется в
лабораторию.
При сборе эякулята мужчине необходимо:
- в течение 2 часов до сдачи материала не мочиться
- помыть руки и половой член с мылом
- отмыть остатки мыла
- высушить руки и половой член свежими одноразовыми салфетками.
Эякулят необходимо собрать в стерильный контейнер в специальном кабинете на ПЗ
«Московская, 96» или в домашних условиях при условии доставки материала в течение 1 часа;
Хранение: при температуре +2 +8 в холодильнике;
Транспортировка: при температуре +2 +8 С
9.
Кровь: Желательно сдавать натощак (4часа голода).Соскоб с конъюнктивы:
Взятие материала должно проводиться до начала применения антибактериальных и
химиотерапевтических препаратов или не ранее, чем через 10–14 дней после их отмены.
Забор осуществляется Зондом тип А предварительно вывернув веко, собрать
эпителиальные клетки с конъюнктивы и смыть в эппендорф с транспортной средой.
Метод забора.
Забор крови осуществляется в пробирку с фиолетовой крышкой, пробирка тщательно
перемешивается, но не встряхивается!
Хранение: в холодильнике (Т +2+8 С0) . В течение 24 часов
Транспортировка: при температуре +2 +8С.
Букальный (щечный) соскоб:
Слюна.
Взятие материала должно проводиться до начала применения антибактериальных и
химиотерапевтических препаратов или не ранее, чем через 10–14 дней после их отмены.
- за 2 часа до взятия эпителия со слизистой полости рта прополоскать рот теплой водой.
Для грудных детей – за 2 часа до взятия материала исключить кормление грудным
молоком.
Порядок взятия: Зонд тип А ввести в полость рта в щечно-десновой карман (в этом месте
скапливается много эпителия), слегка прижать зонд рукой с наружи, зажав между щекой и
десной.
Вращательно-поступательными движениями собрать зондом эпителий. Вывести зонд из
полости рта и сполоснуть в растворе, отжимая от борта эппендорфа, вращая секунд 10,
избегая разбрызгивания раствора. Зонд удалить, крышку эппендорфа закрыть до щелчка.
Хранение и транспортировка: при температуре +2+8
Соскоб из Зева: Взятие материала должно проводиться до начала применения
антибактериальных и химиотерапевтических препаратов или не ранее, чем через 10–14
дней после их отмены.
Зондом типа А взять небольшое количество эпителия и перенести в эппендорф с
транспортной средой, сполоснуть в растворе. Зонд удалить, крышку эппендорфа закрыть
до щелчка.
Моча. В пустой стерильный контейнер с плотно завинчивающейся крышкой собирают
утреннюю первую порцию мочи в количестве минимум 10 мл. Если забор мочи проводят
днем, то перед этим пациент не должен мочиться 1,5-3 часа. Сбор материала
осуществляется после туалета половых органов.
Из мокроты и грудного молока ПЦР
проводятся!!!
исследования НЕ
Взятие материала должно проводиться до начала применения антибактериальных и
химиотерапевтических препаратов или не ранее, чем через 10–14 дней после их отмены.
За 12 часов до взятия (сбора) слюны исключается прием пищи, алкоголя и лекарственных препаратов.
Перед тем, как собрать слюну, необходимо хорошо прополоскать рот теплой водой без использования
раздражающих средств.
Метод забора:
Забор слюны производится в одноразовые стерильные контейнеры, необходимый объем 1-5 мл. У
маленьких детей слюна берется шприцом из-за щечки и переносится в контейнер. Забор слюны можно
производить в течение дня.
Хранение: в холодильнике (Т +2+8 С0) .
Секрет предстательной железы. После массажа предстательной железы сок собирают в
количестве 0,5-1 мл в пустую стерильную пробирку (контейнер). При невозможности получить сок,
сразу после массажа собирают первую порцию мочи в количестве не более 10 мл (в этой порции
содержится сок предстательной железы). Сбор материала производится врачом.
Ликвор, синовиальная жидкость - сбор материала производится врачом в стерильный
контейнер!
Кал на ПЦР диагностику:
Материал (кал) собирается до начала лечения антибактериальными и химиотерапевтическими
препаратами. Если нет других назначений лечащего врача (на фоне лечения).
За 3-4 дня до исследования отменить прием слабительных препаратов, касторового и вазелинового
масла и прекратить введение ректальных свечей. Кал, полученный после клизмы, а также после
приема бария (при рентгеновском обследовании) для исследования не пригоден.
Для исследования собирают свежевыделенный кал, полученный в день исследования естественным
путем..
Не допускается смешивать пробу фекалий с мочой.
Хранение и доставка осуществляется силами пациента в любой ближайший пункт забора нашей
лаборатории при температуре+2+8С в течение 4 часов с момента сбора материала.
В комментариях к заказу обязательно нужно указывать локализацию или биоматериал, принятый на исследование(например, соскоб из конъюктивы)!!!
10.
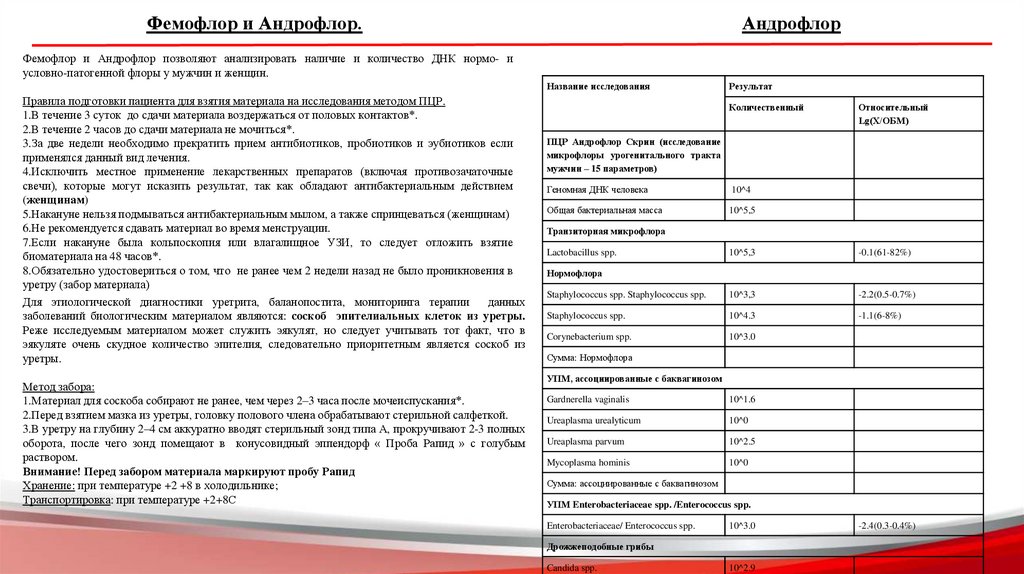
Фемофлор и Андрофлор.Андрофлор
Фемофлор и Андрофлор позволяют анализировать наличие и количество ДНК нормо- и
условно-патогенной флоры у мужчин и женщин.
Название исследования
Правила подготовки пациента для взятия материала на исследования методом ПЦР.
1.В течение 3 суток до сдачи материала воздержаться от половых контактов*.
2.В течение 2 часов до сдачи материала не мочиться*.
3.За две недели необходимо прекратить прием антибиотиков, пробиотиков и эубиотиков если
применялся данный вид лечения.
4.Исключить местное применение лекарственных препаратов (включая противозачаточные
свечи), которые могут исказить результат, так как обладают антибактериальным действием
(женщинам)
5.Накануне нельзя подмываться антибактериальным мылом, а также спринцеваться (женщинам)
6.Не рекомендуется сдавать материал во время менструации.
7.Если накануне была кольпоскопия или влагалищное УЗИ, то следует отложить взятие
биоматериала на 48 часов*.
8.Обязательно удостовериться о том, что не ранее чем 2 недели назад не было проникновения в
уретру (забор материала)
Для этиологической диагностики уретрита, баланопостита, мониторинга терапии
данных
заболеваний биологическим материалом являются: соскоб эпителиальных клеток из уретры.
Реже исследуемым материалом может служить эякулят, но следует учитывать тот факт, что в
эякуляте очень скудное количество эпителия, следовательно приоритетным является соскоб из
уретры.
Метод забора:
1.Материал для соскоба собирают не ранее, чем через 2–3 часа после мочеиспускания*.
2.Перед взятием мазка из уретры, головку полового члена обрабатывают стерильной салфеткой.
3.В уретру на глубину 2–4 см аккуратно вводят стерильный зонд типа А, прокручивают 2-3 полных
оборота, после чего зонд помещают в конусовидный эппендорф « Проба Рапид » с голубым
раствором.
Внимание! Перед забором материала маркируют пробу Рапид
Хранение: при температуре +2 +8 в холодильнике;
Транспортировка: при температуре +2+8С
Результат
Количественный
Относительный
Lg(Х/ОБМ)
ПЦР Андрофлор Скрин (исследование
микрофлоры урогенитального тракта
мужчин – 15 параметров)
Геномная ДНК человека
10^4
Общая бактериальная масса
10^5,5
Транзиторная микрофлора
Lactobacillus spp.
10^5,3
-0.1(61-82%)
Staphylococcus spp. Staphylococcus spp.
10^3,3
-2.2(0.5-0.7%)
Staphylococcus spp.
10^4.3
-1.1(6-8%)
Corynebacterium spp.
10^3.0
Нормофлора
Сумма: Нормофлора
УПМ, ассоциированные с баквагинозом
Gardnerella vaginalis
10^1.6
Ureaplasma urealyticum
10^0
Ureaplasma parvum
10^2.5
Mycoplasma hominis
10^0
Сумма: ассоциированные с баквагинозом
УПМ Enterobacteriaceae spp. /Enterococcus spp.
Enterobacteriaceae/ Enterococcus spp.
10^3.0
Дрожжеподобные грибы
Candida spp.
10^2.9
-2.4(0.3-0.4%)
11.
В основном, материалом для исследований служат соскобы эпителиальных клеток с задне-боковогосвода влагалища (для исследования биоценоза урогенитального биотопа у женщин), соскобы из
цервикального канала и уретры. Решение о необходимости исследовать ту или иную локализацию
(влагалище, уретра, цервикальный канал) принимает лечащий врач на основании жалоб пациентки и
клинической картины.
Забор Урогенитального соскоба у женщин:
Перед забором материала маркируют пробу Рапид (эппендорф с голубой жидкостью).
Процедура взятия материала:
Вводят гинекологическое зеркало во влагалище, осматривают слизистую влагалища и шейки матки,
цервикальную слизь и выделения удаляют при помощи стерильной салфетки, смоченной
физ.раствором
Соскоб эпителиальных клеток
движениями Зондом типа А
берется с заднего-бокового свода влагалища поскабливающими
Фемофлор
Название исследования
Результат
Количественный
ПЦР
Фемофлор
Скрин
(исследование
микрофлоры
урогенитального тракта женщин
– 13 параметров)
Соскоб из цервикального канала:
- Если цервикальный канал узкий, то Зонд тип А ввести в него на глубину 0,5-1,5 см, собрать
материал осторожными вращательными движениями.
- Если цервикальный канал широкий и на поверхности визуализируется зона трансформации
(эрозия цервикального канала), то брать материал необходимо на границе здоровой и измененной
ткани поскабливающими движениями
Общая бактериальная масса
Соскоб эпителиальных клеток из уретры:
-Непосредственно перед взятием материала наружное отверстие уретры обработать тампоном,
смоченным стерильным физиологическим раствором.
Ввести зонд на глубину 1,0-1,5 см, собрать материал осторожными вращательными движениями.
После взятия материала зонды погрузить в эппендорф с Пробой Рапид, несколько раз повращать и
удалить из пробирки. Пробирку плотно закрыть
Оставлять щеточку от зонда в пробирке Запрещено!
Хранение и Транспортировка:
Проба Рапид термосе с хладоэлементом при темпераратуре +2+8С
Gardnerella vaginalis + Prevotella 10^3.6
bivia + Porphyromonas spp.
В случае перезабора эпителиальных клеток обязательно удостовериться о том, что
не ранее чем 2 недели назад не было проникновения в уретру.
Относительный
Lg(Х/ОБМ)
10^7,1
Нормофлора
Lactobacillus spp.
10^7,1
-0.1(74-100%)
Облигатно-анаэробные микроорганизмы
Дрожжеподобные грибы
Candida spp.
10^2.8
Микоплазмы
Ureaplasma spp.
10^0
Mycoplasma hominis
не выявлено
Патогенные микроорганизмы
Mycoplasma genitalium
не выявлено
Trichomonas vaginalis
не выявлено
Neisseria gonorrhoeae
не выявлено
Chlamydia trachomatis
не выявлено
-3.5(<0.1%)
12.
Правила забора материала на Covid 19.Сотрудники, осуществляющие взятие диагностического материала, должны быть обеспечены
средствами индивидуальной защиты: респираторы типа FFP2 или маски, обеспечивающий более
высокий уровень защиты, очки для защиты глаз или защитный экран, одноразовый халат или
защитный костюм, одноразовые латексные (нетриловые) перчатки, шапочка.
Мазки из ротоглотки (зева) и носоглотки берутся двумя отдельными стерильными зондами
типа А, которые, после взятия материала помещается в эппендорф с транспортной средой
ТР – 100 (конусовидный эппендорф с прозрачной жидкостью. Зонды необходимо
обламывать и оставить в транспортной среде (с учетом рекомендации производителя
применяемых тест-систем/наборов реагентов).
Хранение и транспортировка при температуре +18 +25° C.
Время от момента забора до исследования не должна превышать 24 часа.
Транспортировка герметично закрытых контейнеров с образцами в лабораторию осуществляется в
специальных контейнерах.
Крышечку эппендорфа с образцом герметизируют парафилмом (скотчем) так, чтобы она не
открылась, маркируют и присваивают штрих-код.
Образец (эппендорф) каждого пациента помещают в индивидуальный герметичный пакет (zipпакет на молнии) с адсорбирующим материалом (кусочек ваты или бинт в 4 слоя 2х2 см).
Запрещается упаковывать образцы клинического материала от разных людей в одну упаковку, в
один пакетик.
Пакетик с эппендорфом помещают в герметично закрывающийся контейнер для транспортировки
биологических материалов (например, контейнер желтый для колюще-режущих предметов).
Транспортный контейнер опечатывается и маркируется COVID. Контейнер помещают
термосумку.
Сопроводительные документы
биологического материала.
помещаются
в
индивидуальную
упаковку
отдельно
от
13.
Digene-Тест Код 540Вирус папилломы человека Digene-тест (ВПЧ Digene-тест, метод «гибридного захвата»;
Digene HPV Test, Hybrid Capture Technology)
Существует более 100 генотипов вируса папилломы человека. Инфицирование этим вирусом достаточно распространённое явление. Передаётся инфекция обычно половым путём, в редких
случаях возможна вертикальная передача вируса от матери к ребёнку во время родов.
Инфицирование вирусом папилломы может не иметь клинических проявлений, часто наблюдается
естественное очищение организма от вируса, особенно в молодом возрасте. Но персистенция
вируса в эпителии шейки матки в течение длительного времени может вызывать его
патологические изменения.
Рак шейки матки – один из немногих видов злокачественных новообразований, для которых
установлена основная причина возникновения заболевания. Многочисленными исследованиями
показано, что ДНК вируса папилломы человека обнаруживается практически при всех случаях
предраковых состояний и при раке шейки матки. Инфицирование вирусом папилломы
предшествует последующей сквамозной (чешуйчатой) интраэпителиальной дисплазии шейки
матки. Третья стадия интраэпителиального новообразования шейки матки возникает только при
наличии персистирующей инфекции генотипами папилломавируса высокого онкогенного риска.
Доказано, что длительная персистенция (5 - 10 лет) папилломавируса генотипов высокого
онкогенного риска у женщин старше 30 лет связана со значительным ростом риска развития
злокачественных изменений шейки матки. Инфицирование вирусом папилломы генотипов
низкого онкогенного риска может клинически проявляться в виде появления остроконечных
кондилом.
Как правило, организм зараженного человека в течение нескольких месяцев
справляется с инфекцией сам (без лечения). Но рассчитывать на такой исход в
100 % случаев не приходится. Поэтому важно выяснить, как передается
папиллома, какие последствия вызывает заболевание. Если вирус
«закрепляется» в клетках эпителия, то это приводит к развитию папиллом,
кондилом либо подошвенных бородавок.
Типы 1-4 вызывают появление натоптышей, подошвенных бородавок.
Типы 10, 28 и 49 – это плоские бородавки.
Типы 11 и 6 вызывают появление остроконечных кондилом в мочевом пузыре,
на половых органах мужчин и женщин, на анусе, во рту, напоминая пучки
цветной капусты.
36, 42-44, 46-47, 50 типы вызывают плоские кондиломы.
Типы 16, 18, 30-33, 35, 39-40, 52, 55, 57-59, 61-62, 67-70, 72, 80-82 вызывают
предраковые состояния, онкологию, патогенность.
В свою очередь некоторые онкогенные типы штаммов являются типами
низкого уровня риска, а некоторые относятся к высокой степени онкогенности.
ВПЧ Digene-Тест представляет собой исследование, которое обладает самой высокой на сегодняшний день чувствительностью. Данное исследование позволяет выявить
папилломавирус, определить его тип и принадлежность к высокоонкогенной или низкоонкогенной группе и зафиксировать клинически значимые концентрации в тканях. Это может
служить важным прогностическим признаком.
Технология исследования на феномене гибридизации (связывания вирусной ДНК с РНК-зондом) и последующем захвате полученного гибрида моноклональными антителами на
твердой фазе. Далее происходит связывание гибрида антителами, которые помечены ферментом и завершение теста путем проведения хемилюминесценции. Для исследования
возможно использовать различный материал: соскоб эпителиальных клеток, полученный из цервикального канала, влагалища, уретры; ткани, полученные в результате биопсии.
Проведение ВПЧ Digene-Теста вместе с цитологическим исследованием является «золотым стандартом» в диагностике папилломавирусного поражения шейки матки. Поскольку
ВПЧ Digene-Тест определяет концентрации вируса, при которых происходит развитие онкологического процесса, то использую различные методы лечения можно предотвратить
процесс развития неоплазии.
Данный тест рекомендуется для скрининговых исследований у женщин старше 30 лет, а также в случаях неопределенного результата PAP-теста.
14.
Схема забора образца для исследования Digene -Test.Используйте набор для взятия цервикальных проб DNAPAP Cervical Sampler™
1. Сбор материала.
Удалите цервикальную слизь с помощью стерильной марлевой салфетки.
Введите цервикальную щетку на 1-1,5 см в цервикальный канал.
Поверните щетку 3 раза против часовой стрелки.
Не вводите щетку целиком в цервикальный канал.
2. Перенос материала.
Откройте пробирку и поместите щетку в пробирку.
Избегайте касания щетинок щетки внешней стороны пробирки. Отломите щетку от ручки по видимой линии.
3. Транспортировка.
Закройте транспортный флакон крышкой. Отправьте закрытый флакон с собранным материалом в лабораторию для
исследования.
Сроки хранения:
Цервикальные образцы могут храниться до 2 недель при комнатной температуре и доставляться к месту исследования
без охлаждения.
ВАЖНО!!! Беременным пациенткам забор материала на DIGENE-тест ЗАПРЕЩЕН!!!!
Данное исследование возможно выполнить из виалы для жидкостной цитологии.
Для этого осуществляется забор мазка для жидкостной цитологии по всем правилам и на виалу присваивается
второй (одинарный) штрих-код.
В программе «Генезис» в данном случае Digene- Тест будет оформлен под кодом 543.
15.
Полиморфизмы генов системы свертывания. Код 593.Полиморфизмы генов системы свертывания — это комплексное исследование
генетических факторов риска возникновения различных патологий в системе
гемостаза. Важно, что сами полиморфизмы генов системы гемостаза не являются
непосредственной и обязательной причиной развития заболеваний системы
свертывания крови, они только обусловливают риск развития этих патологий при
действии внешних факторов.
При выявлении полиморфизмов у пациента его информируют о повышенном риске
развития того или иного заболевания. Наличие некоторых полиморфизмов, наоборот,
является фактором, снижающим вероятность развития определённой патологии.
пример результата:
Полиморфизмы генов фолатного цикла. Код 598.
Фолатный цикл — это цикл реакций, в ходе которых аминокислота гомоцистеин при участии
ферментов (MTHFR, MTR, MTRR), использующих в качестве коферментов витамины группы В
(В6, В9 (фолиевая кислота) и В12), переходит в аминокислоту метионин, а также образуются
вещества, необходимые для синтеза ДНК.
Нарушение фолатного цикла возникает при мутациях в генах, кодирующих структуру ферментов
(MTHFR, MTR, MTRR), что приводит к нарушению функционирования ферментов фолатного
цикла и процесса перехода гомоцистеина в метионин и, как следствие, повышению уровня
гомоцистеина.
Гомоцистеин обладает выраженным токсическим, атерогенным и тромбофилическим действием,
что обуславливает риск развития ряда патологических процессов:
• эктопия хрусталика,
• остеопороз,
• канцерогенез (колоректальная аденома, рак молочной железы и яичника),
• усиление побочных эффектов химиотерапии,
сердечно-сосудистые заболевания (ишемическая болезнь сердца, инфаркт миокарда,
атеросклероз, атеротромбоз),
• осложнения беременности (фетоплацентарная недостаточность, преждевременная отслойка
нормально расположенной плаценты, поздний гестоз),
• дефекты развития плода (незаращение нервной трубки, анэнцефалии, деформации лицевого
скелета),
• пренатальная смерть плода.
16.
Полиморфизмы генов BRCA1 и BRCA2? Ассоциированные с рискомразвития рака молочной железы и других органов. Код 581.
Делеции локуса AZF Y-хромосомы. Код 580.
На долю наследственных форм приходится 5–10 % случаев рака молочной железы,
30 % из них обусловлены мутациями в генах BRCA1/2 (синдром наследственного
рака молочной железы/рака яичников). Основными показаниями для
генетического тестирования являются онкологически отягощенный семейный
анамнез, рак молочной железы у женщин в молодом возрасте (до 35–50 лет), рак
яичников, рак молочной железы у мужчин, морфологические особенности рака
молочной железы (трижды негативные, медуллярные опухоли), этническая
принадлежность (ашкеназские евреи). В группах высокого генетического риска
проводятся
профилактические
химиотерапевтические
и
хирургические
мероприятия. Показана высокая эффективность профилактических операций в
отношении развития рака молочной железы и рака яичников. Двусторонняя
профилактическая мастэктомия снижает риск развития рака молочной железы на
90–94 %.
Бесплодием страдает 15-20 % пар репродуктивного возраста. В половине случаев оно связано с
"мужским фактором", проявляющимся отклонениями в параметрах эякулята. Частыми причинами
мужского бесплодия являются нарушения структуры и количества сперматозоидов, влияющие на
их подвижность и способность к оплодотворению. Важную роль в развитии таких патологий, как
олигозооспермия и азооспермия, играют отклонения в специфическом участке Y-хромосомы –
AZF-локусе. Комплексное генетическое исследование помогает выявить проблемы по мужской
линии при планировании беременности и максимально быстро принять решение о необходимости
применения вспомогательных репродуктивных технологий.
17.
Полиморфизмы генов, ассоцированные с риском развития артериальнойгипертензии. Код 589.
Установление этиологии эссенциальной АГ позволяет оценить суммарный риск развития
патологического состояния, своевременно назначить профилактические и лечебные мероприятия,
что в совокупности дает возможность существенно ограничить негативное влияние заболевания
на качество жизни пациента.
Гипертоническая болезнь (эссенциальная гипертензия) — мультифакторное заболевание, в основе
которого лежит генетический полигенный структурный дефект, обусловливающий высокую
активность прессорных механизмов длительного действия.
При этом наибольшую актуальность приобретает выявление генетических полиморфизмов в генах
ключевых факторов регуляции сердечно-сосудистой системы, в первую очередь,
ассоциированных с функционированием ренин-ангиотензиновой системы.
Ренин-ангиотензиновая система (РАС) или ренин-ангиотензин-альдостероновая система
(РААС) — система ферментов и гормонов, регулирующих артериальное давление, электролитный
и водный баланс у млекопитающих.
Показания к генетическому анализу:
- артериальная гипертензия не менее чем у двух родственников первой и второй линии родства;
- семейный анамнез ранних сердечно-сосудистых заболеваний (инфаркт миокарда, ишемический
инсульт в возрасте до 50 лет);
- развитие артериальной гипертензии в возрасте до 45 лет;
- повышение давления при отсутствии причин симптоматической гипертензии (заболевания
почек,
эндокринной системы, пороков сердца и сосудов);
- ишемическая болезнь сердца (ИБС);
- острый инфаркт миокарда;
- ишемический инсульт;
- диабетическая нефропатия;
- венозная тромбоэмболия;
- нарушения плацентарной функции;
- нарушения микроциркуляции и сосудистого тонуса;
- сахарный диабет;
- подбор лекарственных препаратов при гипертонии;
Все генетические исследования сдаются один раз в жизни!!
При наличии дополнительных факторов риска:
- пожилой возраст: мужчины старше 55 лет и женщины старше 65 лет;
- курение;
- избыточная масса тела, абдоминальное ожирение;
женщин;
- низкая физическая активность, гиподинамия;
- психоэмоциональные стрессовые ситуации;
- избыточное потребление поваренной соли;
- злоупотребление алкоголем;
- уровень общего холестерина в сыворотке крови более 6,5 ммоль/л (250 мг/дл).
18.
Ошибки на преаналитическом этапе как их избежать:Ошибки на преаналитическом этапе
как их избежать
Выбраковка биоматериала на постаналитическом этапе:
Выбраковка
Как её избежать
Нарушение техники забора биоматериала
Не срезать зонды ножницами, не оставлять
зонды, не переносить самостоятельно
биоматериал из стерильных контейнеров в
эппендорфы.
Образец не дифференцируемыйналичие примесей, ингибирующих
пцр-реакцию: слизь, кровь, следы
лекарственные препаратов.
Нарушение оформления документации
Тщательно проверять соответсвие фамилии на
биоматериале и штрих-коде образа, не
наклеивать штрих-коды образцов друг на друга,
оставлять комментарии о биоматериале
(локализации) в генезисе, при необходимости.
Перед забором биоматериала
обязательно обрабатывать шейку
матки и уретру от слизи, выделений.
Уточнять у пациента правильно ли
он подготовлен к исследованию.
Образец не валиден-в пробе менее
250 эпителиальных клеток.
Тщательно осуществлять забор
материала, в соответствии с
правилами забора.
Неправильно выбрана транспортная среда
описание транспортных сред на слайде №5).
Недостаточно материала
Принимать/осуществлять забор материала в
соответствии с требованием, например,
биологические жидкости (слюна, синовиальная
жидкость) не менее 1 мл и тд.
Нарушение правил транспортировки
Не замораживать, держать в холодильнике при
температуре 2-8 градусов, кроме проб на Covid
*Кросс-контаминация -от пробы к пробе. Например, при вскрытии одного из образцов во время транспортировки.
(8-25 С). Контейнеры должны быть плотно
закрыты
избежание кросс-контаминации.*
Если допущено проливание биоматериала,
тово
выбраковывается
весь материал, который находится
в данном контейнере!!!!!!!!!!
Перезабор материала производится не раннее чем через 3 суток.

















 Медицина
Медицина








